生物可降解胆道支架治疗胆道良性狭窄的研究现状
邱思远,纪任,范卫填
(香港大学深圳医院 肝胆胰外科,广东 深圳 518053)
胆道良性狭窄(benign biliary stricture,BBS)是常见的胆道疾病之一,临床上常采用经内镜或经皮经肝放置胆道支架以解除胆道梗阻[1-2]。目前常用的胆道支架是塑料支架和自膨式金属支架[3]。塑料支架易堵塞、移位、需要频繁更换;金属支架价格昂贵、取出困难。生物可降解胆道支架(biodegradable biliary stent,BDBS)安全有效且无需更换,是极具应用前景的新型支架[4-5]。本文就关于BDBS在体研究现状做一综述。
1 生物可降解胆道支架的种类
理想的BDBS需要有如下特性[4]:(1)可降解性:支架可降解,降解产物可被排出或吸收而不产生蓄积;降解速率需要覆盖组织修复时间;(2)良好的生物相容性:支架及其降解产物必须无毒性、无致畸性,不引起凝血、溶血、免疫排斥等反应;(3)良好的物理特性:支架必须具备良好的弹性,拥有不亚于金属支架的扩张率和径向力;(4)可被修饰性:药物分子或细胞可以固定在其表面或内部以获得治疗的功能。目前符合以上特性且应用于体内的生物可降解胆道支架主要有:聚丙交脂(polylactide,PLA)胆道支架,聚二恶烷酮(polydioxanone,PDX)胆道支架和镁合金胆道支架。
以PLA和PDX制备的可吸收缝线已广泛运用于外科,如Vicryl、Monocryl和PDS缝线[6],其安全性和生物相容性也在近40年的临床应用中得到充分证实。与PLA胆道支架相比,PDX胆道支架柔韧性更优异,水解速率更慢,在胆汁中保留力学特性时间更长[7]。PLA胆道支架径向力远低于金属支架[8],而8 mm的自膨式PDX支架径向力达到普通金属支架的90%[9]。虽然有研究显示PDX支架3周后损失50%的物理强度,但是仍然保持其物理结构长达3~6个月[10]。
镁合金材料具有优良的生物相容性,且强度比PDX更高,是可降解胆道支架的理想材料,已经运用于血管支架和骨科材料,但在胆道支架的研究仍处于初级阶段[11]。西安交通大学王金瑞等[12]首先制备镁合金胆道支架,其在胆汁环境中40 d出现降解,50 d出现降解高峰,90 d完全降解。他们将其运用于犬急性梗阻性黄疸模型中[13]发现镁合金胆道支架组胆道黏膜下胶原纤维沉积较少,新生肌纤维较多,管壁增厚较轻,显示镁合金胆道支架在体内具有良好的生物相容性。北京大学Liu等[14]在兔胆总管内放置镁合金AZ31支架,观察6个月,病理结果显示胆管少量炎性增生,生化检查未显示金属毒性,支架6个月降解,但也发现胆管上皮细胞异型增生,是否有远期影响尚不明确。目前尚无镁合金胆道支架的人体试验报告。
生物工程学也利用新技术在探索新型的BDBS。三维打印技术可以快速生产相对便宜的特定医疗产品[15],在胆道系统的应用是未来可期的领域。Boyer等[16]首次报道了采用三维打印交联聚乙烯醇方法联合胶原蛋白注入成型制备新型的BDBS,并在支架上植入间充质干细胞和胆管上皮细胞。Liu等[17]利用静电纺丝法制备了全覆膜PDX的BDBS。这些探索性研究或可以提高狭窄治愈率、减少支架移位和降低成本,但仍处于探索阶段。
2 BDBS的动物实验进展
BDBS的动物实验主要目的是证明其安全性和有效性。自2003年Ginsberg等[8]首先报道了BDBS的动物体内实验,目前有关BDBS的动物实验研究共十余篇[8-9,13-14,18-31](见表1)。Laukkarinen等[21]在猪胆肠吻合模型中探讨PLA-BDBS对胆肠吻合口的影响,发现放置BDBS组平均胆肠吻合口内径明显大于非支架组,认为胆肠吻合口放置BDBS可以预防胆肠吻合口狭窄。他们也在猪胆囊切除术后胆瘘模型中探索BDBS的治疗作用[19],发现与塑料支架相比,PLA支架组腹腔引流管胆汁引流更少,可更早拔除引流管,两者组织反应没有区别,显示BDBS治疗胆囊切除术后胆瘘是安全有效的,并且可以避免再次干预。以上实验均未发现BDBS严重不良事件。

表1 BDBS的动物实验列表
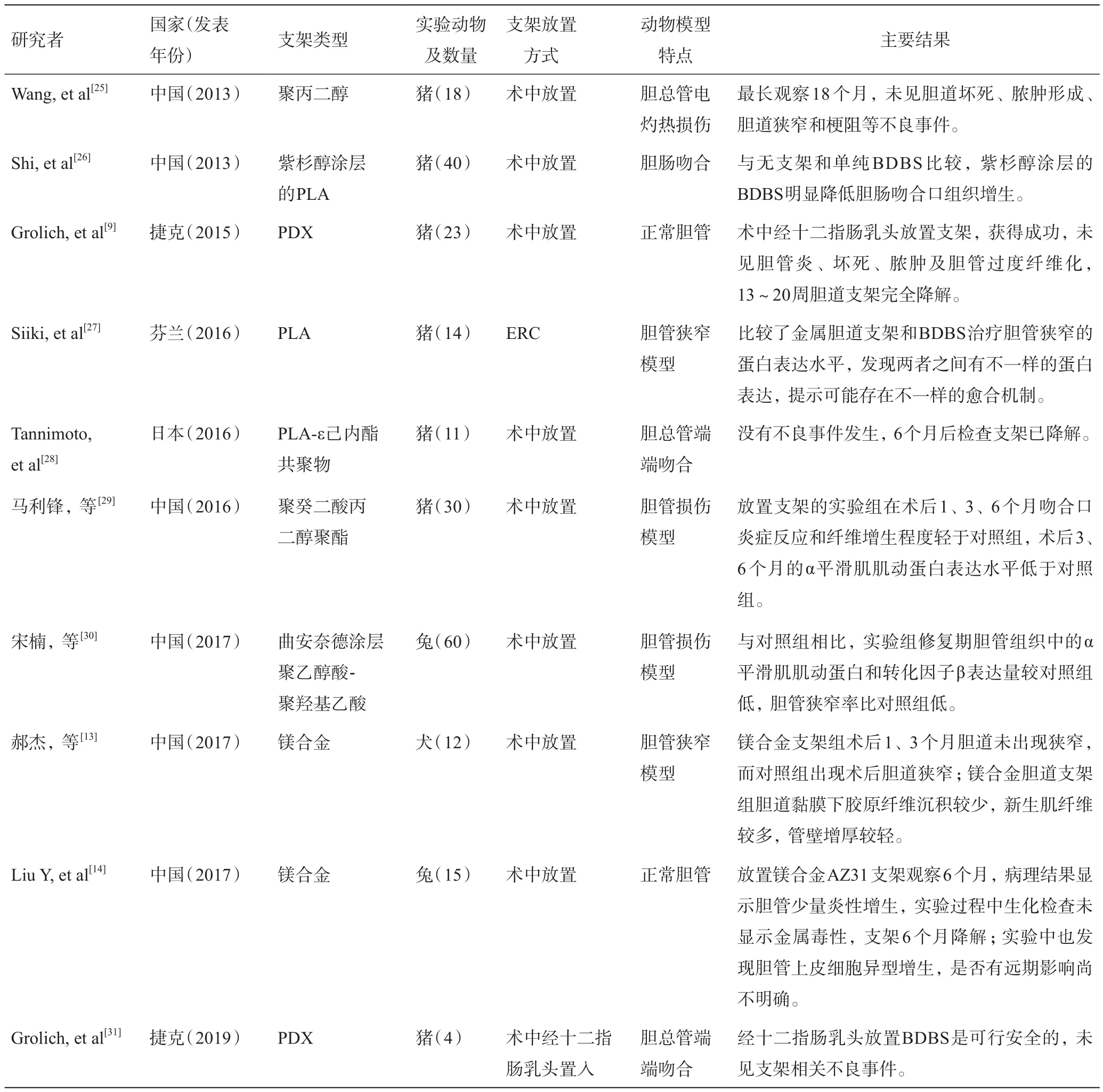
续表1 BDBS的动物实验列表
放置胆道支架后的组织愈合机制的研究有利于探索新的治疗方案,但是在人体临床研究中往往难以获取病理组织,动物实验可以弥补这一不足。Siiki等[27]在猪缺血性胆道狭窄模型中比较了PLA-BDBS和覆膜金属支架治疗狭窄的愈合相关蛋白表达,发现两者的愈合相关蛋白表达有所不同,提示BDBS治疗胆道狭窄可能有不一样的愈合机制,虽然尚不了解这一机制对愈合及远期复发的影响。
BDBS的动物研究的另一个方向是药物洗脱支架的开发。西安交通大学Shi等[26]开发了紫杉醇涂层的PLA支架,在猪胆肠吻合模型中发现:与无支架和单纯BDBS比较,紫杉醇涂层的BDBS明显降低胆肠吻合口组织增生,显示紫杉醇涂层的BDBS可减少吻合口肉芽形成和细胞外基质的过度增殖,从而预防胆肠吻合口狭窄。
3 BDBS的人体临床研究进展
BDBS因其无需二次干预的优点引起临床医师关注。主要是治疗及预防BBS。在治疗方面,2010年Petryl等[32]首次报道了两例使用PDX-BDBS治疗胆肠吻合口狭窄,术后都出现一过性胆管炎,但在其后随访2年,未见狭窄复发。在此之后,BDBS逐渐进入人体临床研究阶段并且临床报道越来越多,表2中为迄今为止国际上BDBS的人体研究报道[32-45]。早期的研究多为案例报告,直至2016年Mauri等[37]报道的一项纳入107例BBS患者的多中心回顾性系列病例研究,采用经皮经肝穿刺放置BDBS治疗方案,手术成功率达98%,平均随访23个月,术后1、2和3年狭窄复发率分别为7.2%、26.4%和29.4%;显示经皮经肝放置BDBS治疗胆道良性狭窄是安全可行的,短期和中期治疗效果令人满意;其中值得关注的是即使在狭窄没有复发的患者中,术后胆管炎的发生率也高达15%。术后胆管炎可能与先前手术、支架降解过程产生的支架碎片迁移或者黏膜炎症反应有关,但是目前没有足够的研究证实或否定这些假设,有待进一步的研究[39]。近期De Gregorio MA等[45]报道了迄今为止样本量最大多中心回顾性系列病例分析,该研究纳入150例BBS患者,所有患者均接受经皮经肝放置BDBS治疗BBS,手术成功率100%,平均随访45个月,治疗后1、3和5年胆管通畅率分别为86.7%、79.6%和78.9%,狭窄复发率为26.6%,总体并发症发生率为17.3%,但无重大BDBS相关并发症。这一结果令人鼓舞,显示BDBS治疗BBS安全有效。

表2 BDBS的人体临床研究列表
在预防BBS方面,2016年Janousek等[38]首次报道了使用PDX胆道支架放置于肝移植胆管端端吻合口,结果显示放置支架的患者未出现胆瘘、短期胆道狭窄以及支架相关并发症,但研究仅纳入5例患者且没有中期和长期的观察结果。BDBS是否有助于降低胆瘘和胆道狭窄发生率仍需要高质量和大样本的临床研究。
虽然临床研究数量不断增多,但多为病例报道或系列病例分析,证据等级较低,缺乏BDBS与塑料支架或金属支架的临床对照研究。唯一一篇临床对照研究来自Siiki团队[41],他们纳入8例应用BDBS治疗胆囊切除术后胆瘘的病例,与同期的24例塑料支架治疗组对比,两组不良事件发生率无统计学差异,两组具有相同的安全性和有效性,而BDBS组术后胆汁引流量明显低于塑料支架组,但是该研究为回顾性分析且纳入的样本量太少,存在偏移,结论难以令人信服,需要大样本的随机对照研究。
早期由于缺乏内镜下BDBS推送装置[35],经皮经肝穿刺是主要的支架放置方式,直至2015年,Siiki等[35]首先报道了经内镜途径放置BDBS治疗胆瘘的案例报告,随后他们报道了经内镜途径放置BDBS治疗BBS的病例报告并逐渐增加病例数量[39-40],目前只有该团队采用经内镜放置BDBS,但笔者相信,由于ERCP的发展和普及,未来经内镜放置BDBS的报道将会越来越多。
4 小结与展望
BDBS的动物实验和人体临床研究已经初步显示安全性和有效性,但仍有大量问题需要进一步研究:(1)目前的临床研究的样本量较少,多为回顾性案例报告,需要设计更好,更大样本量的前瞻性临床研究证实其长期安全性和有效性。(2)BDBS能否成为治疗胆道良性狭窄的最佳选择,需要设计严谨的随机对照研究。(3)BDBS是否更容易导致术后胆管炎,其引起胆管炎的原因也有待进一步的研究阐明。(4)全覆膜BDBS、药物洗脱BDBS、3D打印BDBS和镁合金胆道支架的研究还处于起步阶段,需要更多的实验室和动物实验证据。在欧洲,可降解支架已经广泛运用于食管良性狭窄,《英国食管扩张临床实践指南》[46]建议使用可降解食管支架以减少食管扩张的频率。相信BDBS同样能够在胆道良性狭窄领域创造广阔的应用前景。