西格列汀与二甲双胍分别联合胰岛素对2 型糖尿病患者胰岛素功能及糖脂代谢的影响
霍光强
(新乡市市直机关医院 普内科, 河南 新乡453000)
2 型糖尿病属于临床常见慢性疾病, 胰岛功能发生障碍或出现胰岛素抵抗均可能导致2 型糖尿病的发生[1-2]。 目前, 该病尚无治愈方式, 临床常通过长期药物治疗以控制病情。 二甲双胍是治疗2 型糖尿病的一线药物, 可有效改善胰岛素的敏感性[3]。 西格列汀属于二肽基肽酶-4 抑制剂, 可通过增加活性肠促胰岛素激素水平, 进而改善血糖水平[4]。 鉴于此, 本研究探讨西格列汀与二甲双胍分别联合胰岛素对2 型糖尿病患者胰岛素功能及糖脂代谢的影响, 现报道如下。
1 资料与方法
1.1 一般资料选取2016 年7 月至2019 年9 月我院收治的2型糖尿病患者60 例, 采用随机数字表法分为观察组和对照组各30 例。 观察组男16 例, 女14 例; 年龄31~64 岁, 平均年龄 (46.28 ± 5.61) 岁; 病程1~7 年, 平均病程 (3.87 ± 1.04)年; BMI (27.42 ± 1.80) kg/m2。 对照组男15 例, 女15 例; 年龄32~66 岁, 平均年龄 (47.34 ± 5.76) 岁; 病程1~7.5 年,平均病程 (4.02 ± 1.01) 年; BMI (27.36 ± 1.75) kg/m2。 两组的一般资料比较, 无统计学差异 (P>0.05), 具有可比性。
1.2 入选标准纳入标准: 符合2 型糖尿病诊断标准[5]; 认知能力正常; 对本研究知情并签署同意书; 入组前3 个月未服用相关降糖药物; 甲状腺功能正常。 排除标准: 合并心、 肝、 肾等功能不全; 患有精神障碍; 对本研究药物过敏; 妊娠期或哺乳期女性; 患有凝血功能障碍。
1.3 方法两组患者均采用常规饮食及进行运动干预。 对照组采用二甲双胍联合胰岛素治疗: 于清晨早饭前经皮下注射甘精胰岛素 (Sanofi-Aventis Deutschland GmbH, S20140008), 注射初始剂量为0.2 U/kg, 1 次/d; 同时于饭后口服二甲双胍片(北京京丰制药集团有限公司, 国药准字H11021518), 初始剂量为500 mg/次, 2 次/d, 根据患者血糖变化调整剂量, 最大剂量不得超过2 000 mg/d。 观察组采用西格列汀联合胰岛素治疗: 胰岛素使用方法同对照组, 同时口服西格列汀片 (Merck Sharp & Dohme Ltd., 国药准字J20140094) 治疗, 100 mg/次,1 次/d, 根据患者血糖变化调整剂量, 最大剂量不得超过200 mg/d。 两组均连续治疗6 个月。
1.4 观察指标观察两组患者治疗前、 治疗6 个月后的胰岛素功能指标及糖脂代谢指标。 采集两组患者的静脉血检测空腹血糖 (FPG) 水平, 应用化学发光法检测空腹胰岛素 (FINS)、 计算胰岛素β细胞功能指数(HOMA-β)、胰岛素抵抗指数(HOMA-IR)。 HOMA-β =20 × FINS/(FPG - 3.5), HOMA-IR=FPG × FINS/22.5。 采集两组患者清晨空腹静脉血, 4 000 r/min 离心10 min 后分离血清, 用自动生化分析仪检测总胆固醇(TC)、 三酰甘油 (TG)、 低密度脂蛋白胆固醇 (LDL-C)、 高密度脂蛋白胆固醇 (HDL-C) 水平。
1.5 统计学方法采用SPSS 23.0 统计学软件处理数据, 计量资料以± s 表示, 采用t 检验;P<0.05 为差异有统计学意义。
2 结果
2.1 胰岛素功能指标治疗前, 两 组 的FINS、 HOMA-β、HOMA-IR 水平比较无统计学差异 (P>0.05); 治疗后, 两组的FINS、 HOMA-IR 水平低于治疗前, HOMA-β 水平高于治疗前,且观察组的FINS、 HOMA-IR 水平低于对照组, HOMA-β 水平高于对照组 (P<0.05)。 见表1。
表1 两组患者的胰岛素功能指标比较 (±s)
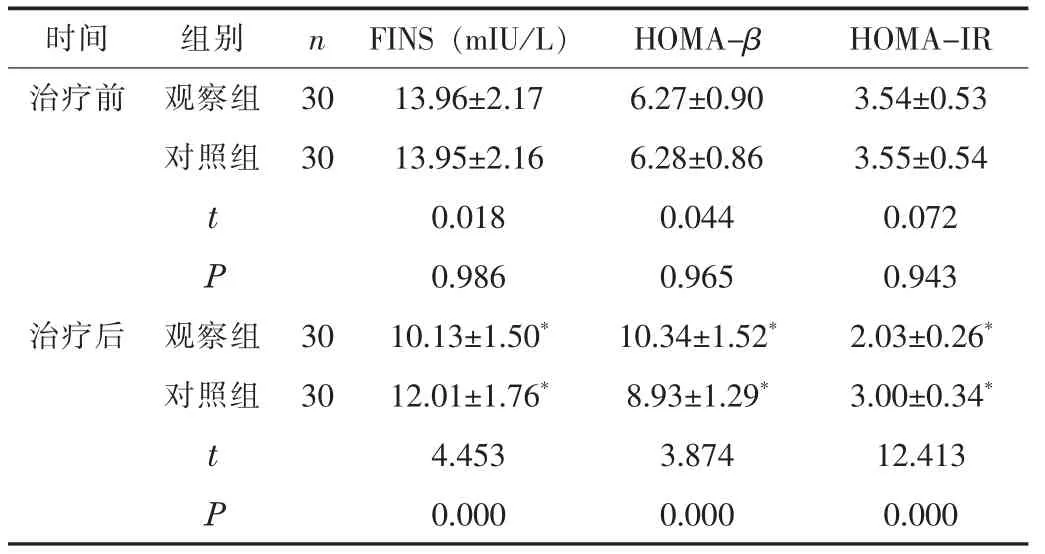
表1 两组患者的胰岛素功能指标比较 (±s)
注: 与本组治疗前比较, *P <0.05。
时间 组别 n FINS (mIU/L)HOMA-β HOMA-IR治疗前 观察组 30 13.96±2.17 6.27±0.90 3.54±0.53对照组 30 13.95±2.16 6.28±0.86 3.55±0.54 t 0.018 0.044 0.072 P 0.986 0.965 0.943治疗后 观察组 30 10.13±1.50* 10.34±1.52* 2.03±0.26*对照组 30 12.01±1.76* 8.93±1.29* 3.00±0.34*t 4.453 3.874 12.413 P 0.000 0.000 0.000
2.2 糖脂代谢指标治疗前, 两组的TC、 TG、 LDL-C、 HDLC、 FPG 水平比较无统计学差异 (P>0.05); 治疗后, 两组的TC、 TG、 LDL-C、 FPG 水平低于治疗前, HDL-C 水平高于治疗前, 且观察组的TC、 TG、 LDL-C、 FPG 水平低于对照组,HDL-C 水平高于对照组 (P<0.05)。 见表2。
表2 两组患者的糖脂代谢指标比较 (±s, mmol/L)
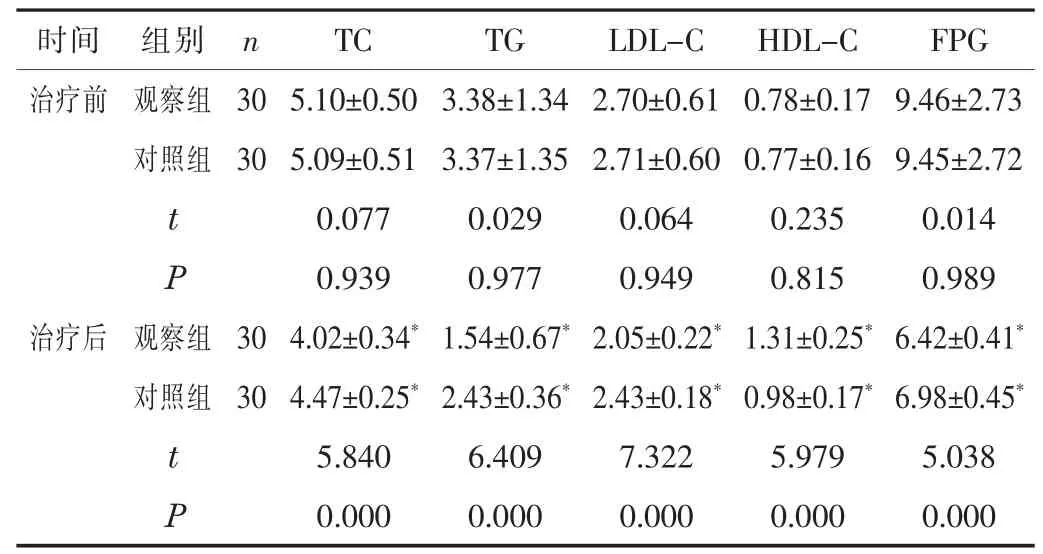
表2 两组患者的糖脂代谢指标比较 (±s, mmol/L)
注: 与本组治疗前比较, *P <0.05。
时间 组别 n TC TG治疗前 观察组 30 5.10±0.50 3.38±1.34对照组 30 5.09±0.51 3.37±1.35 t 0.077 0.029 P 0.939 0.977治疗后 观察组 30 4.02±0.34* 1.54±0.67*对照组 30 4.47±0.25* 2.43±0.36*t 5.840 6.409 FPG 9.46±2.73 9.45±2.72 0.014 0.989 6.42±0.41*6.98±0.45*5.038 P 0.000 0.000 0.000 0.000 0.000 LDL-C 2.70±0.61 2.71±0.60 0.064 0.949 2.05±0.22*2.43±0.18*7.322 HDL-C 0.78±0.17 0.77±0.16 0.235 0.815 1.31±0.25*0.98±0.17*5.979
3 讨论
2 型糖尿病发病机制为患者机体胰岛素敏感性降低, 胰岛β 细胞功能产生缺陷, 导致机体葡萄糖摄取、 利用率降低, 临床表现为机体代谢紊乱、 消化道功能异常等, 严重影响患者生命健康。 故寻找有效改善胰岛素抵抗的治疗方式尤为重要。
甘精胰岛素通过促进脂肪等周围末梢组织摄取葡萄糖、 抑制肝葡萄糖的产生, 进而有效调节机体糖代谢功能, 可模拟机体生理性胰岛素分泌情况, 降糖效果较好[6]。 二甲双胍作为临床首选治疗药物, 其药理作用是有效抑制肝脏糖生成, 促进肌肉、 脂肪等摄取外周葡萄糖能力, 增强葡萄糖无氧酵解过程,进而提高机体对胰岛素的敏感性, 通过降低肠道对葡萄糖的吸收, 增加外周组织细胞表面胰岛素受体数量, 改善胰岛素抵抗; 该药还可降低机体血脂水平, 增加纤维蛋白溶解, 与胰岛素联合使用可有效减少胰岛素用量, 在降低患者血糖含量的同时不会发生低血糖现象[7-8]。 西格列汀是治疗2 型糖尿病的新型药物, 是一种二肽基肽酶-4 抑制剂, 其药理作用是通过延缓胰高糖素样多肽-1 (GLP-1)、 葡萄糖依赖性促胰岛素分泌多肽(GIP) 的降解, 抑制胰高血糖素分泌, 增加胰岛素分泌, 以葡萄糖依赖方式降低机体血糖水平, 延长肠促胰岛素的活性, 改善胰岛素β 细胞功能, 进而发挥降糖效果[9]; 该药还可增加饭后机体脂类氧化, 减少患者食欲, 进而调节血脂代谢且安全性较高, 低血糖等不良反应较少[10]。 本研究结果显示, 治疗后,观察组的FINS、 HOMA-IR、 TC、 TG、 LDL-C、 FPG 水平低于对照组, HOMA-β、 HDL-C 水平高于对照组, 表明西格列汀联合胰岛素治疗2 型糖尿病效果较二甲双胍联合胰岛素更好。
综上所述, 西格列汀联合胰岛素治疗在改善2 型糖尿病患者胰岛素功能及糖脂代谢方面效果更佳, 值得临床推广。

