Cu(Ⅰ)-新亚铜试剂分光光度法间接测定硫普罗宁肠溶胶囊中硫普罗宁
(嘉应学院 化学与环境学院,梅州 514015)
硫普罗宁化学名称为N-(2-巯基丙酰基)-甘氨酸(结构如图1),是一种含有巯基的甘氨酸衍生物,其主要通过侧链具有游离活性的巯基对肝脏细胞进行保护,临床上广泛用于肝脏疾病的治疗[1]。此外,硫普罗宁还能用于治疗老年早期白内障和玻璃体混浊[2]。但过量服用硫普罗宁会引起胃不适、味觉丧失等不良反应[3]。因此,硫普罗宁含量的测定对于生命科学具有重要意义。
图1 硫普罗宁分子结构Fig.1 Molecular structure of tropronin
目前,测定硫普罗宁含量的标准方法[WS1-(X-054)-2002]为滴定法,其他主要测定方法包括分光光度法[4-6]、高效液相色谱法[7-9]、液相色谱-质谱法[10-11]、气相色谱-质谱法[12]、拉曼光谱法[13]和流动注射光度法[14]等,与分光光度法相比,其他方法可能存在操作复杂、选择性较差或仪器价格昂贵等缺点。
本工作通过试验发现,硫普罗宁中的巯基(-SH)能将Cu2+定量还原为Cu(Ⅰ),而Cu(Ⅰ)能与2,9-二甲基-1,10-二氮菲(新亚铜试剂)形成黄色络合物,通过测定络合物的吸光度可间接测定硫普罗宁的含量,据此建立了Cu(Ⅰ)-新亚铜试剂分光光度法测定硫普罗宁含量的方法,以期为药物中硫普罗宁含量的测定提供技术参考。
1 试验部分
1.1 仪器与试剂
岛津UV-2401 型紫外可见分光光度计;722s型可见分光光度计。
硫普罗宁标准溶液:100.0 mg·L-1,称取0.010 g硫普罗宁(分析纯),用水溶解,转移至100 mL容量瓶中,用水定容,摇匀,置于4 ℃冰箱中避光保存,于48 h内使用。其他所需质量浓度均由此溶液稀释制得,现配现用。
Cu2+溶液:200.0 mg·L-1,称取0.078 6 g五水合硫酸铜于100 mL 的烧杯中,用水溶解,加入3 mol·L-1硫酸溶液2.00 mL,转移至100 mL 容量瓶中,用水稀释至刻度,摇匀。
新亚铜试剂溶液:0.010 0 mol·L-1。
硫普罗宁肠溶胶囊(标示值200 mg·粒-1)。
乙酸-乙酸钠缓冲溶液(pH 4.8)。
所用试剂均为分析纯;试验用水为二次蒸馏水。
1.2 试验方法
取出5粒硫普罗宁肠溶胶囊内的药粉并混合均匀,称取0.2 g,用水溶解并定容至500.0 mL,得到硫普罗宁样品溶液。在25 mL 比色管中加入硫普罗宁样品溶液2.00 mL,再加入0.0100 mol·L-1新亚铜试剂溶液1.00 mL,水10.00 mL,摇匀,加入200.0 mg·L-1Cu2+溶液1.00 mL,p H 4.8的乙酸-乙酸钠缓冲溶液4.00 mL,用水稀释至刻度,摇匀,在室温中放置10 min。
同时做试剂空白。用1 cm 比色皿在分析波长为456 nm 处测量此反应体系的吸光度A,以试剂空白作参比。
2 结果与讨论
2.1 分析波长的选择
以100.0 mg·L-1硫普罗宁标准溶液为分析对象,试验考察了此反应体系在波长为400~600 nm时的吸收曲线,结果见图2。
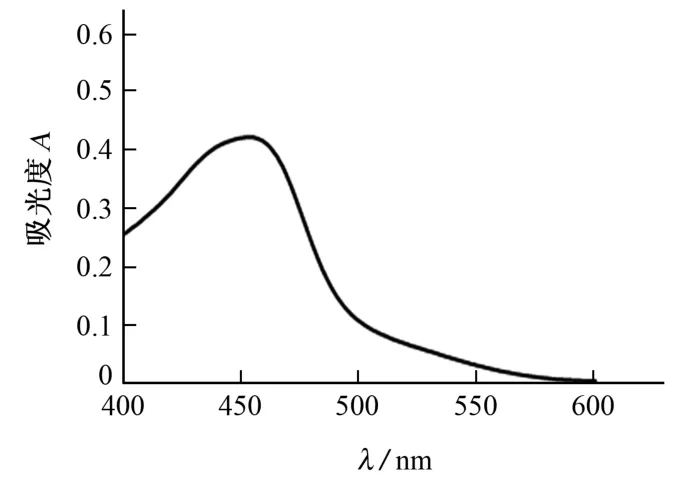
图2 反应体系的吸收曲线Fig.2 Absorption curve of reaction system
由图2 可知,反应体系的最大吸收波长为456 nm,因此,试验选择分析波长为456 nm。
2.2 反应温度的选择
以100.0 mg·L-1硫普罗宁标准溶液为分析对象,试验考察了反应温度分别为20,30,40,50,60,70,80,90 ℃时对反应体系吸光度的影响。结果表明:反应温度为20~80 ℃时,吸光度基本稳定。试验选择反应温度为室温。
2.3 反应时间的选择
以100.0 mg·L-1硫普罗宁标准溶液为分析对象,试验考察了反应时间分别为5,10,20,30,40,50,60,90,120 min 时对反应体系吸光度的影响。结果表明,吸光度在选择的反应时间内基本不变,综合考虑,试验选择反应时间为10 min。
2.4 缓冲溶液酸度的选择
以100.0 mg·L-1硫普罗宁标准溶液为分析对象,试验考察了乙酸-乙酸钠缓冲溶液的pH 分别为3.6,4.0,4.4,4.8,5.0,5.2,5.6时对反应体系吸光度的影响。结果表明,吸光度在pH 为3.6~5.6时基本不变。综合考虑,试验选取缓冲溶液的pH 为4.8。
2.5 缓冲溶液用量的选择
以100.0 mg·L-1硫普罗宁标准溶液为分析对象,试验考察了乙酸-乙酸钠缓冲溶液的用量分别为0.50,1.00,2.00,3.00,4.00,5.00,6.00,7.00,8.00,9.00 mL时对反应体系吸光度的影响。结果表明,吸光度在缓冲溶液用量为3.00~9.00 mL时有较大值且基本不变。综合考虑,试验选取缓冲溶液的用量为4.00 mL。
2.6 Cu2+溶液用量的选择
以100.0 mg·L-1硫普罗宁标准溶液为分析对象,试验考察了Cu2+溶液的用量分别为0.50,1.00,1.20,1.40,1.60,1.80,2.00,2.20,2.40,2.60 mL时 对反应体系吸光度的影响。结果表明,吸光度在所选择的Cu2+溶液用量范围内基本不变。综合考虑,试验选择Cu2+溶液的用量为1.00 mL。
2.7 新亚铜试剂溶液用量的选择
以100.0 mg·L-1硫普罗宁标准溶液为分析对象,试验考察了新亚铜试剂溶液用量分别为0.20,0.40,0.60,0.80,1.00,1.20,1.40,1.60,1.80,2.00 mL时对反应体系吸光度的影响,结果见图3。
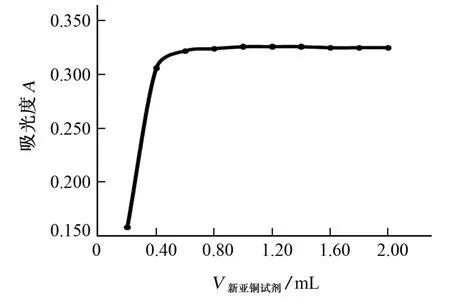
图3 新亚铜试剂溶液用量对吸光度的影响Fig.3 Effect of amount of neocuproine solution on absorbance
由图3可知:反应体系吸光度在新亚铜试剂溶液用量为0.60~2.00 mL 时基本不变。综合考虑,试验选择新亚铜试剂溶液用量为1.00 mL。
2.8 共存物质的影响
选取了对本方法可能造成干扰的葡萄糖、蔗糖、D-果糖、L-谷氨酸、DL-苹果酸、L-丝氨酸、L-腈氨酸、L-精氨酸、D-甘露醇、淀粉、乳糖等11种物质进行试验,相对误差需控制在±5% 以内。以100.0 mg·L-1硫普罗宁标准溶液为分析对象,试验考察了以上11种共存物质对反应体系吸光度的影响。结果表明:1 000倍的葡萄糖、蔗糖、D-果糖、L-谷氨酸、DL-苹果酸、L-丝氨酸、L-腈氨酸,100倍的L-精氨酸、D-甘露醇,200倍的淀粉,500倍的乳糖对硫普罗宁的测定无干扰。
2.9 标准曲线和检出限
按照试验方法对0.800 0,1.600,2.400,3.200,4.000,4.800,5.600,6.400,7.200,8.000,8.800,9.600,10.40,11.20,12.00,12.80,13.60,14.40,15.20,16.00,16.80,17.60,18.40,19.20,20.00 mg·L-1标准溶液系列进行测定,以硫普罗宁的质量浓度为横坐标,其对应的吸光度为纵坐标绘制标准曲线。硫普罗宁的质量浓度在0.800 0~20.00 mg·L-1内符合朗伯-比尔定律,摩尔吸光系数(ε)为8.7×103L·mol-1·cm-1,线性回归方程为y=0.042 01x+0.005 4,相关系数0.999 8。
按照试验方法对试剂空白进行11次平行测定,以3倍测定值的标准偏差(s)和标准曲线斜率(k)的比值计算得检出限(3s/k),以10s/k计算测定下限,检出限和测定下限分别为0.057,0.19 mg·L-1。
2.10 精密度和准确度试验
按照试验方法测定硫普罗宁肠溶胶囊中硫普罗宁的含量,平行测定5 次,平均测定值为200.31 mg·粒-1,与标示值(200 mg·粒-1)相符,且与国家药品标准方法[WS1-(X-054)-2002]分析结果(198.05 mg·粒-1)结果基本吻合;测定值的相对标准偏差(RSD)为0.20%。
2.11 回收试验
按照试验方法对硫普罗宁肠溶胶囊进行加标回收试验,并计算回收率,结果见表1。
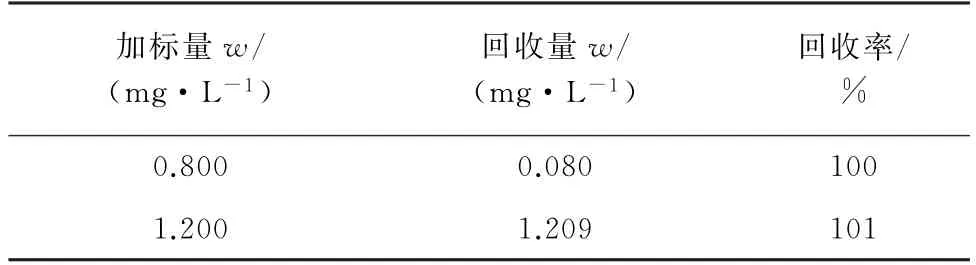
表1 回收试验结果Tab.1 Results of test for recovery
本工作建立了Cu(Ⅰ)-新亚铜试剂光度法测定硫普罗宁肠溶胶囊中硫普罗宁含量的方法,该方法设备简单、样品无需特殊前处理,操作便捷、灵敏度高、选择性好,其测定结果与标准方法的相近,具有一定的实用价值。
致谢:本工作是在嘉应学院化学与环境学院温欣荣老师指导下完成的,在此深表谢意。

