依帕司他对糖尿病周围神经病变患者血清胱抑素C及多伦多临床评分系统的影响
彭少林 杨水冰 沙永红 杨井金 陆小玉 张玲 杨娇娇 唐维 岳成思 杨康 向建平 刘莉 张美彪
(1怀化市第一人民医院内分泌代谢科 国家代谢性疾病临床医学研究中心怀化分中心,湖南 怀化 418000;2吉首大学医学院)
糖尿病周围神经病变(DPN)是一特异的糖尿病微血管并发症,容易造成神经结构改变及功能障碍进而产生麻痛、发凉、感觉减退等临床症状体征。据文献报道,存在10%~20%的糖尿病患者在就诊之初就已然发生了DPN,在糖尿病确诊后的5年、10年、20年,DPN发生率为30%~90%〔1〕。鉴于DPN的发病率高且隐匿性强,如果不够重视其影响或者采取的诊疗疗措施不适当,则有可能产生严重感觉缺失、疼痛、溃疡及感染等并发症,进而导致机体损伤,最终发生截肢致残风险〔2〕。DPN发病机制复杂,严格控制血糖是其治疗前提,基于多种靶点的降糖药物出现为DPN的治疗提供了新武器。依帕司他是一种抑制DPN发病机制中醛糖还原酶的药物,在DPN治疗中有较好的疗效及安全性。研究发现胱抑素(Cys)C为DPN的潜在血清生物标志物〔3,4〕。目前关于依帕司他对DPN的研究绝大部分涉及其神经传导速度等方面影响,较少与CysC联系。本研究旨在探讨依帕司他治疗DPN患者前后血清CysC与多伦多临床评分系统(TCSS)变化,推测其可能的机制及疗效。
1 资料与方法
1.1基本资料 2016年4月至2017年4月就诊于怀化市第一人民医院住院的2型糖尿病患者105例,区组随机化分为单药治疗组(E组)、联合治疗组(EM组)、甲钴胺对照组(M组)各35例。参与研究的入组者均符合WHO 1999年中关于糖尿病的诊断标准及2017版糖尿病防治指南中有关DPN诊断标准〔5〕。排除标准:①伴有脑卒中等脑血管疾病后遗症及颈腰椎疾病;②存在格林巴利综合征;③存在心、肝、肾功能严重受损;④存在静脉栓塞、淋巴管炎在内的严重动静脉血管性疾病;⑤妊娠期、恶性肿瘤、药物试验过敏者;⑥近期(1个月内)有使用或正在使用甲钴胺、依帕司他、大剂量糖皮质激素;⑦存在精神状态异常、行为反常不能进行该项研究者及未履行签署知情同意书。该项研究获得医院伦理委员会的审批,所有入组者由本人或其法定代理人见证下签署知情同意书。治疗12 w后进行随访,删除失访数据并完善补充其他数据资料后最终得到E组33例(男19例,女14例),EM组30例(男12例,女18例),M组34例(男21例,女13例)。三组基线资料无统计学差异(P>0.05)。见表1。
1.2干预方法 基础治疗:入组的研究对象均根据《中国2型糖尿病防治指南》进行生活方式干预(包括糖尿病饮食及运动),同时平稳降糖(口服降糖药物或者胰岛素,入组之前和之后方案基本不变),调控血脂药物基本一致(入组之前和之后方案基本不变)。
E组:基线治疗措施+依帕司他片(商品名称唐林,由扬子江药业集团南京海陵药业有限公司生产,批准文号是国药准字H20040840)50 mg/次,3次/d。EM组:基础治疗措施+依帕司他片(用法同E组依帕司他用法)+口服甲钴胺片(商品名称奇信,由扬子江药业集团南京海陵药业有限公司生产,批准文号是国药准字H20052325)0.5 mg/次,3次/d。M组:基线治疗措施+甲钴胺片(用法同EM组甲钴胺用法)。整个治疗周期为12 w。

表1 3组基线资料水平比较
1.3监测项目及指标 一般临床资料:包括年龄、性别、身高、体重、体重指数、血压、糖尿病病程等。
生化指标检测:前日夜间禁食至少8 h,次日清晨空腹抽取肘静脉血3 ml送至检验科专用生化检测仪器检测血糖(包括空腹及餐后2 h)、糖化血红蛋白、肝功能、肾功能、血脂、CysC等。
神经症状与体征评分:所有研究入组患者采用多伦多临床评分系统(TCSS)〔6〕评估DPN患者的临床症状与体征,由专人登记每一名入组者治疗前后各相关指标数据并汇总。
1.4统计学方法 采用SPSS21.0软件进行方差分析,LSD-t检验及χ2检验。
2 结 果
2.1各组治疗前后血糖控制情况 治疗后3组空腹血糖、餐后2 h血糖、糖化血红蛋白均有不同幅度降低,但均无统计学差异(P>0.05)。见表2。

表2 3组治疗前后血糖控制情况比较
2.2各组CysC水平比较 组内比较,3组治疗前后CysC浓度有统计学差异(P<0.05,P<0.01)。E、EM组治疗后CysC水平较M组明显降低(P<0.05),EM组治疗后CysC较E组下降更明显(P<0.05)。见表3。
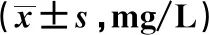
表3 3组治疗前后血清CysC水平变化
2.3各组TCSS变化情况比较 治疗前各组TCSS评分无统计学差异(P>0.05)。组内比较,M组治疗后TCSS评分较治疗前下降,但差异无统计学意义(P>0.05);E、EM组治疗前后TCSS评分差异有统计学意义(P<0.05,P<0.001)。治疗后EM组较其余两组TCSS评分显著下降(P<0.001)。见表4。
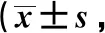
表4 3组治疗前后TCSS评分情况分)
3 讨 论
神经细胞为一永久性细胞,一旦发生损伤则难以进行修复,轻者产生感觉异常等症状,重者发生永久性坏死。DPN的发病具体机制牵涉多种通路,彼此间相互制约联系且较为复杂,一旦发生DPN临床上仅能改善相关症状及体征,难以真正逆转损伤,且目前尚缺乏特效治疗手段。醛糖还原酶(AR)是多元醇通路中催化反应速度最慢的一种酶,高血糖时,AR在人体内极为活跃的接受还原型辅酶Ⅱ提供的氢元素,形成新的化合物后将体内葡萄糖进一步转化成山梨醇,过度激活多元醇通路,造成山梨醇产生过多堆积;此外上述过程中可导致体内肌醇过多消耗、过度氧化应激等,致使神经元细胞的神经结构及功能发生变化导致神经损伤〔7〕。依帕司他为一种AR抑制剂,研究发现其可与AR结合并抑制其活性,这一过程是可逆的、非竞争性的;当其抑制上述酶的活性后,葡萄糖向山梨醇转化过程受到影响,使得山梨醇生成量减少,从而抑制多元醇通路的激活,减轻氧化应激反应,控制细胞炎性反应与程序性死亡,改善微循环障碍,调节能量代谢的失衡,提高钠-钾-三磷酸腺苷(ATP)酶活性,有利于神经组织的损伤修复〔7,8〕。国内的一项多中心研究也显示〔9〕,依帕司他不仅能改善DPN患者麻木、疼痛等临床症状,还能修复神经损伤进而提高神经传导速度〔10,11〕。本研究结果与李平等〔9〕研究结论一致。
CysC是一种微小的小分子蛋白,由120个氨基酸肽链组成,约13 kD,Anastasi团队发现其是一种半胱氨酸蛋白酶可逆性的竞争抑制剂,在细胞内蛋白质和多肽的分解代谢中起重要作用。研究发现〔12~14〕,CysC可作为糖尿病诊断后用于监测神经病变发生的危险因子。CysC是一种内源性半胱氨酸蛋白酶的抑制剂,在体内适宜条件下能够抑制蛋氨酸合成酶等酶的活性,造成分解同型半胱氨酸的代谢过程受阻,使得同型半胱氨酸蓄积,进而导致微血管的内皮细胞受损,同时同型半胱氨酸还可以抑制舒血管物质一氧化氮的合成,使微血管血流减少从而导致神经纤维缺血损伤〔15,16〕。本研究提示联合治疗对CysC影响更大,推测可能机制为依帕司他减轻氧化应激和抑制多酚通路来降低CysC水平。此外,有研究表明CysC还可以激活体内单核/巨噬细胞等炎性细胞产生炎症因子发生炎症反应,血管平滑肌增殖,血管内皮细胞功能受损发生微血管病变引起DPN〔17〕;此外,高水平的CysC可扰乱体内凝血-纤溶系统、损伤血管内皮细胞导致产生DPN〔8〕。研究发现依帕司他能通过抑制蛋白激酶通路上调内皮细胞一氧化氮的产生〔7〕。因此,依帕司他亦可能通过上述机制降低CysC产生。
综上,依帕司他可能通过降低氧化应激反应、控制细胞炎性反应、改善微循环障碍等作用机制来降低DPN患者血清CysC水平。本研究也存在以下不足:该研究推测依帕司他可能通过降低氧化应激反应等来降低CysC水平,但未就具体氧化应激指标(如超氧化物歧化酶等)、内皮细胞功能相关指标(如一氧化氮等)进行检测,下一步需完善。因此,本研究提示依帕司他联合甲钴胺治疗方案降低TCSS评分的作用非常明显,能够显著减缓DPN患者临床症状。由于本研究样本数量偏少,观察周期较短,还需大样本、长时间观察随访。

