新型稀土钙钛矿型复合氧化物LaSrFeNiO6的制备及络合剂对其晶体尺度和催化性能的影响
胡译文,陈晓宇,彭俊峰,郑建东
(滁州学院 材料与化学工程学院,安徽 滁州 239000)
随着现代工业的快速发展,石油、煤炭等矿物燃料燃烧过程的污染问题,激发了人们对新能源的研究兴趣。天然气作为一种低成本的清洁能源,逐渐成为矿物燃料的理想替代品。然而天然气的主要成分甲烷,其火焰燃烧温度通常在1300 ℃以上,易导致大量的NOx排放以及热损失,同时未燃烧充分的甲烷将加剧温室效应。与传统火焰燃烧相比,催化燃烧能够保证甲烷在较低温度下高效氧化,具有较高的能量转化效率、能较好地抑制污染物排放[1-4]。
针对甲烷催化燃烧,贵金属与其氧化物催化剂在低温、低浓度下显示出高催化活性,但贵金属价格昂贵,且会由于烧结,分解或与载体的不良相互作用而失活[5]。钙钛矿型复合氧化物因具有灵活的组分以及可调节的氧化还原能力,成为最有潜力的甲烷燃烧催化剂之一。甲烷在钙钛矿上的氧化活性与氧气利用率相关,受比表面积制约。钙钛矿较高的结晶温度通常会导致较低的比表面积,限制了催化活性[6]。本课题组[7]曾以柠檬酸为络合剂,采用溶胶-凝胶法制备了钙钛矿型催化剂LaSrFeNiO6,其T10%=370 ℃,T90%=535 ℃,催化活性良好。但其比表面积较小,仅7.9 m2·g-1,催化活性受到了限制。王曼[8]用溶胶-凝胶-水热联用法制备了钙钛矿型催化剂,并发现水热处理会使催化剂孔径分布更加多元化,晶体尺寸变小,比表面积增大,从而达到提高催化活性的目的。
采用溶胶凝胶-水热联用法制备了新型稀土钙钛矿型复合氧化物LaSrFeNiO6,其结构经XRD、SEM、BET、H2-TPR和TG-DSC表征。并研究了不同络合剂(EDTA、柠檬酸、EDTA-柠檬酸)对钙钛矿氧化物纳微结构及其催化甲烷燃烧活性的影响。
1 实验部分
1.1 仪器与试剂
Bruker D8 Advance型X-射线衍射仪;JSM-6510LV型扫描电子显微镜;Micromeritics Gemini V 2380型物理吸附仪;TP-5080型全自动多用吸附仪;TA SDT-Q600型同步热分析仪。
La(NO3)3·6H2O(山东西亚化学股份有限公司),Sr(NO3)2(国药集团化学试剂有限公司),Fe(NO3)2·9H2O(上海强顺化学试剂有限公司),Ni(NO3)2·6H2O(西陇化工股份有限公司),C6H8O7·H2O(国药集团化学试剂有限公司),C10H16N2O8(天津博迪化工股份有限公司),分析纯,实验用水为自制去离子水;其余所用试剂均为分析纯。
1.2 催化剂的制备(以1倍EDTA为例)
按照化学计量比称量,在烧杯中加入La(NO3)3·6H2O、Sr(NO3)2、Fe(NO3)2·9H2O、Ni(NO3)2·6H2O和适量去离子水,搅拌下于70 ℃加入EDTA,反应1h。移入烘箱,于120 ℃干燥12 h。研磨后置于坩埚中,放入马弗炉中以3 ℃·min-1升温至500 ℃和800 ℃,保温3 h。冷却至室温,取2 g样品放置于内衬聚四氟乙烯的高压反应釜中,加入适量去离子水,于180 ℃反应4 h。抽滤,滤饼烘干,研磨,放入马弗炉中以3 ℃·min-1升温至600 ℃,保温1 h。冷却至室温,研磨、压片,筛分备用。
用类似的方法制得络合剂用量为2倍EDTA、1倍柠檬酸、2倍柠檬酸、1倍EDTA+1倍柠檬酸的催化剂。
1.3 催化剂的活性测试
催化活性测试在常压、微型反应实验装置中进行。反应器为石英管固定床反应器,直径为10 mm,催化剂用量为500 mg,催化剂床层高10~15 mm。反应气体由空气99%和甲烷1%(体积百分比)组成。以空速50000 h-1通入反应气体后,5 ℃·min-1程序升温,检测催化剂300 ℃至反应完全温度(反应转化率达99%时的温度)时的催化活性。以甲烷转化率为10%和90%时对应的反应温度T10%和T90%表示甲烷催化燃烧的起燃温度和完全转化温度。
2 结果与讨论
2.1 XRD
图1为系列催化剂的XRD谱图。当0.75≤t≤1时,可形成稳定钙钛矿结构[9]。由图1可见,所有催化剂均在2θ=25°、32°、40°、47°、58°附近出现了钙钛矿的特征衍射峰,都可以形成钙钛矿晶型[10]。且除1倍柠檬酸样品外,其余均形成了单一的钙钛矿晶型。在1倍柠檬酸样品的谱图中,出现了杂峰,并且出现了主峰劈裂双峰的现象,经软件分析是碳酸锶的衍射峰,这可以解释为:当柠檬酸量较少时,无法与金属氧化物完全络合,此时溶胶体系的络合网络不均匀且分散性较差,从而使体系中的金属离子含量较多,导致了杂峰的生成。采用Scherrer公式计算出各个样品粒径的平均值[10],结果如表1所示。

2θ/(°)图1 系列催化剂的X-射线衍射分析谱图Figure 1 XRD spectrum of a series of catalysts

表1 系列催化剂的粒径Table 1 Particle size of series catalyst
可以看出,随着柠檬酸量的增大,衍射峰强度变弱,位置无明显移动,样品粒径减小。这是因为在焙烧过程中,大量的柠檬酸将会剧烈燃烧,产生的CO2和水蒸气气流将阻碍了颗粒间的团聚,使体系更加分散,同时催化剂中金属离子的含量较少,导致粒径减小[11]。由于EDTA可以在催化剂表面形成吸附界面膜,能够降低表面张力及胶粒间的引力,从而阻止颗粒间的团聚[12]。从而使得1倍EDTA样品的粒径小于1倍柠檬酸样品的粒径。但随着EDTA量的增大,样品的粒径也在增大,这说明过量的EDTA反而会限制颗粒分子的运动,使其发生定向团聚现象。由此可见,EDTA的加入量也是反应中需要斟酌的一个因素。而1倍EDTA+1倍柠檬酸样品的峰形最尖锐,且粒径也较小,这说明当EDTA与柠檬酸联合作为络合剂时,有效促进了钙钛矿氧化物完整晶型的生成,且联合络合剂表现出协同作用,一定程度上提高了体系的分散程度。

2.2 SEM
为比较用溶胶-凝胶法1倍EDTA+1倍柠檬酸联合作为络合剂制备催化剂。SEM图像如图2所示(其中a为以1倍EDTA+1倍柠檬酸联合作为络合剂,溶胶-凝胶法制得催化剂的SEM,b为以1倍EDTA+1倍柠檬酸联合作为络合剂时,溶胶-凝胶-水热联用法制得催化剂的SEM)。可以看出:样品表面粗糙,都为不规则状形貌,且颗粒大小差别较大,部分颗粒间发生团聚现象。这是EDTA与柠檬酸对于金属离子络合能力的不同而导致的。通常在反应过程中,金属离子与柠檬酸的络合是分步进行的:首先金属离子先与OH-反应生成沉淀,随后柠檬酸与沉淀物发生络合反应生成络合物,而金属离子与EDTA络合反应快速、完整、无累积可以一步络合。故当它们联合作为络合剂时,会出现反应速率差,因此在溶胶-凝胶过程中金属离子的络合分布以及后续的晶体生长过程都是不均匀的,从而导致了最终形成的颗粒大小不一、且发生一定程度团聚的现象[13-14]。对比a,b两图,可以看出a图中颗粒尺寸明显大于b图中颗粒尺寸,这是因为在水热处理时,部分金属离子会溶解,然后在高压反应釜中二次长晶,从而使体系的结晶度增大,晶粒尺寸减小。

图2 系列催化剂的扫描电镜图Figure 2 SEM spectra of a series of catalysts
2.3 BET
表2为比表面积测定结果。由表2可以看出,采用溶胶-凝胶-水热联用法后,除1倍柠檬酸样品外,其余4组样品的比表面积均较文献[7]制备的LaSrFeNiO6催化剂比表面积(仅为7.9 m2·g-1)、有所提升。这是因为在水热处理过程中,晶粒团聚体发生松散,部分金属离子再次溶解,经过对流、吸附、分解、脱附等过程重新结晶,从而使晶核变小,比表面积也随之变大[8,15]。2倍柠檬酸样品的比表面积大于1倍柠檬酸样品的比表面积,这与络合时前驱体凝胶分子的结构有关。当柠檬酸量较多时,前驱体凝胶分子呈平面网状,焙烧时能够充分燃烧,从而制得的样品具有较大的比表面积[16]。2倍EDTA样品的比表面积大于1倍EDTA样品的比表面积,这是因为EDTA的加入会与处于B位的Fe3+、Ni2+形成络合物,提高了体系的分散性,且在一定范围内这种分散性与EDTA的增加量成正比。同时我们观察到,以EDTA为络合剂制备的催化剂的比表面积总大于以柠檬酸为络合剂制备的催化剂,这是因为EDTA与金属离子络合形成笼型配合物,且比例为1/1,这将有效地消除各种离子之间的差异,并有助于金属离子在前驱体中的分子水平混合。以1倍EDTA+1倍柠檬酸为联合络合剂所制得的样品,与加入相同量络合剂的样品(2倍EDTA、2倍柠檬酸)相比,其比表面积最大,这是因为,在联合络合剂与金属离子络合过程中,金属离子与EDTA形成主要络合物。另一方面,柠檬酸结构中的羟基基团将使得柠檬酸与EDTA间发生聚合反应,金属离子与柠檬酸之间的二次络合作用和酸之间的聚合作用可使金属-EDTA络合物固定,并通过均匀分散金属-EDTA络合物,可有效保持金属离子的分子水平混合,从而提高体系分散度、均匀度,使比表面积达到最大化[17]。

表2 系列催化剂的比表面积Table 2 Specific surface area of series catalysts
2.4 H2-TPR
图3为H2-TPR谱图。由图3可见,在H2-TPR的条件下,通常A位金属离子难以被还原,因此TPR谱图中显示H2消耗峰是由B位金属离子的还原而产生的。以330~370 ℃为中心的低温还原峰可能是Ni3+→Ni2+的还原,低温还原峰温度越低,反应越容易进行,氧缺位结构越容易产生[18,19]。以470~525 ℃为中心的宽的还原峰是可能是Fe4+→Fe3+以及Ni2+→Ni0的还原,Fe4+的产生是因为Sr掺入,使Fe3+转化为Fe4+。650 ℃之后的高温还原峰可能是Fe3+的深度还原产生的[19]。随着柠檬酸量的增加,低温还原峰稍有前移且峰面积有所增加,说明在柠檬酸在焙烧过程中燃烧分解产生的碳物种可以还原金属离子,使得样品的还原能力提高[16]。2倍EDTA、1倍EDTA+1倍柠檬酸样品的高温还原温度较低,且还原峰面积较大,这表明此时催化剂中金属和氧结合的能力较弱,可以提供更多的活性氧用于氧化反应,表现出优异的甲烷燃烧反应活性[10,20]。

Temperature/℃图3 系列催化剂的H2-TPR曲线Figure 3 H2-TPR spectra of a series of catalysts
2.5 TG-DSC
图4为1倍EDTA+1倍柠檬酸样品在焙烧前干胶前驱体的TG-DSC曲线。
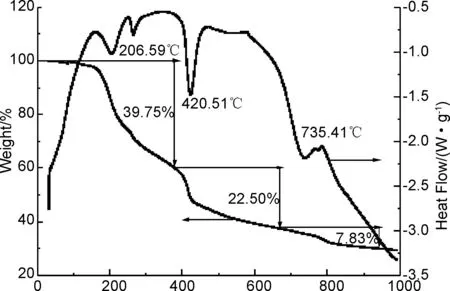
Temperature/℃图4 1倍EDTA+1倍柠檬酸样品干胶前驱体的TG-DSC曲线Figure 4 TG-DSC curve of dry gel precursor of 1EDTA +1citric acid sample
在50~380 ℃,干胶前驱体共减少了39.75%的重量,这是前驱体表面游离态水分的逸出和EDTA、柠檬酸及其盐分子结合水的脱除以及EDTA和柠檬酸的燃烧氧化分解产生的,对应DSC曲线上的几个吸热峰。380~670 ℃共减少了22.50%的重量,其中380~430 ℃的失重比较迅速,这是金属碳酸盐的剧烈分解,对应DSC曲线上420.51 ℃的强吸热峰;430~670 ℃的失重主要是在形成钙钛矿结构的过程中,各种化合物相互作用失去氧的重量。DSC曲线在735.41 ℃有一弱吸热峰,但之后在TG曲线上已无明显失重现象出现,说明相变过程以接近尾声,钙钛矿晶型以渐形成[21]。
2.6 催化性能
(1) 催化甲烷燃烧性能
催化剂活性测试结果如图5和表3所示。文献[7]以溶胶-凝胶法制备的LaSrFeNiO6催化剂的完全转化温度为535 ℃。从表5中可以看出,除1倍柠檬酸样品外,其余四组催化剂的完全转化温度均有不同程度的降低,其中1倍EDTA+1倍柠檬酸样品的催化活性最好,完全转化温度为494℃。而2倍EDTA、1倍EDTA、2倍柠檬酸样品的完全转化温度分别为506 ℃、509 ℃、516 ℃,催化活性也有一定的提高。这是因为本实验较之前多了一步水热处理过程,而水热处理伴随着溶吸-解吸可以使晶体二次生长,从而使晶粒尺寸变小,比表面积增加,从而提高了催化活性。H2-TPR结果表明:1倍EDTA+1倍柠檬酸和2倍EDTA样品的低温还原峰面积较大,说明它们在低温下的氧缺位较易吸附氧并使之成为活性氧,在燃烧反应过程中,活性氧的消耗与再生与处于B位的Fe、Ni离子的化合价变化同时发生,形成催化氧化循环[22],从而有效提高催化活性。

Temperature/℃图5 系列催化剂的催化活性曲线Figure 5 Catalytic activity curves of series catalysts

表3 系列催化剂活性与表面活化能数据Table 3 Catalytic activities and surface activation of catalysts
(2) 催化反应活化能
甲烷催化燃烧反应可以按照准一级反应去计算反应的表观活化能。根据计算公式得到表观活化能,结果如图6、表3所示。将活化能的大小排序,得Ea(1倍柠檬酸)>Ea(2倍柠檬酸)>Ea(1倍EDTA)>Ea(2倍EDTA)>Ea(1倍EDTA+1倍柠檬酸)可以看出,活化能的下降趋势与催化活性相匹配,即活化能越小,催化活性越好。1倍EDTA+1倍柠檬酸样品的活化能最低,为78.41 kJ·mol-1,催化活性最好,T10%=382 ℃、T90%=494 ℃。
通过溶胶-凝胶-水热联用法,采用不同络合剂(EDTA、柠檬酸、EDTA-柠檬酸)制备了系列LaSrFeNiO6复合氧化物催化剂,XRD分析表明,在马弗炉中经过500 ℃、600 ℃和800 ℃煅烧后,均形成了钙钛矿晶型结构;水热处理过程中部分金属离子重新溶解并经过对流、吸附、分解、脱附等过程重新结晶,可以提高体系的结晶度,降低晶粒尺寸,增大晶体比表面积,并改善催化活性;由于金属离子与柠檬酸之间的二次螯合作用和酸之间的聚合作用,EDTA与柠檬酸共同作为络合剂时有协同作用。与单一络合剂所制备的催化剂相比,其比表面积最大(24.4 m2·g-1)、催化活性最好、反应活化能也最小,其中起燃温度382 ℃,完全转化温度494 ℃,反应活化能78.41 kJ·mol-1。

