白蛋白结合型紫杉醇联合奈达铂一线治疗晚期食管癌患者的临床观察
海军军医大学附属长海医院肿瘤科,上海 200433
中国食管癌的发病率及死亡率占全球一半以上,不同于欧美国家,中国90%以上食管癌病理学类型为鳞状细胞癌,而欧美国家50%为腺癌[1-2]。近年来,随着新药的发展,中国晚期食管癌的治疗取得了一些进步,但预后总体较差,长期生存率较低,其治疗仍是个难题。目前食管癌常用的治疗方案是氟尿嘧啶联合顺铂,其疗效一般且不良反应较大,因此亟待探索更有效的治疗方案。白蛋白结合型紫杉醇和奈达铂均为第三代紫杉类和铂类化疗药,具有高效低毒的临床特性,新近研究显示其对鳞癌更具有优势[3-4]。据此,我们回顾性分析海军军医大学附属长海医院2016年2月—2019年2月收治的晚期食管鳞癌31例患者经一线白蛋白结合型紫杉醇联合奈达铂方案化疗的疗效及耐受情况。
1 资料和方法
1.1 临床资料
收集海军军医大学附属长海医院肿瘤科2016年2月—2019年2月采用白蛋白结合型紫杉醇联合奈达铂一线治疗31例晚期食管鳞癌患者的临床资料。其中男性23例,女性8例;年龄45~75岁,中位年龄62岁;术后复发转移19例,发现时已经有远处转移12例。所有患者均符合以下标准:①经病理学检查明确为食管鳞状细胞癌;② 至少有一处可经影像学评估测量的病灶;③既往未进行过化疗或距离术后辅助化疗时间超过6个月。④ PS评分为0~1分;⑤ 预计生存期≥3个月;⑥ 治疗前血常规及肝肾功能基本正常,无化疗禁忌证。
1.2 治疗方案
白蛋白结合型紫杉醇130 mg/m2,第1、8天,静脉滴注30 min;奈达铂70 mg/m2,第1天,静脉滴注60 min以上;每21 d为1个周期。用药至疾病进展或毒性不能耐受,最多治疗8个周期,联合治疗周期结束后疗效达稳定以上的患者给予替吉奥单药(40~60 mg,口服,每日2次,第1~14天,每3周重复)维持治疗。化疗过程中予以止吐、保肝等支持治疗。每次化疗前后复查血常规及肝肾功能,若发生3/4级骨髓抑制,立即予以粒细胞集落刺激因子(granulocytecolony stimulating factor,G-CSF)等支持治疗;若出现4级不良反应则下个周期用药剂量减少20%~25%。
1.3 疗效和不良反应评估
所有患者每2个周期进行影像学检查,疗效评估采用实体瘤疗效评价标准(Response Evaluation Criteria in Solid Tumors,RECIST)1.1标准,分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD)。客观缓解率(objective response rate,ORR)为CR+PR病例占可评价病例的百分数,CR或PR患者需经4周后再证实;疾病控制率(disease control rate,DCR)为CR+PR+SD病例占可评价病例的百分数。无进展生存期(progression-free survival,PFS)定义为本方案化疗开始至出现疾病进展时间。按美国国立癌症研究所通用毒性标准(National Cancer Institute Common Toxicity Criteria,NCI-CTC)5.0评估不良反应,常见不良反应分为5级。
1.4 统计学处理
采用SPSS 22.0统计软件对数据进行统计分析。P<0.05为差异有统计学意义。
2 结果
2.1 疗效
31例患者最少用药周期为2个周期,最多用药8个周期,累计完成184个周期,平均每例患者接受化疗5.9个周期。所有患者均可评价客观疗效,其中CR为1例(3.2%),PR为20例(64.5%),SD为9例(29.0%),PD为1例(3.2%),ORR为67.7%,DCR为96.8%,中位PFS为9.4个月(表1)。
2.2 不良反应
本方案主要的不良反应包括骨髓抑制、感觉神经异常、关节/肌肉酸痛、消化道反应、肝功能异常及脱发,大部分患者经对症及支持治疗后均能按计划完成化疗。其中发生的3级不良反应有中性粒细胞下降、血小板下降、感觉神经病变和关节肌肉酸痛;有1例患者因3级血小板降低和自身意愿将奈达铂减量至原剂量的80%;有1例患者在行第4个周期治疗滴注奈达铂55 min时出现过敏反应停用奈达铂;无白细胞水平降低性发热和化疗相关死亡病例。其他不良反应如肝功异常、恶心、呕吐、乏力等,多为1~2级,经及时对症治疗后症状均可缓解(表2)。

表1 患者临床特征及疗效Tab.1 Clinical characteristics and efficacy
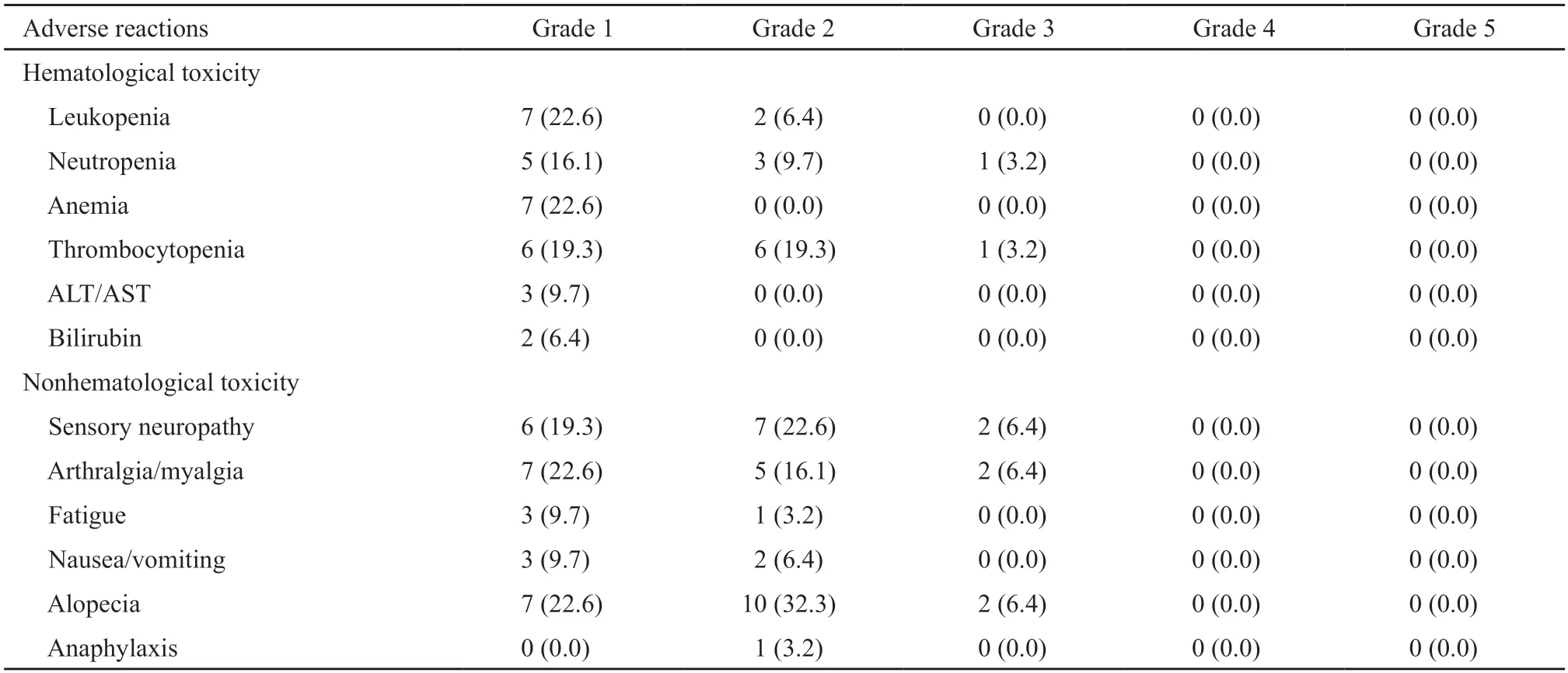
表2 白蛋白结合型紫杉醇联合奈达铂治疗晚期食管癌的不良反应Tab.2 Adverse reaction of albumin-bound paclitaxel plus nedaplatin in advanced ESCC n(%)
3 讨 论
晚期食管癌预后较差,5年生存率小于10%,中位生存期一般只有7~12个月[2]。目前已有诸多的临床试验证实,与最佳支持治疗相比,化疗可明显延长晚期食管癌患者的生存期,提高生活质量[3]。国内外指南推荐的方案是氟尿嘧啶类药物/紫杉类药物联合铂类药物。然而,对晚期食管癌患者,其一般情况多数较差,PS评分多在1~2分,如何进行治疗方案的优化,提高患者的耐受性并改善其生活质量,目前尚缺乏大规模临床研究。
白蛋白结合型紫杉醇是将紫杉醇与白蛋白结合而成的新型化疗药物,与传统的溶剂型紫杉醇相比,白蛋白结合型紫杉醇疗效更高且不良反应减轻,并具有良好的可溶性,用药前无需给予抗组胺药,应用更加便捷。奈达铂(顺式二胺乙醇酸铂)是铂类药物衍生物,以与顺铂相同的方式与DNA结合,抑制DNA复制,显示出与顺铂相似的抗肿瘤活性,但其对肾脏和胃肠道的毒性较小。临床研究显示,紫杉醇联合奈达铂对晚期食管癌的ORR为41.7%~43.6%,与基于顺铂的方案相比,基于奈达铂的方案具有相当的疗效,但却有更低的毒性和更好的耐受性[5-6]。
Wang等[7]回顾分析应用纳米白蛋白结合型紫杉醇联合顺铂(nab-TP组)对比溶剂型紫杉醇联合顺铂(sb-TP组)一线治疗晚期食管鳞癌患者的疗效和安全性,结果显示,nab-TP组对比sb-TP组的ORR为50%vs30%,DCR为81%vs65%,中位PFS为6.1个月vs5.0个月,中位OS为12.5个月vs10.7个月。两组中最常见的不良反应包括贫血、白细胞减少、中性粒细胞减少、发热性中性粒细胞减少和血小板减少症。而He等[18]报告了紫杉醇联合奈达铂一线治疗晚期食管鳞癌疗效和安全性的Ⅱ期研究,该研究结果显示,在36例可评估疗效的患者中,有2例(5.1%)CR,16例(41.0%)PR,ORR为46.1%,所有患者的中位PFS和中位OS分别为7.1个月和12.4个月,3/4级毒性包括中性粒细胞减少症(15.4%)、恶心(10.3%)、贫血(7.7%)、血小板减少症(5.1%)、呕吐(5.1%)和中性粒细胞减少症(2.6%)。
本研究结果显示,该方案的ORR为67.7%,DCR为96.8%,中位PFS为9.4个月。进一步对不同亚组患者进行分析,发现食管下段、术后复发转移、仅一处器官转移及肿瘤生物标志物鳞状上皮细胞癌抗原(squamous cell carcinoma antigen,SCC-Ag)正常的患者PFS较长。主要的3/4级血液学毒性包括中性粒细胞减少(3.2%)、血小板减少(3.2%);3/4级非血液学毒性主要为感觉神经毒性(6.4%)、关节肌肉酸痛(6.4%)和脱发(9.7%);有1例患者输注奈达铂时出现过敏反应停用奈达铂;未出现因不良反应停止治疗及相关死亡患者。我们的研究结果显示,白蛋白结合型紫杉醇联合奈达铂一线治疗晚期食管鳞癌的有效率及不良反应均优于Wang等[9]和He等[10]的研究,这可能与我们研究中患者PS评分均为0~1分、患者后续行替吉奥单药维持治疗、白蛋白结合型紫杉醇采用每周给药以及奈达铂剂量降低有关。
综上所述,白蛋白结合型紫杉醇联合奈达铂一线治疗晚期食管鳞癌具有较好的疗效,且不良反应可耐受,安全性较好。本研究样本量较小,有待通过进一步前瞻性随机对照研究进行分析。

