输尿管软镜与经皮肾镜治疗肾结石的效果比较
张佳铖,于德新
(安徽医科大学第二附属医院泌尿外科, 安徽合肥230000)
肾结石是最常见的泌尿系统结石,占泌尿系结石的40 %~50 %[1]。手术是治疗肾结石的主流方式,具有较高结石清除率,受到广大临床医师的认可[2]。随着腔镜外科技术的不断发展,临床上已出现多种微创术式,其中经皮肾镜取石术(percutaneous nephrolithotripsy, PCNL)和输尿管软管碎石术(flexible ureteroscopic lithotripsy, FURL)是治疗直径在3 cm以内肾结石的常用方法,但两种术式疗效及安全性存在差异,临床上对于选择何种术式尚存在一定争议[3-4]。笔者对比了PCNL术和FURL术治疗不同部位及不同负荷肾结石的疗效差异,重点分析两种术式对患者肾功能的影响。现报道如下。
1 资料与方法
1.1 一般资料
收集2016年1月~2019年1月本院就诊的肾结石患者进行研究。
纳入标准:①经B超、尿路平片或肾盂造影检查确诊为单发性肾结石;②结石直径为1~3 cm;③具有手术指征,耐受手术治疗;④临床资料完整,知情并签署知情同意书;⑤研究资料经医院伦理委员会审核批准。
排除标准:①合并心肺肝等脏器功能障碍者;②伴有输尿管畸形、肾盂积水、肾囊肿、肾结核及尿路感染者;③既往盆腔外伤史或盆腔手术史者;④凝血功能障碍、免疫性疾病及传染病活动期患者;⑤已接受体外冲击波碎石患者;⑥妊娠期或哺乳期女性。
经筛选后共95例患者纳入研究,根据手术方案不同分为两组,FURL组50例,男32例,女性18例;年龄35~63岁,平均(47.84±9.31)岁;结石直径1~3 cm,平均(1.97±0.53)cm;病变体侧:左侧29例,右侧21例;结石位置:肾盂21例,中盏16例,下盏13例。PCNL组45例,男31例,女性14例;年龄37~65岁,平均(49.84±8.91)岁;结石直径1~3 cm,平均(1.86±0.61)cm;病变体侧:左侧24例,右侧21例;结石位置:肾盂21例,中盏13例,下盏11例。两组患者一般资料比较,差异无统计学意义(P>0.05),详见表1。

表1 两组一般资料比较Tab.1 Comparison of general data between two groups
1.2 手术方法
PCNL组:接受经皮肾镜钬激光碎石术,气管插管全麻后取截石位。将F5输尿管导管插入患侧输尿管至结石部位,更换体位为俯卧位,超声检查肾脏状况,于腋后线和肩胛下角线第11肋间用18G穿刺针穿刺至目标肾盏,置入导丝并固定。采用筋膜扩张器扩张至F18,建立经皮肾通道,置入输尿管镜,搜索结石。采用爱科凯能钬激光机碎石,采用500 μm光纤,功率2.5~3.0 J,频率20~25 Hz,由结石外缘逐层粉碎,用脉冲水将碎石经取石通道取出,较大结石块可用取石钳夹出;确认无结石残留后,留置5F双J管及F18肾造瘘管。术后3 d移除肾造瘘管,术后15~30d移除双J管。术后检测患者生命体征,注意体温及造瘘口情况,给予常规抗生素治疗预防感染。
FURL组:接受输尿管软镜碎石术,气管插管全麻后取截石位,将F8/9.8 wolf输尿管插入尿道检查尿道膀胱状况。将输尿管镜插入患侧输尿管并检查输尿管及肾盂,留置导丝,置入F12-14波士顿输尿管鞘,退出输尿管硬镜,置入输尿管软镜,观察肾集合系统及肾结石状况。接通200 μm钬激光光纤,调整功率后进行碎石操作。将结石粉碎至2 mm大小,较大结石碎片采用套石篮取出,术中维持冲洗液通畅。检查无结石残留及活动性出血后,退出光纤、输尿管软管和输尿管鞘。留置5F双J管15~30 d,术后给予常规抗生素预防感染。
1.3 观察指标
①手术指标:记录手术时长、患者下床时间、住院时间、术后24 h视觉模拟评分(VAS)及结石清除情况;②并发症:记录患者术后2 w内发热、尿血、漏尿等并发症情况;③实验室指标:于术前1 d及术后3 d抽取患者空腹静脉血4 mL和洁净中段尿液4 mL,采用酶联免疫法检测血清胱抑素C(CysC)及尿肾损伤因子(KIM-1)水平,应用生化分析仪检测血肌酐(Scr)水平。
1.4 统计学方法
2 结果
2.1 两组手术情况比较
FURL组手术时长、下床时间、住院时间以及术后VAS评分均小于PCNL组(P<0.05);而两组一次结石清除率比较,差异无统计学意义(P>0.05),详见表2。
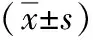
表2 两组手术情况比较Tab.2 Comparison of operation between the two groups
2.2 两种手术方案对不同部位肾结石的清除效果
FURL组中肾盂结石清除率显著高于PCNL组,FURL组中肾下盏结石清除率则低于PCNL组(P<0.05);两组肾中盏结石清除率差异无统计学意义(P>0.05),详见表3。
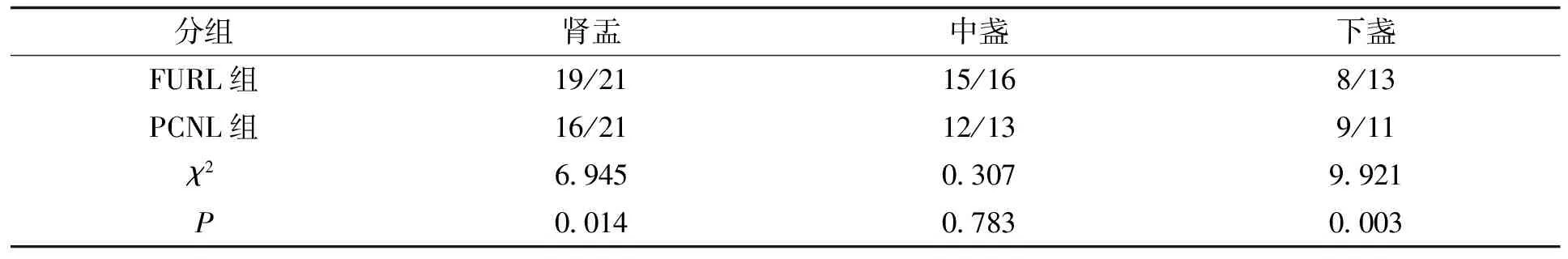
表3 两种手术方案对不同部位肾结石的清除效果Tab.3 Removal effect of two operation schemes on different parts of kidney stones
2.3 两种手术方案对不同负荷肾结石的清除效果
FURL组大负荷结石清除率显著低于PCNL组,FURL组小负荷结石清除率则高于PCNL组(P<0.05)。见表4。

表4 两种手术方案对不同负荷结石的清除效果Tab.4 Removal effect of two kinds of operation schemes on different loads of stones
2.4 两组手术并发症情况比较
两组术后发热、尿血等并发症发生率,差异无统计学意义(P<0.05),详见表5。

表5 两组手术并发症情况比较Tab.5 Comparison of surgical complications between the two groups n (%)
2.5 两组手术前后CysC、Scr及KIM-1水平比较
术前,两组患者血清CysC、Scr及尿KIM-1水平比较,差异无统计学意义(P>0.05);术后3 d,两组患者血清CysC、Scr及尿KIM-1水平均明显升高,其中FURL组血清CysC、Scr及尿KIM-1水平均显著低于PCNL组(P<0.05),详见表6。
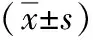
表6 两组手术前后血CysC、Scr及尿KIM-1水平比较Tab.6 Comparison of blood CysC, SCR and urine KIM-1 levels before and after operation between the two groups
3 讨论
尿路结石是泌尿系统的多发疾病,临床主要表现为腰部疼痛、尿血、排尿困难等,严重影响患者工作和生活[5]。目前,中国泌尿系统结石患病率在1 %~5 %,年新发病率为0.15 %~0.2 %,且呈逐年升高趋势[6]。临床上对于尿路结石的治疗方法多种多样,随着微创技术的发展,陆续出现PCNL术、体外冲击波碎石、输尿管镜碎石等微创术式[7-8]。PCNL术具有创伤小、恢复快以及结石清除率高等优点,被泌尿外科诊治指南推荐为>2cm肾结石的首要治疗方法[9-10]。但PCNL术操作难度大,需留置肾造瘘管,术后存在大出血、感染等风险,给患者带来较大困扰[11]。
随着输尿管软管技术的快速发展,其在泌尿系统疾病治疗方面的应用范围和适应症越来越广。输尿管软镜能够自主弯曲,有助于顺利通过腔道进入肾脏,减少对泌尿系统损伤,并在直视下完成碎石操作,视野良好,极大提高了结石清除率[12]。本研究对比了PCNL术和FURL术对直径在肾结石的临床治疗效果,结果显示FURL组手术时长、下床时间、住院时间以及术后VAS评分均小于PCNL组,说明肾结石患者性FURL术后恢复较快,且疼痛程度较低。在结石清除率方面,FURL术对肾盂结石和小负荷肾结石的清除率显著高于PCNL组,但对肾下盏结石和大负荷肾结石的清除率低于PCNL组;分析输尿管软镜镜体纤细柔软,能够较为容易进入肾盂和肾中盏,配合钬激光碎石,提高碎石成功率;而肾下盏形态扭曲,FURL治疗肾下盏过程中,镜体弯曲角度较大,操作难度大且容易损坏输尿管软镜,从而影响了结石的清除效果。
PCNL术治疗肾结石需建立穿刺通道,会损伤肾皮质,若操作不当容易发生出血和周围脏器损伤的风险。FURL术利用人体自然腔道进行手术,创伤小,不建立肾穿刺通道,对肾组织无直接伤害,对身体创伤较轻微,术后恢复较快,且极大降低了术后并发症的发生;但FURL术在经输尿管手术过程中可能会引起输尿管损伤,增加输尿管狭窄等远期并发症。本研究通过随访发现,两组术后发热、尿血等并发症发生率无明显差异,提示两种术式在肾结石治疗过程中安全性接近。
肾结石手术过程中手术麻醉、气管插管、手术创伤以及脏器损伤等均是重要应激源,会引起机体一系列氧化应激反应,导致氧化和抗氧化系统失衡[13]。肾脏功能极易受创伤刺激、缺氧缺血、氧化应激等因素影响而发生损伤,加强围术期对肾脏功能的保护越来越受到临床医师的关注,选择合理有效的手术方案是围术期保护肾脏功能的关键[14-16]。本研究发现,两组患者术后血清CysC、Scr及尿KIM-1水平均明显升高,表明PCNL术和FURL术在治疗过程中均会对患者肾功能产生一定影响,其中FURL组患者血清CysC、Scr及尿KIM-1水平低于PCNL组,提示FURL术对脏器组织的损伤程度更小,更有助于对肾功能的保护。
综上所述,FURL术和PCNL术在肾结石治疗方面各有优势,其中FURL术创伤小,对肾功能影响轻微,对肾盂结石以及小负荷结石的清除效率相对较高;PCNL术则对肾下盏结石的清除率较高,但对患者肾功能会有一定损伤。实际临床上,应对患者结石位置、负荷以及患者身体状况进行科学评估,选择理想术式,以提高治疗效果。

