计算模拟软件在“有机化学”教学中探索性能力的培养
王 群,宋小东,林小龙,孙玉希,潘文慧
( 1. 绵阳师范学院生命科学与技术学院,四川绵阳 621000;2. 绵阳师范学院光致功能材料重点实验室,四川绵阳 621000;3. 山东省曲阜师范大学生命有机分析重点实验室,山东曲阜 273165;4. 北京市食品风味化学重点实验室,北京 100048)
0 引言
大学生探索性能力的培养,对于促进大学生的全面发展以及为后续科研之路的铺垫均有着十分重要的意义[1].传统的“有机化学”教学,多采用听取教师讲解与学生课后进行总结的归纳式方法学习这门课程.这些传统教学方法的缺点在于使大部分学生对有机分子的结构、原理的理解仅停留在记忆层次上,而对有机分子的三维构型变化、微观机理的深入理解存在着较大困难.
随着计算模拟软件的快速发展,各种计算化学软件得到大力开发,也被教师们广泛地应用到各种课堂教学中,并获得了一定的教学效果.例如:武海等人[2]将ChemOffice、Gaussian及Sybyl三种模拟软件应用到“分析化学”教学中的共轭效应分析、荧光光谱分析等,不仅使学生对微观机理的理解变得相对容易,且激发了学生的科研兴趣.赵力维等人[3]采用Gaussian09软件在课堂上对“有机化学”中亲核取代反应机理、防晒产品的设计等进行了探讨,不仅使学生对教材中的生涩概念、反应机理的理解变得相对容易,且大大激发了学生的学习兴趣.赵顺平等人[4]将Material Studio(MS)软件应用到化学教学的课程当中,对化合物的立体模型、分子的电荷分布、分子的波谱性质以及反应的动态过程模拟等在课堂上进行了展示,也使得教学效果得到了一定的提升.
综上所述,以上的文献中几乎是教师自行在课堂上采用计算模拟软件在有机化学教学中的展示,虽然取得了一定的教学效果,但几乎未让学生参与软件的使用.在本课题的研究中,教师将“有机化学”的传统教学与学生自行使用计算模拟软件解决“有机化学”中的疑难点结合起来进行教学改革.此种教学方法,不仅有助于学生理解复杂的结构与机理,增加学生探索微观世界的兴趣,更重要的是,学生的探索性能力也得到了有效的提升.
1 Materials Studio软件的介绍
Materials Studio是美国Accelrys公司生产的一款计算模拟软件,可以在PC机上直接使用,界面直观明了.该软件支持Windows、SGIIRIX以及Red Hat Linux等多种操作系统.该软件采用了先进的模拟思想和计算方法,可以应用于量子力学、分子动力学及介观动力学等方法进行模拟计算[5];该软件不仅可以研究小分子体系,还可以研究蛋白质、聚合物等大分子体系,而且可以应用于多种学科领域,比如:材料、化学、生物及物理等,掌握此软件的使用原理、方法,对于学生未来的科研之路也有所帮助.
MS软件主要包含了五大模块,其中Visualizer是基本环境;Discover、Compass、Forcite及Sorption等模块主要应用于分子力学与分子动力学;Dmol3及CASTEP等主要应用于量子力学.在本课程的教学中,主要使用两大模块.首先使用Visualizer模块,用此模块构建有机分子的三维模型,观察及分析模拟前后的分子模型的结构变化等;然后采用Dmol3模块进行结构的优化、性能的计算及结果的分析等[6].
2 学生使用MS计算模拟软件在“有机化学”学习中的探索实例
2.1 差分电荷密度和Mulliken布居电荷理解休克尔规则
1930年德国化学家Hückel指出,成环的化合物具有平面的离域体系,且π电子数满足4n+2规则时,则这些环状化合物具有类似苯环的芳香性.因此,在课堂上教师给学生讲解环丙烯正离子、环戊二烯负离子、环庚三烯负离子等离子具有的π电子数分别为为2、6和10个,且均满足环状闭合的离域体系,因此这些环状离子具有芳香性[7].在课堂上教师还详细讲解了环丙烯和环丙烯正离子的区别,环丙烯正离子具有芳香性,环丙烯不具有芳香性.这是因为环丙烯中C1原子是sp3杂化,没有空的p轨道,因此不能和C2、C3原子的两个p轨道形成的π电子构成离域体系(图1).而在环丙烯正离子中C1原子是sp2杂化,有一个空的p轨道,虽然此空轨道上没有电子,但仍然可以和C2、C3原子构成p…π共轭的离域体系,因此环丙烯正离子具有芳香性.对于这个知识点学生们是可以理解的,但学生对于什么是离域体系,为什么环丙烯正离子空的p轨道和C2、C3原子的p轨道能够形成大的离域体系存在很大的疑问.因此,在学习了MS软件中的差分电荷密度和Mulliken电荷等相关理论知识之后,学生们采用上述两种方法自行解释了环丙烯正离子具有离域π电子的原因,且观察到了形象生动的电子云图,对满足4n+2电子的环状闭合体系具有芳香性这个知识点有了更深的理解.

图1 电子云密度图(a)环丙烯, 和(b)环丙烯正离子.Fig.1 Electron density maps of (a) cyclopropylene, and (b) cyclopropylene positiveion.
分子中各原子差分电荷密度(deformation density)是原子之间电子云密度的差值,颜色越亮的区域表示电子云密度越大.红色区域电子云密度较大,蓝色区域电子云密度较小[8].学生们首先对环丙烯和环丙烯正离子的结构进行了几何优化,然后计算了两个构型的差分电荷密度,如图1所示.通过差分电荷密度分析发现环丙烯中各原子电子云密度是不相同的,C1电子云密度最小,如图1a所示.而环丙烯正离子中C1、C2、C3原子电子云分布均匀,形成一个大的离域体系,如图1b所示.Mulliken布居电荷分布可以更明确地观察到分子中各原子之间的电荷分布状态[9].通过Mulliken布居电荷发现,环丙烯正离子所有的C原子中电荷均是0.120 e,H原子电荷均是0.213 e.而在环丙烯中C1为-0.233 e,C2和C3为-0.057 e,H4和H5为0.092 e,H6和H7为0.087 e.C2和C3,H6和H7电荷相同,说明C2和C3之间形成了一个π电子体系,C2和C3与C1电荷不同,说明它们之间未构成离域的电子体系.这些结果也与分电荷密度结果相吻合.
因此,通过差分电荷密度和布居电荷学生能够直观地了解环丙烯正离子具有离域体系,不仅解决了他们学习中碰到的难题,而且激发了他们的探索兴趣.
2.2 局域态密度探索苯与环己烷电子的离域性
电子的离域性不仅可以通过差分电荷密度图和Mulliken布居电荷数据直观的显示,而且原子的局域态密度一定程度上也反映电子的离域性[10].在有机化学芳香烃的学习过程中,学生们对苯环形成离域的大π键,而六个C原子的环己烷却没有形成离域体系理解有一定的难度.因此学生在学习了态密度的相关理论之后,教师引导学生通过局域态密度理论对两种分子的离域性进行判断,也取得了满意的学习效果.
学生首先采用MS软件建立了苯环和环己烷的模型,对两种结构进行几何结构优化之后,对苯和环己烷的态密度进行了分析,如图2所示.结果发现苯的态密度在能量状态-15到15 eV之间有态密度电子存在,而环己烷只是在-13到12 eV之间有态密度电子存在.研究报道表明态密度峰跨度越大,电子的离域性越强[11],因此,苯相对于环己烷有更强的离域性.同时,文献表明态密度峰越尖锐,则电子定域性越强[12],图2a和2b比较可知,环己烷的峰更尖锐,定域性更强.通过对环己烷和苯环中态密度的分析,学生不仅掌握了深奥的态密度理论,而且对电子离域性的理解也更加透彻了.同时,也大大激发了学生在遇到问题时自行进行探索解决的兴趣.
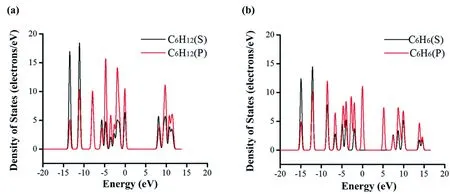
图2 局域态密度图(a)环己烷, 和(b)苯.Fig.2 Partial density states of (a) cyclohexane, and (b) benzene.
2.3 采用Mulliken布居电荷探索苯胺与乙酰氯反应的机理
在《有机化学》的学习中,苯环的傅克酰基化反应是苯环中引入酰基的比较重要的一类反应,属于苯环的亲电取代反应.比如:苯与乙酰氯CH3COCl在AlCl3催化作用下,会生成乙酰苯,如方程式(1)所示.但是苯胺与CH3COCl在AlCl3催化作用下生成的产物是乙酰苯胺(产物1),是苯胺作为亲核试剂进攻乙酰氯中的羰基碳正离子引起的亲核取代反应,如方程式(2)所示[7].学生们在课堂中提出了疑问?因为-NH2是供电子基团,取代苯环上H原子后,可以使苯环活化,因此CH3COCl与苯胺发生反应时,应该在苯环的邻对位生成取代产物(产物2和产物3),如方程式(3)所示,但为什么却不是呢?带着这样的疑问,学生分别就苯和苯胺的布居电荷以及几种产物的总能量两方面对这个反应进行了探索性分析.
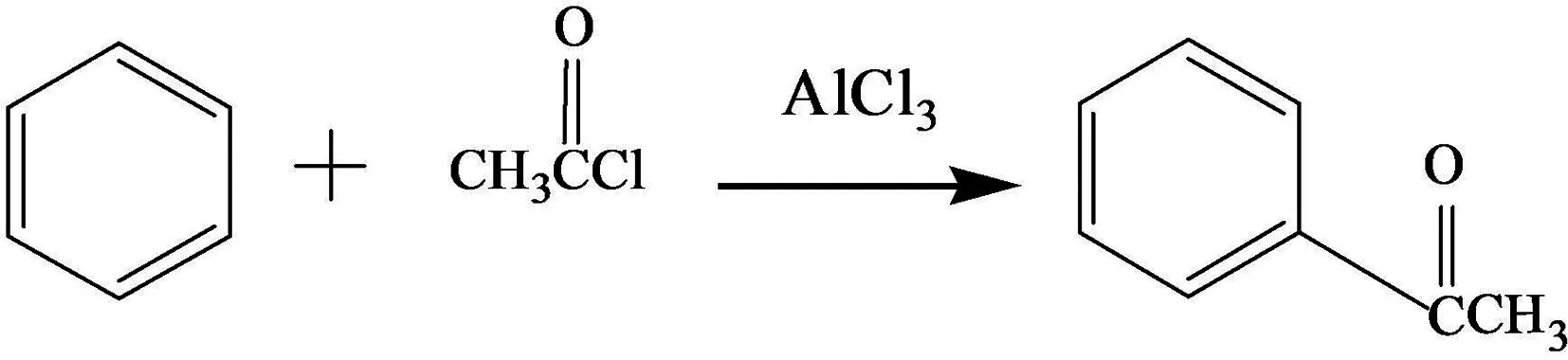
(1)
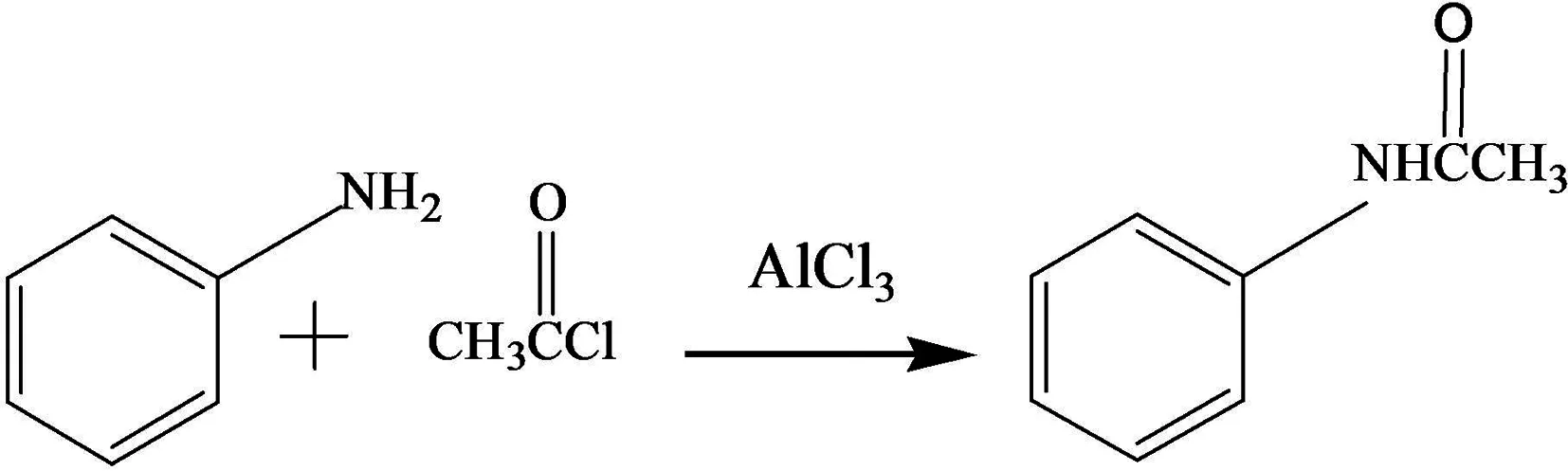
(2)
(产物1)
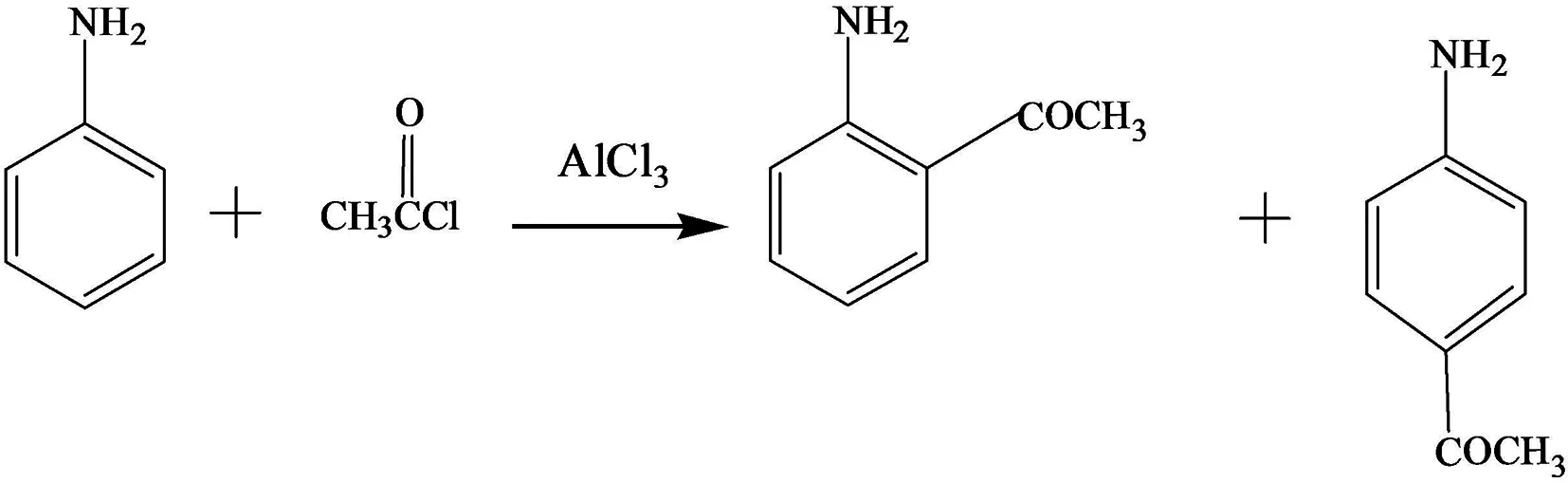
(3)
(产物2) (产物3)
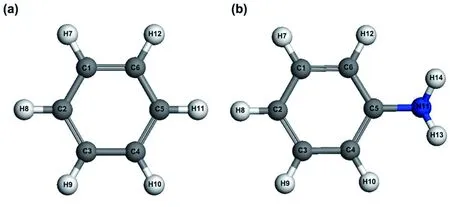
图 3 (a)苯和(b)苯胺的三维结构.Fig.3 The three-dimensional structures of (a) benzene, and (b) phenylamine.
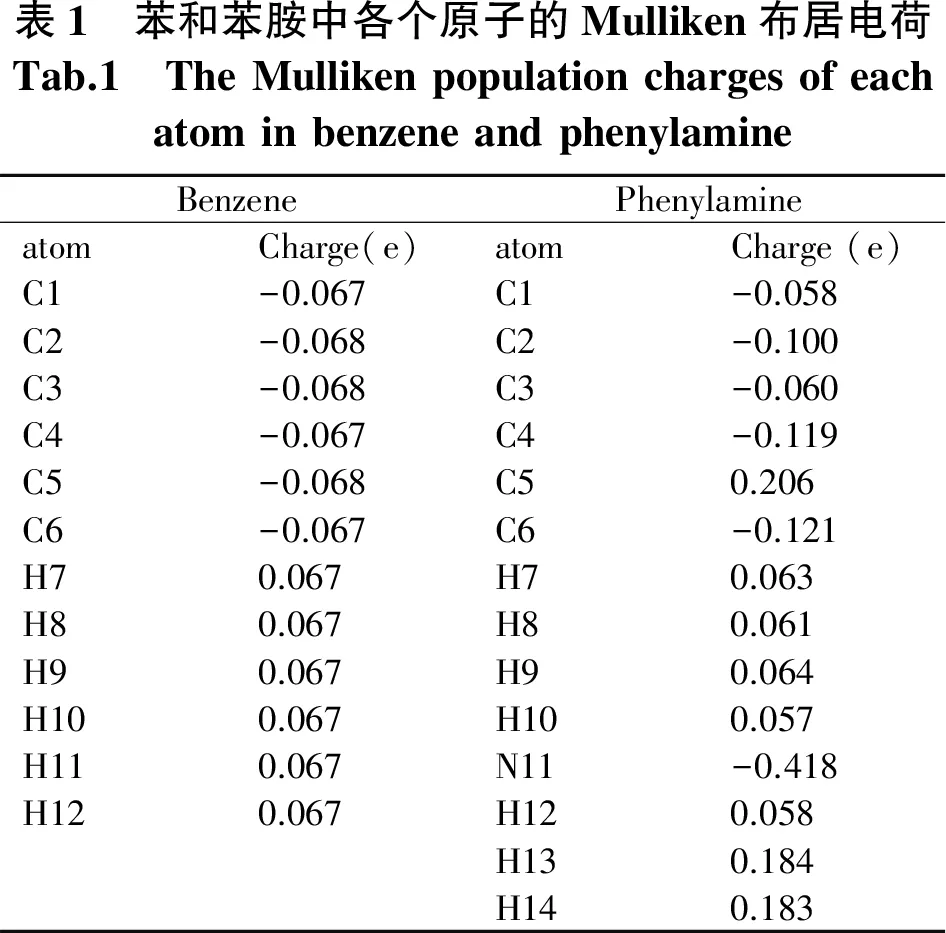
学生们首先对苯和苯胺的结构进行了优化,如图3所示.然后他们对结构优化之后的苯及苯胺进行了Mulliken布居电荷的计算,结果如表1所示.通过表1中的布居电荷分析发现苯环中所有碳原子和氢原子电荷几乎相等,说明所有的C原子都是等价的,这也和苯环形成一个离域的大π体系的结论一致[7].但是通过布局电荷发现在苯胺中电荷密度最大的是N原子,与N原子相连的C原子居然带了正电荷,因此说明-NH2不仅能和苯环形成p…π共轭效应,而且还具有吸电子诱导效应,此时带电量最多的N原子会作为亲核试剂进攻CH3COCl中非常活泼的羰基碳正离子,形成乙酰苯胺(产物1).
同时,学生对三种产物的总能量进行了分析,能量越低,产物越稳定.产物1的总能为-2204.06 Kcal/mol,产物2和产物3的总能分别为-2193.81 Kcal/mol和-2198.92 Kcal/mol,因此从能量方面分析也可以发现苯胺与乙酰氯发生反应,产物应该是乙酰苯胺.
3 学生课程报告及学术论文
本研究将MS软件应用于“有机化学”的教学,在课程结束之后, 学生6至8 人一组完成一个课程项目作为教学效果的考证,有的是对“有机化学” 课程中遇到的问题进行探索分析,也有的是对有机化学某个研究领域进行的探索性研究.学生的课题报告如表2 所示,他们在提出研究课题之前首先要提出这些课题的研究设想,比如,课题4《染料吸附材料中苯环类氨基酸与本征、缺陷石墨烯之间的相互作用》,该课题提出的设想为:氨基酸分子既有阴离子官能团(如-COO-),也有阳离子官能团(如-NH3+),因为阴离子官能团能有效吸附阳离子染料,而阳离子官能团能高效地固定阴离子染料.因此,氨基酸分子功能化的石墨烯可更有效地去除工业中的有机染料污染物.同时,由于π…π相互作用,含芳香环的氨基酸对含芳香环的染料有增强吸附能力的作用.巧合的是,苯丙氨酸(Phe)和酪氨酸(Tyr)是典型的芳香氨基酸,它们不仅含有-COO-、-OH、-NH3+等活性官能团,而且还具有芳香环.因此,研究Phe和Tyr功能化石墨烯对于染料的吸附具有重要意义.然而,学生调研文献发现,目前还没有关于Phe和Tyr改性石墨烯吸附染料的报道.此外,石墨烯,尤其是缺陷石墨烯与Phe(或Tyr)之间的相互作用机制尚未见详细报道.因此,学生提出了该研究课题.
在课题思想提出之后,学生查阅相关文献并写出开题报告;然后,学生对要解决的问题进行研究,并定期向教师汇报研究进展,如果遇到不能解决的问题及时与小组同学或教师进行探讨,寻求解决方案;最后在学期末学生对研究的课题进行汇报总结,教师对学生的汇报进行成绩评定.
通过MS计算软件的学习,学生的探索性能力大大增强,部分学生还对开展的课题研究进行总结,并撰写学术论文.目前已指导2018级学生撰写5篇学术论文,现已出版两篇,三篇正在投稿中.

表2 MS软件在有机化学课堂中应用的报告题目Tab.2 Report topics of MS Software application in "Organic Chemistry" class
4 结论
在“有机化学”的教学过程中,紧随时代步伐,将计算模拟软件融入到教学中,让学生以计算机为辅助工具、量子化学为手段来研究和解决实际学习中的化学问题,不仅提高了学生探索微观世界的兴趣,而且大大培养了学生的探索性能力.这种教学方式,将教学方法的创新、现代教育理念及探索性能力的培养结合起来,必将为大学化学的改革提供新的思路.
——碳正离子的产生及稳定性比较

