miR-485-5p通过靶基因FLOT2调控甲状腺癌细胞增殖、凋亡的分子机制
张磊 李国良 孟帮柱 刘东明 常宏 韩立坤
(内蒙古民族大学附属医院内分泌科,内蒙古 通辽 028000)
甲状腺癌发病率及致死率极高且患者预后较差,严重影响患者生命安全及生活质量〔1〕。因而寻找治疗及诊断甲状腺癌的分子标志物对提高临床诊疗效果均具有重要意义。微小RNA(miRNA)作为内源性非编码小RNA分子,研究显示miRNA可在胃癌、肝癌等多种恶性肿瘤中扮演抑癌或癌基因角色,并可能作为诊断及判断疾病进展的潜在分子标志物〔2〕。miR-485-5p在肝癌组织中表达下调,过表达miR-485-5p可通过调控EMMPRIN的表达进而抑制肝癌细胞增殖和转移〔3〕。研究显示miR-485-5p在乳腺癌组织中下调表达,miR-485-5p过表达可抑制乳腺癌细胞的迁移侵袭能力〔4〕。然而,miR-485-5p对甲状腺癌细胞恶性生物学行为的影响研究尚未见报道。通过靶基因预测软件得到脂筏标记蛋白(FLOT)2可能是miR-485-5p的靶基因,研究报道FLOT2在肝癌组织及细胞中上调表达并可促进肝癌细胞的增殖、迁移侵袭,同时乳腺癌组织及细胞中FLOT2表达上调且与乳腺癌患者的不良预后相关〔5,6〕。本研究通过证实FLOT2是否为miR-485-5p的靶基因,探究miR-485-5p靶向FLOT2对甲状腺癌细胞增殖及凋亡的机制。
1 材料与方法
1.1材料与试剂 甲状腺癌细胞株SW579、FTC-133、KAT-18与甲状腺上皮细胞TEC均购自中国科学院细胞库。miR-485-5p mimic、miR-485-5p抑制剂(anti-miR-485-5p)及其各自阴性对照均购自广州锐博生物科技有限公司;FLOT2 siRNA(si-FLOT2)及其阴性对照(si-NC)均购自上海吉玛制药技术有限公司;DMEM培养基、胰蛋白酶、胎牛血清、青霉素及链霉素均购自美国Gibco公司;LipofectamineTM2000购自上海阳光生物科技有限公司;RNA提取及实时荧光定量PCR(qRT-PCR)实验所需试剂均购自美国Thermo Fisher公司;四甲基偶氮唑蓝(MTT)检测试剂盒购自武汉艾美捷科技有限公司;细胞凋亡检测试剂盒购自大连美仑生物技术有限公司;双荧光素酶报告基因检测试剂盒购自北京全式金生物技术有限公司;放射免疫沉淀法(RIPA)蛋白裂解液及其他蛋白免疫印迹实验所需试剂均购自美国Sigma公司;含半胱氨酸的天冬氨酸蛋白水解酶(cleaved-caspase)-3、细胞周期蛋白(Cyclin)D1、p21、p27、B淋巴细胞瘤(Bcl)-2、Bcl-2相关X蛋白(Bax)单克隆抗体均购自美国Abcam公司;辣根过氧化物酶(HRP)标记的IgG二抗购自武汉博士德生物工程有限公司。
1.2细胞培养、转染及分组 取出冻存甲状腺癌细胞株SW579、FTC-133、KAT-18与甲状腺上皮细胞TEC,放入37℃恒温水浴锅内,待细胞融化后加入含有10%胎牛血清DMEM培养基的细胞生长液,同时含有100 U/ml青霉素、0.1 mg/ml链霉素,1 000 r/min离心10 min,弃上清液,置于37℃、体积分数5%CO2培养箱培养,待细胞生长融合至80%左右时传代培养。取对数生长期甲状腺癌SW579细胞,胰蛋白酶消化细胞,以5×103个细胞/ml接种于6孔板,37℃、体积分数5% CO2培养箱培养,待细胞生长融合至80%时更换为不含胎牛血清的DMEM培养基,参照Lipofectamine2000转染试剂盒说明书分别将miR-485-5p mimic与miR-NC加入到SW579细胞,分别为miR-485-5p组、miR-NC组。为了探究FLOT2对SW579细胞生物学行为的影响,本研究分别将si-FLOT2与si-NC转染到SW579细胞,分别为si-FLOT2组、si-NC组。后续实验中为验证miR-485-5p是否通过抑制FLOT2表达而影响SW579细胞增殖及凋亡,分别将FLOT2过表达载体(pcDNA-FLOT2)与空载体(pcDNA)分别与miR-485-5p mimic共同转染入SW579细胞,分别为miR-485-5p+pcDNA组、miR-485-5p+pcDNA-FLOT2组。上述各组转染6 h后更换为完全DMEM培养基。继续培养48 h收集细胞。
1.3qRT-PCR检测细胞中miR-485-5p及FLOT2 mRNA表达水平 取不同甲状腺癌细胞、正常甲状腺上皮细胞及转染各组对数生长期SW579细胞,RNA提取:分别加入Trizol裂解细胞提取细胞总RNA,置于冰上5 min,分别加入氯仿(200 μl),室温放置5 min后12 000 r/min离心15 min,吸取水相层置于另一EP试管内,加入500 μl异丙醇,室温放置20 min后12 000 r/min离心15 min,弃上清,加入乙醇混合(75%)后12 000 r/min离心5 min,弃上清,所有操作需在通风橱内进行,最后将EP试管置于超净工作台晾干,加入适量无RNA酶水,利用紫外分光光度计检测RNA浓度与纯度,置于-80℃超低温冰箱保存待测。反转录:按照反转录试剂盒说明书配置反应体系并进行普通PCR扩增得到cDNA。qRT-PCR:根据试剂盒说明书配置反应体系,完成后置于实时荧光定量PCR仪检测各基因Ct值,反应条件为95℃ 5 min,95℃ 30 s,60℃ 30 s,72℃ 30 s,共循环40次。miR-485-5p以U6为内参基因,FLOT2以GAPDH为内参基因,反应结束后,采用 2-ΔΔCt法计算miR-485-5p及FLOT2 mRNA相对表达量。
1.4Western印迹检测FLOT2、CyclinD1、p21、p27、Bcl-2、Bax、cleaved-caspase-3蛋白表达 取1.2中所有分组细胞,分别加入蛋白裂解液提取蛋白,经二喹啉甲酸(BCA)定量蛋白后进行十二烷基硫酸钠-聚丙烯酰胺凝胶(SDS-PAGE)电泳反应,转膜、封闭后分别加入各蛋白一抗(1∶500),洗膜后加入二抗(1∶1 000),TBST洗膜,ECL显影后置于凝胶成像系统及Quantityone软件检测条带灰度值,蛋白相对表达量=目的蛋白条带灰度值/内参照条带灰度值。
1.5MTT检测细胞增殖 收集转染后各组SW579细胞,胰蛋白酶消化后制备细胞悬浮液,以每孔100 μl体积细胞悬浮液接种于96孔板(浓度3×105个/ml),分别于培养12、48、72 h时加入浓度为5 mg/ml的MTT溶液50 μl,室温孵育4 h,弃上清,分别加入二甲基亚砜(DMSO)溶液150 μl,放入摇床内10 min,置于酶标仪检测各孔吸光度(OD),检测波长为490 nm,每组实验均设置3次重复。
1.6流式细胞术检测细胞凋亡 收集各组对数生长期SW579细胞,预冷磷酸盐缓冲液(PBS)洗涤细胞,采用胰蛋白酶消化细胞,10 000 r/min离心5 min,分别加入PBS洗涤细胞,加入1 ml结合缓冲液,再次离心后弃上清,分别加入200 μl结合缓冲液,再次分别加入5 μl膜联蛋白(Annexin)V-异硫氰酸荧光素(FITC)与碘化丙锭(PI),室温避光孵育20 min,分别加入400 μl结合缓冲液置于流式细胞仪检测并计算细胞凋亡率。
1.7荧光素酶报告基因检测 靶基因预测库预测miR-485-5p与FLOT2的3′UTR存在结合位点,将含有miR-485-5p结合位点的FLOT2的3′UTR片段插入PGL3荧光素酶报告基因载体,分别构建野生型(WT-FLOT2)与突变型(MUT-FLOT2)的FLOT2 3′UTR荧光素酶报告载体,将WT-FLOT2、MUT-FLOT2分别与miR-485-5p mimic、miR-NC共转染,培养箱内派样48 h后收集细胞,严格按照双荧光素酶报告基因检测试剂盒说明书操作并检测各组SW579细胞的荧光素酶活性。
1.8统计学处理 采用SPSS19.0软件进行t检验、单因素方差分析。
2 结 果
2.1miR-485-5p和FLOT2在甲状腺癌细胞和甲状腺上皮细胞中的表达 甲状腺癌细胞SW579、FTC-133、KAT-18中的miR-485-5p相对表达量与甲状腺上皮细胞TEC差异有统计学意义(P<0.05),3种甲状腺癌细胞中SW579细胞相对表达量最低;而FLOT2 mRNA及蛋白表达显著升高(P<0.05),3种甲状腺癌细胞中SW579细胞表达水平最高,选择SW579细胞作为后续研究。见图1、表1。
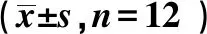
表1 miR-485-5p和FLOT2在甲状腺癌细胞和甲状腺上皮细胞中的表达
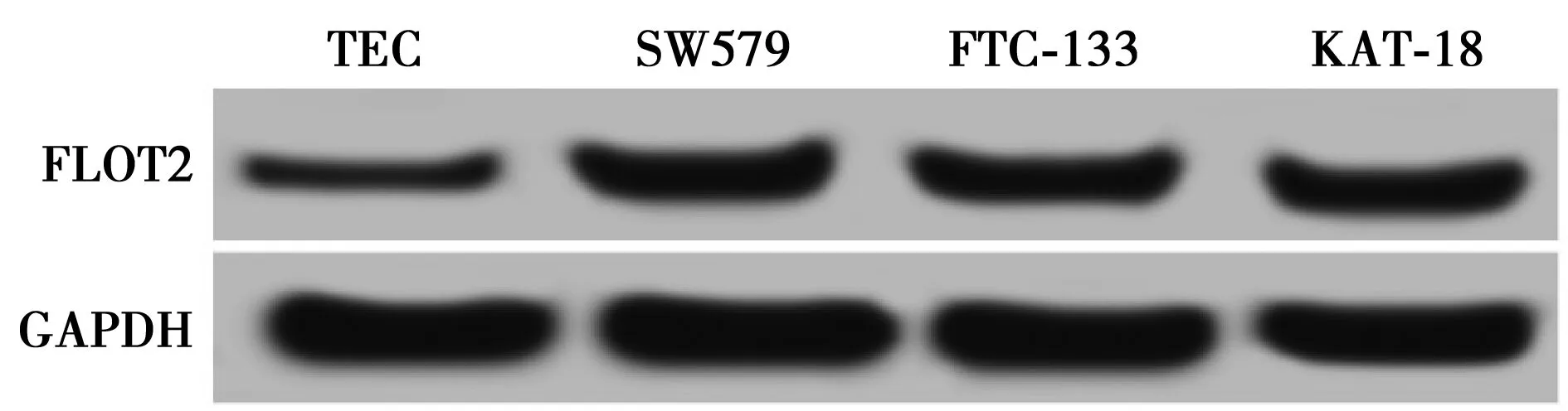
图1 FLOT2蛋白表达
2.2miR-485-5p过表达对甲状腺癌SW579细胞增殖的影响 qRT-PCR检测结果显示转染后miR-485-5p组SW579细胞中miR-485-5p相对表达量明显升高(P<0.05),提示转染成功。MTT检测结果显示转染后12 h内,miR-NC组与miR-485-5p组甲状腺癌SW579细胞OD值差异无统计学意义(P>0.05)。转染48 h开始miR-485-5p组与miR-NC组相比,SW579细胞OD值差异有统计学意义(P<0.05)。Western印迹检测结果显示miR-485-5p组细胞增殖相关蛋白CyclinD1蛋白表达显著低于miR-NC组(P<0.05),而p21、p27蛋白表达显著高于miR-NC组(P<0.05),见图2,表2。
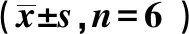
表2 miR-485-5p过表达对甲状腺癌SW579细胞增殖的影响

图2 细胞增殖相关蛋白表达
2.3miR-485-5p过表达对甲状腺癌SW579细胞凋亡的影响 流式细胞术检测结果显示,miR-485-5p组SW579细胞凋亡率显著高于miR-NC组(P<0.05)。Western印迹检测结果显示,与miR-NC组相比,miR-485-5p组SW579细胞中抗凋亡蛋白Bcl-2蛋白表达明显降低(P<0.05),而Bax与cleaved-caspase-3蛋白均明显升高(P<0.05),见图3、图4、表3。
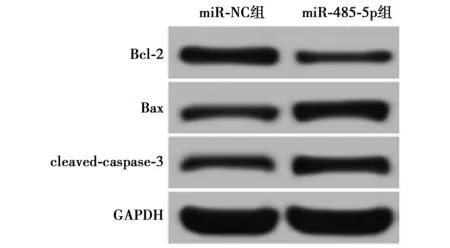
图3 凋亡相关蛋白表达
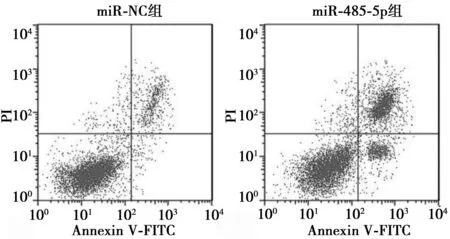
图4 细胞凋亡流式图
表3 miR-485-5p过表达对甲状腺癌SW579细胞凋亡的影响
2.4抑制FLOT2表达对甲状腺癌SW579细胞增殖和凋亡的影响 与si-NC组相比,si-FLOT2组SW579细胞中FLOT2蛋白表达明显降低(P<0.05);转染48 h后,si-FLOT2组SW579细胞OD值明显降低(P<0.05);si-FLOT2组SW579细胞凋亡率明显增加(P<0.05);Western印迹结果显示CyclinD1与Bcl-2蛋白表达下调(P<0.05),而p21与Bax蛋白表达上调(P<0.05),见图5、表4、表5。
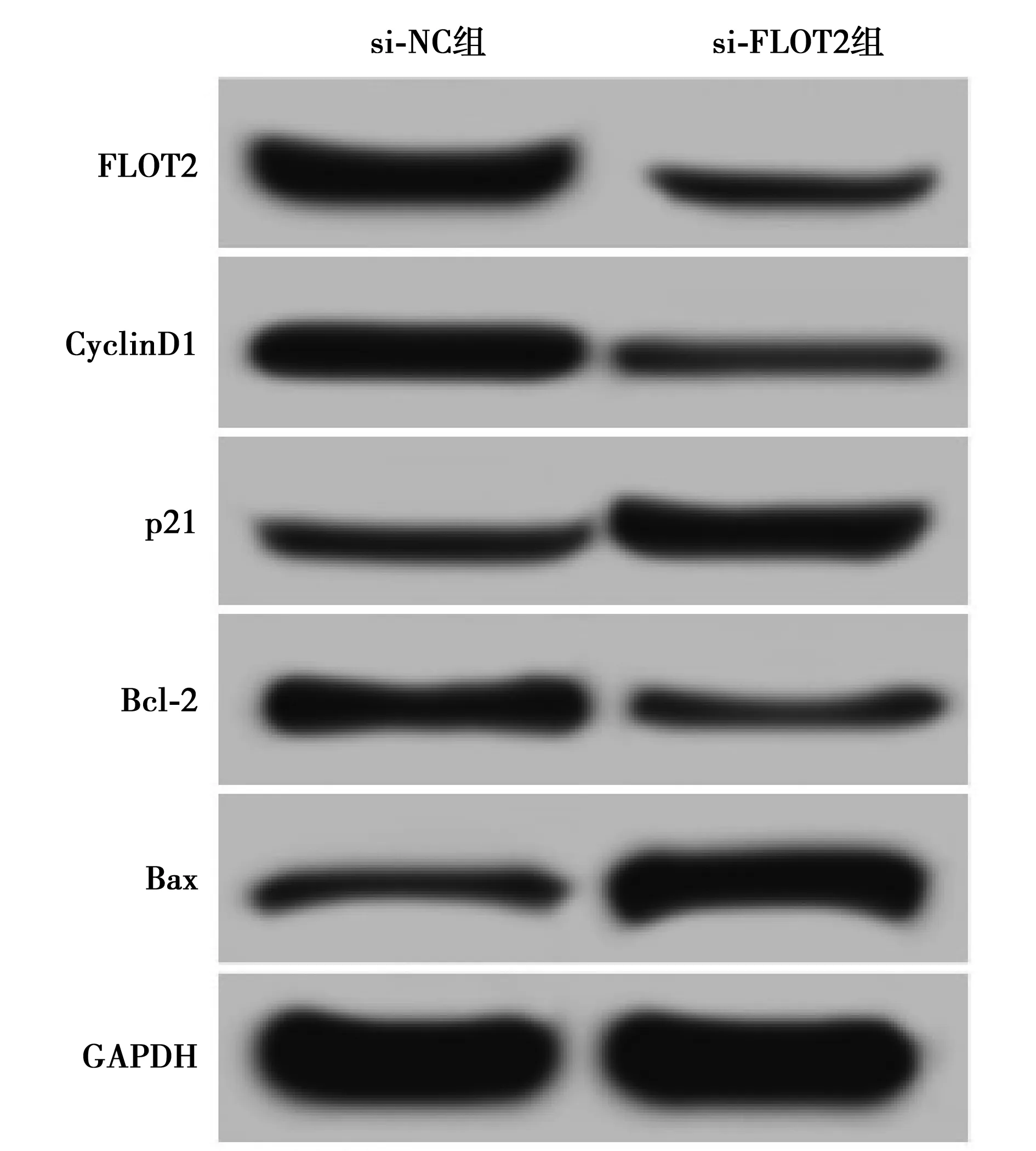
图5 FLOT2和增殖、凋亡相关蛋白表达
表4 抑制FLOT2表达对甲状腺癌SW579细胞增殖和凋亡的影响

表5 抑制FLOT2表达对甲状腺癌SW579细胞增殖和凋亡相关蛋白表达的影响
2.5miR-485-5p靶向调控FLOT2的表达 双荧光素酶报告实验结果显示WT-FLOT2与miR-485-5p mimic共转染组SW579细胞荧光素酶活性(0.42±0.05)显著低于WT-FLOT2与miR-NC共转染组(1.04±0.08;t=16.098,P=0.000),而MUT-FLOT2与miR-485-5p mimic共转染组SW579细胞荧光素酶活性(1.03±0.09)与MUT-FLOT2与miR-NC共转染组(1.01±0.07)相比差异无统计学意义(t=0.430,P=0.677)。Western印迹检测结果显示,miR-485-5p组FLOT2蛋白表达(0.22±0.03)显著低于miR-NC组(0.63±0.06,P<0.05),anti-miR-485-5p组(0.89±0.08)显著高于anti-miR-NC组(0.61±0.05,P<0.05),见图6、图7。

图6 互补的核苷酸序列
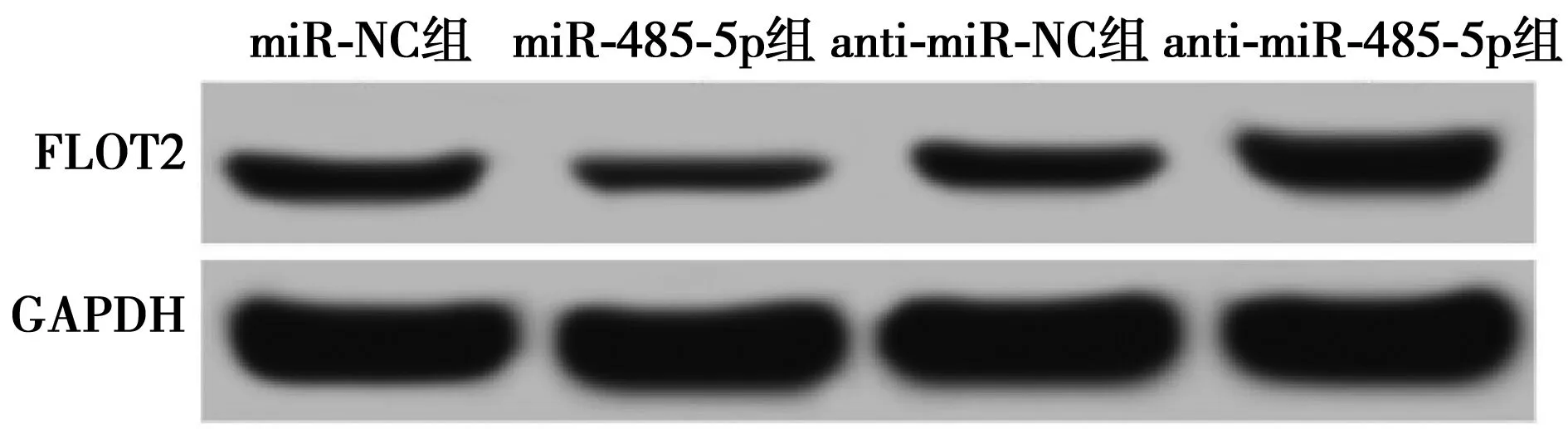
图7 miR-485-5p靶向调控FLOT2的表达
2.6FLOT2过表达逆转了miR-485-5p过表达对甲状腺癌SW579细胞增殖和凋亡的影响 Western印迹检测结果显示,miR-485-5p+pcDNA-FLOT2组SW579细胞中FLOT2蛋白表达明显高于miR-485-5p+pcDNA组(P<0.05)。与miR-485-5p+pcDNA组相比,MTT检测结果显示在共转染培养48 h后miR-485-5p+pcDNA-FLOT2组SW579细胞OD值显著升高,而细胞凋亡率显著降低,Western印迹结果显示CyclinD1与Bcl-2蛋白表达显著升高(P<0.05),而p21与Bax蛋白表达显著降低(P<0.05)见图8、表6、表7。
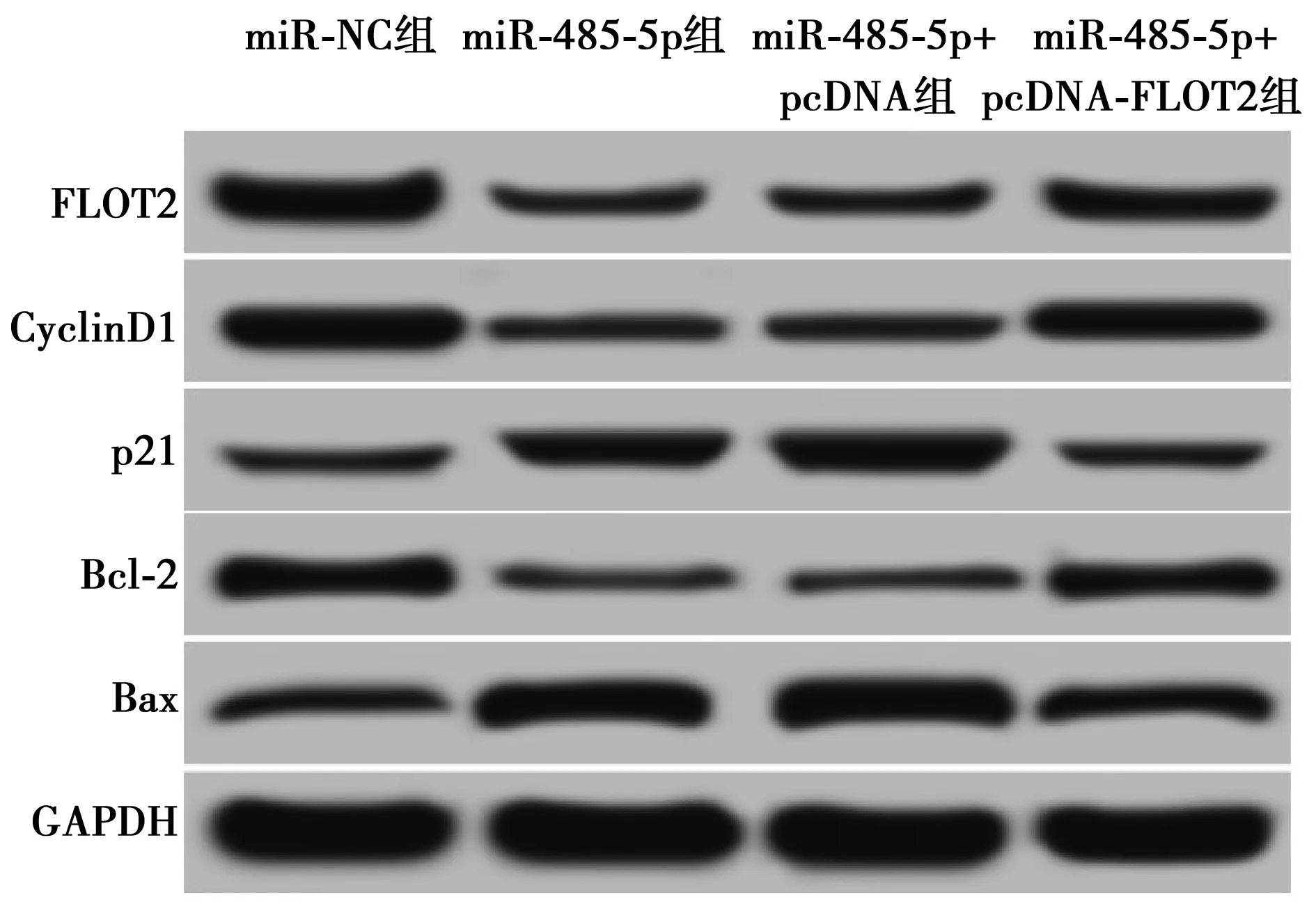
图8 FLOT2和增殖、凋亡相关蛋白表达
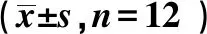
表6 FLOT2过表达逆转了miR-485-5p过表达对甲状腺癌SW579细胞增殖和凋亡的影响

表7 FLOT2过表达逆转了miR-485-5p过表达对甲状腺癌SW579细胞增殖和凋亡相关蛋白表达的影响
3 讨 论
甲状腺癌患者早期临床症状较隐匿,目前临床主要采用手术与非手术治疗,可在一定程度上改善患者临床症状,但早期诊断及治疗方法均具有一定局限性导致甲状腺癌患者死亡率升高〔7,8〕。甲状腺癌发生及发展涉及多种基因或信号通路蛋白,因此探究甲状腺癌发病机制对寻找早期诊断及治疗甲状腺癌的分子标志物具有重要指导意义。miRNA可调控细胞增殖及凋亡,研究显示miRNA可影响甲状腺癌细胞增殖、迁移及侵袭等恶性生物学过程〔9〕。因此,寻找甲状腺癌发生及发展相关的miRNA对揭示其发病机制及提高靶向治疗效果均具有重要意义。
miR-485-5p在结直肠癌细胞中呈低表达并可抑制癌细胞增殖及侵袭〔10〕,梁昆等〔11〕研究表明通过上调miR-485-5p表达可有效抑制前列腺癌细胞增殖。胃癌组织及细胞中miR-485-5p表达下调,上调miR-485-5p表达可通过抑制靶基因FLOT1表达进而抑制胃癌细胞增殖、迁移及侵袭〔12〕。乳腺癌细胞中miR-485表达水平降低,上调miR-485表达后可抑制乳腺癌细胞迁移及侵袭〔13〕。Chen等〔14〕研究表明miR-485-5p过表达后可通过靶向调控高迁移率族蛋白(HMGA)2表达进而抑制膀胱癌细胞侵袭。由此猜测miR-485-5p在甲状腺癌细胞中呈低表达并可发挥抑癌基因作用。本研究结果说明miR-485-5p表达水平降低可促进甲状腺癌发生。通过上调miR-485-5p表达后发现SW579细胞增殖活性明显降低,CyclinD1蛋白表达明显降低,而p21与p27蛋白表达明显升高,p21与p27属于细胞周期依赖性激酶抑制因子家族成员,并可抑制CyclinD1与细胞周期依赖性激酶结合〔15〕。提示miR-485-5p过表达可上调p21与p27蛋白表达水平,抑制CyclinD1蛋白表达,促使SW579细胞周期阻滞,抑制细胞增殖。但关于其是否通过诱导细胞周期阻滞还需通过流式细胞术检测细胞周期。Bcl-2属于抗凋亡蛋白,Bax属于促凋亡蛋白,Bax表达上调可激活cleaved-caspase-3蛋白表达进而诱导细胞凋亡〔16〕。本研究结果提示miR-485-5p过表达可上调Bax、cleaved-caspase-3蛋白表达,并抑制Bcl-2蛋白表达进而诱导SW579细胞凋亡。
FLOT2在鼻咽癌细胞中表达上调,抑制FLOT2表达可能通过转化生长因子(TGF)-β信号通路进而抑制鼻咽癌细胞迁移及侵袭〔17〕。 FLOT2作为细胞膜重要组成成分,范双石等〔18〕研究表明 FLOT2在喉鳞状细胞癌中呈高表达,并可能与癌症发生进展及患者不良预后有关。本研究结果提示 FLOT2可能参与甲状腺癌发生过程。研究报道沉默 FLOT2表达可通过上调p21、p27蛋白表达进而抑制乳腺癌细胞增殖〔19〕。本研究提示抑制FLOT2表达可有效降低SW579细胞增殖能力并提高细胞凋亡水平。相关研究表明miR-485可通过抑制磷脂酰肌醇-3激酶(PI3K)/蛋白激酶B(AKT)/mTOR信号通路而抑制靶基因 FLOT2表达,进而抑制肺腺癌细胞迁移及侵袭〔20〕。本研究双荧光素酶报告基因实验验证FLOT2是miR-485-5p的靶基因,在miR-485-5p mimic转染的SW579细胞中加入pcDNA-FLOT2质粒可逆转miR-485-5p过表达对甲状腺癌细胞增殖及凋亡的作用,提示miR-485-5p可通过作用于靶基因FLOT2抑制甲状腺癌细胞增殖并诱导细胞凋亡。
综上,miR-485-5p在甲状腺癌细胞中下调表达,FLOT2上调表达,miR-485-5p过表达可通过靶向FLOT2抑制甲状腺癌细胞增殖并促进细胞凋亡,为揭示甲状腺癌发病机制提供新思路,并可能作为临床靶向治疗甲状腺癌的潜在靶点。

