顶空固相微萃取葡萄酒挥发性物质的条件优化
李媛媛,李德美*,张亚东,王 燕,王宗义
(1.北京农学院 食品科学与工程学院,北京 102206;2.农产品有害微生物及农残安全检测与控制北京市重点实验室,北京 102206)
挥发性物质影响了葡萄酒的感官特性以及葡萄酒的品质特征。在过去的十几年中,研究人员从葡萄酒中已经鉴定并量化了大约800多种[1-2],包括醇类,酯类,脂肪酸,酮类,酚类等[3-4]。目前,在进行葡萄酒挥发性物质分析时,需要针对分析物不同的物理或化学性质进行分离和富集[5],根据萃取原理可将前处理的方法分为三类,第一类是根据样品和萃取溶剂的沸点不同,采用同时蒸馏萃取法[6]等;第二类是根据相似相容原理,采用液-液萃取法[7]等;第三类根据香味物质对固相萃取柱附能力不同,采用固相萃取法[8]等。其中顶空固相微萃取法(headspace-solidphase micro extraction,HS-SPME)是目前被广泛应用于葡萄酒中挥发性物质分析研究的萃取方法之一,其具有简单、快速、高效、经济、无溶剂、检出限较低等特点,适用于从葡萄酒中提取和浓缩挥发性和半挥发性物质[9]。
近年来,对葡萄酒挥发性物质的相关研究有大量文献报道,这些研究主要集中在葡萄酒风味物质形成机理及影响因素[10-11]和不同萃取方法的萃取效果的对比研究等[12-13],但是,关于优化提取条件的研究较少。
本研究选取两款种植面积最广的葡萄品种所酿造的葡萄酒:霞多丽干白葡萄酒和赤霞珠干红葡萄酒,通过对顶空固相微萃取条件进行优化,并对优化后的方法进行验证,建立葡萄酒挥发性物质测定的最佳分析条件,以期为今后葡萄酒研究工作提供有益参考。
1 材料与方法
1.1 材料与试剂
2015年霞多丽干白葡萄酒:天瑜酒庄;2016年赤霞珠干红葡萄酒:烟台张裕葡萄酒股份有限公司;12%(V/V)乙醇模拟酒溶液;NaCl、无水乙醇:北京化工厂;内标物和三个标准品的详细信息见表1。

表1 内标物和标准品名称、来源、纯度、定量和定性离子Table 1 Name,source,purity,quantitative and qualitative ions of internal standard and standard substances
1.2 仪器与设备
7890A/5975C型气质联用仪、DB-5MS毛细色谱柱(30m×0.32 mm×0.25 μm)、HS-SPME手动进样手柄:美国Agilent公司;50/30 μm DVB/CAR/PDMS萃取头:美国Supelco公司;DF-101S型恒温加热磁力搅拌器:巩义市英峪予仪器公司。
1.3 试验方法
1.3.1 香气成分分析
样品前处理:将10 mL酒样、不同添加量的NaCl、50 μL 2-辛醇内标物(质量浓度为400 mg/L)和磁力转子放入20 mL顶空瓶中,在恒温加热磁力搅拌器中平衡10min,经过不同的萃取温度和时间后在GC进样口解吸5 min,解吸温度260 ℃。
色谱条件:初始温度50 ℃,保持2 min,以4.0 ℃/min升至160 ℃,再以6.0 ℃/min升至250 ℃保持5 min;载气为氮气(N2),流速1 mL/min,无分流进样。
质谱条件:电子电离(electron ionization,EI)源;电子能量70 eV;离子源温度230 ℃;传输线温度250 ℃;四级杆温度150 ℃;SCAN全扫描。
定性分析[14]:运用计算机自带数据库美国国家标准与技术研究院(nationalinstitute ofstandardsand technology,NIST)08.L进行检索和分析,结合相关文献[15-17],确定化学成分。
定量分析:采用内标法-标准曲线法对标准品含量进行定量分析。
1.3.2 准确度检测
标准曲线构建:将3个标准品分别配制成5个不同浓度梯度的模拟酒溶液,萃取后进行仪器分析得到线性方程(n=3)。回收率测定:向12%(V/V)乙醇模拟酒溶液中别加入一定量已知浓度的3种标准品溶液,根据检出总值以及加标量计算回收率和相对标准偏差(relative standard deviation,RSD)(n=3)。
1.3.3 单因素试验
依据顶空固相微萃取技术的相关文献报道[18-19],选取NaCl添加量、萃取时间和萃取温度为单因素试验中的研究因素,以研究其对葡萄酒中挥发性物质检测获得总峰面积的影响。
1.3.4 响应面优化试验
根据单因素试验结果和Box-Behnken中心组合试验设计原理,以挥发性物质总峰面积(Y)为响应值,进行3因素3水平响应面试验,确定两款不同的葡萄酒挥发性物质萃取的最佳条件,响应面试验因素与水平见表2。

表2 萃取条件优化响应面试验因素与水平Table 2 Factor and levels of response surface experiments for extraction condition optimization
2 结果与分析
2.1 萃取条件单因素试验分析
2.1.1 NaCl添加量与总峰面积的关系
按照方法1.3.1,加入1.5 g、2.0 g、2.5 g、3.0 g和3.5 g NaCl,添加量相应为0.15 g/mL、0.20 g/mL、0.25 g/mL、0.30 g/mL和0.35 g/mL。在40 ℃条件下萃取30 min,研究不同NaCl添加量与风味物质总峰面积的关系,以选取合适的NaCl添加量。结果见图1。

图1 NaCl添加量对总峰面积的影响Fig.1 Effect of NaCl content on total peak area
由图1可知,在保持萃取时间和萃取温度恒定的条件下,当NaCl添加量未超过0.25 g/mL时,检测出赤霞珠葡萄酒挥发性物质总峰面积随着样品中NaCl添加量的增加而增大,但霞多丽干红葡萄酒珠葡萄酒挥发性物质总峰面积随着样品中NaCl添加量的增加呈现先下降后增长的趋势,当NaCl添加量超过0.25 g/mL时,总峰面积不再增加反而降低,这可能是由于样酒中无机盐达到饱和状态,挥发性物质在葡萄酒中的溶解度不再受无机盐浓度的影响,再加入无机盐也不会提高检测物质的挥发性,甚至可能造成抑制挥发作用,故总峰面积不增反减。因此,本试验选定样品中NaCl添加量为0.25 g/mL。
2.1.2 萃取时间与总峰面积的关系
萃取时间选择25 min、30 min、35 min、40 min、45 min,研究不同萃取时间与风味物质总峰面积的关系,以选取合适的萃取时间。结果见图2。
萃取时间是指顶空瓶中的样品、顶部空间和涂层纤维三相之间从萃取开始至达到平衡所需要时间,搅拌样品和加温等方法均可缩短平衡时间。针对不同的萃取样品,萃取时间大致为20~50 min,最常用的萃取时间为30 min[20],平衡萃取效果,从而选取最佳萃取时间。
由图2可知,在保持样品中NaCl添加量与萃取温度恒定的条件下,两款样品风味物质总峰面积变化的规律不同。霞多丽干白葡萄酒萃取时间在25~35 min范围时,挥发性物质总峰面积呈现先下降后增长的趋势;萃取时间在35~45 min范围时,呈现下降趋势;总体而言,在35 min左右时,峰值达到最大。赤霞珠干红葡萄酒萃取时间在25~45 min范围时,挥发性物质总峰面积呈现先上升后下降的趋势,在萃取时间为35 min时,挥发性物质总峰面积达到最大值,与霞多丽干白葡萄酒相比,其挥发性物质总峰面积随萃取时间变化而波动的趋势相对平稳。本试验选取35 min作为萃取时间,并进行下一步分析。

图2 萃取时间对总峰面积的影响Fig.2 Effect of extraction time on total peak area
2.1.3 萃取温度与总峰面积的关系
按照方法1.3.1,加入2 gNaCl,在20 ℃、30 ℃、40 ℃、50 ℃及60 ℃条件下萃取30 min,研究不同萃取温度与风味物质总峰面积的关系,以选取合适的萃取温度,结果见图3。

图3 萃取温度对总峰面积的影响Fig.3 Effect of extraction temperature on total peak area
萃取温度一般在20~60 ℃之间,不宜过高,以免改变葡萄酒基质的原始成分[21]。由图3可知,在样品中NaCl添加量与萃取时间固定时,两样品挥发性物质测定峰值随萃取温度而变化的规律不同。霞多丽干白葡萄酒萃取温度在20~40 ℃范围时,挥发性物质总峰面积呈现先下降后增长的趋势;萃取温度在40~60 ℃范围时,挥发性物质总峰面积呈现下降趋势;总体而言,萃取温度40 ℃时,挥发性物质峰面积最大。赤霞珠干红葡萄酒萃取温度在20~40 ℃范围时,挥发性物质总峰面积呈现先增加后下降的趋势,萃取温度40 ℃时,挥发性物质峰面积最大。随着温度升高,分子热运动越快,挥发性物质在样品和涂层纤维中的扩散系数越大,萃取效果越好,但是,温度过高则会使得不易挥发的大分子物质吸附在萃取头上,易挥发的小分子物质很难吸附在萃取头上[22],降低挥发性物质在涂层纤维上的分配系数。本试验选取40 ℃作为萃取温度。
2.2 响应面优化分析
2.2.1 建立模型
利用Design-Expert 8.0.5b设计响应面试验,共设计了17个试验点,12个析因试验,5个中心点试验,试验设计及结果见表3。

表3 干白、干红葡萄酒萃取条件优化响应面设计及结果Table 3 Design and results of response surface methodology for extraction conditions optimization of dry white and dry red wine
2.2.2 模型显著性检测
对该模型进行显著性检验和方差分析,结果见表4、表5。并得到初步回归方程如下:

由表4、表5可知,两种拟合模型P值均<0.01,说明模型差异极显著,表明试验方法可行;失拟项均不显著(P1=0.206>0.05;P2=0.158>0.05),说明回归方程拟合度较好,试验误差比较小。
由表4可知,回归模型中B、A2、AB、AC对总峰面积的影响显著(P<0.05);B2、C2、BC对挥发性物质总峰面积的影响极显著(P<0.01)。由表5可知,回归模型中C对挥发性物质总峰面积的影响显著(P<0.05);回归模型中A、B、A2、B2、C2、BC对总峰面积的影响极显著(P<0.01)。从表4和表5所列的F值大小可知,本试验设定的三个影响因素对两个样品中挥发性物质总峰面积影响程度依次为B>A>C。
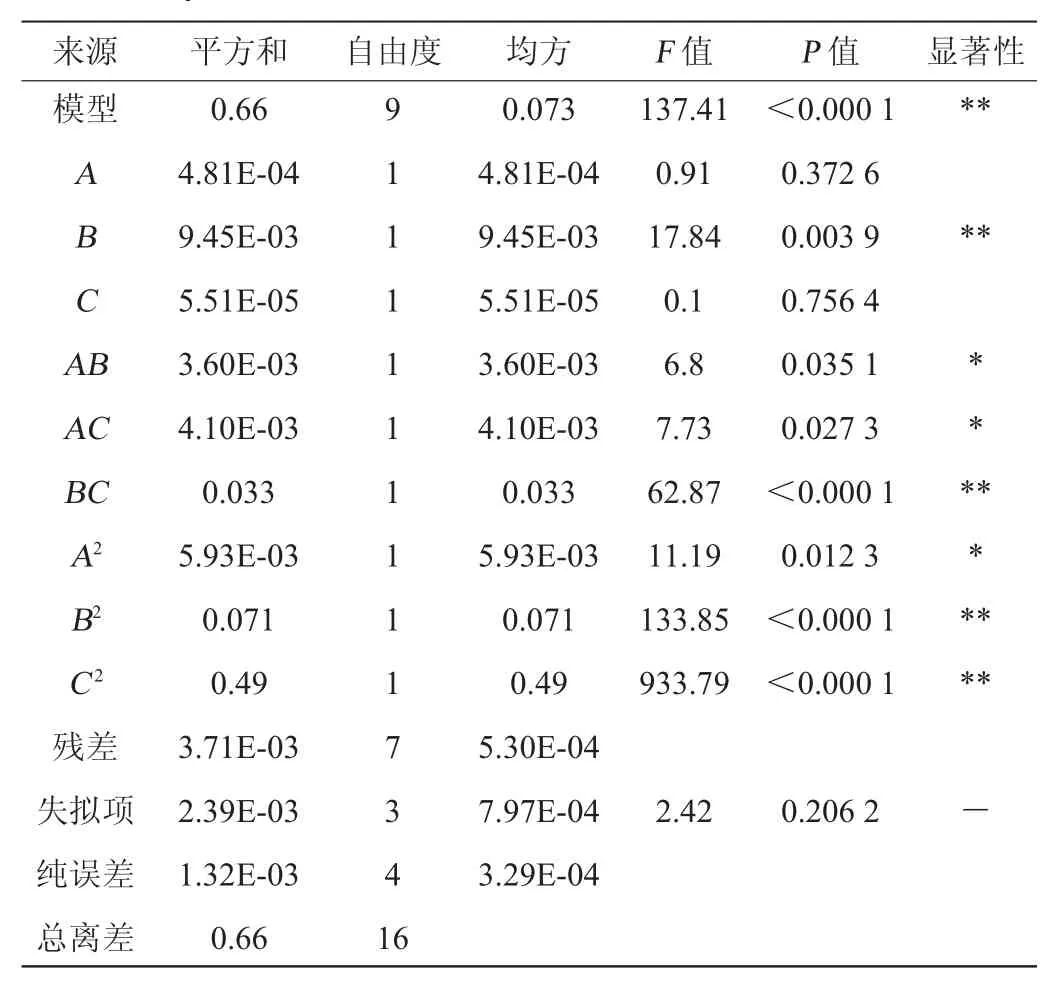
表4 霞多丽干白葡萄酒回归方程方差分析Table 4 Variance analysis of the regression equation of Chardonnay dry white wine

表5 赤霞珠干红葡萄酒回归方程方差分析Table 5 Variance analysis of the regression equation of Cabernet Sauvignon dry red wine
霞多丽干白葡萄酒和赤霞珠干红葡萄酒挥发性物质萃取时,NaCl添加量、萃取时间、萃取温度三个因素交互作用对样品中挥发性物质测定总峰面积的响应面及等高线见图4。由图4可知,曲线走势的坡度越陡,说明该因素对挥发性物质测定峰面积的影响越显著;坡度越平滑,影响则越小,三种因素两两交互作用对样品中挥发性物质测定总峰面积均有一定程度的影响。

图4 各因素交互作用对总峰面积影响的响应面和等高线Fig.4 Response surface plots and contour lines of effects of interaction between each factor on total peak area
通过对回归模型进行验证,得到霞多丽干白葡萄酒挥发性物质最适萃取条件为NaCl添加量0.259 g/mL,萃取时间34.17 min,萃取温度40.35 ℃;赤霞珠干红葡萄酒挥发性物质萃取时最适条件为:NaCl添加量为0.256 g/mL,萃取时间为35.80 min,萃取温度为39.81 ℃。在此条件下,预测总峰面积分别为1.958×1010和1.455×1010。考虑到试验可操作性,选择NaCl添加量为0.25 g/mL、萃取时间35 min和萃取温度40 ℃条件下,实际总峰面积分别为1.955×1010和1.427×1010。最适条件预测总峰面积与实际总峰面积相近,说明优化后的萃取条件具有可行性。
2.3 HS-SPME分析方法验证
由表6可知,正己醇、正己酸乙酯和辛酸标准品在利用本试验优化的最佳萃取条件下得到的保留时间相差较小,表明其稳定性良好,因此,该萃取条件结合色谱条件可以较为准确地对未知挥发性物质进行定性分析。

表6 标准品的保留时间、回归方程、相关系数、回收率Table 6 Retention time,regression equation,correlation coefficient and recovery of standard
由表6可知,正己醇、正己酸乙酯和辛酸标准品的相关系数均在0.990以上,结果表明标准曲线的线性良好,该方法能很好地对未知挥发性物质进行定量分析。相对标准偏差(RSD)反映波动的相对大小,数据之间的波动性越大,RSD也越大,一般小于2%[23]。回收率在98.3%~100.53%范围内,表明该方法准确度较高。标准品回收率试验的RSD处于0.59%~0.91%范围内,表明数据波动不大,具有良好的准确度和精密度。
3 结论
本试验基于HS-SPME-GC-MS方法,对霞多丽干白葡萄酒和赤霞珠干红葡萄酒挥发性物质的萃取条件进行了优化,并对优化后的萃取条件进行了验证。对响应面优化法获得的试验数据分析,两款样品均在NaCl添加量为0.25 g/mL,萃取时间为35 min,萃取温度为40 ℃的萃取条件下效果最佳。表明此方法具有一定的通用性。通过对优化的萃取条件进行定性和定量试验验证得出,该方法稳定性良好,准确度及精确度较高,结果表明该萃取条件试验效果较好,具有可行性。

