HPLC-MS/MS法在伊马替尼、达沙替尼与尼洛替尼治疗CML患者血药浓度监测中的应用
王 磊,孙文利,杨梓艺,刘 瑞,王红春,刘红星,2△
1.河北燕达陆道培医院,河北廊坊 065201;2.北京陆道培血液病研究院,北京100176
慢性粒细胞白血病(CML)是骨髓造血干细胞克隆性增殖形成的恶性肿瘤,占成人白血病的15%[1],全球年发病率为(1.6~2.0)/10万。中国CML患者较西方更为年轻化,国内几个地区的流行病学调查显示CML中位发病年龄为45~50岁,而西方国家CML的中位发病年龄为67岁[2-5]。CML患者常伴随BCR/ABL基因突变,而伊马替尼能特异性靶向抑制由BCR/ABL1基因编码的癌蛋白的酪氨酸激酶活性,提高了CML患者的生存率,同时伊马替尼易诱发耐药和患者不耐受。达沙替尼和尼洛替尼已经在世界范围内被批准为伊马替尼不耐受和伊马替尼耐药患者的治疗药物[6]。达沙替尼作为CML二线治疗用药,其可抑制BCR/ABL1激酶和SRC家族激酶以及多种其他肿瘤中异常活化的激酶,包括C-Kit、促红细胞生成素肝细胞(EPH)受体激酶和血小板衍生生长因子受体β(PDGFR),可克服以下原因导致的伊马替尼耐药:BCR/ABL1过表达、BCR/ABL1激酶区域突变、激活包括SRC家族激酶在内的其他信号通路和多药耐药基因过表达[7-16]。尼洛替尼是一种氨基嘧啶衍生物,与伊马替尼相比,能更加有效和选择性地抑制BCR-ABL1的未突变形式和大多数突变形式的酪氨酸激酶活性[17-22]。尼洛替尼对Ph+白血病治疗有效[19],已被批准用于伊马替尼不耐受和伊马替尼耐药的Ph+CML慢性期(CML-CP)和CML急性期(CML-AP)患者的治疗。在CML患者的酪氨酸激酶抑制剂治疗中,治疗性药物监测是一种新的剂量优化策略,以获得更快、更有效的临床疗效[20],本实验室采用高效液相色谱-串联质谱法(HPLC-MS/MS)对伊马替尼、达沙替尼和尼洛替尼进行血药浓度检测,以期获得此种药物最佳疗效和避免不良反应及治疗失败的发生。
1 材料与方法
1.1仪器与试剂 主要检测仪器:AB Sciex 4000Qtrap质谱仪(配有Shimadzu 20A色谱系统)、Analyst V1.5.2工作站(AB公司)。主要试剂:色谱甲醇(Fisher公司)、蒸馏水(广州屈臣氏)、色谱甲酸(迈瑞达科技有限公司)、色谱乙酸铵(迈瑞达科技有限公司);伊马替尼、伊马替尼-d8、达沙替尼、达沙替尼-d8、尼洛替尼、尼洛替尼-d3均为HPLC级,购自Toronto Research Chemicals公司。
1.2方法
1.2.1液相色谱及质谱条件 采用Ultimate XB-C18色谱柱(4.6 mm×50 mm,5 μm),柱温60 ℃,流速:0.8 mL/min;流动相A为0.1%甲酸甲醇溶液(A),流动相B为0.1%甲酸-2 mmol/L乙酸铵水溶液,进样量为1 μL。梯度洗脱:0.01~0.30 min,60%A;0.30~0.50 min,A相浓度线性改变至90%;0.50~0.70 min,A相浓度线性改变至100%;0.70~0.90 min,A相浓度为线性改变至90%;0.90~1.10 min,A相浓度线性改变至60%,保持1.90 min后停止。质谱条件:电喷雾电离源(ESI),正离子检测,监测模式为多反应监测模式(MRM);离子喷射电压为4 500 V;辅助加热气温度(TEM)为500 ℃;雾化气(Gas1)为55psi;辅助加热气(Gas2)为55psi;气帘气:30 psi;碰撞气压力:中等;用于定量分析的离子反应:伊马替尼 m/z 494.3→394.1,达沙替尼 m/z 488→401,尼洛替尼 m/z 530.2→289.2;各种质谱参数见表1。
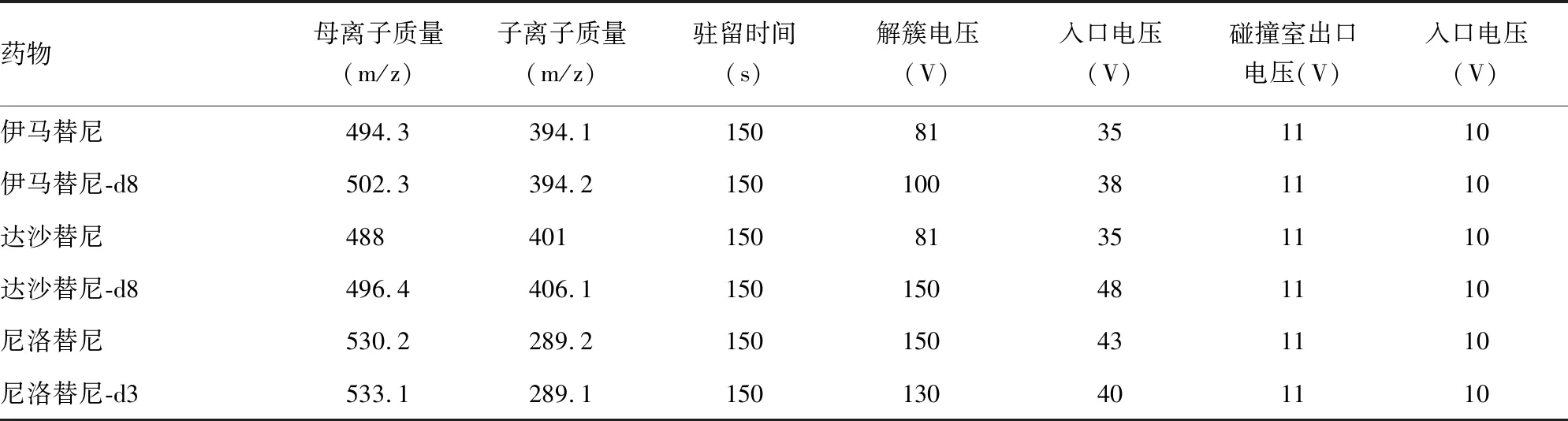
表1 质谱参数
1.2.2标准品贮备液与内标贮备液的配制 精密称取标准品伊马替尼2.500 mg、达沙替尼 1.000 mg、尼洛替尼 5.000 mg,分别置于3个小烧杯中,用适量甲醇溶解,分别转移至3个10.0 mL容量瓶中,用甲醇定容,得0.25 mg/mL伊马替尼、0.10 mg/mL达沙替尼和0.50 mg/mL尼洛替尼贮备液。然后分别用甲醇-超纯水(1∶1配制)依次稀释贮备液,得到7个梯度(1~7号)的混合标准工作液,伊马替尼标准工作液的浓度分别为0.5、1.0、2.5、5.0、10.0、20.0、25.0 μg/mL;达沙替尼的浓度分别为10、50、100、250、500、1 000、2 500 ng/mL;尼洛替尼的浓度分别为0.5、1.0、2.5、5.0、10.0、20.0、25.0 μg/mL。精密称取标准品伊马替尼-d8 1.000 mg、达沙替尼-d8 1.000 mg,尼洛替尼-d3 1.000 mg,分别置于3个小烧杯中,用适量甲醇溶解,分别转移至3个10.0 mL容量瓶中,用甲醇定容,得0.10 mg/mL伊马替尼-d8母液、0.10 mg/mL达沙替尼-d8母液和0.10 mg/mL尼洛替尼-d3母液,作为内标贮备液。分别移取各内标贮备液适量,用甲醇稀释,配成一定浓度的混合内标液使用。
1.2.3上样检测前处理 取待测标本100 μL置于1.5 mL EP管中,然后加入0.1%甲酸-2 mmol/L乙酸铵水溶液100 μL,涡旋振荡0.5 min,再加入混合内标液800 μL,涡旋振荡0.5 min,13 000 r/min离心10 min,取上清液检测。
1.2.4标准曲线的制备 分别在7个1.5 mL EP管中加入空白血浆90 μL,并加入含有各浓度梯度伊马替尼、达沙替尼和尼洛替尼的标准混合工作液10 μL;得伊马替尼浓度分别为50、100、250、500、1 000、2 000、2 500 ng/mL,达沙替尼浓度分别为1、5、10、25、50、100、250 ng/mL,尼洛替尼浓度分别为50、100、250、500、1 000、2 000、2 500 ng/mL;按“1.2.3”项下方法处理后进样检测,分别以伊马替尼/伊马替尼-d8峰面积比值(Y)对伊马替尼浓度(X),达沙替尼/达沙替尼-d8峰面积比值(Y)对达沙替尼浓度(X),尼洛替尼/尼洛替尼-d3峰面积比值(Y)对尼洛替尼浓度(X),作线性回归分析,得到伊马替尼、达沙替尼和尼洛替尼检测的标准曲线。
1.2.5回收率、精密度试验 分别在3个1.5 mL EP管中加入空白血浆90 μL,并加入含有伊马替尼、达沙替尼和尼洛替尼的2、3、5号标准混合工作液各10 μL;得伊马替尼的浓度分别为100、250、1 000 ng/mL,达沙替尼的浓度分别为5、10、50 ng/mL,得尼洛替尼的浓度为100、250、1 000 ng/mL;按“1.2.3”项下方法处理后进样测定,各浓度日内重复测定5次,计算相对回收率及日内精密度,并连续测定5 d以计算日间精密度,精密度以相对标准偏差(RSD)表示。
1.2.6稳定性试验 分别在3个1.5 mL EP管中加入空白血浆90 μL,并加入含有伊马替尼、达沙替尼和尼洛替尼2、3、5号标准混合工作液各10 μL;得伊马替尼浓度分别为100、250、1 000 ng/mL,达沙替尼浓度分别为5、10、50 ng/mL,伊马替尼浓度分别为100、250、1 000 ng/mL;取1批标本按“1.2.3”项下方法处理后置于4 ℃自动进样器中,放置72 h后分别测定各标本的浓度;其余标本于4 ℃冰箱中放置72 h后取出放至室温,然后按“1.2.3”项下方法处理后进样测定,考察其稳定性。
1.2.7临床应用 收集2015年11月至2018年5月于河北燕达陆道培医院服用伊马替尼、达沙替尼和尼洛替尼治疗的CML患者血浆标本共530例,其中伊马替尼治疗患者标本249例,达沙替尼治疗的患者标本278例,尼洛替尼治疗的患者标本3例。纳入研究的患者均肝肾功能均正常,自愿签署了知情同意书;伊马替尼和达沙替尼均为1天1次给药,而尼洛替尼为1天2次给药。临床标本采集时间为患者下一次服药前,采集静脉血3 mL,混匀,EDTA抗凝,对由于抽血错误和服药错误导致的异常值标本予以剔除。室温(20~25 ℃)下标本存放时间不超过4 h,当日进行HPLC-MS/MS法检测。
2 结 果
2.1色谱质谱行为 伊马替尼-d8、达沙替尼-d8、尼洛替尼及尼洛替尼-d3二级碎片离子质谱图,见图1。伊马替尼、达沙替尼和尼洛替尼质谱色谱图见图2,血中没有物质干扰伊马替尼、达沙替尼和尼洛替尼的测定,出峰时间分别是1.72、2.15、2.64 min,各个峰型良好,可采用面积定量。
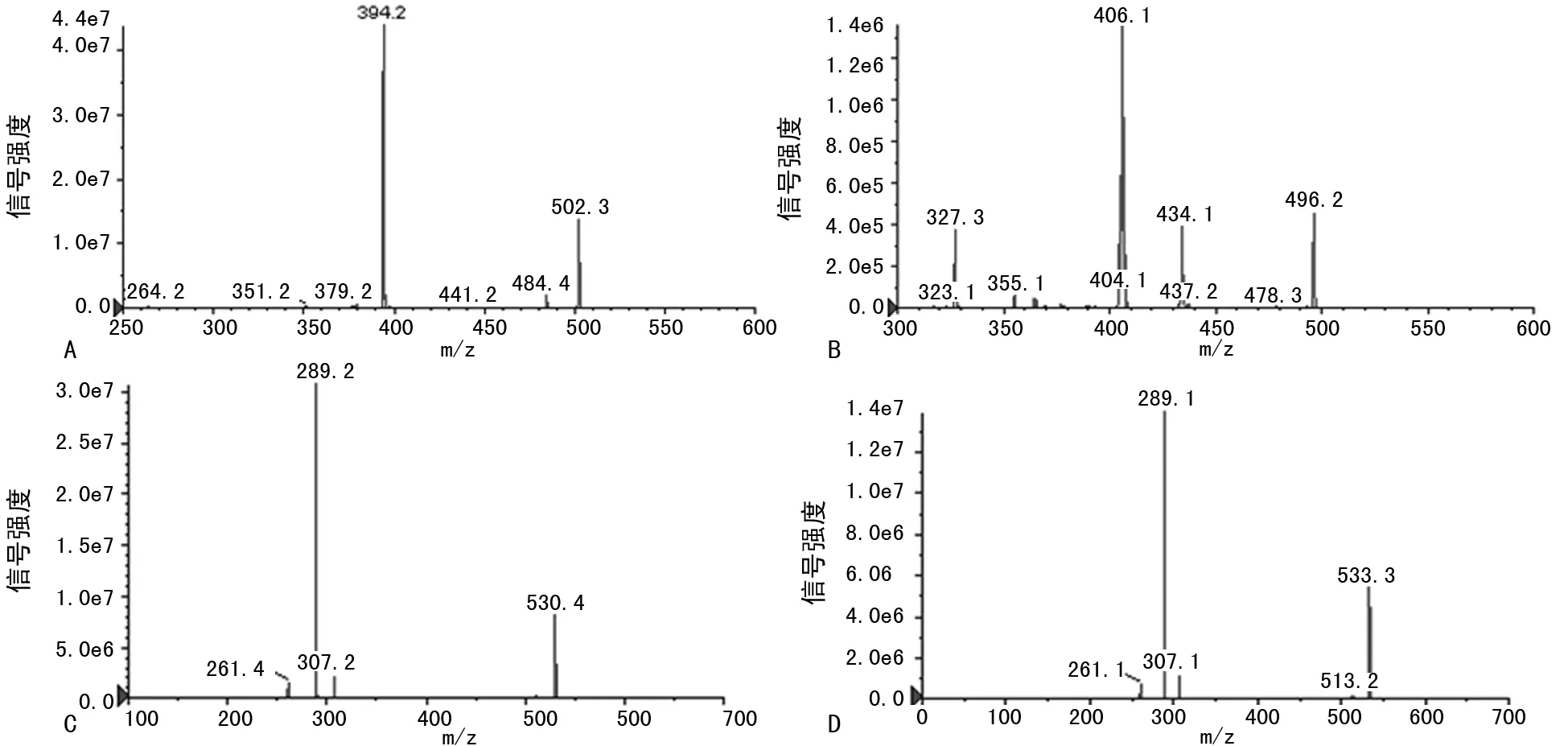
注:A为伊马替尼-d8;B为达沙替尼-d8;C为尼洛替尼;D为尼洛替尼-d3。
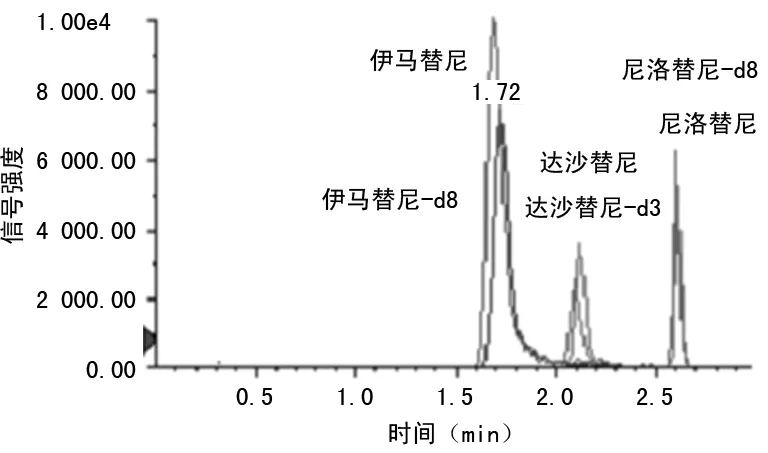
图2 伊马替尼、达沙替尼和尼洛替尼质谱色谱图
2.2标准曲线 伊马替尼标准曲线回归方程:Y=0.001 17X+0.006 17(r=0.999 5),表明伊马替尼在50~2 500 ng/mL线性关系较好,可用于定量,其最低定量限为5 ng/mL;达沙替尼标准曲线回归方程:Y=0.013 7X+0.000 435(r=0.999 2),表明达沙替尼在1~250 ng/mL线性关系较好,可用于定量;尼洛替尼的回归方程:Y=1.1e+0.03X+1.05e+0.04(r=0.998 5),表明尼洛替尼在50~2 500 ng/mL线性关系较好,可用于定量。见图3。
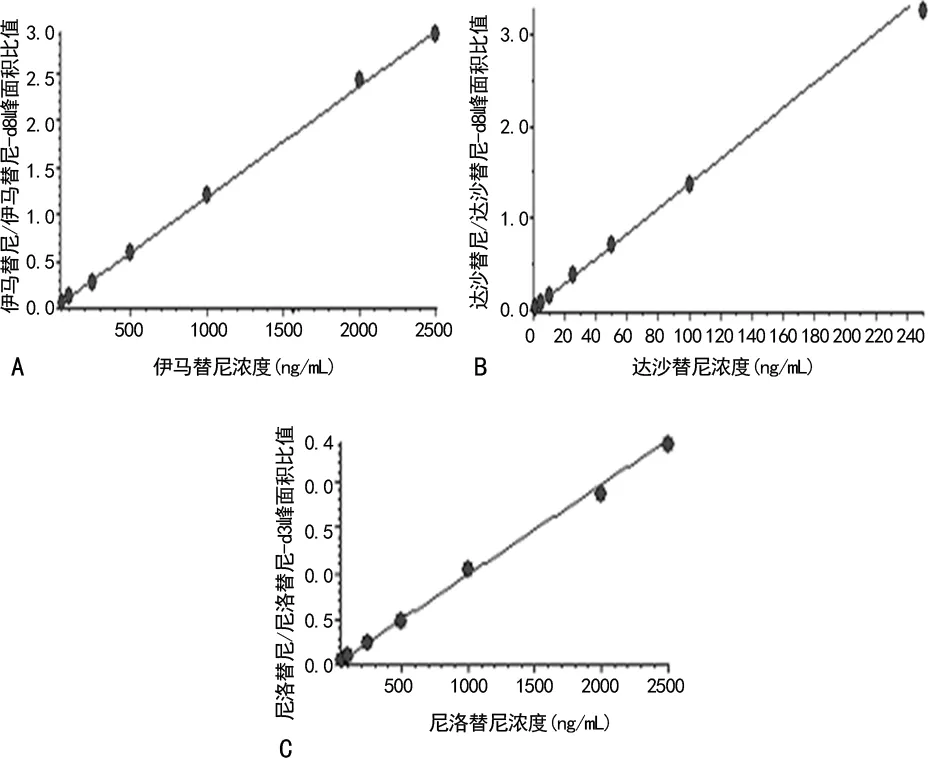
注:A为伊马替尼;B为达沙替尼;C为尼洛替尼。
2.3方法学评价 伊马替尼、达沙替尼和尼洛替尼的相对回收率和日内、日间精密度见表2。伊马替尼、达沙替尼和尼洛替尼的相对回收率在90.0%~110.0%,日内及日间精密度RSD均小于5%,表明该方法的准确度和重复性均较好。
表2 回收率和精密度试验结果
2.4稳定性考察结果 在4 ℃条件下,血浆标本/处理后的血浆标本放置72 h后,伊马替尼、达沙替尼和尼洛替尼浓度均基本保持不变,在此条件下测定CML患者血浆中伊马替尼、达沙替尼和尼洛替尼浓度的稳定性良好,见表3。
表3 稳定性考察结果
2.5临床应用结果 伊马替尼血药浓度为1 400(1 030~1 845)ng/mL,符合伊马替尼有效谷浓度>1 000 ng/mL的要求,有个别几例患者检测结果偏高,易产生急性毒性,与临床符合。达沙替尼血药浓度为7(3~14)ng/mL,符合达沙替尼100 mg每日1次给药谷浓度<2.5 ng/mL的要求,其不良反应较小;峰浓度>50 ng/mL,表明达沙替尼吸收较好,有效。尼洛替尼3例,结果均在线性范围内。见图3。由此可见,建立的HPLC-MS/MS法能满足临床对伊马替尼、达沙替尼和尼洛替尼血药浓度检测的需求。
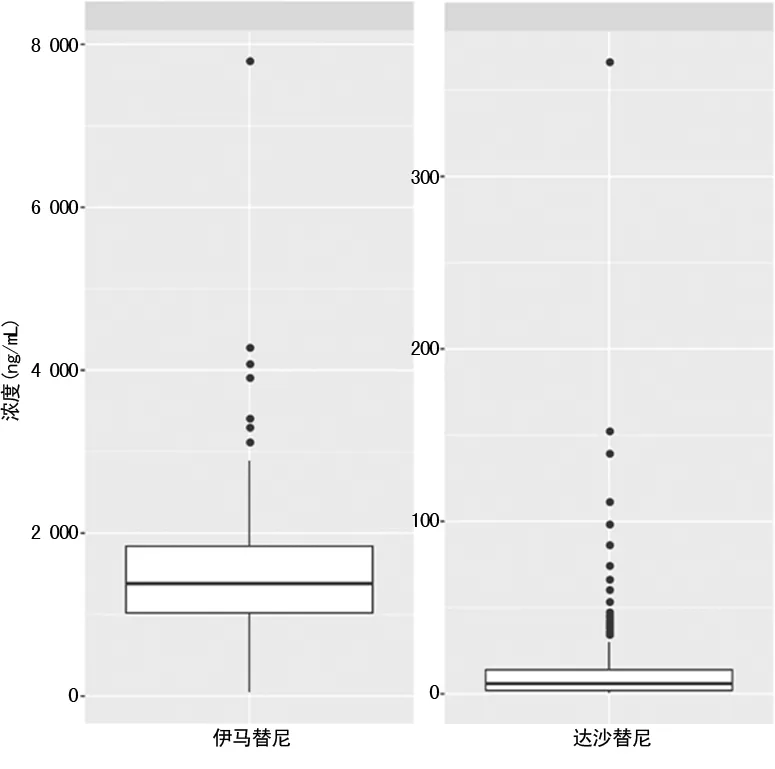
图4 血药浓度结果箱式图
3 讨 论
伊马替尼和达沙替尼二级碎片离子质谱图详见王磊等[22]的前期研究。本实验采用HPLC-MS/MS法同时检测伊马替尼、达沙替尼和尼洛替尼,前处理采用甲醇蛋白沉淀,高速离心的方法去除蛋白,各峰型良好,出峰时间短,3 min内各检测物均被检测。另外采用同位素内标法定量,可最大限度避免基质效应的影响。该方法检测灵敏度高、准确度好,可满足临床对CML患者血药浓度检测的需求。
酪氨酸激酶抑制剂的药物浓度监测仍处于初级阶段,但已经积累的证据表明,基于药物动力学指标的剂量调整对大多数CML患者接受酪氨酸激酶抑制剂治疗有益[20]。CML患者酪氨酸激酶抑制剂血药浓度监测结合BCR-ABL监测,能更好地实现CML患者的无病生存,提高CML患者的生存率[21-22]。进行酪氨酸激酶抑制剂血药浓度检测有助于保证治疗效果,另外,还可以避免不良反应,能为适时减少剂量提供参考依据,一定程度上减轻患者经济负担。本课题组建立的HPLC-MS/MS法可同时检测一代和二代酪氨酸激酶抑制剂,有助于CML患者合理使用药物,避免药物剂量不足导致的疗效欠佳和剂量过大导致的毒性反应;同时,还有助于避免耐药的发生,可为患者更换酪氨酸激酶抑制剂提供参考。酪氨酸激酶抑制剂血药浓度检测有望被临床纳入日常血药浓度监测的范围,尤其对长期服用酪氨酸激酶抑制剂的CML患者尤为重要。

