替吉奥联合顺铂同步放化疗与单纯放疗治疗局部中晚期食管癌疗效比较
翟玉洁 苏毅鹏
1.滨州医学院附属医院肿瘤科,山东滨州 256600;2.滨州医学院附属医院神经内科,山东滨州 256600
食管癌约占消化道肿瘤的7%[1]。每年全世界大约有30 万人死于食管癌,各国食管癌的发病率和死亡率差异很大。我国是食管癌的高发地区[2],目前食管癌的发病率占我国恶性肿瘤的第5 位,死亡率占第4 位[3],每年平均病死约15 万人[4]。食管黏膜下层富含淋巴管,且缺乏浆膜层,容易出现淋巴结及远处转移,预后较差[5]。男多于女,发病年龄多超过45岁,大约30%~40%的患者是70 岁以上的老年人[6]。局部中晚期的食管癌患者采用同步放化疗是否获益及是否耐受是目前国内食管癌研究的重点。本研究对局部中晚期食管癌采用替吉奥联合顺铂同步放化疗与单纯放疗的疗效及安全性进行比较观察。
1 资料与方法
1.1 一般资料
回顾性分析2016 年6 月~2019 年6 月我科收治的食管癌患者。入选患者均满足以下条件:(1)所有患者组织病理学证明均为食管鳞癌(均采用第6 版2002 UICC 分段分期标准);(2)未接受化疗及放疗、靶向治疗等一切抗肿瘤治疗;(3)无手术指征患者;(4)治疗前无食管穿孔及出血,无明显的气管侵犯;(5)钡餐造影病变长度≤10cm;(6)ECOG评分0 ~2 分;(7)能进食流质或半流质食物;(8)均接受顺铂联合替吉奥同步放化疗或单纯放疗治疗。排除标准:(1)合并其他部位恶性肿瘤;(2)合并严重的糖尿病、高血压,心、肺、肝、肾等主要器官功能障碍患者;(3)有明显溃疡、食管穿孔及出血患者;(4)接受手术及单纯化疗患者;(5)有远处转移患者;(6)妊娠期或哺乳期。共41 例食管癌患者符合条件纳入研究,男29 例,女12 例;病变部位:颈段2 例,胸上段15 例,胸中段11 例,胸下段13 例;病变长度:≤5cm 19 例,>5cm 22 例;有溃疡20例,无溃疡21例;Ⅱ期 3例,Ⅲ期 33例,Ⅳa期 5例。其中替吉奥联合顺铂同步放化疗组20 例,单纯放疗组21 例。见表1。
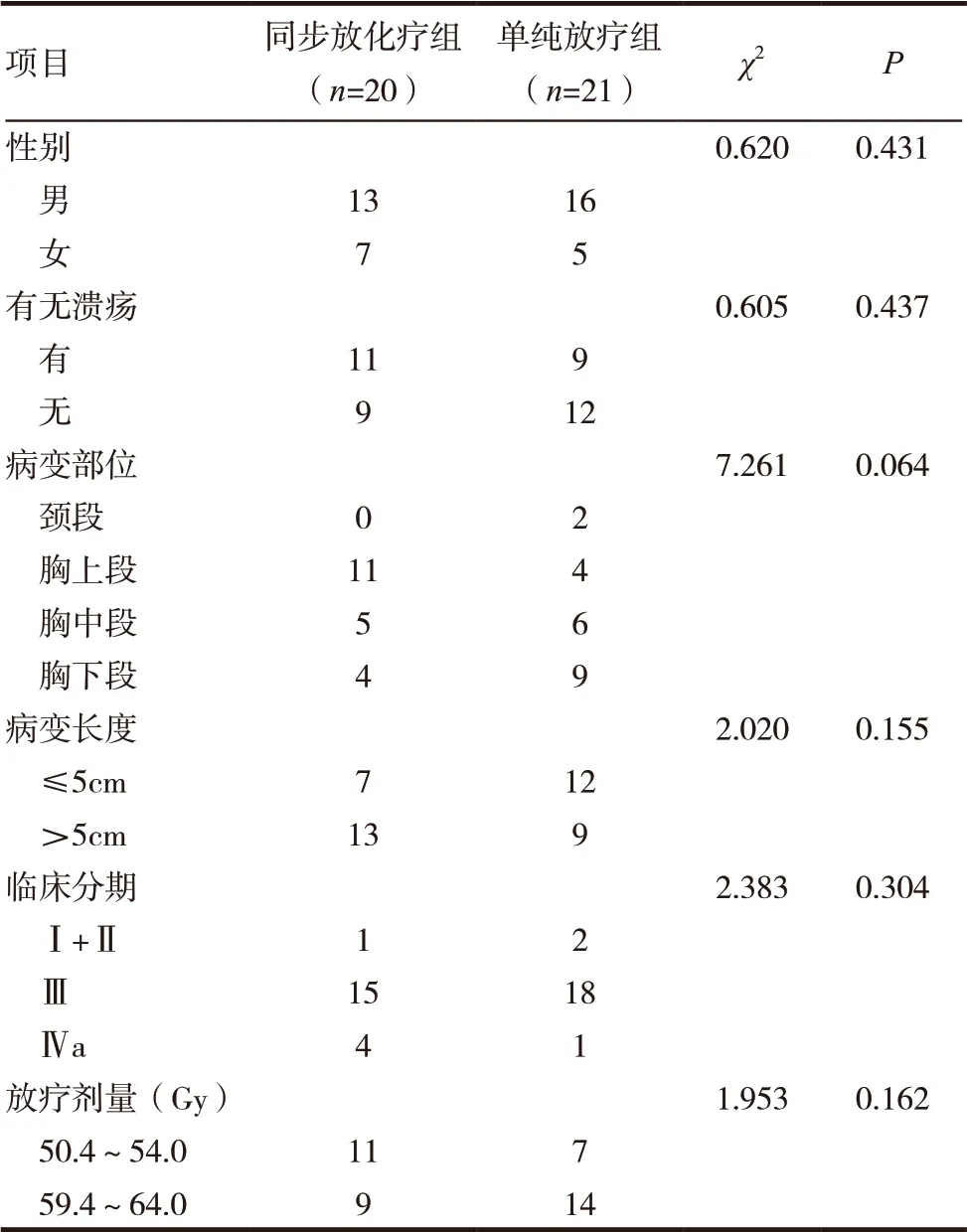
表1 同步放化疗组及单纯放疗组患者临床资料特征
1.2 治疗方法
1.2.1 放疗 仰卧位,热塑体膜固定体位,激光灯系统确定体表标志点,轴位CT 增强扫描定位,5mm/层,扫描范围:上界至环甲膜,下界至腹腔干下缘。传输图像至TPS 计划系统。肿瘤靶体积(gross tumor volume,GTV):根据上消化道钡餐、胸部CT 及MR 等影像学检查确定的食管部位,同时结合胃镜检查可见的肿瘤长度;转移淋巴结(GTVnd),以影像学检查为准。临床靶体积(clinical target volume,CTV):在GTV 基础上下各外扩3cm,左右前后方向均外扩0.8cm,需包括相应的高危淋巴引流区,外扩后解剖屏障进行适当的调整;GTVnd 基础上均匀外扩0.5cm 为CTVnd。计划靶体积(planning target volume,PTV):在CTV 基础上均匀外扩0.5cm 为PTV。采用调强适形放射治疗技术,瓦里安TRILOGY、23EX 医用直线加速器6MV X 线外照射,常规分割,5 次/周。放疗剂量:DT 50.4 ~64.0Gy。危及器官受量限制:双肺:V5 <65%,V20 <30%,V30 <20%,双肺平均剂量<17Gy;脊髓:最大点剂量<45Gy;心脏:V30<40%,平均剂量<26Gy。
1.2.2 化疗 化疗方案采用替吉奥联合顺铂方案:替吉奥(齐鲁制药有限公司,H20100151)80mg/m2分两次口服,第1 ~14 天,联合顺铂(齐鲁制药有限公司,H37021357)75mg/m2分3d 使用,第1 ~3天,21d 为1 个周期。于放疗开始第1 天应用,放疗结束后对一般情况好、疗效评定有效的患者,继续行2 个周期替吉奥单药巩固化疗。治疗期间常规每周检测血常规,出现Ⅰ级骨髓抑制时给予口服升白升血小板药物,Ⅱ级及以上骨髓抑制时给予重组人粒细胞刺激因子、白介素-11 治疗。对于放射性食管炎患者,轻者观察,重者给予应用激素、口服黏膜麻醉剂及止痛药物、鼻饲,甚至暂停放疗。
1.3 疗效评价
放疗结束后1 ~3 个月左右行食管钡餐、颈胸腹部CT 检查评价食管癌近期疗效。参照食管钡餐造影分级法和RECIST 标准,食管癌近期疗效分为完全缓解(CR)、部分缓解(PR)和无缓解(NR)。总有效率为(CR+PR)例数/总例数×100%。治疗期间定期复查血常规及肝功生化。记录患者的不良反应,包括骨髓抑制(白细胞减少、贫血、血小板减少)及放射性食管炎的发生情况。骨髓抑制的分级采用世界卫生组织抗癌药物急性与亚急性毒性反应分级标准,分0 ~Ⅳ级来评价。放射性食管炎的分级采用美国放射治疗肿瘤协作组急性放射损伤分级标准,分0 ~Ⅳ级来评价。
1.4 统计学处理
本研究数据均应用SPSS22.0 统计软件进行统计学处理,计数资料以率(%)表示,采用χ2检验,P <0.05 为差异有统计学意义。
2 结果
2.1 两组患者近期疗效比较
治疗结束1 ~3 个月疗效评价。单纯放疗组完全缓解(CR)+部分缓解(PR)的患者有9 例,无缓解(NR)的患者12 例,有效率为42.8%(9/21);同步放化疗组完全缓解(CR)+部分缓解(PR)的患者为10 例,无缓解(NR)的患者10 例,有效率为50.0%(10/20),差异无统计学意义(P >0.05)。见表2。
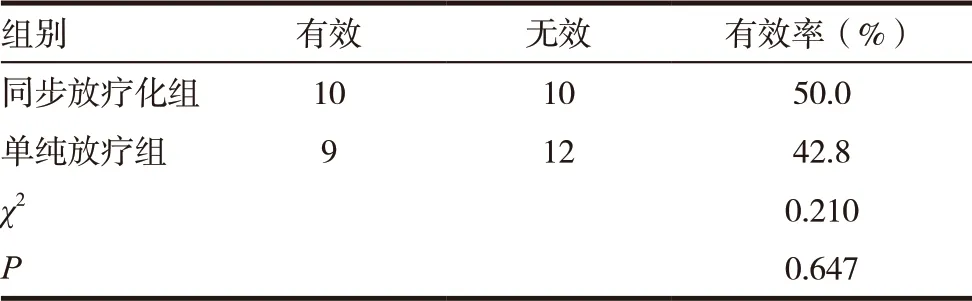
表2 同步放化疗组及单纯放疗组有效率比较
2.2 两组不良反应比较
同步放化疗组和单纯放疗组的白细胞减少发生率分别为90.0%和52.4%,前者高于后者,差异无统计学意义(χ2=7.799,P >0.05);两组血小板减少的发生率分别为25%和21%,差异无统计学意义(χ2=4.103,P >0.05);两组贫血的发生率分别为25% 和38.1%,差异无统计学意义(χ2=2.453,P >0.05)。两组放射性食管炎的发生率分别为75%和80.9%,以1、2 级放射性食管炎为主,差异无统计学意义(χ2=2.221,P >0.05)。见表3。
3 讨论
早期食管癌首选的治疗方法是手术治疗,术后5 年生存率达90%。单纯手术治疗的ⅡA ~Ⅲ期的食管鳞癌患者术后5 年生存率在20%~34%,术后90%的患者出现复发或远处转移[7-9]。手术与放化疗联合应用的综合治疗是局部中晚期食管癌的理想治疗模式[10-11]。由于起病隐匿,大部分患者就诊时已属中晚期,失去根治性手术治疗机会[12]。晚期患者可采取单纯放疗或同步放化疗的治疗模式[13-14]。手术或放化疗等治疗方式的治愈率<25%,主要的失败原因是局部未控、复发或远处转移。RTOG8501 试验结果显示采用同步放化疗的局部中晚期食管癌患者5 年生存率(27%)明显优于单纯放疗[15-16]。RTOG9405 试验将放疗剂量增加到64.8Gy,中期评价时,由于生存率改善不明显而提前结束。2011 年NCCN 指南将同步放化疗作为不可手术切除食管癌的治疗方式[17]。顺铂联合氟尿嘧啶(PF)被认为是食管癌化疗主要方案之一[18]。大量Ⅲ期临床试验以同期放化疗为标准治疗方案的也多采用PF 方案。对于老年食管癌患者,局部放疗同步替吉奥单药治疗和放疗结束后替吉奥单药维持化疗,能够产生生存获益并且毒副反应可耐受[19]。替吉奥是一种口服氟尿嘧啶衍生物,由替加氟、吉美嘧啶、奥替拉西钾组成的复方制剂。研究表明,口服替吉奥后增加双氢嘧啶脱氢酶抑制酶活性,增加了氟尿嘧啶浓度,其半衰期显著延长[20]。该回顾性研究中同步放化疗组采用顺铂联合替吉奥,在两组患者不良反应的观察中,骨髓抑制及放射性食管炎的发生率均无差异。
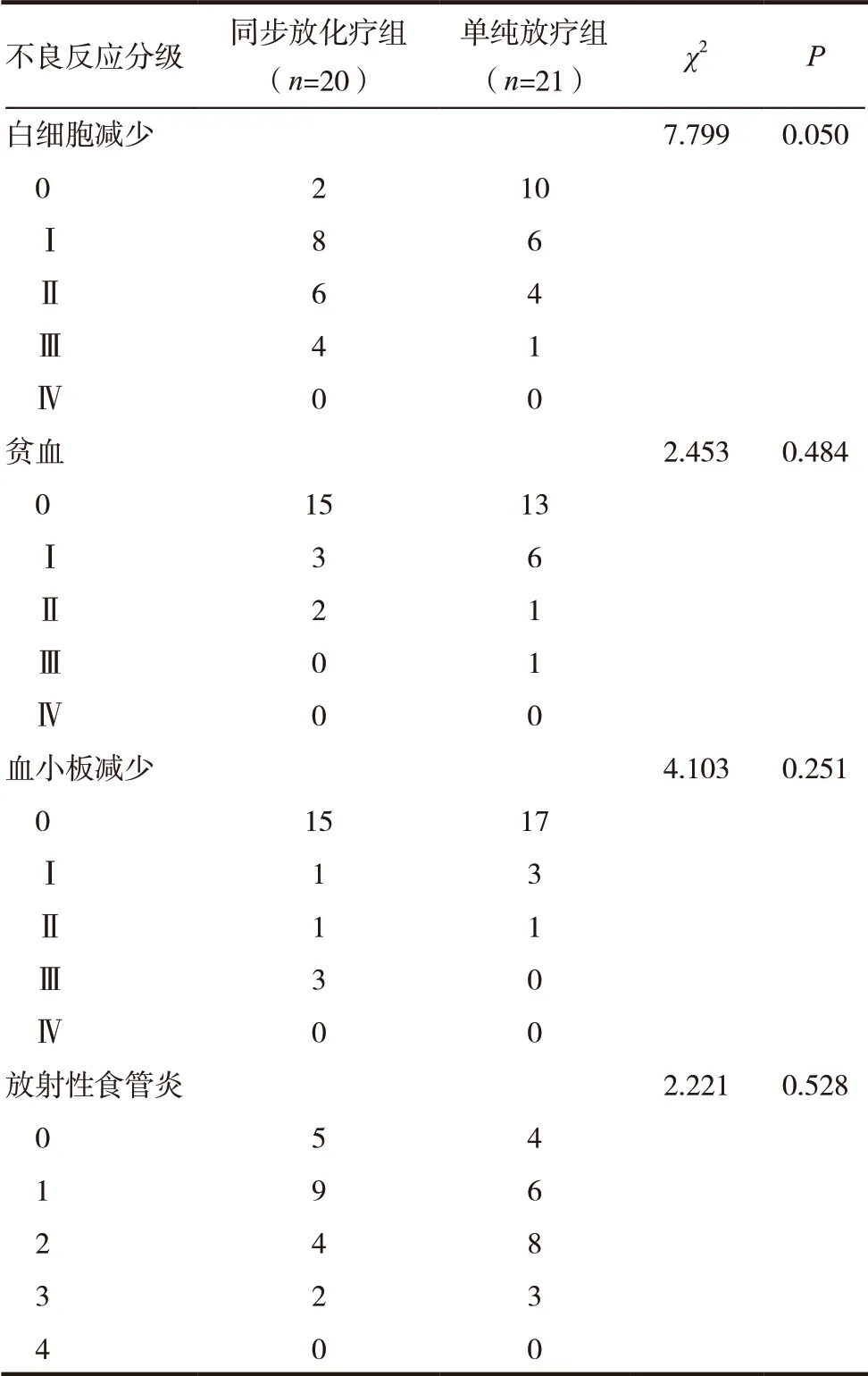
表3 同步放化疗组及单纯放疗组不良反应比较
但是RTOG8501 试验中入选的多为Ⅱ期患者,研究人种多为白种人和黑人,放疗剂量偏低,食管腺癌所占比例高于我国,老年患者仅占26%,因此上述经验难以完全借鉴[21]。
近年来国内开展多项食管癌同步放化疗在安全性及有效性方面的临床研究,其结论并非完全一致。王军等[22]发现同步放化疗可显著提高食管鳞癌患者的近期疗效及1、3、5 年生存率,但副反应如≥3 级放射性食管炎、>2 级放射性肺炎及>3 级骨髓抑制等发生率也明显增加。因此认为同步放化疗适用于我国非手术治疗的食管鳞癌患者。然而,谭立君等[23]发现同期放化疗与单纯放疗相比并未提高总生存(OS)和无进展生存(PFS),放疗50.0 ~ 59.9Gy 同步化疗与同剂量单纯放疗相比提高了OS(P=0.030),但与高剂量60 ~70Gy 同步化疗相比OS 却未提高。对评估无法接受或不能完成同步放化疗者,可采取3DRT 技术放疗60 ~70Gy,从而保证患者能获得根治剂量的放疗而延长生存时间。王利利等[24]发现并非所有≥70 岁的老年食管癌患者同步放化疗均能带来生存获益,获益人群主要集中在70 ~75 岁年龄段。本研究提示同步放化疗组与单纯放疗组患者的近期疗效无差异,与国内部分研究结果一致,考虑原因在于同步放化疗组中部分患者的放疗剂量为DT50.4Gy,而单纯放疗组中的放疗剂量大部分高于前者,故推测放疗剂量的提高可能对近期疗效有一定的影响。但是RTOG 试验研究发现提高放疗剂量至DT64.8Gy 试图减少局部复发率,但研究发现高剂量组并未提高局控率及远期生存率。同时在局部进展期食管癌种同步放化疗与单纯放疗在远期生存率方面有无差异需进一步随访分析。根据本研究结果提示针对部分食管癌患者无法完成同步放化疗或拒绝化疗的患者采用单纯放疗的治疗方案也是有临床获益的。因此不能手术的局部中晚期食管癌最佳治疗模式的选择、放疗剂量等仍需进一步探索研究。
近年来,随着科学技术的发展,放射治疗的模式发生了很大的改变,放射治疗已由传统治疗模式转为精确治疗模式,最大限度地提高肿瘤组织的放射剂量,尽最大可能保护周围正常组织,减少了放射治疗的副作用。而同步放化疗则是利用放射治疗与全身化疗的互补协同作用,提高局部的控制率,减少远处转移,增加生存,从而提高临床疗效。本研究提示同步放化疗组与单纯放疗近期疗效并无差异,但由于本研究病例数偏少,且是回顾性分析,因此还需要大样本及随机对照试验研究,进一步评价疗效并延长随访。因此目前国内局部中晚期食管癌选择同步放化疗还是单纯放疗的治疗模式不能一概而论,仍需进一步对大宗病例研究及生存期、复发率的随访统计,进一步选择出同步放化疗的优势人群,延长及提高我国局部中晚期食管癌患者的生存时间及生活质量。

