虎掌南星生品及不同炮制品指纹图谱和5种核苷类成分含量的比较研究
曹淼淼 朱建光 张振凌 杜莉杰 杨佳宁


摘 要 目的:建立虎掌南星生品及不同工藝炮制品的指纹图谱,并测定其中5种核苷类成分的含量,比较生品与不同炮制品之间成分的差异。方法:分别以虎掌南星生品、河南省中药饮片炮制规范制品(简称“《规范》炮制品”)和产地加工炮制一体化新工艺炮制品(简称“一体化新工艺炮制品”)(各12份)为考察样品,采用高效液相色谱(HPLC)法进行分析[色谱柱为SymmetryShield RP18,流动相为乙腈(A)-0.1%乙酸(B)水溶液(梯度洗脱),流速为0.8 mL/min,柱温为30 ℃,检测波长为270 nm,进样量为15 ?L]。应用《中药色谱指纹图谱相似度评价系统》(2004A版)软件分别建立3种虎掌南星样品的HPLC指纹图谱并进行相似度评价;通过与对照品图谱比较对色谱峰进行指认。同时,对其中5种核苷类成分(腺嘌呤、次黄嘌呤、尿苷、黄嘌呤、肌苷)进行定量分析,并采用SPSS 21.0软件对36份样品进行聚类分析。结果:指纹图谱及含量测定的方法学考察结果均符合相关要求。3种样品与其各自对照指纹图谱的相似度均大于0.990。在虎掌南星生品中确定了22个共有峰,在2种炮制品中均确定了16个共有峰(2种炮制品中消失的6个峰相同);指认出了3种样品中均含有的5种核苷类成分,分别为腺嘌呤(3号峰)、次黄嘌呤(7号峰)、尿苷(8号峰)、黄嘌呤(9号峰)、肌苷(11号峰)。含量测定结果显示,2种炮制品中5种核苷类成分的总含量均降低,总含量高低排序为生品>一体化新工艺炮制品>《规范》炮制品。聚类分析结果显示,36份样品可聚为2类,其中生品单独聚为一类,2种炮制品聚为另一类。结论:本研究建立的方法稳定、可行,可用于虎掌南星生品及不同炮制品的质量评价。虎掌南星经炮制后指纹图谱发生了明显变化,5种核苷类成分的总含量均降低,但一体化新工艺炮制品中总含量略高于《规范》炮制品。
关键词 虎掌南星;指纹图谱;含量测定;炮制工艺;核苷类成分;聚类分析
ABSTRACT OBJECTIVE: To establish the fingerprint of raw products and different processed products of Pinellia pedatisecta, to determine the contents of 5 kinds of nucleosides, and to compare the differences of components between the raw products and processed products. METHODS: P. pedatisecta raw products, processed products by Processing Standard of Chinese Medicine in Henan Province (called “Standard processed product” for short) and processed products by new integrated processing technology in the production area (called “new integrated processed product” for short) were collected as investigation objects (12 batches of each). The determination was performed on SymmetryShield RP18 column with mobile phase consisted of acetonitrile (A)-0.1% acetic acid aqueous water solution (B) (gradient elution) at the flow rate of 0.8 mL/min, with the column temperature of 30 ℃, the detection wavelength of 270 nm, and the injection volume of 15 ?L. HPLC fingerprints of 3 kinds of P. pedatisecta samples were established by using Similarity Evaluation System of TCM Chromatographic Fingerprints (2004 A version) , and the similarity of fingerprints was evaluated. The chromatographic peaks were identified by comparing with the reference chromatogram. Five nucleosides (adenine, hypoxanthine, uridine, xanthine, inosine) were quantitatively analyzed. SPSS 21.0 software was used for cluster analysis of 36 batches of samples. RESULTS: The results of fingerprint and content determination met the relevant requirements. The similarity of 3 kinds of sample with their control fingerprint were all greater than 0.990. There were 22 common peaks in the raw products of P. pedatisecta, and 16 common peaks were identified in the 2 kinds of processed products (the same 6 peaks disappeared from 2 kinds of processed products). Five components were identified in 3 kinds of samples, such as adenine (peak 3), hypoxanthine (peak 7), uridine (peak 8), xanthine (peak 9) and inosine (peak 11). Results of content determination showed that total contents of 5 kinds of nucleosides in 2 kinds of processed products were all decreased; the contents of them in descending order was raw product>new integrated processed products>Standard processed products. Results of cluster analysis showed that 36 batches of samples could be clustered into 2 categories, i.e. raw product was clustered into one category and 2 kinds of processed products into other one. CONCLUSIONS: Established method is stable, feasible and suitable for the quality evaluation of raw products and different processed products of P. pedatisecta. Fingerprints have changed significantly and the total content of 5 kinds of nucleosides in P. pedatisecta are all decreased after processing, but that of new integrated processed products is slightly higher than that of Standard processed products.
KEYWORDS Pinellia pedatisecta; Fingerprint; Content determination; Processing technology; Nucleosides; Cluster analysis
虎掌南星系天南星科半夏属植物掌叶半夏(Pinellia pedatisecta Schott)的干燥块茎,具有燥湿化痰、祛风解痉、消痞散结的作用[1],河南禹州、河北安国等地为其主要道地产地[2]。虎掌南星中的主要化学成分包括生物碱类[3]、多糖类[4]、核苷类[5]、凝集素类[6-7]和氨基酸类[8],具有祛痰[9]、抗衰老[10]、鎮静[11]、镇痛[12]、抗白血病[13]、抗肿瘤[14]等药理作用,临床上常用于治疗冠心病、免疫疾病和多种癌症。其中的核苷类成分属于广义的生物碱,在虎掌南星中含量较高且药理作用明显[15]。虎掌南星生品有毒,炮制后不仅可降低其毒性、增强其祛痰作用,还可延长戊巴比妥钠致小鼠睡眠的时间[16],并且炮制后还具有促进凝血作用[17]。目前,2015年版《中国药典》(一部)尚未收载此药材或其炮制品,但在《河南省中药饮片炮制规范》(2005年版)(以下简称“《规范》”)[18]中收载有制虎掌南星。按照《规范》中记载,制虎掌南星是以虎掌南星生品(鲜品经除杂、去皮、洗净、干燥等产地加工后所得)为原材料进行加工炮制,且在炮制过程中需多次用水浸泡,这可能会造成水溶性有效成分(如核苷类成分等)流失,从而影响其药效。
目前,国内有关制虎掌南星的报道多是由虎掌南星生品加工炮制而成,而由虎掌南星鲜品直接加工炮制的相关研究甚少,且未见不同炮制工艺对虎掌南星中核苷类成分含量影响的报道,炮制前后化学成分结构及含量的变化也未明确。本课题组前期建立了产地加工炮制一体化新工艺(以下简称“一体化新工艺”),该工艺则以虎掌南星鲜品为原材料直接进行炮制,减少了传统炮制工艺中繁琐的浸泡等水处理过程[19]。因中药指纹图谱是对中药物质群整体作用的反映,能够成为中药自身的“化学条形码”,是一种综合分析多种成分的有效手段,可为药材的分类和饮片质量提供参考[20]。因此,本研究在前期研究基础上,进一步通过建立虎掌南星生品及不同工艺炮制品的高效液相色谱(HPLC)指纹图谱,对其中5种共有的核苷类成分进行含量测定,并结合聚类分析,探究虎掌南星生品及不同炮制品之间的成分差异,为其炮制工艺的优化提供参考。
1 材料
1.1 仪器
LC-20AD型HPLC仪(日本Shimadzu公司);PS224S型万分之一天平(北京赛多利斯科学仪器有限公司);YP10002型电子天平(上海衡际科学仪器有限公司);GTR16-2型高速离心机(北京时代北利离心机有限公司);KQ-500DV型数控超声波清洗机(昆山市超声仪器有限公司);DTC-22型隔膜真空泵(巩义市英峡予华仪器厂);UPT-Ⅱ-10T型优普系列超纯水器(成都超纯科技有限公司);HH-6型数显恒温水浴锅(上海比朗仪器有限公司)。
1.2 药品与试剂
虎掌南星新鲜药材购自河南华夏药材有限公司(批号:20191017,产地:河南禹州),经河南中医药大学药学院生药教研室陈随清教授鉴定为天南星科半夏属植物掌叶半夏(P. pedatisecta Schott)的新鲜块茎;腺嘌呤对照品(批号:PS020156,纯度:≥98%)、次黄嘌呤对照品(批号:PS020061,纯度:≥98%)、尿苷对照品(批号:PS010290,纯度:≥98%)、黄嘌呤对照品(批号:PS020191,纯度:≥98%)、肌苷对照品(批号:PS010437,纯度:≥98%)、尿嘧啶对照品(批号:PS020117,纯度:≥98%)、鸟苷对照品(批号:PS020191,纯度:≥98%)、腺苷对照品(批号:PS020195,纯度:≥98%)、胸腺嘧啶对照品(批号:PS020196,纯度:≥98%)均购自成都普思生物科技股份有限公司;乙酸、乙腈、甲醇为色谱纯,其余试剂均为分析纯,水为双蒸水。
2 方法与结果
2.1 虎掌南星生品及炮制品的制备
2.1.1 生品 取同一批虎掌南星鲜品12份,每份100 g,洗净,去除外皮和须根,挖出芽点,晒干,用水润透,切片,烘干,即为传统加工生品(样品编号为S1~S12)。
2.1.2 《规范》炮制品 取同一批虎掌南星生品12份(取鲜品,按“2.1.1”项下方法制备而得,下同),每份100 g。参照《规范》中虎掌南星项下炮制方法进行炮制[18]:用水浸泡,每日换水2~3次,泡至切开口尝微有麻辣感时取出,再与捣碎的生姜(12 g)、白矾(12 g)同入锅内,加水适量煮至内无白心,取出,晾至六成干,切薄片,干燥,即得(样品编号为C1~C12)。
2.1.3 一体化新工艺炮制品 取同一批虎掌南星鲜品12份,每份100 g。按照前期建立的产地加工炮制一体化新工艺方法进行炮制[19]:先取白矾(12 g)、生姜(10 g)加水煮沸,然后趁热加入虎掌南星鲜品,继续煮沸60 min后,浸泡2 d,再以原汁加压(加压温度为125 ℃)37 min,取出,清水洗净,晾至七成干,切薄片,干燥,即得(样品编号为Y1~Y12)。
2.2 虎掌南星不同炮制品指纹图谱的研究
2.2.1 色谱条件 色谱柱:SymmetryShield RP18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%乙酸水溶液(B),梯度洗脱(0~6 min,100%B;6~30 min,100%B→90%B;30~40 min,90%B→87%B;40~45 min,87%B→85%B;45~55 min,85%B→70%B;55~70 min,70%B→65%B;70~75 min,65%B→100%B);流速:0.8 mL/min;柱温:30 ℃;检测波长:270 nm;进样量:15 ?L。
2.2.2 供试品溶液的制备 分别取虎掌南星生品和炮制品粉末(过80目筛,下同)各约1 g,精密称定,置于50 mL锥形瓶中,加水20 mL,称定质量,超声(频率:40 kHz,功率:500 W)45 min,放至室温,用水补足减失的质量,以5 000 r/min离心5 min,取上清液,用0.45 μm微孔滤膜滤过,取续滤液,即得。
2.2.3 混合对照品溶液的制备 分别取各种对照品适量,置于同一量瓶中,精密称定,加水溶解并制成含腺嘌呤0.025 g/L、次黄嘌呤0.042 g/L、尿苷0.034 g/L、黄嘌呤0.019 g/L、肌苷0.031 g/L、尿嘧啶0.041 g/L、鸟苷0.022 g/L、腺苷0.029 g/L、胸腺嘧啶0.018 g/L的混合對照品溶液。
2.2.4 精密度试验 取虎掌南星样品粉末(编号:Y1)约1 g,按“2.2.2”项下方法制备供试品溶液,然后按“2.2.1”项下色谱条件进样,连续测定6次,记录色谱图。以3号峰(腺嘌呤)为参照峰(该峰峰形较好,峰面积稳定适中,且与相邻峰的分离度良好)测得各共有峰相对保留时间的RSD为0.111%~0.712%、相对峰面积的RSD为1.173%~4.706%(n=6),表明该方法精密度良好。
2.2.5 重复性试验 取虎掌南星样品粉末(编号:Y1)约1 g,共6份,分别按“2.2.2”项下方法制备供试品溶液,然后按“2.2.1”项下色谱条件进样测定,记录色图谱。以3号峰(腺嘌呤)为参照峰测得各共有峰相对保留时间的RSD为0.093%~0.416%、相对峰面积的RSD为1.715%~3.855%(n=6),表明该方法重复性良好。
2.2.6 稳定性试验 取虎掌南星样品粉末(编号:Y1)约1 g,按“2.2.2”项下方法制备供试品溶液,在室温下放置0、2、4、6、8、10、12 h时,分别按“2.2.1”项下色谱条件进样测定,记录色谱图。以3号峰(腺嘌呤)为参照峰测得各共有峰相对保留时间的RSD为0.052%~0.851%、相对峰面积的RSD为0.777%~3.478%(n=6),表明样品溶液在室温条件下放置12 h内基本稳定。
2.2.7 虎掌南星指纹图谱的建立及共有峰的指认 分别取虎掌南星生品和2种炮制品(各12批)约1 g,按“2.2.2”项下方法制备供试品溶液,然后分别按“2.2.1”项下色谱条件进样测定,记录色谱图。将3种样品的色谱数据分别导入《中药色谱指纹图谱相似度评价系统》(2004A版)中,分别以样品S1、C1、Y1的图谱为参照图谱,设置时间窗宽度为0.5 s,采用多点校正法进行色谱峰匹配,分别生成3种样品的共有模式,并采用中位数法生成相应的对照指纹图谱。此外,取“2.2.3”项下混合对照品溶液,按“2.2.1”项下色谱条件进样测定,记录色谱图。通过对比样品指纹图谱和混合对照品图谱中各峰的保留时间进行色谱峰指认。结果发现,2种炮制品的图谱较为相似,而生品与前两者的图谱差异较大。其中,在生品的图谱中共确定了22个共有峰,并指认出了9种核苷类成分,分别为腺嘌呤(3号峰)、尿嘧啶(4号峰)、次黄嘌呤(7号峰)、尿苷(8号峰)、黄嘌呤(9号峰)、肌苷(11号峰)、鸟苷(12号峰)、腺苷(13号峰)、胸腺嘧啶(15号峰);但在《规范》炮制品和一体化新工艺炮制品中仅确定了16个共有峰(16个峰相同),均仅指认出了5种核苷类成分,分别为腺嘌呤(3号峰)、次黄嘌呤(7号峰)、尿苷(8号峰)、黄嘌呤(9号峰)、肌苷(11号峰)。虎掌南星生品及不同工艺炮制品的叠加指纹图谱和对照指纹图谱见图1~图3,混合对照品图谱见图4。
2.2.8 虎掌南星指纹图谱的相似度分析 采用《中药色谱指纹图谱相似度评价系统》(2004A版)软件,分别以3种样品的对照指纹图谱为参照,进行对应炮制品的整体相似度评价,结果见表1。
表1结果显示,3种样品(各12批)与其各自对照指纹图谱之间的相似度均大于0.990。这表明虎掌南星同一种样品之间具有较高的相似性,提示其炮制程度及饮片质量均一、稳定。
2.3 不同样品中5种核苷类成分含量的测定
2.3.1 色谱条件 同“2.2.1”项下色谱条件。
2.3.2 溶液的制备 (1)供试品溶液:按“2.2.2”项下方法制备。(2)混合对照品溶液:分别精密称定腺嘌呤、次黄嘌呤、尿苷、黄嘌呤、肌苷对照品适量,置于同一10 mL量瓶中,加水溶解并定容至刻度,得到上述5种成分质量浓度分别为2.193、1.282、0.964、1.608、1.909 mg/mL的混合对照品贮备液;分别精密量取该贮备液0.20、0.20、0.20、0.50、0.25 mL,置于不同10 mL量瓶中,加水稀释并定容至刻度,得到混合对照品溶液①~⑤(分别用作腺嘌呤、次黄嘌呤、尿苷、黄嘌呤、肌苷线性关系考察的母液)。混合对照品溶液①中腺嘌呤质量浓度为0.043 85 mg/mL,混合对照品溶液②中次黄嘌呤质量浓度为0.025 64 mg/mL,混合对照品溶液③中尿苷质量浓度为0.019 28 mg/mL,混合对照品溶液④中黄嘌呤质量浓度为0.080 40 mg/mL,混合对照品溶液⑤中肌苷质量浓度为0.047 72 mg/mL。(3)阴性对照溶液:以水为阴性对照。
2.3.3 色谱条件与系统适用性试验 取“2.3.2”项下混合对照品溶液②、供试品溶液(编号:Y1)和阴性对照溶液各适量,按“2.2.1”项下色谱条件进样分析,记录色谱图。结果显示,5种核苷类成分的色谱峰与其相邻峰间的分离度均大于1.5,理论板数均不低于10 000,且阴性对照溶液对测定无干扰,详见图5。
2.3.4 线性关系考察 精密吸取“2.3.2”项下混合对照品溶液①~⑤适量,分别逐级稀释1、2、10、20、30倍后,按“2.2.1”项下色谱条件进样测定,记录色谱图。以对照品峰面积为纵坐标(y)、质量浓度为横坐标(x)绘制标准曲线,并计算回归方程。结果显示,腺嘌呤、次黄嘌呤、尿苷、黄嘌呤、肌苷分别在各自的质量浓度范围内具有良好的线性关系(r均不小于0.999 8),结果见表2。
2.3.5 定量限与检测限考察 取“2.3.2(2)”项下混合对照品溶液②适量,加水倍比稀释后,按“2.2.1”项下色谱条件进样测定,记录色谱图。以信噪比10 ∶ 1、3 ∶ 1分别计算定量限、检测限。结果,腺嘌呤、次黄嘌呤、尿苷、黄嘌呤、肌苷的定量限分别为0.055、0.036、0.014、0.026、0.017 μg/mL,检测限分别为0.016、0.011、0.003、0.008、0.005 μg/mL。
2.3.6 精密度试验 取“2.3.2(2)”项下混合对照品溶液②,按“2.2.1”项下色谱条件连续测定6次,记录峰面积。结果,腺嘌呤、次黄嘌呤、尿苷、黄嘌呤、肌苷峰面积的RSD分别为1.19%、1.16%、1.73%、1.85%、1.56%(n=6),表明仪器精密度良好。
2.3.7 重复性试验 取同一批虎掌南星样品粉末(编号:Y1)6份,每份约1 g,按“2.2.2”项下方法制备供试品溶液,然后按“2.2.1”项下色谱条件进样测定,记录峰面积,并根据标准曲线计算各成分的含量。结果,腺嘌呤、次黄嘌呤、尿苷、黄嘌呤、肌苷含量的RSD分别为2.19%、1.49%、2.44%、0.76%、1.92%(n=6),表明该方法重复性良好。
2.3.8 稳定性试验 取同一批虎掌南星样品粉末(编号:Y1)约1 g,按照“2.2.2”项下方法制备供试品溶液,分别在室温下放置0、2、4、6、8、10、12 h时,按“2.2.1”项下色谱条件进样测定,记录峰面积。结果,腺嘌呤、次黄嘌呤、尿苷、黄嘌呤、肌苷峰面积的RSD分别为0.89%、1.57%、1.36%、1.52%、1.47%(n=7),表明样品溶液在室温条件下放置12 h内基本稳定。
2.3.9 加样回收率试验 取已知含量的虎掌南星样品粉末(编号:Y1)6份,每份约0.5 g,精密称定,置于具塞锥形瓶中,精密加入5种对照品适量,按“2.2.2”项下方法制成供试品溶液后,再按“2.2.1”项下色谱条件进样测定,记录峰面积。结果,腺嘌呤、次黄嘌呤、尿苷、黄嘌呤、肌苷的平均加样回收率分别为100.49%、99.50%、101.13%、102.05%、99.35%,RSD分别为2.34%、1.19%、2.65%、1.64%、0.79%(n=6),表明该方法准确度较好,结果见表3。
2.3.10 耐用性试验 取虎掌南星样品粉末(编号:S1)适量,按“2.2.2”项下方法制成供试品溶液,在“2.2.1”项下其他色谱条件不变的情况下,分别在不同浓度流动相B(0.08%、0.10%、0.12%乙酸水溶液)、不同流速(0.7、0.8、0.9 mL/min)、不同柱温(25、30、35 ℃)条件下进样测定,记录峰面积,并根据标准曲线计算样品中5种核苷类成分的含量。结果,在不同条件下测得的5种核苷类成分含量的RSD均小于3%(n=3),表明该方法耐用性良好,能滿足含量测定的要求。
2.3.11 样品含量测定 分别取虎掌南星生品和2种不同炮制品(各12批)适量,按“2.2.2”项下方法制备供试品溶液,然后按“2.2.1”项下色谱条件进样测定,记录峰面积,并根据标准曲线计算样品中5种核苷类成分的含量。每批样品测定3次,取平均值,结果见表4。
表4结果显示,生品中黄嘌呤的含量最高,平均含量为0.922 5 mg/g;《规范》炮制品和一体化新工艺炮制品中黄嘌呤的平均含量分别为0.042 5、0.065 3 mg/g。《规范》炮制品和一体化新工艺炮制品中,肌苷的平均含量分别为0.468 8、0.518 6 mg/g,约为生品的13倍;而腺嘌呤、尿苷、黄嘌呤的含量较生品明显降低。一体化新工艺炮制品中,腺嘌呤、次黄嘌呤、黄嘌呤、肌苷的含量均比《规范》炮制品略高,而尿苷的含量差异很小。
2.4 虎掌南星不同工艺样品的聚类分析
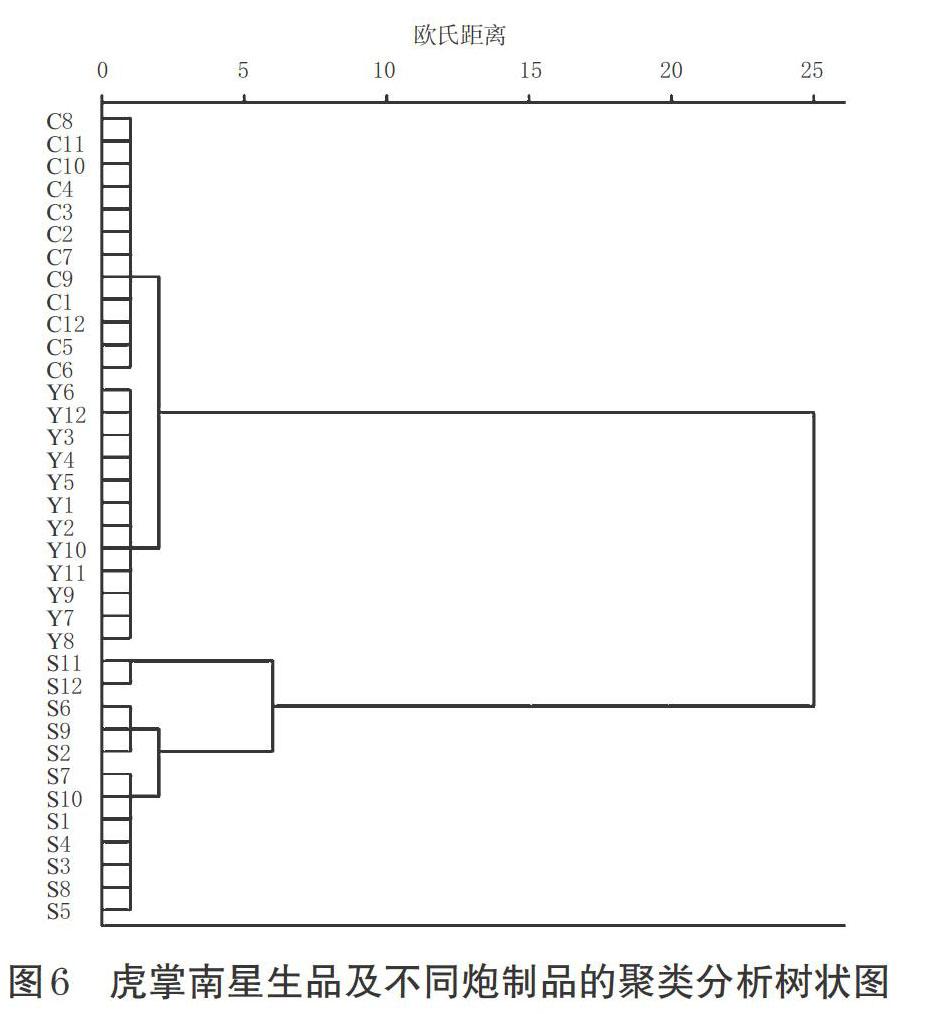
以虎掌南星样品中腺嘌呤、次黄嘌呤、尿苷、黄嘌呤、肌苷的含量为原始数据,运用 SPSS 21.0软件中的质心聚类法,以欧式距离为度量标准区间,对36批虎掌南星样品进行聚类分析,结果见图6。
由图6可知,36批虎掌南星样品共聚为2类:虎掌南星生品聚为一类;2种炮制品聚为另一类。以上结果提示,虎掌南星生品与不同炮制品之间的核苷类成含量存在差异,也提示2种工艺所炮制的饮片质量较接近。
3 讨论
据文献报道,虎掌南星水提物中富含核苷类成分,而核苷类成分可参与DNA代谢过程,具有抗肿瘤、抗病毒、抗心律失常等多种生物活性,是生物细胞维持生命活动的基本组成元素[15],其含量的升高或降低对于糖代谢、酶活性改变、受损肝脏的恢复有显著影响[21]。目前,虎掌南星多采用水浸泡加热的方式炮制,而核苷类为水溶性成分,且性质不稳定,在炮制过程中易发生水解[22]。笔者通过前期预试验发现,加热温度、加热时间和浸泡天数是影响水溶性成分含量的主要因素。由本研究结果中不同样品的色谱图也可知,虎掌南星中核苷类成分的色谱峰出峰时间多集中于前15 min,此时水相的比例较大,且生品中该时段的色谱峰多而高,而炮制品中该时段色谱峰峰面积减小甚至部分峰消失。这提示虎掌南星炮制后的化学成分不仅发生了量的改变,同时其种类也发生了显著的变化。对比生品和不同炮制品的色谱图,发现炮制品中除肌苷的含量有大幅度升高外,腺嘌呤、尿苷、黄嘌呤的含量均明显降低,且尿嘧啶、鸟苷、腺苷和胸腺嘧啶在炮制后几乎检测不到。针对此现象,笔者推测可能有以下两个方面的原因:一方面可能与煎煮时间及煎煮方式有关;另一方面可能是由于白矾溶液呈酸性,而核苷呈碱性,炮制过程中两者发生了化学反应。此外,由于传统工艺是由生品加水浸泡至内无干心后与辅料常压煮沸,在反复换水浸泡的过程中,溶于水的核苷类成分会随之流失。而本课题组建立的一体化新工艺是将药材鲜品直接进行加压蒸煮,避免了药材重复换水处理的过程,最大程度地减少了有效成分的流失,故而采用该法炮制的样品中核苷类成分的总含量比《规范》炮制品高。与生品比较,不同工艺炮制品中肌苷的含量有明显升高的趋势,这可能是加热过程中发生了降解或形成了新的聚合物引起的。
聚类分析结果显示,虎掌南星生品与不同工艺炮制品中核苷类成分有显著差异,可将两者有效区分开,说明生品在炮制过程中成分发生了显著变化。将2种炮制品HPLC指纹图谱进行对比分析发现,两者相似度较高,表明2种不同工艺虎掌南星制品的质量总体差异不明显。但是结合核苷类成分的含量来看,一体化新工艺炮制品比《规范》炮制品中核苷类成分含量略高,并且前者不仅缩短了炮制时间,减少了干燥次数,同时降低了资源消耗成本,稳定了饮片质量,更加适用于虎掌南星的炮制以及产业化的发展需求。
综上所述,本研究建立的方法稳定、可行,可用于虎掌南星生品及不同炮制品的质量评价。虎掌南星经炮制后指纹图谱发生了明显变化,5种核苷类成分的总含量均降低,但一体化新工艺炮制品中上述成分总含量略高于《规范》炮制品。然而,本研究仅通过指纹图谱和聚类分析的方法比较了虎掌南星生品及不同炮制品成分的不同,关于炮制前后其化学成分具体发生了何种转变,以及是否产生了新的药理活性等问题还有待进一步研究。
参考文献
[ 1 ] 李志勇,李彦文,周凤琴,等.傅里叶变换红外光谱法快速鉴别虎掌南星[J].中国药房,2011,22(31):2919-2921.
[ 2 ] 李彦文,李志勇,郭庆梅,等.虎掌南星的本草考证[J].现代中药研究与实践,2012,26(4):18-20.
[ 3 ] 弓建红,王俊敏,张振凌,等.虎掌南星(掌叶半夏)的化学成分及药理活性研究进展[J].河南科学,2020,38(3):386-396.
[ 4 ] 莫雪林,刘玉杰,李涛,等.虎掌南星多糖含量及单糖组成研究[J].中药与临床,2017,8(6):13-16.
[ 5 ] 陆丹,池玉梅,赵懿清,等.虎掌南星药材的质量标准研究[J].中成药,2013,35(6):1274-1278.
[ 6 ] 毛善虎,郁红礼,吴皓,等.掌叶半夏凝集素蛋白刺激巨噬细胞的致炎作用研究[J].中国中药杂志,2017,42(13):2497-2502.
[ 7 ] 刘玎,陈劲,刘志,等.掌叶半夏凝集素基因PPA2抗蚜功能分析[J].生物技术通报,2016,32(10):180-187.
[ 8 ] 居羚,池玉梅,王天鹤.虎掌南星中氨基酸含量测定[J].亚太传统医药,2016,12(9):30-31.
[ 9 ] 聂容珍,陈文政,林嘉娜,等.天南星科有毒中药及炮制品的药效比较研究[J].中药药理与临床,2016,32(4):53- 56.
[10] 張萌,张明星,黄海霞,等.掌叶半夏化学成分及药理作用研究进展[J].上海中医药杂志,2019,53(6):92-94.
[11] 潘多,张慧茹,曹美娇,等.虎掌南星化学成分及其抑菌活性[J].中成药,2019,41(4):823-827.
[12] 王芹,王胜飞,张永太,等.天南星总黄酮纳米凝胶对Walker256骨癌痛模型大鼠的镇痛作用研究[J].上海中医药杂志,2015,49(11):62-66.
[13] WANG W,MAO SH,YU HL,et al. Pinellia pedatisecta lectin exerts a proinflammatory activity correlated with ROS-MAPKs/NF-κB pathways and the NLRP3 inflammasome in RAW264.7 cells accompanied by cell pyroptosis[J]. Inter Immunophar,2019,66(1):1-12.
[14] 姜爽,李建睿,苑广信,等.天南星多糖对荷瘤小鼠的抗肿瘤活性[J].中国老年学杂志,2014,34 (18):5183-5184.
[15] 王金艳,王晨光,张劲松,等.灵芝孢子粉中核苷类成分分析[J].菌物学报,2016,35(1):77-85.
[16] 林坤河,韦建华,邓超成,等.炮制对天南星化学成分及药理作用的影响研究概况[J].广西中医药,2018,41(4):73-75.
[17] 杨中林,朱谧,顾萱.天南星各种炮制品的药效学初步研究[J].中国药科大学学报,1998,29(5):342-344.
[18] 河南省食品药品监督管理局.河南省中药饮片炮制规范[S].郑州:河南人民出版社,2005:83.
[19] 曹淼淼,朱建光,张振凌,等.虎掌南星加工炮制一体化工艺优化[J].中成药,2020,42(5):1299-1305.
[20] 卢森华,甘洋萦,唐莲,等. HPLC特征指纹图谱结合化学计量学评价不同寄主来源的桑寄生药材质量[J].中国药房,2020,31(7):794-799.
[21] 奚若明.中国化工医药产品大全 :第2卷[M].北京:科学出版社,1996:175-178.
[22] 游静,张德全,潘兴娇,等.高效液相色谱法同时测定太白贝母与暗紫贝母中9种核苷类成分的含量[J].食品与发酵工业,2016,42(1):174-179.
(收稿日期:2020-03-13 修回日期:2020-05-20)
(编辑:林 静)

