首发精神分裂症病人血糖、血脂水平与认知损害的相关性研究
何 潇,郎小娥,薛晓燕,侯 鑫,梁 瑛,柴 娜,侯钦强
精神分裂症是严重的精神疾病,其认知功能损害被认为是继阳性和阴性精神病性症状之外的第三类核心症状,首发精神分裂症病人在用药前已经存在广泛的认知损害[1],严重影响病人的社会功能,给病人家庭及社会带来沉重的负担,研究显示精神分裂症所致的伤残相关寿命损失年(years lived with disability,YLDs)为1 340万人,占2016年全部YLDs的1.7%[2]。精神分裂症病人发生代谢紊乱的风险高,其罹患糖尿病的概率是一般人群的2~4倍[3],发生代谢综合征的概率是普通人群的3倍[4]。精神分裂症病人的代谢紊乱早期发生并可伴随终生,是心血管疾病发生的重要危险因素,常常也预示着不良的医学结局和精神病学预后。首发精神分裂症(first episode schizophrenia,FES)病人在使用抗精神病药物之前已经存在糖脂代谢紊乱,糖脂代谢可以对认知功能产生多方面的影响,其机制尚不清楚且存在争议,有研究认为高糖、高脂可以加重精神分裂症病人的认知损害,也有研究认为高糖、高脂可对认知功能的某些方面产生一定的保护作用,本研究旨在探讨FES病人血糖、血脂水平与认知损害的相关性。
1 资料与方法
1.1 临床资料 选取2018年8月—2019年12月就诊于山西医科大学第一医院精神卫生科的92例首发精神分裂症病人作为病例组。纳入标准:①符合美国精神障碍诊断与统计手册第4版(DSM-Ⅳ)精神分裂症诊断标准,阳性和阴性症状量表(Positive and Negative Syndrome Scale,PANSS)评分总分>60分;②汉族、右利手,年龄18~45岁;③首次发病,总病程<2年,未使用过任何长效或者短效抗精神病药物。排除标准:①有精神活性物质滥用史;②患有其他精神系统、神经系统疾病;③处于妊娠期或者哺乳期妇女;④正在接受无抽搐改良电休克、经颅磁刺激、经颅直流电刺激等治疗;⑤诊断糖尿病、高脂血症及正在服用控制血糖及调节血脂相关药物;⑥患有严重内分泌疾病;⑦肥胖。招募与病例组年龄、性别相匹配的健康志愿者92名作为健康对照组,排除标准与病例组相同。
1.2 方法
1.2.1 研究方法 本研究为横断面调查研究,所有研究对象均签署知情同意书,研究方案获得医院伦理委员会批准。
1.2.2 一般资料收集 收集研究对象性别、年龄、受教育年限、是否吸烟饮酒,测量身高、体重,计算体质指数(body mass index,BMI)等。
1.2.3 实验室指标测定 抽取两组研究对象的空腹静脉血,测定空腹血糖(fasting blood glucose,FBG)、总胆固醇(total cholesterol,TC)、三酰甘油(triglyceride,TG)、高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)、糖化血红蛋白(glycosylated hemoglobin,HbA1c)、空腹胰岛素(fasting serum insulin,FIns);采用稳态模型评估胰岛素抵抗指数(HOMA-IR),即 HOMA-IR=FBG×FIns/22.5。
1.2.4 疾病严重程度及认知功能评估 由两名经过一致性培训的主治医师进行评估,采用PANSS量表评估病例组疾病严重程度,采用重复性神经心理状态测验(Repeatable Battery for the Assessment of Neuropsychological Status,RBANS)评估两组研究对象的认知功能。RBANS由5个神经状态构成:即刻记忆、视觉广度、语言、注意、延迟记忆,具体分为12个分测验:词汇学习、故事记忆、图形描述、线条定位、图片命名、语义流畅性、数字广度、符号数字匹配、词汇再现、词汇再认、故事回忆、图形记忆,分数越高,认知功能越好。
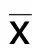
2 结 果
2.1 两组一般资料及实验室指标比较 两组性别、年龄、受教育年限、BMI比较,差异无统计学意义(P>0.05)。病例组HbA1c、TG、FIns及HOMA-IR水平高于对照组(P<0.05);病例组HDL-C水平低于健康对照组(P<0.05);两组FBG、TC、LDL-C水平比较,差异均无统计学意义(P>0.05);病例组RBANS总分及各因子分均低于对照组(P<0.05)。详见表1。
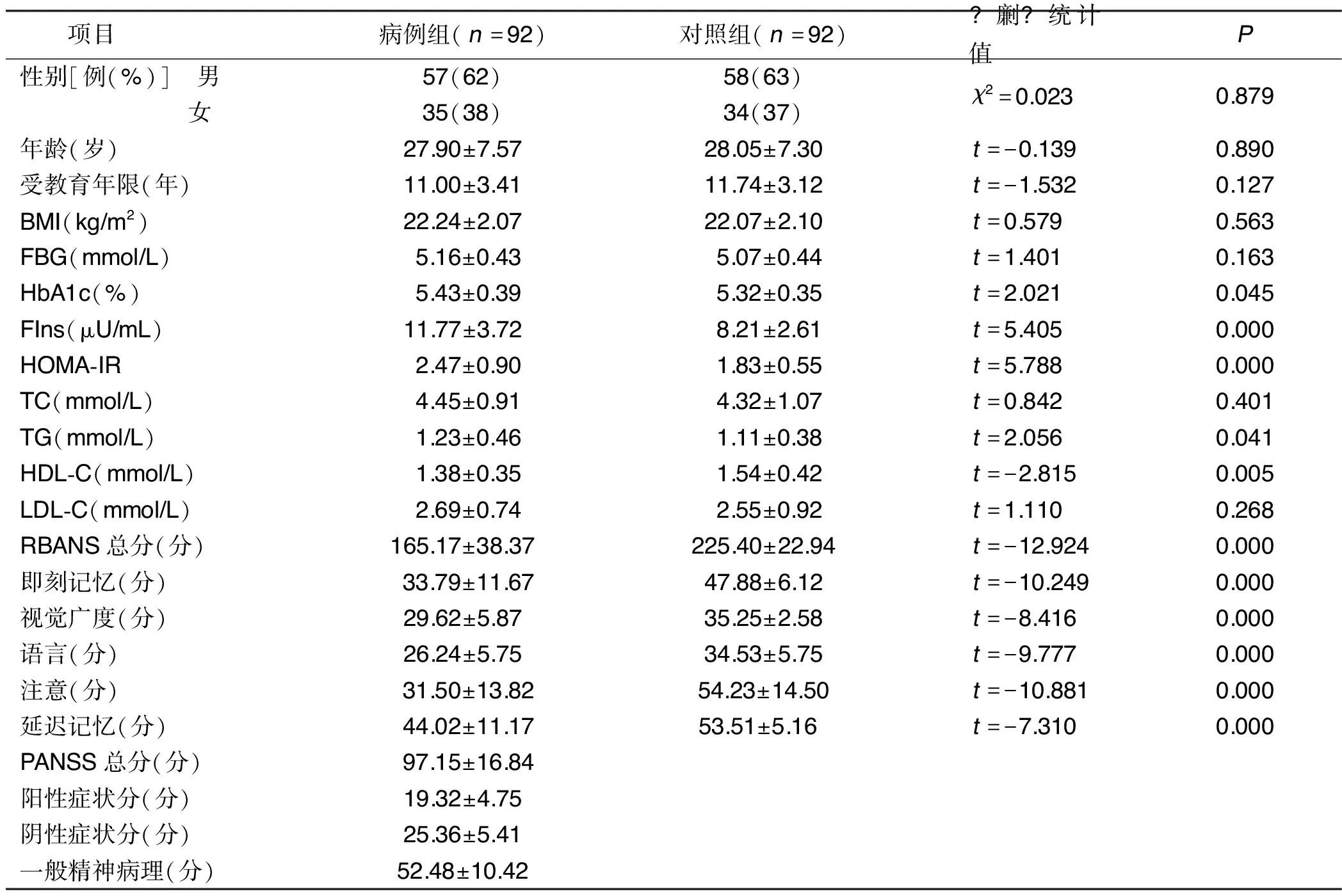
表1 两组一般资料及实验室指标比较
2.2 病例组血糖、血脂水平与疾病严重程度及认知损害的相关性 病例组HbA1c水平与PANSS总分、阴性症状分及一般精神病理症状分呈正相关(P<0.05);FIns、HOMA-IR水平与阴性症状分呈正相关,与RBANS总分、注意、延迟记忆评分呈负相关(P<0.05)。详见表2。病例组HDL-C水平与PANSS总分及一般精神病理症状分呈负相关(P<0.05),与RBANS总分及即刻记忆分呈正相关(P<0.05),未发现TC、TG、LDL-C水平与认知损害的相关性。详见表3。经年龄、性别、BMI校正后,以Pearson分析存在相关性的HbA1c、HOMA-IR、HDL-C(因HOMA-IR与FIns存在多重共线性,故只纳入HOMA-IR)为自变量进行多元线性回归分析,结果显示:低年龄、高HbA1c及低HDL-C水平是疾病严重程度的危险因素,高HOMA-IR及低HDL-C水平是认知损害的危险因素。
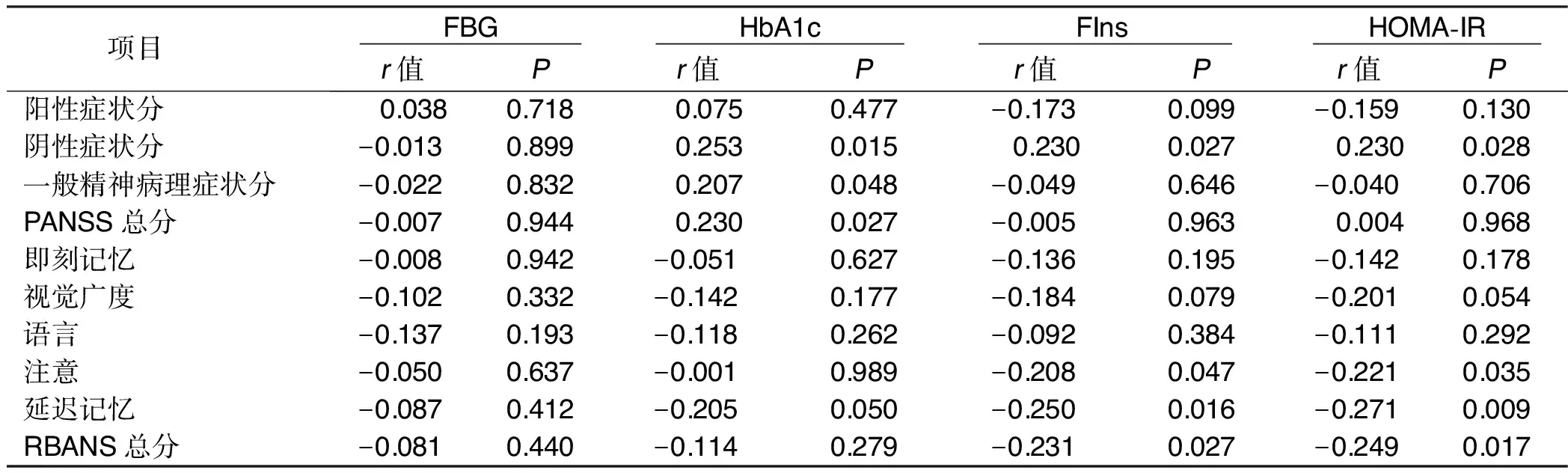
表2 糖代谢指标与疾病严重程度及认知损害的相关性

表3 脂代谢指标与疾病严重程度及认知损害的相关性
3 讨 论
本研究发现FES病人较健康对照组具有更高的糖脂代谢异常风险,其HbA1c、FIns、HOMA-IR、TG水平高于健康对照组,HDL-C水平低于健康对照组,差异有统计学意义,与既往部分研究结果一致[5-7]。表明FES病人在使用抗精神病药物之前已经存在葡萄糖稳态的受损及胰岛素抵抗[8-9],其机制尚不清楚,首先可以排除精神病症状应激所致糖代谢异常,因为HbA1c水平反映病人近2~3个月的血糖控制水平,应激所致的糖代谢异常病人HbA1c水平一般不升高。但也有学者持不同的观点,认为FES在未用药时,高FBG、TC、TG、LDL-C的发生率远低于普通人群[10]。精神分裂症是2型糖尿病的危险因素,胰岛素抵抗的发生先于2型糖尿病10~15年,且会导致2型糖尿病和代谢综合征。美国的大型研究RASE-ETP发现56.5%的精神分裂症病人存在脂代谢异常,但只有0.5%的病人接受降脂药的治疗[11],因此,及早检测FES病人的糖脂代谢相关指标,以便提前干预,减少不良事件的发生。
本研究发现FES病人的高HbA1c水平会加重病人的病情,尤其是阴性症状,高FIns、HOMA-IR水平会加重病人的阴性症状及认知损害,还发现FES病人的FIns、HOMA-IR水平与注意、延迟记忆评分呈负相关。既往研究发现共病糖尿病的精神分裂症病人比只患精神分裂症的病人认知损害更严重,尤其是即时记忆和注意方面[12],且共病糖尿病的精神分裂症病人的HbA1c水平与RBANS总分及各因子分存在负相关[13],本研究在FES病人中未发现这种相关性。海马在记忆中起着核心作用,研究发现精神分裂症病人的记忆损害与海马的激活不足有关[14],葡萄糖调节受损及胰岛素抵抗会导致海马体积减小从而引起记忆受损[15]。胰岛素能够透过血脑屏障,海马区的胰岛素抵抗是认知损害的危险因素,激活胰岛素受体后可以提高大鼠记忆任务的执行能力,增强人的词语记忆能力、注意[16]。胰岛素抵抗引起认知损害可能与以下机制有关:发生胰岛素抵抗后,影响了磷脂酰激醇3-激酶/蛋白激酶B(PI3K/AKT)通路的激活,从而影响哺乳动物雷帕霉素靶蛋白(mTORC1)的激活,进而调节突触密度及突触后致密蛋白95(PSD-95)来影响突触可塑性,胰岛素抵抗降低了突触可塑性,加重了病人认知损伤;胰岛素抵抗还可影响PI3K/丝裂原活化蛋白激酶(MAPK)/细胞外信号调节激酶(ERK)通路的激活,从而影响谷氨酸和γ-氨基丁酸受体激活,减少蛋白的合成,破坏树突棘的稳定性,进而影响海马功能,加重病人记忆功能损害。精神分裂症病人早期的糖尿病预防对改善认知及总体健康是非常有益的[17],因此,要早期监测病人的糖代谢水平。
本研究发现血脂各指标中,只有低HDL-C水平会加重病人病情,损害病人的即刻记忆及总体认知功能,这与Lancon等[18]的观点一致,认为血脂4项中只有低HDL-C与认知损害有关。HDL-C具有逆向转运胆固醇的作用,HDL-C水平下降,会导致脂质沉积,使血脑屏障的通透性增加,高碳酸物质扩散到血管周围引起神经胶质细胞和神经元的损伤,从而引起认知损伤[19];HDL-C还通过参与胰岛素抵抗的形成及血糖的调节来影响认知功能,低HDL-C会导致胰岛素敏感的组织胆固醇过量沉积,引起该组织的炎症反应,从而造成胰岛素抵抗,低HDL-C和血浆胰岛素可增加脂解及氧化,使血糖升高[20],这与本研究所观察到的胰岛素抵抗导致认知损伤的结论一致。但也有学者认为高脂可能是认知损害的保护因素,Elias等[21]认为高胆固醇与更好的语言流利度、推理、运动速度及注意相关,Krakowski等[22]也发现高胆固醇水平与更好的言语记忆相关。
综上所述,FES病人具有更高的糖脂代谢风险,葡萄糖调节受损、胰岛素抵抗、低HDL-C会加重病人的认知损害;FES病人的FIns、HOMA-IR水平与注意、延迟记忆评分呈负相关,提示要关注精神分裂症病人的代谢风险,早期监测,早期干预,以改善病人的总体认知及预后。

