外科治疗DeBakeyⅠ型和Ⅲ型夹层合并胸腹主动脉瘤的结果对比
马明星,常 谦,于存涛,舒 畅,钱向阳,孙晓刚,马 琼,魏 波,胡晓鹏
中国医学科学院 北京协和医学院 国家心血管病中心阜外医院心血管外科,北京 100037
无论是DeBakeyⅠ型还是Ⅲ型主动脉夹层(aortic dissection,AD),存在夹层病变的远端主动脉均可因持续扩张形成胸腹主动脉瘤(thoracoabdominal aortic aneurysm,TAAA)需要再次手术干预[1-2]。目前国内已报道的TAAA治疗结果中,AD是最主要的病因[3-4]。DeBakeyⅠ型和Ⅲ型夹层在急性期的病理生理改变和治疗原则上截然不同,而进入慢性期后这两型夹层的远端主动脉在病情演变上仍有不同。相较于Ⅰ型,Ⅲ型夹层的远端主动脉再处理几率更高[5]。目前,尚不明确手术治疗这两种不同类型TAAA的结果有何差异。本研究比较了手术治疗DeBakeyⅠ型和Ⅲ型夹层合并TAAA的早期结果和中期随访结果,以期总结相关经验,评估治疗策略和手术风险。
资料和方法
资料及分组2009年1月至2017年12月在中国医学科学院阜外医院接受胸腹主动脉替换术的患者。纳入标准:(1)依据病史、临床症状、体征、主动脉计算机断层扫描造影(computed tomography angiography,CTA)或磁共振造影检查(magnetic resonance angiography,MRA)资料明确诊断为TAAA;(2)合并DeBakeyⅠ型和Ⅲ型主动脉夹层。排除标准:(1)同期行全主动脉替换者;(2)替换范围局限于胸降主动脉或腹主动脉者。共130例患者纳入研究,根据夹层发病情况和DeBakey分型标准分为Ⅰ型组(n=47)和Ⅲ型组(n=83)。本研究经中国医学科学院阜外医院伦理委员会批准,所有患者均豁免知情同意。
诊断标准TAAA的解剖分型依据Crawford分型标准[6]。马凡综合征诊断依据改良Ghent标准[7],综合评价包括家族史、主动脉根部Z评分、晶状体脱位、致病性FBN1基因突变和全身系统评分后完成诊断。术后30 d死亡包括术中死亡、院内死亡或转院后死亡。术后肾功能衰竭依据KDIGO标准[8],定义为血肌酐水平超过基础值3倍或≥353.6 μmol/L,或需要透析者。肺部并发症包括:气管切开、再次气管插管、呼吸机辅助>72 h和肺部感染。脊髓损伤:即时为术后清醒时即已出现;延迟为术后清醒时无损伤表现;截瘫为双下肢肌力0级;轻瘫为双下肢肌力1~4级。脑卒中为有神经系统症状,头部CT有影像学证据。主要不良事件包括术后30 d死亡、肺部并发症、脊髓损伤、脑卒中、急性肾功能衰竭和血液透析。
手术指征及方法符合以下条件者,应行手术治疗:(1)马凡综合征患者:TAAA直径≥5.0 cm或扩张速度≥0.5 cm/年;非马凡综合征患者:TAAA直径≥5.5 cm或扩张速度≥1.0 cm/年。(2)出现胸背痛、腹痛症状,用其他病因不能解释。(3)主动脉瘤已经破裂或有破裂倾向者。所有患者均采用双腔气管插管,左后外侧胸部切口及腹直肌旁切口显露胸腹主动脉,采用四分支人工血管(Hemashield,MAQUET,Wayne,NJ),依具体病情在不同循环管理方式(直接阻断、深低温停循环、股-股转流和主动脉-髂动脉转流)下,顺序分段阻断完成手术。其中,人工血管主干近端在适宜水平端端吻合于近端主动脉,动脉管法重建T8~L1间通畅肋间动脉,远端与包含腹腔干、肠系膜上动脉和右肾动脉开口的血管片端端吻合,而对于马凡综合征及内脏动脉开口相距较远者采用分支法分别重建,左肾动脉、双侧髂动脉分别与相应的分支血管吻合完成全部重建。具体手术步骤详见文献[3-4]。
随访通过门诊和电话完成出院患者随访,心脏彩超、主动脉CTA在出院前,出院后3、6个月分别完成,以后每年复查1次。2018年7月31日为本研究截止日期。截止日期前死亡者记录为死亡,至截止日期未死亡者记录为删失。
统计学处理采用SPSS 24.0统计软件,符合正态分布的计量资料以均数±标准差表示,组间比较采用t检验;不符合正态分布的计量资料以M(Q1,Q3)表示,组间比较采用非参数检验;分类变量以例数(百分比)表示,组间比较采用卡方检验或Fisher精确检验;生存分析和免于再干预分析采用Kaplan-Meier方法分析,log-rank检验比较两组间生存率和免于再干预率的差异;P<0.05 为差异有统计学意义。
结 果
术前一般情况Ⅰ 型患者较 Ⅲ 型更年轻[(36.7±10.5)岁比(40.7±10.4)岁;t=-2.095,P= 0.038],男性(85.1%比 60.2%;χ2=8.710,P=0.003)、有家族史者(14.9% 比3.6%;χ2=3.905,P=0.048)、CrawfordⅡ型者(100.0% 比86.7%;χ2=5.201,P=0.023)和合并马凡综合征者(51.1%比32.5%;χ2= 4.324,P= 0.038)比例更高;Ⅲ型患者较Ⅰ型有症状者(71.1%比48.9%;χ2=6.320,P=0.012)和Crawford Ⅲ型者(9.6% 比0;χ2=7.473,P=0.006)比例更高(表1)。
手术情况除Ⅲ型组患者使用深低温停循环技术(deep hypothermia circulatory arrest,DHCA)更多(19.3%比6.4%,χ2= 3.998,P=0.046)外,两组患者在急诊手术比例、预防性脑脊液引流、手术时间、术中用血量方面差异均无统计学意义(P均>0.05)(表2)。
术后早期情况术后30 d,全组死亡9例(6.9%),脊髓损伤9例(6.9%),其中,即时轻瘫3例,迟发轻瘫2例,即时截瘫2例,迟发截瘫2例。除2例轻瘫患者恢复外,永久轻瘫3例,永久截瘫4例。脑卒中3例(2.3%),急性肾功能衰竭者31例(23.8%),住院期间需要透析者18例(13.8%),出院后仅1例患者需要永久透析,二次止血者24例(18.5%)。Ⅰ型患者较Ⅲ型患者术后30 d死亡率高,但差异无统计学意义(10.6% 比4.8%;χ2= 0.803,P= 0.370);Ⅲ型患者较Ⅰ型患者在二次止血(22.9%比10.6%;χ2=2.993,P=0.084)、肺部感染(20.5% 比10.6%;χ2=2.068,P=0.150)和住院透析(18.1%比6.4%;χ2=3.437,P=0.064)发生率高,但差异也无统计意义;两组在脊髓损伤、脑卒中和其他肺部并发症方面差异也均无统计学意义(P均>0.05)。Ⅲ型患者术后主要不良事件发生率较Ⅰ型患者更高,但差异无统计学意义(51.8%比38.3%;χ2=2.199,P=0.138)(表3)。
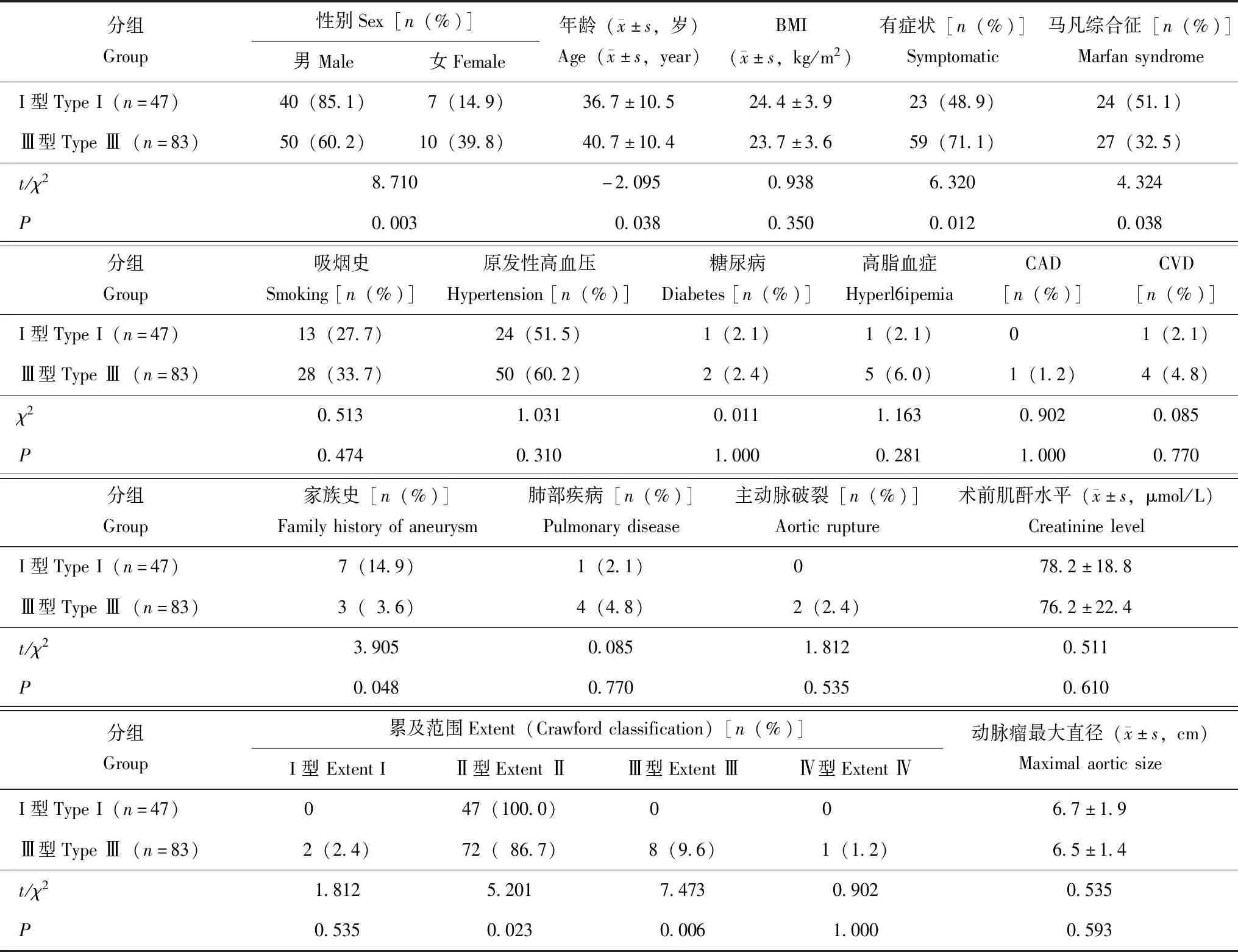
表1 两组患者术前情况比较Table 1 Patient information before surgery
BMI:体质量指数;CAD:冠心病;CVD:脑血管病
BMI:body mass index;CAD:coronary heart disease;CVD:cerebrovascular disease
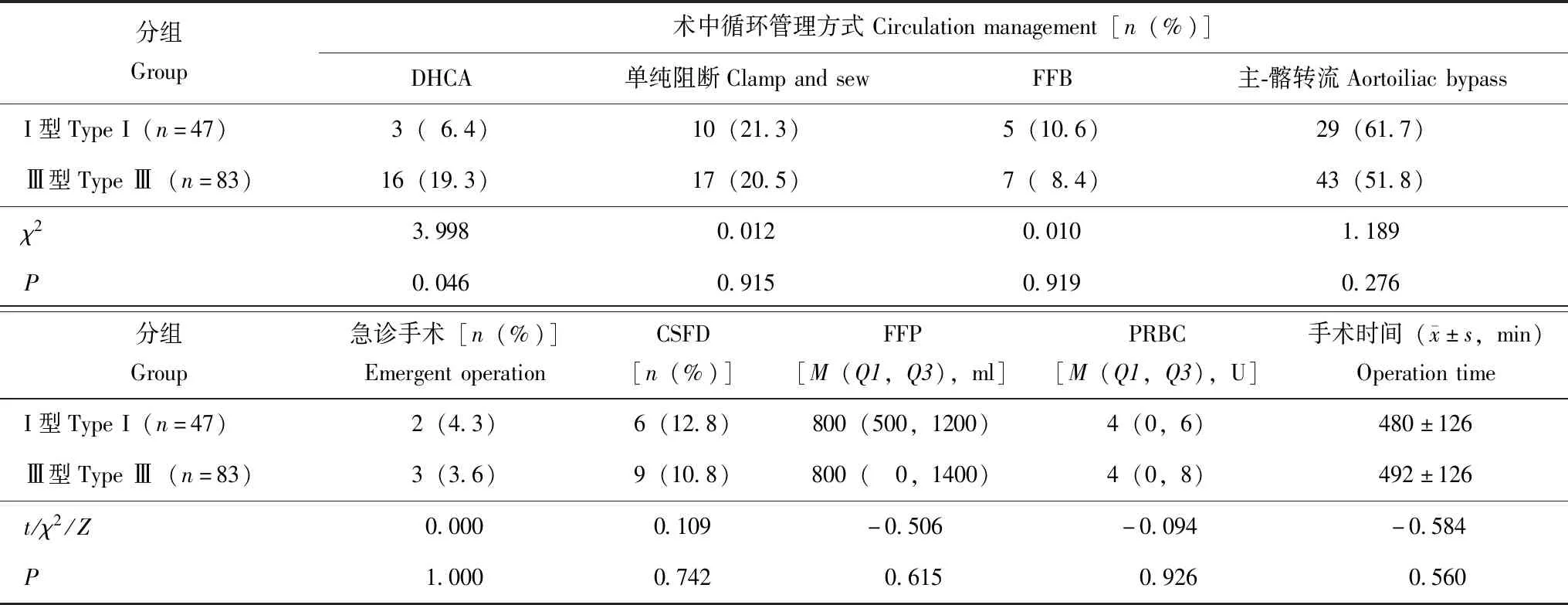
表2 两组术中情况比较Table 2 Intraoperative details in two groups
DHCA:深低温停循环;FFB:股静脉-股动脉转流;CSFD:脑脊液引流;FFP:新鲜冰冻血浆;PRBC:悬浮红细胞
DHCA:deep hypothermia circulatory arrest;FFB:femoral venous-femoral artery bypass;CSFD:cerebrospinal fluid drainage;FFP:fresh frozen plasma;PRBC:packed red blood cells

表3 两组间术后早期情况比较[n(%)]Table 3 Early outcomes after surgical repair [n(%)]
SCI:脊髓损伤;ARF:急性肾功能衰竭;AF:心房纤颤
SCI:spinal cord injury;ARF:acute renal failure;AF:atrial fibrillation
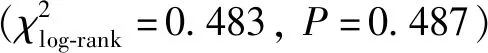

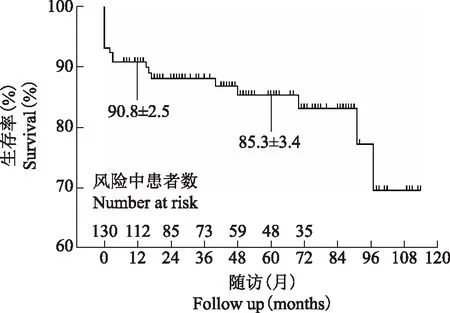
图1外科治疗主动脉夹层合并胸腹主动脉瘤的中期生存分析
Fig1Mid-term survival after open repair of thoracoabdominal aortic aneurysm for patients with distal aortic dissections
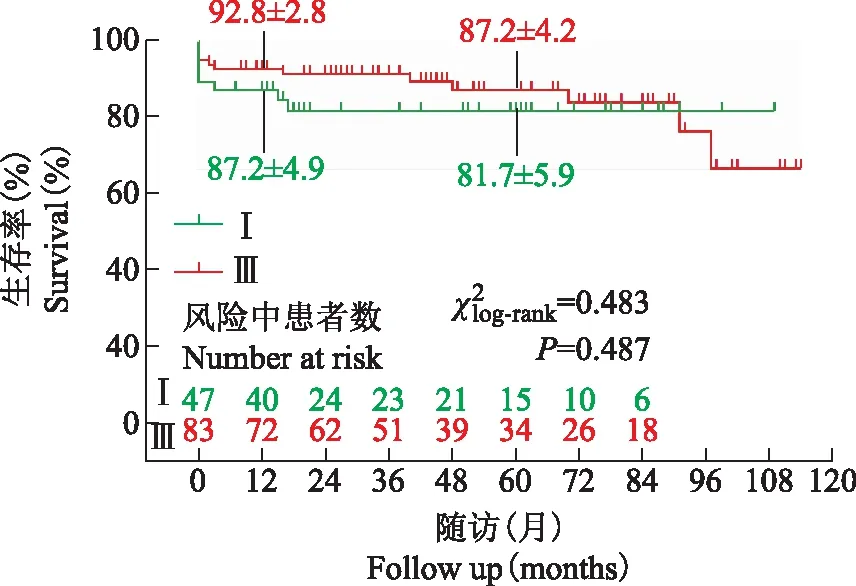
图2外科治疗DeBakeyⅠ型夹层和Ⅲ型夹层合并胸腹主动脉瘤的中期生存分析
Fig2Mid-term survival after open repair of thoracoabdominal aortic aneurysm stratified by DeBakey typeⅠand type Ⅲ aortic dissections
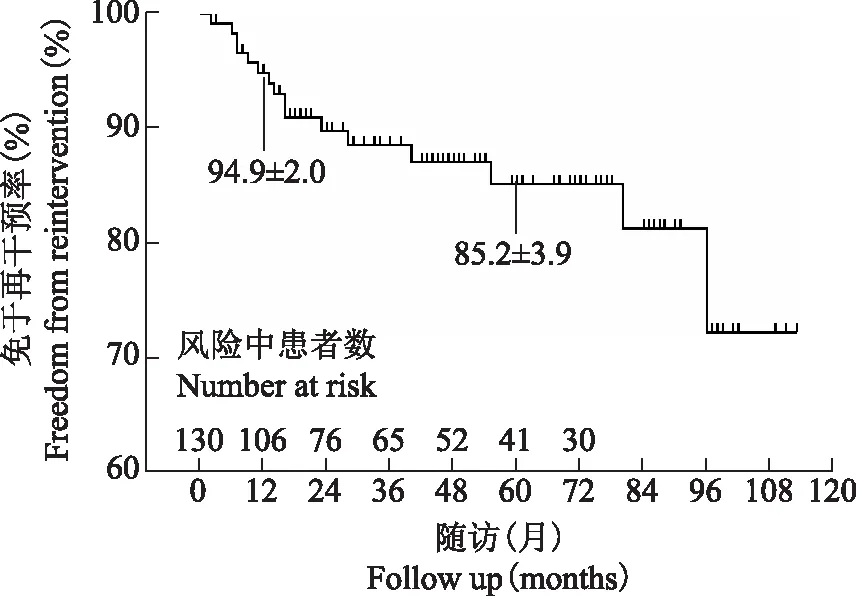
图3外科治疗主动脉夹层合并胸腹主动脉瘤的中期免于再干预分析
Fig3Mid-term freedom from overall reintervention after open repair of thoracoabdominal aortic aneurysm for patients with distal aortic dissections
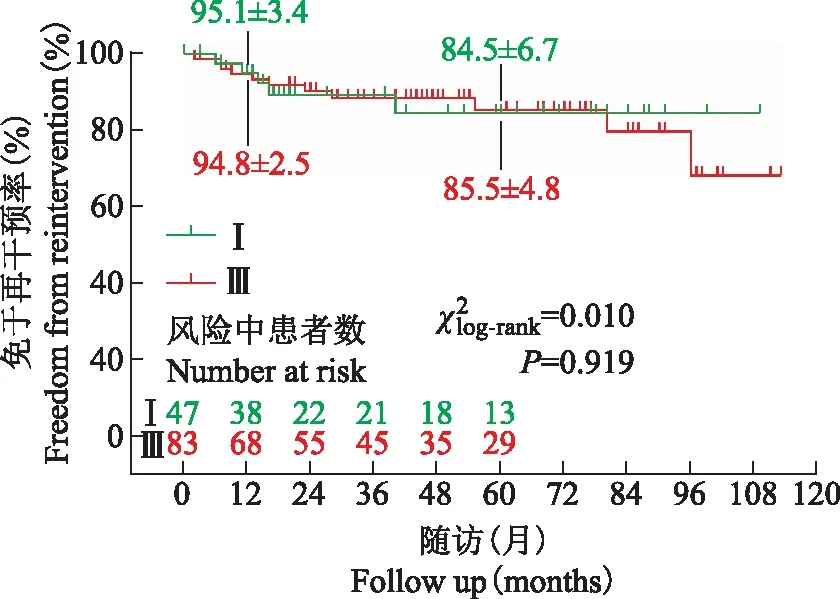
图4外科治疗DeBakeyⅠ型夹层和Ⅲ型夹层合并胸腹主动脉瘤的中期免于再干预分析
Fig4Freedom from overall reintervention after open repair of thoracoabdominal aortic aneurysm for patients with distal aortic dissection stratified by DeBakey typeⅠand type Ⅲ aortic dissections
讨 论
手术治疗DeBakeyⅠ型和Ⅲ夹层合并TAAA的对比研究较少,两类患者术前特征在已有的报道中并不一致。Gambardella等[9]研究显示,DeBakeyⅠ型和Ⅲ夹层患者的术前一般资料无显著差别,平均年龄在59岁左右。而Preventza等[10]结果显示,DeBakeyⅠ型夹层患者比Ⅲ型夹层更年轻,合并冠心病和脑血管疾病者却较多。但这两项研究均未列出合并马凡综合征等结缔组织疾病的情况。分析我院130例患者的术前资料和人群特征,其结果与国外报道有一定差异。相较于DeBakey Ⅲ型者,Ⅰ型者更年轻,解剖分型属于Crawford Ⅱ型者也更多,推测其原因可能与I型组合并马凡综合征者比例更高有关。在合并原发性高血压、冠心病、糖尿病等方面,两组间无明显差异。
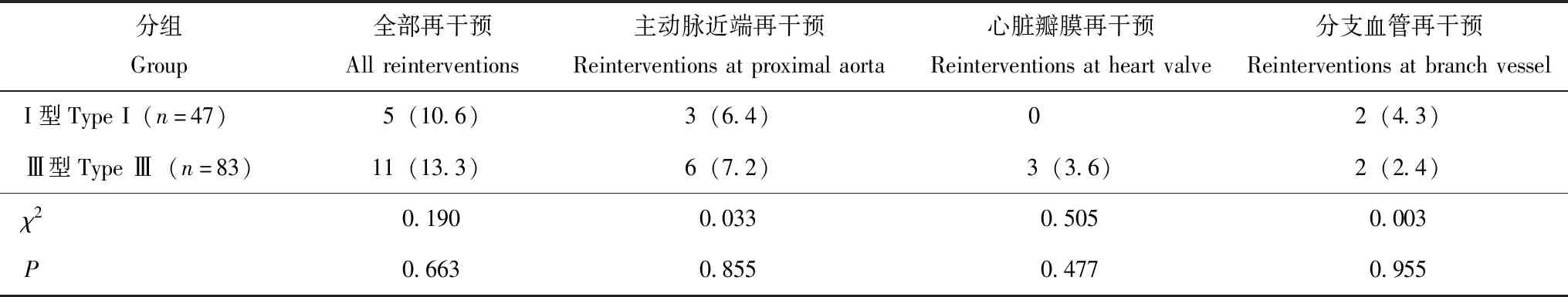
表4 两组间再干预情况比较[n(%)]Table 4 Reinterventions after surgery[n(%)]
对于合并主动脉夹层的TAAA患者,我院的手术策略不同于欧美国家。由相关报道可见,欧美国家医生更倾向于以主动脉瘤直径为指导,对于尚未达到手术治疗直径标准的病变主动脉节段予以保留,以期降低围手术期风险,待远期扩张达到标准后再行手术治疗[11]。采用此策略,Cosseli等[11]报道了继发于慢性DeBakeyⅠ型夹层的远端主动脉瘤的外科治疗结果,手术死亡率为7.1%,永久脊髓损伤3%,血液透析者7.1%,其中胸降主动脉瘤者13.6%,Crawford I型者33.3%,Crawford Ⅱ型者40.4%,Crawford Ⅲ型者7.1%,Crawford Ⅳ型者5.6%。考虑到我国此类患者更加年轻,预期寿命更长,合并马凡综合征比例高,高血压整体控制欠理想,且随访意识不强,我院的手术治疗策略更为积极。除替换已经达到手术治疗标准的主动脉节段外,对于已经扩张但尚未达到手术治疗标准的夹层累及节段也予以一并替换,以降低再次手术几率和等待再次手术过程中的破裂风险。本项研究的总体结果为,手术死亡率6.9%,永久脊髓损伤5.4%,血液透析者13.8%,其中Crawford I型者1.5%,Crawford Ⅱ型者91.5%,Crawford Ⅲ型者6.2%,Crawford Ⅳ型者0.8%。可见,尽管本组患者的手术策略更加积极,但手术后早期结果与国外的报道相近。
国外研究显示,DeBakeyⅠ型和Ⅲ型患者术后死亡率差异无统计学意义,但是Ⅲ型者稍高[9-10]。本组资料与之不同,DeBakeyⅠ型组的术后早期死亡率高于Ⅲ型组,尽管差异也无统计学意义,该结果可能与本研究中DeBakeyⅠ型患者的主动脉替换范围全部为Crawford Ⅱ 型有关。多项研究表明,Crawford Ⅱ 型者的主动脉替换范围最广泛,术后早期死亡率最高[6,12]。Cosseli等[13]曾报道442例Crawford Ⅱ型TAAA的手术结果,术后早期死亡率为10%,与本组资料相似。
DeBakeyⅠ型组中早期死亡5例,死亡原因分别为:术中顽固性室颤(1例),术后多器官功能衰竭(1例),弥散性血管内凝血(disseminated intravascular coagulation,DIC)(3例)。死于DIC的3例患者均在首次手术时置入支架象鼻血管,支架血管直径分别为26、28、30 mm。在TAAA手术时,左肺与主动脉黏连紧密,游离过程耗时较长,左肺损伤严重,术后止血困难。推测左肺与主动脉紧密黏连可能与降主动脉夹层急性期炎症反应严重,以及象鼻支架直径较大加重术后降主动脉与周围组织炎症反应有关。该结果提示尽管在急性DeBakeyⅠ型夹层手术时同期实施支架象鼻手术有利于二期TAAA手术的近端阻断和吻合,但是支架血管型号的选择不宜过大。
在术后并发症上,两组的脊髓损伤无显著差异。但是,Ⅲ型组术后二次止血、肺部感染和住院透析较Ⅰ型组更多见,其原因可能与Ⅲ型组中DHCA技术的使用比例更高有关。目前,在TAAA手术时使用DHCA技术是否合理存在较大争议。Kouchoukos等[14]和Corvera等[15]报道了使用DHCA技术的良好结果,30 d死亡率为3.6%~7.8%,脊髓损伤2.6%~5.3%,住院透析3.6%~4.1%。然而,Safi等[16]和Cosseli等[17]结果显示,DHCA技术增加了TAAA手术的死亡率和并发症发生率,30 d死亡率为28%~29%,脊髓损伤13%,肾衰7%~15%,肺部并发症67%,气管切开22%,二次止血6%。我院既往研究也发现,TAAA手术时使用DHCA会增加术后二次止血、气管切开的发生率和术后早期的死亡率[18]。目前我院在TAAA手术时不常规使用DHCA技术,主要将其应用于胸主动脉近端不能安全阻断者。
目前,TAAA术中远端灌注技术对于腹腔脏器和脊髓保护的作用已被广泛认可,主要包括左心转流、股股转流和上-下半身动脉的自体转流技术。我院最常采用的是主-髂转流(属上-下半身动脉的自体转流技术),左心转流技术已开始应用,但相关经验较少。
由于手术切除了扩张的病变主动脉组织,降低了主动脉破裂风险,且主动脉再干预率低,两组间的5年生存情况和再干预情况无显著差异。这一结果同最近国外的临床报道类似[9-10]。
高龄或合并多种、严重基础疾病的TAAA患者,外科手术风险较高,而开窗技术和多分支腔内支架血管技术的微创化给此类患者提供了新的治疗机会[19]。但是,这一技术主要适用于真性动脉瘤者,而慢性主动脉夹层扩张形成的胸腹主动脉瘤有其自身特点,如真腔狭窄、内膜片增厚僵硬、分支血管开口位置在真假腔内复杂多变等,这些会增加腔内技术的应用困难[20],并影响远期效果。2019年Oikonomou等[21]报道的71例慢性夹层合并TAAA的治疗结果显示,尽管院内死亡和截瘫结果可接受,分别为5.6%和4.2%,但是术后3年的再干预率因内漏而较高,为47.4%。因此,全腔内介入技术治疗TAAA创伤小,但再干预率高,目前主要适用于高龄(预期寿命短)、合并症多、体弱而不能耐受开放手术的高危患者。本组均为慢性夹层合并TAAA患者,较为年轻,合并症少,且同时合并马凡综合征者多。开放手术是此类患者的首选治疗措施,而且随访结果中主动脉相关的再干预率较低也支持了开放手术治疗效果的有效性和持久性。
本项研究为单中心、回顾性研究,随访时间短,样本量小,未能进行倾向性评分对照研究。随着样本量增加和随访时间延长,两组间远期结果的差异有可能显现,尤其是I型组中合并马凡综合征的比例较高,有待多中心、大样本和前瞻性队列研究及长期随访结果进一步明确两组间的差异。
综上,DeBakeyⅠ型和Ⅲ型TAAA患者的临床基线资料有较大不同。尽管差异无统计学意义,DeBakeyⅠ型者术后早期死亡率相对较高,而DeBakey Ⅲ型者术后并发症相对更常见。在中期生存率和免于心血管再干预方面,两组间未见明显差异,有待于进一步长期随访研究。
——以渤海A 油藏为例

