g-C3N4/BiVO4复合光催化剂制备及其光催化性能研究
李家科,李文涛,刘 欣
(景德镇陶瓷大学 材料科学与工程学院,江西 景德镇 333403)
0 引 言
随着社会经济的快速发展,能源危机和环境污染问题日趋严重,开发新能源、解决环境污染成为可持续发展需要解决的首要问题。半导体光催化氧化作为一种绿色、环保的污染治理手段已成为相关领域的研究热点[1-2]。其中以TiO2为代表的光催化材料在降解有机废水、重金属离子还原等方面得到较多应用,但太阳光能利用率低导致其与实践应用还有一些距离[3]。因此,开发新型具有可见光响应的光催化材料成为研究焦点。
钒酸铋(BiVO4)是一种新型半导体催化剂,其中单斜白钨矿型BiVO4禁带宽度约为2.4 eV,能够被可见光激发产生光催化反应,但钒酸铋具有电子-空穴易复合、表面吸附能力差等问题导致其可见光催化性能并不理想,需要通过改性以提高其可见光催化活性[4-5]。氮化碳(C3N4)是由C元素和N元素构成的有机聚合物,它有5种结构类型,其中类石墨相氮化碳(g-C3N4)具有半导体特性,其禁带宽度约为2.7 eV。g-C3N4具有稳定性强、电子结构独特和良好的可见光催化活性等特点,但同样存在电子-空穴易复合的问题,导致其光催化性能较低[6-7]。
为了降低电子-空穴易复合,提高光催化性能,通常采用离子掺杂、复合等方法对光催化剂进行改性处理。光催化剂复合是一种常见的光催化剂改性方法,是将二种或二种以上能级匹配的光催化剂进行复合,促进光生电子-空穴分离,提高光量子效率,达到改善光催化活性目的[8-11]。本工作以三聚氰胺为原料,在热解法制备g-C3N4基础上,采用水热合成BiVO4过程中加入一定量g-C3N4,从而制得g-C3N4/BiVO4复合光催化剂,主要研究了g-C3N4的复合量对合成g-C3N4/BiVO4复合光催化剂性能的影响,并对光催化机理进行了探讨。
1 实 验
1.1 g-C3N4/BiVO4复合光催化剂制备
1.1.1 原料与试剂
实验所用原料:硝酸铋(Bi(NO3)3·5H2O)、偏钒酸铵(NH4VO3)、三聚氰胺(C3N6H6)、硝酸(HNO3)、氨水和无水乙醇等均为分析纯,实验用水为去离子水。
1.1.2 制备过程
g-C3N4粉体制备:称取一定量的三聚氰胺(C3N6H6)于坩埚,并置于马弗炉中,以5 ℃/ min升到650 ℃、保温60 min,保温结束后自然冷却至室温,即得到g-C3N4粉体;g-C3N4/BiVO4粉体制备:准确称取0.01mol的Bi(NO3)3·5H2O溶于适量稀HNO3以及0.01mol NH4VO3溶于适量浓氨水,待二者完全溶解后在磁力搅拌条件下混合,然后按复合比(理论合成质量比,下同)加入一定量的g-C3N4粉体( g-C3N4∶BiVO4= 0∶1、0.2∶1、0.4∶1、0.6∶1、0.8∶1),持续搅拌30min后调节溶液的pH=7、并定容为100 mL,然后移取该溶液80 mL于聚四氟乙烯内衬(容积为100 mL)的不锈钢反应釜中,在140 ℃反应10 h后自然冷却,然后用蒸馏水、无水乙醇清洗沉淀3次,最后置于80 ℃烘箱干燥后即得g-C3N4/BiVO4粉体。
1.2 样品的性能及表征
采用D8-Advance型XRD(德国Brucker公司)分析粉体的物相组成,分析采用Cu靶(λ= 0.154178 nm),扫描速度为4°/min;采用JSM-6700LV型FE-SEM(日本电子公司)观察粉体的微观形貌;采用ASAP-2020型吸附仪(美国Micromeritics公司)检测粉体的比表面积;采用UV-5100型UV-Vis检测模拟污染物(亚甲蓝溶液、浓度10 mg/L)的吸光度(测定波长为664 nm);粉体光降解亚甲蓝溶液实验在反应器中进行,所用光源为高压汞灯(功率125 W,主波长365 nm),具体检测和计算过程见相关文献[12]。
2 结果与讨论
2.1 试样的物相组成分析
合成试样的XRD图谱如图1所示,图2为图1中的局部放大。从图1可以看出,热解三聚氰胺得到C3N4的衍射峰与标准卡片(JCPDS NO.87-1526)基本一致,在12.8°和27.6°处有两个特征峰,且在27.6°位置的衍射峰强度最高,是芳香物层间堆积的特征峰,表明合成产物为类石墨相氮化碳(g-C3N4)[13]。水热法合成试样衍射峰与标准卡片(JCPDS NO.14-0668)一致,表明合成试样为单斜相钒酸铋(m-BiVO4),且衍射峰峰形完整,峰强度高,表明合成m-BiVO4结晶度较好[5]。此外,从图1还可以看出,当g-C3N4与BiVO4复合后,合成试样的图谱中出现两者的特征衍射峰,且随着g-C3N4复合量的增加,BiVO4衍射峰强度逐渐减弱,g-C3N4的衍射峰强度逐渐增强。此外,从局部放大图2可以看出,在复合试样中,与BiVO4衍射峰强度相比,g-C3N4衍射峰强度较微弱,这是由于在复合试样中,BiVO4为主要成分,所占比例较大,另外,相比于水热法合成的BiVO4而言,热解得到的g-C3N4晶粒尺寸小、结晶度不够造成的(见随后的SEM分析)。

图1 合成试样的XRD图谱Fig 1 XRD patterns of the synthetic samples

图2 图1局部放大图Fig 2 Partial enlargement in Fig 1
2.2 试样的形貌分析
合成试样的SEM照片如图3所示。从图可以看出,热解三聚氰胺制备的g-C3N4(图3(a))呈不规则片状结构,颗粒尺寸较小且团聚严重。采用水热法合成的纯BiVO4(图3(b))呈较规则的短棒状,棒尺寸较均匀,径向尺寸约为300 nm,少数颗粒首尾相连,但整体分散性较好。当BiVO4和g-C3N4复合后,合成试样的形貌、尺寸均发生明显变化(如图3(c)、3(d)),当g-C3N4复合量较少时(如图3(c)),试样以大颗粒状BiVO4为主,在大颗粒表面附着少量小颗粒g-C3N4,小颗粒分布较均匀,但大颗粒BiVO4呈现明显团聚,此外,从图中还可以明显看出,g-C3N4、BiVO4在颗粒大小上存在显著差别,这也证实了XRD的分析;当复合量由g-C3N4∶BiVO4= 0.4∶1增加到0.8:1时,合成试样中的小颗粒数量增加,并且几乎覆盖所有大颗粒表面(见图3(d))。从SEM分析中可知,g-C3N4和BiVO4复合对粉体的微观形貌有着显著影响,同样也会对光催化性能产生影响[14-15]。

图3 合成试样的SEM照片Fig 3 SEM images of the synthetic samples
2.3 试样的光催化性能
图4为试样光降解亚甲蓝的曲线图。从图4可以看出,随着光照时间的延长,亚甲蓝的降解率逐渐增大,说明合成试样均具有一定光催化性能。在暗室环境下搅拌30 min,亚甲蓝的降解率(即t = 0时刻)差别较大,纯BiVO4对亚甲蓝的降解率最低,为9.7%,而g-C3N4对亚甲蓝的降解率最高,达20.4%。此外,从图中还可以看出,在暗室环境下,g-C3N4/BiVO4复合试样对亚甲蓝的降解率随g-C3N4复合量的增加逐渐增大。产生上述实验现象的原因为,在暗室环境下,亚甲蓝的降解实际上是光催化剂对亚甲蓝的吸附,且光催化剂的比表面积越大吸附能力越强,从而表现为亚甲蓝的浓度降低越大。从表1中试样比表面积可知,纯BiVO4比表面积最小,仅为4.57m2/g,纯g-C3N4比表面积最大,为13.56 m2/g,这得益于合成的g-C3N4粒径小,且呈片状结构(图3(a)),因而具有相对较大的比表面积[2],而复合试样比表面积随着g-C3N4量增加而增大,是由于g-C3N4在复合试样中含量增加的结果。

图4 合成试样的光催化性能Fig 4 Photocatalytic performances of the synthetic samples
开启光源后,随着光照时间的延长,亚甲蓝的降解率逐渐增加,但不同试样在相同光照条件下对亚甲蓝的降解率有所不同。从图4中可知,纯BiVO4和g-C3N4对亚甲蓝的降解率相对较低,在光照150 min后,对亚甲蓝的降解率分别为54.8%和66.2%。此外,从图4还可以看出, g-C3N4/BiVO4对亚甲蓝的降解率随g-C3N4复合量的增加呈现先增加后减小趋势,当g-C3N4∶BiVO4=0.4∶1(质量比)时,复合光催化剂的光催化性能达最佳,在光照150 min时,亚甲蓝的降解率达80.8%,比纯BiVO4和g-C3N4分别提高47.5%和22.1%。随后再增加g-C3N4的复合量,亚甲蓝的降解率反而减小,如当g-C3N4∶BiVO4(质量比)比值增加到0.8∶1时,在相同条件下,对亚甲蓝降解率降低到71.7%。产生上述实验现象可以从两个方面进行分析和解释,首先,由于随着g-C3N4量在复合催化剂中增加,提高了其比表面积,增加了对光的吸收,使光催化剂产生更多的光生电子和空穴。同时,比表面积的增加也可以提高光生电子-空穴对的分离效率,提高光量子产率,从而促进光催化效率提高[16],但过多g-C3N4复合量会覆盖BiVO4的表面活性中心,反而使光催化效率降低[17]。

表1 合成试样的比表面积
此外,从光催化剂复合的能带结构来看,依靠相互作用形成p-n结,可以有效提高光生电子、空穴的分离效率,促进光催化剂的催化性能提高[18-19]。g-C3N4禁带宽度为2.7 eV,其导带位置为-1.12 eV,价带位置是+1.58 eV;BiVO4禁带宽度为2.4 eV,导带位置为+0.34 eV,价带位置为+2.74 eV。图5所示为g-C3N4/BiVO4光催化机理示意图,由于二者能带结构非常匹配,匹配的能带结构使得它们结合在一起时形成异质结,在光照条件下,g-C3N4导带中被激发的电子很容易跃迁到BiVO4导带上,同时,BiVO4价带产生的空穴迁移到g-C3N4价带上,使得光生电子与空穴有效分离,从而提高光量子产率,增强光催化性能。
为了研究光催化动力学,把图4中的数据进行处理,然后再经过拟合得到结果如图6所示。从图中可以看出,ln(Ct/C0)与光降解时间t之间呈线性关系,且相关系数R2均接近1(见表2),这说明试样降解亚甲蓝反应符合一级动力学方程[20]。此外,从图6和表2中可以看出,不同试样的光降解的动力学方程有所不同,纯BiVO4和g-C3N4的催化反应速率常数较小(即斜率),随着g-C3N4∶BiVO4复合比值增加,反应速率常数增加,当g-C3N4∶BiVO4=0.4∶1时,催化反应常数(k值) 达到0.00953最大值,随后在增加g-C3N4∶BiVO4比值,反应速率常数减小。由于g-C3N4∶BiVO4=0.4∶1时,合成试样具有最大催化反应速率常数,所以具有最高的光催化性能,这也从动力学角度证实不同复合比例试样具有不同光催化性能的原因。
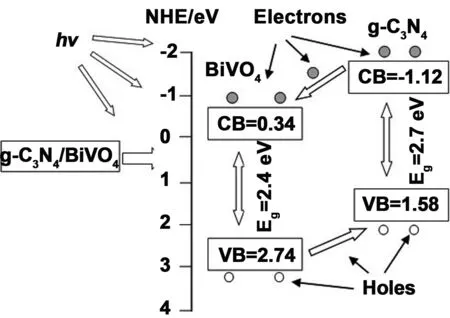
图5 g-C3N4/BiVO4复合光催化剂的催化机理示意图Fig 5 Schematic diagram of photocatalytic mechanism of g-C3N4/BiVO4 composite photocatalyst
表2 试样降解亚甲蓝溶液的反应方程、速率常数和相关系数
Table 2 Reaction equation, rate constant values and correlation coefficient for the degradation of methylene bluewith the synthetic samples
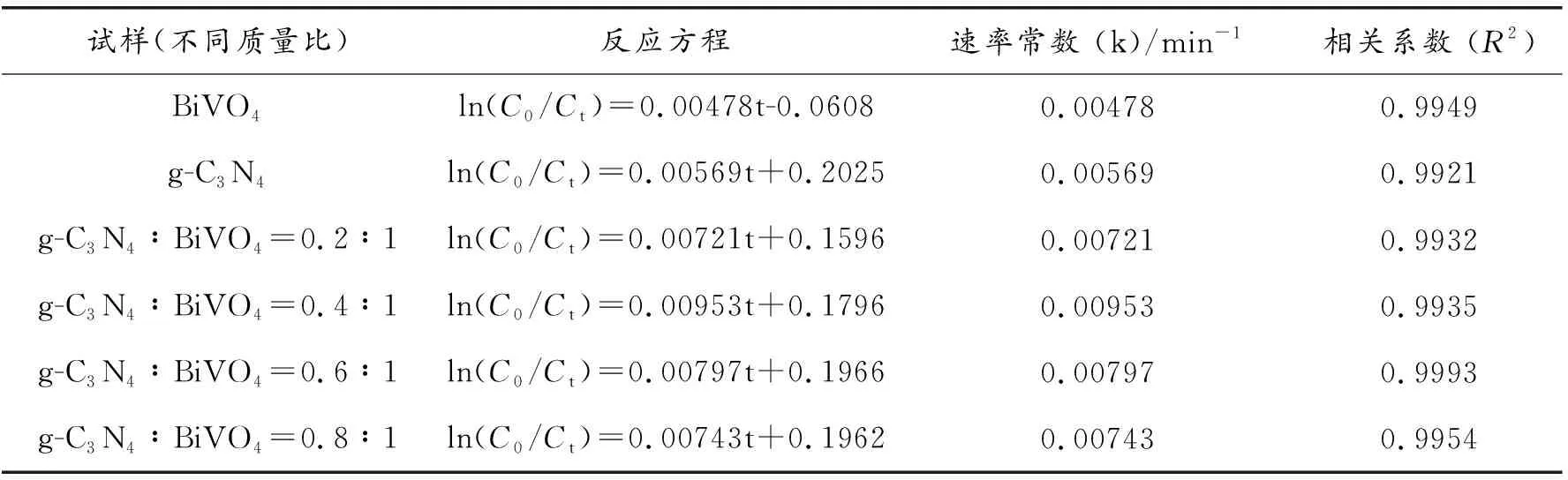
试样(不同质量比)反应方程速率常数 (k)/min-1相关系数 (R2)BiVO4ln(C0/Ct)=0.00478t-0.06080.004780.9949g-C3N4ln(C0/Ct)=0.00569t+0.20250.005690.9921g-C3N4∶BiVO4=0.2∶1ln(C0/Ct)=0.00721t+0.15960.007210.9932g-C3N4∶BiVO4=0.4∶1ln(C0/Ct)=0.00953t+0.17960.009530.9935g-C3N4∶BiVO4=0.6∶1ln(C0/Ct)=0.00797t+0.19660.007970.9993g-C3N4∶BiVO4=0.8∶1ln(C0/Ct)=0.00743t+0.19620.007430.9954

图6 试样降解亚甲蓝的ln (C0/Ct )与光照时间之间关系Fig 6 Irradiation time as a function of ln (C0/Ct ) of degradation of methylene blue with the synthetic samples
3 结 论
(1) g-C3N4/BiVO4光催化性能较纯BiVO4和g-C3N4有显著提高,得益于g-C3N4、BiVO4匹配的能带结构,使二者复合时形成异质结,促进光生电子和空穴的分离,提高光量子产率。同时, 也得益于g-C3N4与BiVO4复合提高了复合光催化剂的比表面积,增加其吸附能力。
(2) 随着g-C3N4复合量的增加,g-C3N4/BiVO4的光催化性能呈现先增加后减小趋势,当g-C3N4∶BiVO4复合比为0.4∶1时,g-C3N4/BiVO4光催化性能最佳,在高压汞灯照射150 min条件下,对亚甲蓝溶液的降解率达到80.8%,比纯BiVO4和g-C3N4光催化性能分别提高47.5%和22.1%,且光催化反应符合一级动力学方程。

