PLCE1 基因突变致激素耐药型肾病综合征1 例报告并文献复习
李旺辉 苏达永 强瑞雪 郝志宏 于 力
1.广州开发区医院儿科(广东广州 510730);2.广州市第一人民医院儿科(广东广州 510180)
原发性肾病综合征(primary nephrotic syndrome,PNS)是儿科常见的疾病,可分为激素敏感型肾病综合征(steroid -sensitive nephrotic syndrome,SSNS)和激素耐药型肾病综合征(steroid-resistant nephrotic syndrome,SRNS)[1]。SRNS患儿预后差,反复迁延不愈者最终发展至终末期肾病(end stage renal disease,ESRD),需要肾替代治疗[2],是临床中非常棘手的问题。因此,寻找导致SRNS根源一直是研究的热点。目前已明确多种基因突变可导致SRNS,尤其是编码足细胞骨架分子相关蛋白的单基因突变在SRNS 中发挥重要的作用[3-6]。目前研究表明,8 个不同的单基因突变能够导致SRNS,包括NPHSl,NPHS 2,WT 1,ACTN4,CD2AP,TRPC6,LAMB2,PLCE1等。其中PLCE1基因则是近年新发现的与儿童SRNS相关的基因[7-8]。文章总结1 例因PLCE 1基因突变致SRNS 患儿的临床特征和基因变异的特点,并复习相关文献。
1 临床资料
患儿,女,2009年2月出生,起病年龄2岁,临床诊断为PNS。父母亲体健,非近亲婚配;否认家族遗传性疾病史。患儿因PNS 多次复发,先后采用激素、环磷酰胺、环孢素A、他克莫司和吗替麦考酚酯等治疗,尿蛋白一直呈阳性,多次住院治疗。5岁时第一次肾穿刺病理检测为“系膜增生性肾小球肾炎(轻-中度)”;7 岁时第二次肾穿刺病理为“局灶节段性肾小球硬化(focal and segmental glomerulosclerosis,FSGS)”。常规询问病史、体格检查、乙肝血清学检查、淋巴细胞CD 系列检测、血糖、胸透及心电图检查结果,除外其他系统疾病。尿沉渣中蛋白质+++、红细胞30~50/HP,白细胞2~5/HP;24小时尿蛋白定量7 428 mg/d。
考虑患儿原发性肾病综合征起病年龄小,频繁复发,激素耐药,肾脏病理为FSGS,多种免疫抑制剂联合治疗效果不佳,激素不良反应增加。患儿9 岁时经医院伦理委员会批准、监护人签署知情同意书后,抽取患儿及其父母各2 mL 外周血,置EDTA 抗凝管中混匀,送嘉检医学检验有限公司行肾病综合征磷脂酶Cε1 (phospholipase C epsilon-1,PLCE1) 基因外显子DNA 检测,并结合患儿临床特征、突变预测、突变位点正常人频率、突变类型等,采用Sanger测序方法验证患儿及其父母相关的基因变异位点。
基因序列分析显示,患儿外周血细胞检测到PLCE1基因的两个杂合变异c.577G>A(p.V193I)和c.2770G>A(p.G924S),见图1。Sanger 测序验证显示,c.577G>A(p.V193I)基因变异来自患儿母亲(杂合状态);患儿父母均无c.2770G>A(p.G924S)基因变异,为新发突变。c.577G>A(p.V193I)和c.2770G>A(p.G924S)变异均为罕见的错义变异,曾在相关PNS病例中被报道,为致病性变异(PMID24533735)。到目前为止,这2个变异在参考人群基因数据库中频率较低,变异所在区域不同物种的氨基酸序列中度保守,分析预测这2个变异可能影响蛋白质结构和功能。患儿最终确诊为PNS(肾炎型,激素耐药型,PLCE1基因突变)。明确诊断后,患儿应用糖皮质激素和环孢素A治疗,并获得缓解。
2 讨论
PLCE1基因定位于常染色体10q23.32-q24.1,全长297581 bp,共含有33 个外显子。其编码蛋白为磷脂酶Cε 1(phospholipase C epsilon-1,PLCε 1)。PLCε 1 蛋白是最新发现的一种磷脂酶C(phospholipase C,PLC)同工酶,在成熟的肾小球足细胞表达,参与肾小球毛细血管袢的形成和正常发育[9]。近来发现,PLCEl基因突变可以引起常染色体隐性遗传性肾病综合征。PLCEl基因移码或无义突变可导致婴儿早发性肾病综合征,其病理特征为弥漫性肾小球硬化(diffuse mesangial sclerosis,DMS);而错义突变可导致FSGS[10]。2006年研究者揭示了PLCE1基因的结构,并用全基因组连锁分析的方法证实PLCE1基因的突变导致家族性常染色体隐性遗传型肾病综合征以来,共发现了13种PLCE1基因突变可导致SRNS,这13 种突变可分为5 种类型:4 种无义突变、5 种碱基小缺失、1种碱基小插入、1种错义突变和2种剪接突变,分别发生在PLCE1基因第2、3、10、14、16、18、21、24、25、29外显子和第9、14内含子上[11]。据报道,13种突变均为点突变,尚未发现基因的重组或大片段缺失[12]。
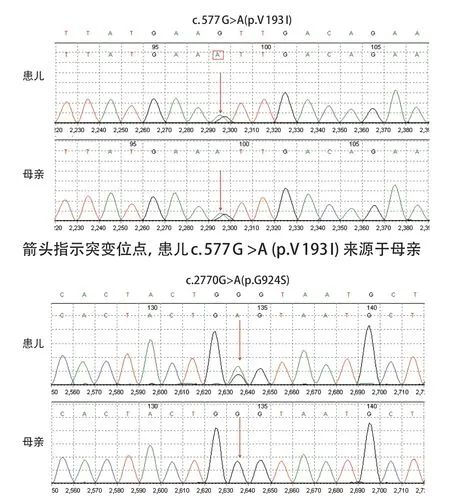
图1 PLCE1 基因验证测序图
研究发现,纯合的PLCE1突变可导致肾脏发育异常并减少蛋白podocin和nephrin的表达而增加发生肾病综合征的易感性[13];也有学者认为突变的PLCE 1可降低足细胞迁移率诱发类固醇抵抗性肾病综合征[14]。虽然目前对于PLCE1造成肾病综合征的具体机制尚不清楚,但众多的研究已让人们对不同类型PLCE 1突变致病特点有了初步的了解。具有PLCEl基因纯合移码或无义突变可导致PLCE 1酶功能缺乏使肾小球发育停止,导致肾脏形态学或功能异常,引起早发性的DSM;PLCEl基因纯合错义突变可导致PLCE1酶活性下降而使肾小球血管慢性损伤,引起发病较晚的FSGS[15]。DMS是先天性肾病综合征的特殊类型,其主要临床特征为出生后1年内发病,常于5岁前迅速进展至终末期肾衰竭,而FSGS 蛋白尿的初发年龄相对较晚,进展到ESRD的时间较DMS慢。目前对于突变的PLCE 1导致DMS 的观点尚有争议,有研究认为PLCE1突变是导致DMS的主要因素,但也有研究发现2例激素耐药型肾病综合征儿童的父亲同时也被发现有同样的PLCE1基因突变,但其父亲均无肾病综合征表现,故不排除其他致病基因可能[12]。
临床实践发现,利用全外显子组测序检测PLCE1在诊断类固醇抵抗性肾病综合征及其治疗中有重要的实用价值。国外研究显示,PLCE 1、NPHS 2和SMARCAL1是检测到的最常见的基因变异[16]。然而国内研究显示,PLCE1变异发现率仅为5.6%[17],NPHS1和PLCE1可能是最常见的变异类型[18]。PLCE1基因变异所致SRNS具有一定的家族遗传性及年龄分布特点。研究显示,0~6岁的SRNS患儿中可检出PLCE1变异,其中以3~12 月龄检出率最高,而6 岁后再无PLCE 1变异检出[19]。因此,PLCE 1基因变异所致的SRNS 具有一定的早发性,且临床病理以DMS 和FSGS 为主,大多对激素和各种免疫抑制剂耐药且预后较差,其原因可能是PLCE 1基因变异区位于EF 手型(EF-hand)结构域;结构域上,而EF结构域中的第1021~1030个氨基酸是金属离子结合的位点,主要参与酶的催化合成,当PLCE1基因发生变异时,机体无法完成正常的蛋白翻译,容易产生SRNS[20-21]。以往报道,由基因变异引起的肾病综合征患儿对糖皮质激素和其他免疫抑制剂治疗都无明显效应。如PLCE 1基因错义变异所致的2 例SRNS 患儿的发病年龄分别为2岁和8岁10月龄,且分别于5岁和 12岁进展到ESRD[22];亦有携带PLCE 1基因无义变异的肾病综合征患儿对激素或环孢素A 治疗有效报道[13]。提示PLCE 1变异引起的肾病综合征对糖皮质激素和环孢素有一定的敏感性,但其药物作用机制尚不明确。
本例患儿为PNS,激素耐药型。患儿起病年龄小,从最初的频繁复发到激素耐药,肾脏病理为FSGS,多种免疫抑制剂联合治疗效果不佳,激素的不良发育增加。患儿PLCE1基因存在2个杂合错义变异 c.577G>A(p.V193I)和c.2770G>A(p.G924S),其中c.577G>A(p.V 193 I)来自患儿母亲(杂合变异),c.2770 G>A(p.G 924 S)为新发变异,均为已报道的致病性变异。这2个变异在参考人群基因数据库中频率较低,变异所在区域不同物种的氨基酸序列中度保守,预测这2个变异可能影响蛋白质结构和功能,使患儿激素耐药,多种免疫抑制剂效果不佳;因随访期限尚不足,其远期预后尚不明确。
PLCE 1变异可导致早发性肾病综合征,在所有具有基因纯合移码的个体中,其肾脏病理为DMS;而在具有错义变异的个体中,其肾脏病理则表现为FSGS,因此PLCE1变异可导致从严重的早发性DMS到FSGS 的一系列组织学表型。肾脏病理为DMS 的PLCE 1变异的个体的肾小球未成熟,且肾组织中Nephrin与Podocin蛋白表达也会降低,表明PLCE1对于毛细血管环阶段的肾小球的正常发育至关重要[23]。值得注意的是,PLCE1变异引起的PNS对糖皮质激素和环孢素有一定的敏感性。这可能是由于在肾小球发育过程中存在着关键时间窗,而在此期间使用糖皮质激素或环孢菌素A 治疗可以改善PLCE 1功能丧失所带来的肾小球发育缺陷。因此,这种治疗方式仅仅适用PLCEl基因纯合移码或无义变异所导致的早期弥漫性肾小球硬化而不是错义变异的PLCE 1导致的晚发性肾病综合征局灶节段性肾小球硬化。这可能意味着错义变异的PLCE 1等位基因能够保证肾小球的适当发育,但在儿童后期可能会干扰肾小球修复过程,从而导致晚期局灶节段性肾小球硬化。这种延缓发病过程可能会导致治疗关键时间窗丧失。后续研究需要对具有PLCE 1变异的个体及其治疗反应进行评估从而证实这些假设。
激素耐药型肾病综合征的治疗临床工作中的重点难点,本例患儿起病后尿蛋白一直呈阳性,多次住院治疗无改善,经明确为PLCE1基因变异后使用糖皮质激素和环孢菌素A 治疗,病情好转。故针对SRNS患儿应尽早行肾穿刺明确病理类型,基于病理类型选择更有效的免疫抑制剂的治疗。针对早发型肾病综合征及SRNS 儿童应考虑到基因突变诱发可能,尽早行基因检测和变异位点分析,找出致病基因特点,对临床诊断和判断预后有重要意义。

