一种特异性识别半胱氨酸的荧光探针的合成及性能研究
陈彩霞,厉凯彬,韩得满
(台州学院 医药化工与材料工程学院,浙江 台州 318000)
0 引言
半胱氨酸(Cys)、同型半胱氨酸(Hcy)和谷胱甘肽(GSH)是哺乳动物体内的三大生物硫醇,它们在生物体内的生理和病理过程中发挥着至关重要的作用[1]。其中,Cys是一种含有巯基的还原性氨基酸,也是人体必需的氨基酸之一。它可以由人体内的蛋氨酸(甲硫氨酸,人体必需氨基酸)转化而来。Cys在蛋白质合成,解毒,金属结合,翻译后修饰和代谢等过程中发挥着重要的作用[2-3]。然而,生物体内硫醇浓度的异常可能会引发多种疾病,Cys的缺乏将会导致儿童生长缓慢、肝脏损伤、皮肤疾病等病症[4];血浆中Hcy的浓度过高会诱发心血管疾病、阿尔兹海默病以及骨质疏松等疾病[5];机体内GSH的浓度的异常会增加白血病、癌症以及艾滋病的发生率[6-7]。因此,迫切需要开发一种有效的方法来选择性地检测Cys、Hcy和GSH。
用于检测巯基物质的方法有很多,包括电化学法、高效液相色谱法(HPLC)以及毛细管电泳法(CE)等[8-9]。相比于这些,荧光探针具有结构多样性、合成成本低、较好的细胞膜渗透性、生物安全性、功能可设计性等优点,已成为快速灵敏检测样品的有效方法[10-12]。最近,已开发出大量用于生物硫醇的荧光探针,相应的设计策略通常基于硫醇基团的强亲核性以及各种反应机理,如迈克尔加成,环化,裂解反应等[13-15]。但由于相似的结构和反应性,大多数报道的文献难以区分这三种巯基氨基酸(Cys/Hcy/GSH)[16-19]。
因此,开发用于区分Cys/Hcy/GSH的选择性荧光探针是非常具有挑战性的。本文报道了一种能特异性识别Cys的荧光探针。该探针是将N-羟乙基-4溴-1,8-萘酰亚胺与SBD-Cl通过哌嗪相连制备而成的,制备方法简单,操作容易,稳定性较好,对Cys响应时间较短,紫外和荧光光谱上都能表现出其独特的变化。
1 实验部分
1.1 实验试剂和仪器
实验中所购买的化学试剂均为分析级。相关的化学反应都在氮气的保护下进行,并不定时地使用硅胶预涂的E-Merck铝板通过TLC监测反应。所有的试验用水均为去离子水。此外,使用四甲基硅烷(TMS)作为内标在Bruker AM-400光谱仪上记录1H和13C NMR光谱。使用标准条件(ESI,70eV)在Waters LCT Premier XE光谱仪上记录高分辨率质谱。使用梅特勒托利多FE28型pH计缓冲溶液pH值的测定。使用安捷伦Cary 60 UV-Vis分光光谱仪进行紫外-可见光谱的测定。使用Varian Cary Eclipse荧光光谱仪进行荧光光谱的测定。
1.2 化合物1的合成
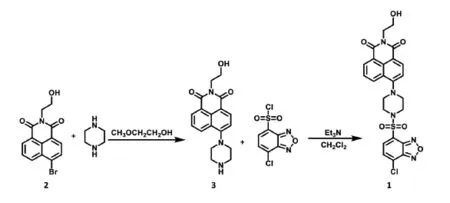
图1 化合物1(探针)的合成路线
第一步:在氮气的保护下,准确称取N-羟乙基-4溴-1,8-萘酰亚胺(2.0 g,6.26 mmol),哌嗪(697 mg,8.10 mmol)置于50 mL圆底烧瓶中,加入20 mL乙二醇单甲醚溶解,在100℃的条件下回流搅拌反应10小时。TLC检测反应完全,停止反应,待混合物冷却至室温,抽滤,所得固体先用少量乙二醇单甲醚溶液洗涤,再用石油醚冲洗,最后放入真空干燥箱内干燥,产物为化合物3,直接用于第二步反应。
第二步:在氮气的保护下,称取第一步产物3(200 mg,0.62 mmol)置于50 mL圆底烧瓶中,加入20 mL二氯甲烷溶解,向上述溶液中滴加208µL三乙胺,再用2 mL二氯甲烷溶解SBD-Cl(126 mg,0.50 mmol),并滴加到上述混合液中,25℃搅拌反应1小时。利用薄层色谱检测反应完全后停止反应,旋转蒸发除去溶剂,并用柱层析(流动相比例:甲醇/二氯甲烷=1/20)分离提纯得到最终产物1 124 mg,产率为98.4%。1H NMR(400 MHz,DMSO-d6)δ 8.44(d,J=8.0 Hz,1 H),8.39(d,J=8.0 Hz,1 H),8.32(d,J=8.0 Hz,1 H),8.11(d,J=8.0 Hz,1 H),7.99(d,J=8.0 Hz,1 H),7.75(t,J=8.0 Hz,1 H),7.35(d,J=8.0 Hz,1 H),4.79(t,J=2.0 Hz,1 H),4.12(t,J=8.0 Hz,2 H),3.57(q,2 H),3.53(m,4 H),3.30(m,4 H);13C NMR(100 MHz,DMSO-d6)δ 164.1,163.6,155.2,149.7,146.7,136.8,133.2,132.4,131.2,131.1,129.5,126.7,126.6,125.8,124.7,123.2,117.0,116.2,58.3,52.5,46.1,42.1;HR-ESI-MS m/z:[M+Na]+calcd.for 564.0721 found 564.0714。
1.3 光谱测试
1.3.1 标准溶液和PBS缓冲溶液的配制
准确称量化合物1(1.0 mg)溶于1.845 mL DMSO中,得[M]=1×10-3mol/L的探针标准溶液。利用Na2HPO4、NaH2PO4配制pH=7.4的磷酸缓冲溶液备用。
1.3.2 随时间变化紫外吸收光谱曲线的测定
准确移取20µL探针1标准溶液,加入到1 mL PBS缓冲溶液和1 mL DMF溶液混合体系中,向其中分别加入50µM Cys,Hcy和GSH,分别测定紫外吸收光谱曲线随时间的变化。
1.3.3 随时间变化荧光光谱曲线的测定
准确移取20µL探针1标准溶液加入1 mL PBS缓冲溶液和1 mL DMF溶液混合体系中,向其中各加入0-50µM Cys,测定并观察荧光光谱曲线随着Cys浓度的变化,激发波长为400 nm。
1.3.4 探针1在不同pH下对Cys的响应测试
准确移取20µL探针1标准溶液加入1 mL HCl-Tris缓冲溶液(pH=2-12)和1 mL DMF溶液混合体系中,向其中各加入50µM Cys,测定并观察探针1在不同pH下对Cys的响应效果。
1.3.5 选择性的测定
分别准确移取20µL探针1标准溶液加入1 mL PBS缓冲溶液和1 mL DMF溶液中,分别向其中加入50 µM的Cys、GSH、Hcy、丙氨酸(Ala)、精氨酸(Arg)、甘氨酸(Gly)、色氨酸(Trp)、苏氨酸(Thr)、苯丙氨酸(Phe)、亮氨酸(Leu)、丝氨酸(Ser)、脯氨酸(Pro)、组氨酸(His)、甲硫氨酸(Met),放置 20 min 后分别测定在不同干扰物存在下荧光发射光谱曲线变化。
2 结果与讨论
2.1 探针1的合成表征
如图1所示,探针1是N-羟乙基-4溴-1,8-萘酰亚胺与SBD-Cl通过哌嗪相连制备而成的,合成简便,便于放大合成,其化学结构和1H NMR,13C NMR,HR-MS分析结果一致。(详细数据见1.2)
2.2 探针的光谱性能测试
为了研究探针的应用价值,以2 mL PBS-DMF(v/v=1:1,pH=7.4)混合溶液为测试体系,研究了探针对Cys的检测性能。如图2所示,当加入过量的Cys后,335 nm处的吸收峰消失,同时400 nm处的吸收峰增强,之后400 nm处的吸收峰红移至410 nm,这表明探针1与Cys的反应过程分两步进行。当加入过量的Hcy/GSH后,只发生335 nm处吸收峰消失和400 nm处吸收峰增强,未出现光谱红移的现象,说明探针1与Hcy/GSH反应只有一步反应。
如图3(a)所示为探针在不同浓度Cys(0-50µM)存在下的荧光光谱图,荧光强度随着Cys浓度的增加而增强,且荧光发射峰由530 nm红移至570 nm。而当加入Hcy/GSH 30 min,530 nm处荧光强度小幅度增强,但并没有发生红移的现象,如图3(b)所示。pH往往是影响探针传感性能重要条件,因此,我们探究了不同pH条件下探针1对Cys的响应情况,如图3(c)所示。探针1在pH=2-12的范围内具有很好的稳定性,且在pH=7-12范围内对Cys较佳的响应效果。这表明探针1可用于在生理环境的pH范围下对Cys的检测。
另外,研究了探针1对Cys的选择性,如图3(d)所示。探针1对Cys具有很好的荧光响应,能对Hcy/GSH产生一定的荧光响应,但其不能使光谱发生红移现象。另外,探针1对其他不含巯基氨基酸(Ala、Arg、Gly、Trp、Thr、Phe、Leu、Ser、Pro、His、Met)不产生荧光响应。上述实验结果表明,探针1对Cys具有优良的选择性。
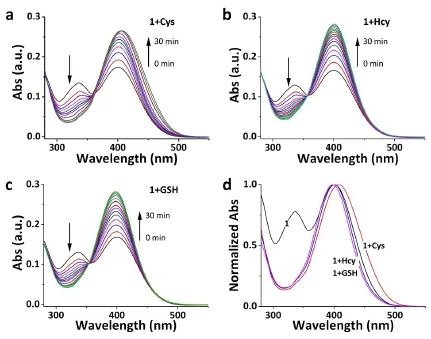
图2 探针1在不同氨基酸下的紫外光谱曲线变化图
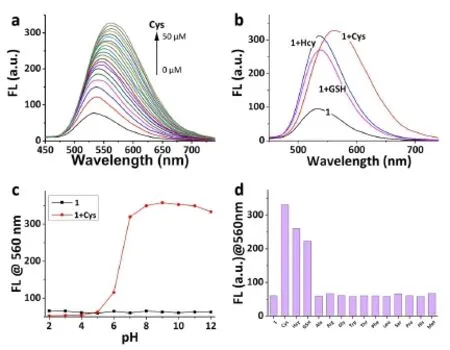
图3 探针1对氨基酸响应的荧光光谱数据图
因此,根据以上紫外荧光光谱性能数据及文献[11]和[13]中报道的有关硫醇响应探针的反应机理,我们推测探针1响应硫醇的反应机理如图4所示。探针1与Cys发生两步反应,Cys分子内的巯基先取代探针分子中的氯原子,随后发生一步分子内重排反应,氨基进一步取代硫原子;由于Hcy/GSH分子内的氨基距离巯基较远,无法发生重排反应。

图4 探针1与Cys和Hcy/GSH的反应机制
3 结论
本文通过两步常规反应,将N-羟乙基-4溴-1,8-萘酰亚胺与SBD-Cl通过哌嗪相连制备得到一种能够用于选择性检测Cys的荧光探针化合物,其化学结构与1H NMR、13C NMR、HR-MS分析结果一致。该探针合成方法简单,光谱性能稳定性较好,可以快速、灵敏地与Cys响应,紫外光谱曲线发生比率型变化,荧光光谱曲线增强同时伴有30 nm的红移。该研究结果为发展新型硫醇类荧光探针提供了思路。

