食品多种重金属元素的检测及其应用
戴 军, 李清洵, 刘海浪, 费晓庆, 蒋彩云
(1.南京市计量监督检测院,江苏 南京 210049; 2.江苏经贸职业技术学院 ,江苏 南京 211168;3.南京海关动植物与食品检测中心,江苏 南京 210001)
1 材料与方法
1.1 材料与试剂
Cr、Zn、As、Cd、Hg和Pb元素标准贮备液(1000 mg/L,均经国家认证并被授予标准物质证书);72Ge、103Rh、185Re内标元素贮备液(1000 mg/L,均经国家认证并被授予标准物质证书);硝酸(65%,Analysis level,Merck,Germany);过氧化氢(30%,Merck Germany)。
1.2 仪器与设备
电感耦合等离子体质谱仪(Agilent 7900CX,USA);Elix Essential型超纯水系统(Millipore,USA);微波消解仪;消解管(四氯氟乙烯);XS204型电子天平(Mettler-Toledo,Awitzerland)。
1.3 方法
1.3.1 样品的选择与处理
按照食品来源将食品分为奶制品、冷饮制品、水产品等。按照样品的分类随机挑选样品,每类至少10个。主要参照GB 5009.268—2016《食品中多元素的测定》处理样品。
1.3.1.1 固态样品
干样:豆类、干制水果、菌类、谷类、焙烤食品、茶叶等,取可食部分,必要时高速粉碎均匀;将固体乳制品、蛋白粉、面粉等呈均匀状的粉状样品摇匀。
鲜样:将水产品、鲜样蔬菜、水果等样品洗净、晾干,取可食部分粉碎均匀;取蛋类、肉类等样品的可食部分,匀浆均匀。
1.3.1.2 液态样品
将软饮料、调味品等液态样品摇匀。
1.3.1.3 半固态样品
将半固态样品搅拌摇匀。
1.3.1.4 速冻及罐头样品
将速冻食品及罐头样品解冻,匀浆均匀。
1.3.2 实验方法
1.3.2.1 标准溶液的配制
混标溶液的配制:用2%的硝酸溶液配制含As、Cr、Cd、Pb、Zn的混标溶液,浓度梯度分别为0、0.5、1、5、10、20、50、100、200、500、1000 μg/L。使用5%的盐酸配制浓度梯度为0.1、0.2、0.5、1 μg/L的Hg标液。
内标溶液的配制:用2%的硝酸分别配制72Ge、103Rh、185Re三种元素的内标元素,浓度皆为100 μg/L。
1.3.2.2 样品的消解
准确称取0.2~0.5 g样品(精确至0.001 g)于消解管中(消解管需提前一天浸泡在20%的硝酸中,使用前用超纯水洗净并烘干),之后加入10 mL的65%的硝酸。如果是难消解的样品,那么加入2 mL 30%的过氧化氢;如果是含有二氧化碳或乙醇的样品,那么先在加热板上低温加热半小时,除去二氧化碳或乙醇,再加入6~10 mL的硝酸。
将加入硝酸后的消解管放置半小时,盖上内盖,旋紧外盖,之后放入微波消解仪。样品消解仪温度条件见表1。消解模式为:20 min后温度升到190 ℃,之后保持190 ℃ 20 min,最后20 min将温度降至60~70 ℃。消解结束后,将样品溶液倒入离心管,用纯水定容至50 mL,同时做质控样与空白样。

表1 样品消解仪温度条件
1.3.2.3 样品分析
打开电脑和ICP-MS系统,按照测定要求调谐仪器,将已经配制好的元素标准溶液注入电感耦合等离子体质谱仪,同步使用蠕动泵加入内标,测定元素分析谱线的信号响应值。以待测元素的浓度为横坐标,以待测元素的信号响应值为纵坐标,绘制标准曲线。接着,将经过前处理的空白液、质控液、样品液依次注入电感耦合等离子体质谱仪中,同步使用蠕动泵加入内标,并测定元素分析谱线的信号响应值,依照标准曲线得出对应浓度。
2 结果与分析
2.1 仪器干扰校正
ICP-MS干扰可分为两大类:质谱干扰和非质谱干扰(基体效应)。
质谱干扰:应用碰撞反应池技术,以氦气作为反应气,通过碰撞解离与动能歧视消除多原子离子干扰,同时选择合适的同位素,尽量避免同量异位素以及等离子体气等背景离子所形成的多原子离子的质谱干扰。同步校正仪器内设的干扰校正方程。
非质谱校正:标准溶液的基质与样品基质存在差异,测定时可能会产生基体效应从而影响分析结果的准确性。应采用在线内标溶液,以校正仪器灵敏度漂移并减弱基体效应的影响。
2.2 元素同位素和内标的选择
以与待测元素质量数和电离能相近为原则,选择72Ge、103Rh、185Re作为内标元素,详见表2。

表2 待测元素同位素和内标元素选择表
2.3 准确度实验
本实验在样品测量之前均进行标准物质的检测——质控检测。分别称取0.5 g左右的鸡肉和芹菜,处理方式同样品一样,得出的各元素含量误差均在允许误差范围之内。
2.4 精密度实验
样品元素含量大于1 mg/kg时,在相同的条件下获得的两次独立测定实验结果的绝对差值不超过算术平均值的10%;小于或等于1 mg/kg且大于0.1 mg/kg时,在相同的条件下获得的两次独立测定实验结果的绝对差值不超过算术平均值的15%;小于或等于0.1 mg/kg时,在相同的条件下获得的两次独立测定实验结果的绝对差值不超过算术平均值的20%。
2.5 实际样品检测
通过校正仪器等措施,确保本实验的准确可靠性。在此基础上进行样品的检测,得出的各样品数据见表3—13。

表3 奶制品与冷饮制品元素测定结果

表4 水产品元素测定结果

表5 食用菌类元素分析表

表6 蔬菜及其制品元素测定结果

表7 肉及肉制品元素分析表
续表7:

肉及肉制品Cr/(mg/kg)Zn/(mg/kg)As/(mg/kg)Cd/(mg/kg)Hg/(mg/kg)Pb/(mg/kg)壹号土猪上肉0.00729919.7824530.0009190.0000250.000204<0.000冻优选羊后腿0.02330221.6664880.0021310.0004430.000125<0.000肥牛肉片0.05460822.4880040.003684<0.0000.000143<0.000羔羊外脊切片0.01773624.1684150.0017350.0000240.0000850.003444羊排0.02868725.6371110.0034500.0027190.0001850.025413精致肥牛片0.02319127.3077450.0043090.0006260.000167<0.000猪肾0.01286533.2761040.0043370.0498130.0087230.011499大黄瓜条(牛肉)0.01062035.6379820.0024470.0000920.000437<0.000牛腱子0.01326649.5165940.006187<0.0000.0000960.123462猪肝0.00874598.7826420.0023250.0187240.0017940.004737
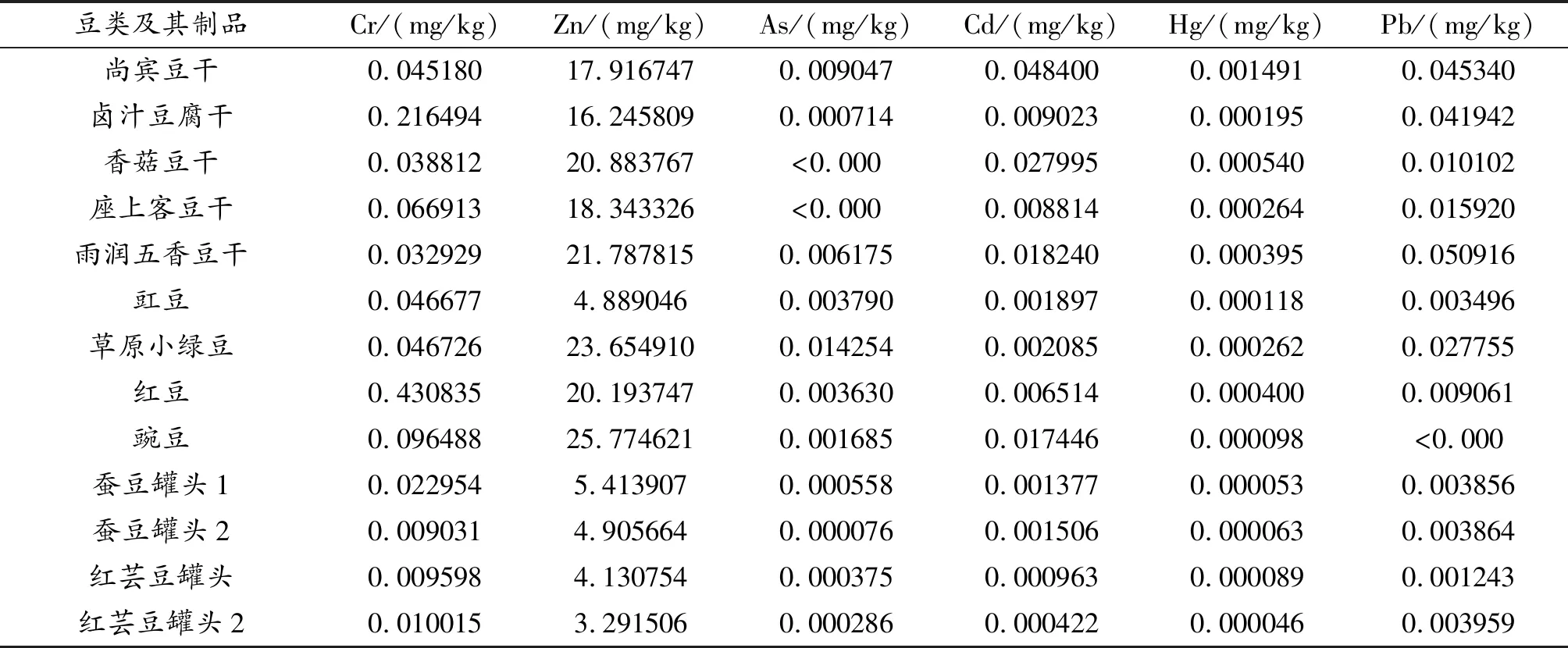
表8 豆类及其制品元素分析表

表9 谷物制品元素分析表

表10 水果及其制品元素分析表

表11 谷物制品元素分析表
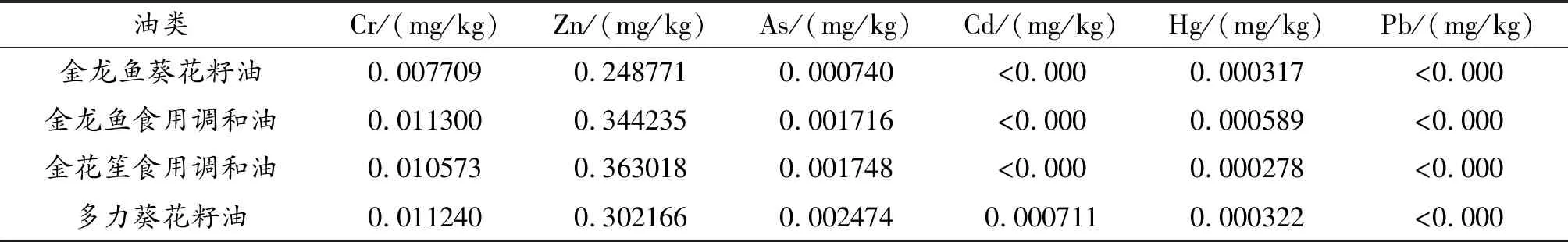
表12 油类元素分析表

表13 蜂产品元素分析表
2.6 检测数据在风险评估中的应用
2.6.1 数据分析
奶制品富含Zn元素,Cr、As、Cd、Hg、Pb元素的含量较少,但是在冰淇淋等冷饮制品(尤其是巧克力冰淇淋)中各元素含量都显著增加。通过表14可知,冷饮制品Hg的限量为0.5 mg/kg,Pb的限量为0.5 mg/kg。江鱼、海鱼的As含量很高,在花蛤等双贝壳的海产品中Pb的含量偏高。在蔬菜中所测的六种元素含量均正常。在水果及其制品中所测六种元素含量非常少。食用菌Zn的含量较高。所测肉制品的六种元素含量均正常,但牛羊肉及猪肝猪肾的Zn元素含量偏高。在豆制品的六种元素中,Zn含量偏高。油类制品各元素含量均正常。蜂产品的蜂胶Cr元素含量偏高。
2.6.2 各类食品风险评估
人体对Cr元素的需求量较少。除蜂胶、动物内脏外,其余产品Cr含量均不高。Zn元素是人体需求的主要元素之一。乳制品、牛羊肉、动物肝肾脏、食用菌和豆制品都含有较高的Zn元素。过量的Zn元素会导致Zn中毒,不能盲目补充Zn。As对人体造成的伤害巨大。水产品(尤其是壳类产品)的Pb、Hg含量较高。食品各元素的限量见表14。
3 结论
本文采用微波消解法进行样品前处理,通过电感耦合等离子体质谱仪(ICP-MS)对奶制品、水产品等12类食品的Cr、Zn、As、Cd、Hg、Pb六种重金属元素进行测定,并将测定结果进行分类、整理,以期为食品安全风险评估提供理论和技术依据。

表14 样品中各元素的限量

