6例囊性中性粒细胞性肉芽肿性乳腺炎的临床病理学及预后特征分析
刘 敏 朱 庆 蔡茹艺 张 瑞 张红凯
(首都医科大学附属北京中医医院病理科,北京 100010)
肉芽肿性小叶性乳腺炎(granulomatous lobular mastitis,GLM)通常被认为是一种致病原因不清的特发性乳腺炎,以形成肉芽肿性结构为主要特征。临床表现包括乳房肿块、脓肿形成、皮肤破溃等;临床常难以与乳腺癌区别。对“肿物”进行穿刺检查,病理可以确诊。但由于缺乏特异治疗手段,病变常迁延不愈,对患者生理和心理造成较大影响。囊性中性粒细胞性肉芽肿性乳腺炎(cystic neutrophilic granulomatous mastitis,CNGM)是乳腺肉芽肿性病变中的一种独特类型:它与细菌感染密切相关且具有独特的组织学形态,因此部分学者建议应单独为其命名。
CNGM的临床表现通常与GLM类似:多见于年轻女性、近期有哺乳史、发现乳腺肿物而影像学检查往往不能除外恶性病变可能[1];但其镜下有特征性形态学改变:病变区域可见以乳腺小叶为中心的亚急性炎性反应病变,中央可见透明空泡样小囊腔(直径约200~800 μm),囊壁由中性粒细胞围绕,外层被较为广泛的含大量组织细胞、淋巴细胞及浆细胞、多核巨细胞的肉芽肿性结构围绕[2]。该名称2011年由Renshaw 等[3]采用,并认为其与革兰阳性细菌——棒状杆菌感染有关。其后部分研究[4-5]也证实其与细菌相关。但由于抗炎治疗的效果欠佳,因此有人[6-7]对其与细菌感染的关系仍有不同意见。还有研究[8]显示,虽经抗感染、激素等治疗,该病仍易复发。由于该病名称使用时间不长,国内外明确报道病例数目较少,因此现对首都医科大学附属北京中医医院近期具有典型形态学特征的病例进行报道,以期增加大家对此病的认识,积累更多经验。
1 病例资料
一般情况及检查:收集2019年5月至2019年12月首都医科大学附属北京中医医院病理科确诊的6例CNGM患者的临床及病理资料。6例患者均为女性,平均年龄(32.3±2.4)岁(30~37岁),全部有哺乳史,哺乳时间3~48个月,患者在发病时间1周至4个月时就诊,就诊时孩子1~5岁;其中4例表现为一侧乳腺肿块,2例患者为双乳肿块(患者先后出现左乳及右乳肿物,间隔2至12个月发病),肿块最大径约1~8.8 cm,质硬,边界尚清,活动度一般,伴有局部疼痛及压痛;4例患者伴有受累乳腺表面皮肤发红,1例发病时间较长者(>1 个月)伴表面皮肤破溃,还有3例患者在后期也出现溃口;1例患者乳头凹陷伴乳头粉渣样分泌物,1例患者乳头略短伴乳头黄色分泌物,其余4例患者乳头无内陷,无溢液,全部患者均未见皮肤橘皮样变及酒窝征。
所有患者经乳腺B超提示多发不规则低回声区或结节,5例患者可见腋下多发淋巴结肿大,临床因不能完全除外乳腺癌行粗针穿刺检查。其中3例患者外周血白细胞总数、中性粒细胞百分比和绝对值均升高,2例患者还伴有外周血C反应蛋白和红细胞沉降率升高;1例患者泌乳素浓度持续升高(最高157.48 ng/mL)伴双小腿结节红斑,1例患者泌乳素浓度波动升高(最高67.65 ng/mL)。所有患者均未见低烧、午后潮热等结核感染症状。
所有收集的组织标本经病理常规固定、包埋、制片和苏木精-伊红(hematoxylin-eosin,HE)、抗酸及Gram染色以明确诊断。所有Gram染色切片均设置批次阳性(已知Gram染色阳性标本)和阴性(正常乳腺组织)对照。由两名病理医师分别阅片并最后确诊。
病理特征:患者组织标本经HE染色可见明确肉芽肿性炎样结构形成,病理诊断符合GLM,并且均可见到以乳腺小叶为中心的肉芽肿、中心小脓肿及伴明显中性粒细胞围绕的囊状空腔等特征性结构(图1A,B),符合CNGM的诊断。Gram染色结果显示在6例穿刺活检标本中均发现革兰染色阳性/阴性的杆菌。其中发现革兰阳性菌 4例(图1C,D),革兰阴性菌2例。多数情况下,Gram染色仅见少量细菌,并且通常仅存在于1或2个空泡内(并常位于空泡边缘)。这些细菌在HE染色的切片中并不明显。有趣的是,细菌仅在囊腔内发现,未见于囊腔外的组织内。抗酸染色未找到抗酸杆菌,同时结核杆菌DNA检测结果均为阴性。
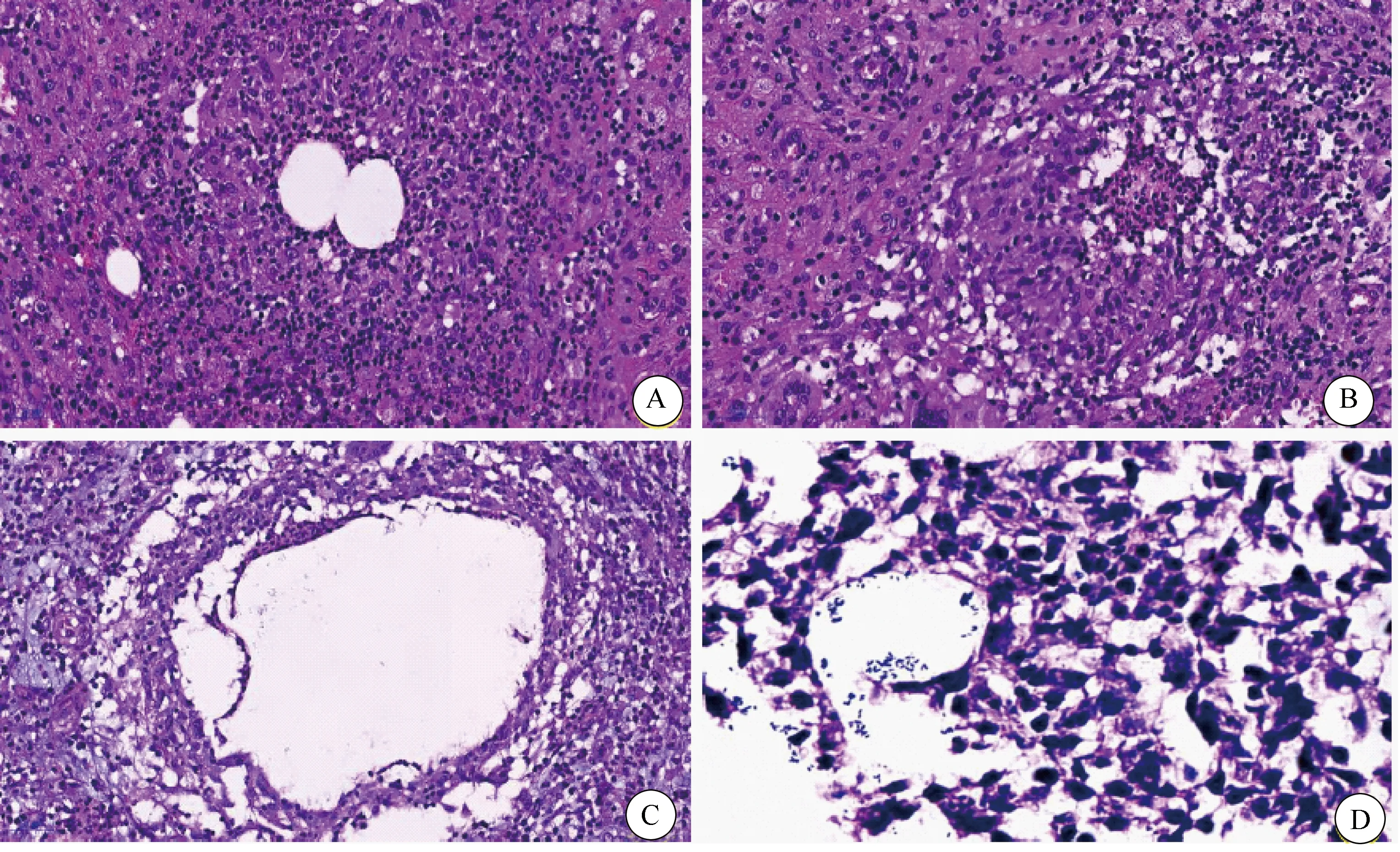
图1 组织标本染色
治疗及预后:所有患者从发病到本次研究随访约经过15~295 d。2名患者经中药内服及药膏外敷及贴敷治疗以及必要时切开引流排脓和对破溃创口清创等治疗1~5个月后,症状减轻或消失(表现为乳腺肿块缩小,疮口愈合,自觉疼痛及压痛减轻至消退);1例患者行肿物切除术后切口愈合良好;以上3例患者经随访2~42周未见复发。1例患者伴高泌乳素血症并伴双小腿结节性红斑,间断口服溴隐亭8 d进行降泌乳素治疗,但病情迁延,患者目前结块较前缩小和变软伴皮色紫暗,无明显渗出,仍在门诊随诊观察;1例患者为相继12个月出现双侧乳腺肿块,有/无可触及结块伴溃口,患者穿刺液细菌培养及穿刺液找抗酸杆菌均(-),曾出现泌乳素升高(67.65 ng/mL),经中药内服外敷及切开引流排脓治疗3个月后,结块缩小但仍有溃口伴较多黄稠脓液;1例患者为相继2个月出现双侧乳腺肿块,后自行破溃,曾在外院静脉滴注抗生素、理疗、穿刺引流,肿物无明显缩小,后在本院经中药贴敷及清创治疗仅3周,可见左乳局部红肿伴5 mm溃口及脓性分泌物,目前门诊继续治疗观察中。
2 讨论
GLM是一类发生在育龄妇女、病因不明、治疗效果不佳、在临床常常导致皮肤溃烂、迁延不愈,被临床称为“不死的癌症”的良性炎性反应性疾病。临床表现及影像检查难以与乳腺癌鉴别,明确诊断常需病理学诊断。
GLM早期形态学改变无特异,可见乳腺小叶及间质内大量淋巴细胞及浆细胞浸润;中期形态学可见上皮样组织细胞增生并形成肉芽肿结构,其中央可见小脓肿(化脓性肉芽肿);后期病变区域可见纤维母细胞增生。虽然前期的研究[9]显示这类乳腺肉芽肿性炎性反应可伴有小脓肿形成,但并未发现特定种类细菌与之有关,因此,又将其称为特发性肉芽肿性小叶性乳腺炎。直到2003年,Taylor等[10]在34例肉芽肿性小叶性乳腺炎的组织内发现一种Gram染色阳性的棒状杆菌与之密切相关,因此,推测其发病可能与此类棒状杆菌有关;此后国外文献[2]又有少量类似病例报道,并将这种具有较为特异病理学特征——病变区域可见以乳腺小叶为中心的亚急性炎性反应性病变,炎性反应中央可见透明空泡样小囊腔(直径约200~800 μm),囊壁由中性粒细胞围绕,外层被较为广泛的含大量组织细胞、淋巴细胞及浆细胞、多核巨细胞的肉芽肿性结构围绕的病变称为CNGM。而在国内,即使近期发表的关于GLM的较大样本的研究[11]显示少数病例具有类似病理改变,有时小囊腔内也可见细菌,但其并未如国外文献[2]一样改称CNGM,而仍将其归于一直沿用的“肉芽肿性乳腺炎”的范围内。因此,不能确知他们报道的病例是否与国外报道[2]的CNGM有差别。而笔者对近期临床工作中所见的6例具有典型CNGM病例特征的肉芽肿性病例进行总结,以期引起临床重视及提供一定的诊治参考。
在本文的病例中,与之前文献[2]所报道的CNGM的病例相似——除了形态学上的类似外,在小囊腔内见到革兰染色阳性的杆菌。而引起CNGM的杆菌多为克氏棒状杆菌[2]。棒状杆菌属细菌具有亲脂性,这可能解释它们总是分布在肉芽肿的脂质空腔周围[12];而囊腔壁上数量不等的中性粒细胞性微脓肿结构的形成可能与中性粒细胞的功能缺陷有关[13]。但克氏棒状杆菌体外培养很难成功[2],因此依靠细菌培养的方法鉴别细菌种类阳性率很低;在HE染色状态下通常细菌数目较少,不易观察而易被忽视;这些可能是该病在很长一段时间未被认识的原因。目前,随着分子生物学进步,鉴别细菌种属的方法还常用PCR的方法。但部分研究[2]显示,分子检测的阳性率也并未见优于Gram染色,推测可能是由于组织甲醛固定或细菌较少原因所致。而在部分具有典型特征的CNGM病例中,却并未能检出特异细菌。而在本文的病例中,有2例还检出Gram阴性菌,这与此前的报道[2]不完全符合。而CNGM与细菌的关系还需更多样本的研究进行证实。
在病理诊断过程中,需要将CNGM与其他病因所导致的肉芽肿性乳腺炎进行鉴别诊断:如结核分枝杆菌所致的结核病、真菌感染所致的肉芽肿性炎、全身系统性疾病如结节病、乳腺外伤后引起的乳腺脂肪坏死等疾病。通常结核分枝杆菌常会导致伴干酪样坏死的肉芽肿,但一般不会含有大量的中性粒细胞脓肿;结节病所形成的是境界清楚的非坏死性(主要由上皮样组织细胞所构成)的肉芽肿;真菌感染时一般通过PAS/六胺银等特殊染色可见真菌[14]。
CNGM的临床表现和影像表现均与GLM类似:患者为经产妇,年龄较轻(20~40岁)。患者通常近期于乳腺内出现可触及的肿块及炎性反应(红、肿、热、痛、窦道形成)或类似乳腺癌(乳头内陷和局部淋巴结肿大)的症状和体征;部分患者可出现乳头溢液。
目前对CNGM的治疗还存在争论,缺乏共识。常规抗生素治疗或激素治疗效果欠佳,病程迁延不愈。西医的治疗方法常为综合性治疗手段,包括外科手术切除、引流、抗生素和激素联合治疗,但效果也不能令人满意[15]。在本文的病例中,通过口服解郁、活血等传统中医药治疗,对于有脓肿破溃的病例联用外科引流,不采用激素、抗生素及脓肿切除治疗,疗程常在1~6个月之间,患者乳房形态通常能保持良好,效果较为满意。
总之,本研究总结了笔者近期诊断的CNGM病例的组织病理学以及临床特征,在其中也发现了Gram染色的细菌,但本文的病例并未接受抗生素的治疗,而是主要采取中医保守治疗,结合外科引流方法,取得较好的疗效。因此,笔者认为有关棒状杆菌与CNGM的发病及治疗方面的关系仍需进一步的研究;而将其作为一种独特的疾病进行区分,将有助于更好地认识此病。

