艾拉莫德治疗原发性干燥综合征疗效及安全性的Meta分析
房艳华,黄建峰
连南瑶族自治县人民医院药剂科,广东 清远 511500
原发性干燥综合征(primary Sjogren's Syndrome,pSS)是一种影响唾液腺和泪腺等外分泌腺为主的自身免疫性疾病,发病机制至今仍未完全明确,患者最常表现为眼睛干涩和口干的症状,但高达50%可能另外发展出腺外表现,如关节炎、血管炎、多发性神经病、肺纤维化或间质性肾炎[1]。近年来,越来越多的证据表明B淋巴细胞活化增加参与pSS发病机理[2]。因此,基于病因学,B 细胞耗竭疗法目前被认为是治疗pSS的新希望,这治疗方法能够在pSS 的早期阶段阻止疾病的进展[3-4]。艾拉莫德(Iguratimod,IGU)是一种新型的改善病情的抗风湿药物。研究表明[5],它具有抑制NF-KB 的活化,进而抑制炎性细胞因子的产生;同时它还可以直接与B淋巴细胞作用,抑制免疫球蛋白的产生;此外,它还具有选择性抑制COX-2 酶的活性。虽然近年来不断有艾拉莫德治疗原发性干燥综合征的随机对照研究,但对其尚缺乏系统研究与评价。本文通过对最终纳入的9 篇文献进行严格的质量评价和分析,以期对艾拉莫德治疗原发性干燥综合征的疗效及安全性做出评价,为临床应用提供一定的指导意义。
1 资料与方法
1.1 文献检索策略 计算机检索万方科技期刊全文数据库、中国生物医学文献数据库、维普及中国学术期刊(CNKI)全文数据库、PubMed、EMBASE、Cochrane library、Web of science 中有关艾拉莫德治疗原发性干燥综合征的RCT,截至2019 年7 月。采用主题词结合自由词方式进行检索,中文检索词包括“艾拉莫德(艾得辛、T-614)”“随机”“随机对照试验”“干燥综合征”;英文检索词包括:“Iguratimod (IGU)”“Elamode”“T-614”“Disease-modifying anti-rheumatic drugs (DMARDs)”“Randomized controlled trials(RCT)”“Sjogren's syndrome(SS)”。
1.2 纳入标准 ①研究类型:随机对照试验,无论是否采用盲法;②研究对象:经临床明确诊断为原发性干燥综合征的患者;③干预措施:试验组接受艾拉莫德治疗或在对照组基础上联合艾拉莫德治疗,对照组接受安慰剂治疗或传统药物治疗;④结局指标:血沉(erythrocyte sedimentation rate,ESR)、类风湿因子(rheumatoid factor,RF)、血小板计数、血清IgG、Schirmer 试验、唾液流率、干燥综合征患者报告指数(Sjogren's syndrome reported index,ESSPRI)、干燥综合征疾病活动指数(European league against rheumatism SS disease activity index,ESSDAI)、总有效率、药物不良反应发生率;⑤文献语种限为中、英文。
1.3 排除标准 ①资料雷同或重复发表的文献;②动物试验、病例报道、综述、会议摘要且无全文;③数据不全,联系作者无果或无法计算结果的研究;④自身对照的研究;⑤有合并类风湿关节炎、系统性红斑狼疮、皮肌炎、硬皮病等其他免疫系统疾病的研究。
1.4 文献筛选、资料提取及质量评价 由2名研究者独立筛选文献、提取资料并交叉核对。如有分歧,则通过讨论协商决定结果。筛选文献时先阅读题目和摘要,排除不相关的文献后对筛余的文献通过进一步阅读全文以确定是否纳入。资料提取内容主要包括:①纳入研究的基本信息:研究题目、第一作者、发表年份等;②研究对象的基线特征;③结局指标等重要信息。2名研究者独立采用Cochrane风险偏倚评估工具评价研究的方法学质量,意见不一致时,通过讨论协商决定结果。
1.5 统计学处理 采用Review Manager 5.3软件进行统计分析。统计变量为连续型变量则用均数差(Mean Difference,MD)及95% 可信区间(Confidence interval,CI)为效应指标,若为二分类变量则采用相对危险度(Relative risk,RR)及95%CI 为效应指标,对纳入文献的数据进行异质性检验,如各研究数据无明显异质性时(P>0.1,I2<50%),则采用固定效应模型分析。如各研究间有明显异质性(P<0.1,I2>50%),则采用随机效应模型分析并慎重解释所得的结果,最后可得到结局指标的森林图结果、合并MD值和合并RR值以及95%CI。
2 结果
2.1 检索结果及质量评价结果 数据库检索获得相关文献共332篇,逐层筛选后最终纳入9文献[6-14],均为中文文献,9 项RCT 中共纳入642 例原发性干燥综合征患者(试验组321例,对照组321例)。纳入的文献均采用随机对照方法,其中4篇文献[7-10]采用随机数表随机分配,1 篇文献[6]采用计算机法随机分配,1 篇文献[14]采用信封式随机分配,其余文献未提及具体方法,仅出现随机字样;1 篇文献[13]仅出现盲法字样;其余均缺乏分配隐藏及盲法的具体描述。文献筛选流程如图1所示,文献基本资料情况如表1所示,文献质量评价如图2、图3所示。
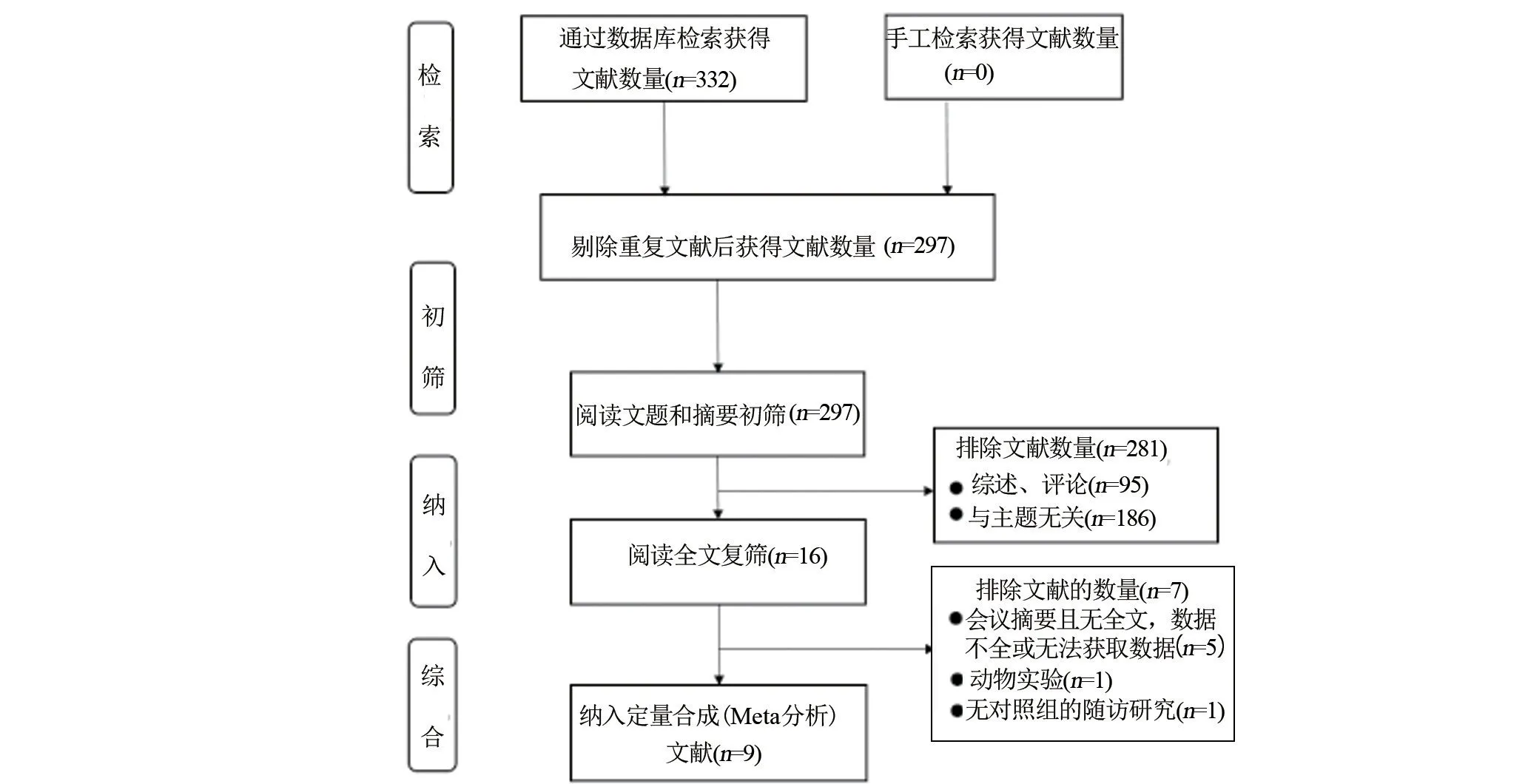
图1 文献筛选流程图
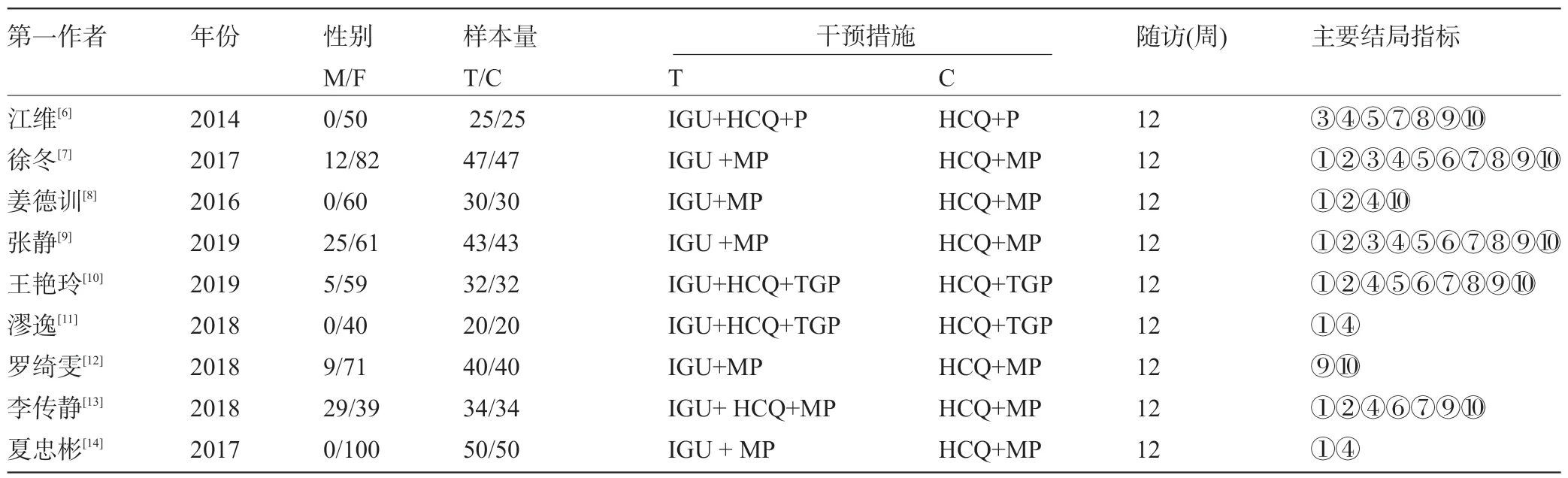
表1 纳入文献的基本资料
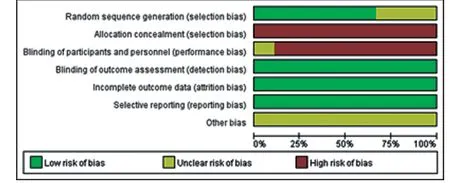
图2 纳入研究的偏倚风险图
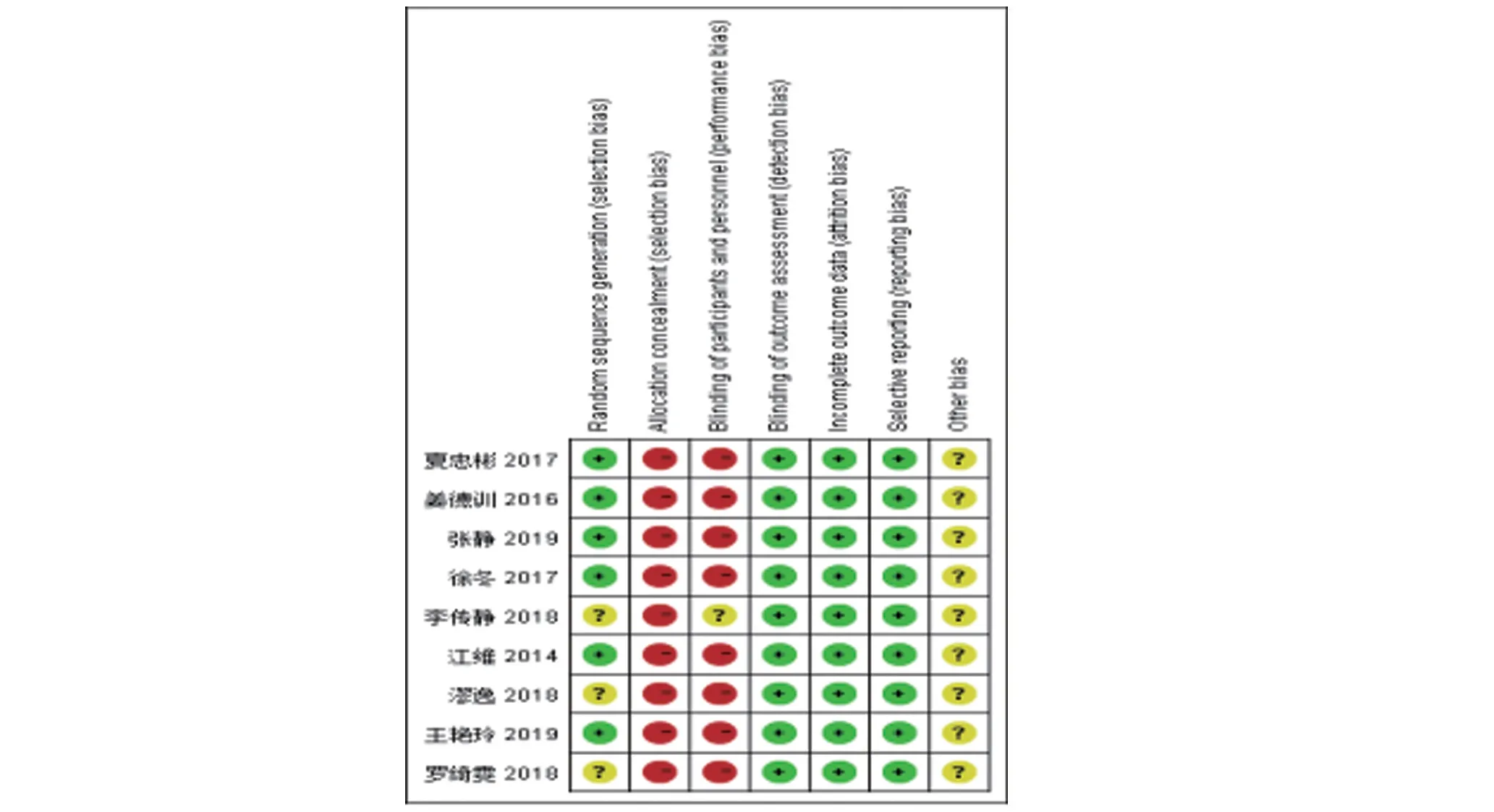
图3 纳入研究的偏倚风险总结图
2.2 发表偏倚检验结果 使用Stata12.0 软件对以RF、IgG为结局指标的研究进行Egger's test,结果表明P均>0.05,提示不存在发表偏倚(见表2)。

表2 RF和IgG的Egger's test结果
2.3 Meta分析结果
2.3.1 血清学指标比较
2.3.1.1 血沉 7 篇文献[7-11,13-14]报道了血沉在治疗前后的变化,共纳入512 例原发性干燥综合征患者。异质性检验P>0.1,I2=0%,表明纳入的研究同质,采用固定效应模型分析,结果显示,试验组降低血沉作用优于对照组,差异具有统计学意义[MD=-5.49,95%CI(-7.80,-3.19),P<0.000 01](图4)。
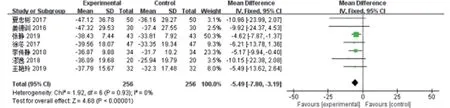
图4 试验组与对照组ESR比较的Meta分析
2.3.1.2 类风湿因子 6 篇文献[7-10,13-14]报道了类风湿因子在治疗前后的变化,共纳入472例原发性干燥综合征患者。异质性检验P>0.1,I2=0%,表明纳入的研究同质,采用固定效应模型分析,结果显示,试验组降低类风湿因子作用优于对照组,差异具有统计学意义[MD=-5.68,95%CI(-8.30,-3.06),P<0.000 1](图5)。
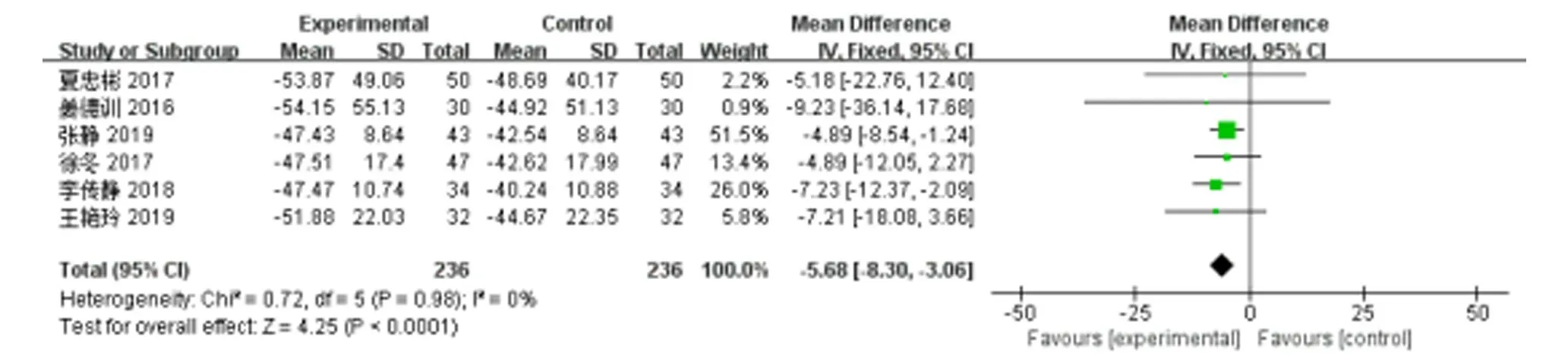
图5 试验组与对照组RF比较的Meta分析
2.3.1.3 血小板计数 3篇文献[6-7,9]报道了血小板计数在治疗前后的变化,共纳入230 例原发性干燥综合征患者。异质性检验P<0.1,I2=69%,表明研究间存在统计学异质性,采用随机效应模型分析,结果显示,试验组提升血小板计数作用优于对照组,差异有统计学意义[MD=16.54,95%CI(10.12、22.96),P<0.000 01](图6)。

图6 试验组与对照组血小板计数比较的Meta分析
2.3.1.4 血清IgG 8 篇文献[6-11,13-14]报道了血清IgG在治疗前后的变化,共纳入562例原发性干燥综合征患者。异质性检验P<0.1,I2=83%,表明研究间存在高度异质性,考虑干预因素存在一定差异,以干预因素进行亚组分析,结果示各亚组中试验组降低血清IgG 作用均优于对照组,亚组合并结果示[MD=-2.87,95%CI(-4.41,-1.33),P<0.000 3](图7),并采用逐篇剔除法进行敏感性分析,合并效应量及I2结果无明显变化,提示结果尚稳定。
2.3.2 外分泌腺体功能比较
2.3.2.1 Schirmer 试验 4 篇文献[6-7,9-10]报道了Schirmer 试验结果(泪腺分泌功能)在治疗前后的变化,共纳入394 例原发性干燥综合征患者。异质性检验P<0.1,I2=91%,表明研究间存在高度异质性,考虑干预因素存在一定差异,以干预因素进行亚组分析,结果示各亚组中试验组泪腺分泌功能改善程度均优于对照组,亚组合并结果示[MD=2.61,95%CI(2.33,2.89),P<0.000 01](图8),并采用逐篇剔除法进行敏感性分析,合并效应量及I2结果无明显变化,提示结果尚稳定。

图7 试验组与对照组血清IgG比较的Meta分析
2.3.2.2 唾液流率 4 篇文献[7,9-10,13]报道了唾液流率(唾液腺分泌功能)在治疗前后的变化,共纳入312例原发性干燥综合征患者。异质性检验P<0.1,I2=60%,表明研究间存在统计学异质性,采用随机效应模型分析,结果显示,试验组唾液腺分泌功能改善程度优于对照组,差异具有统计学意义[MD=0.42,95%CI(0.30,0.54),P<0.000 01](图9)。

图8 试验组与对照组Schirmer试验比较的Meta分析

图9 试验组与对照组唾液流率比较的Meta分析
2.3.3 患者临床症状评分比较
2.3.3.1 ESSPRI 评 分 5 篇 文 献[6-7,9-10,13]报 道 了ESSPRI评分在治疗前后的变化,共纳入362例原发性干燥综合征患者。异质性检验P≥0.1,I2=48%,表明研究间的统计学异质性较小,采用固定效应模型分析,结果显示,试验组降低ESSPRI 评分优于对照组,差异有统计学意义[MD=-2.12,95%CI(-2.37,-1.88),P<0.000 01](图10)。
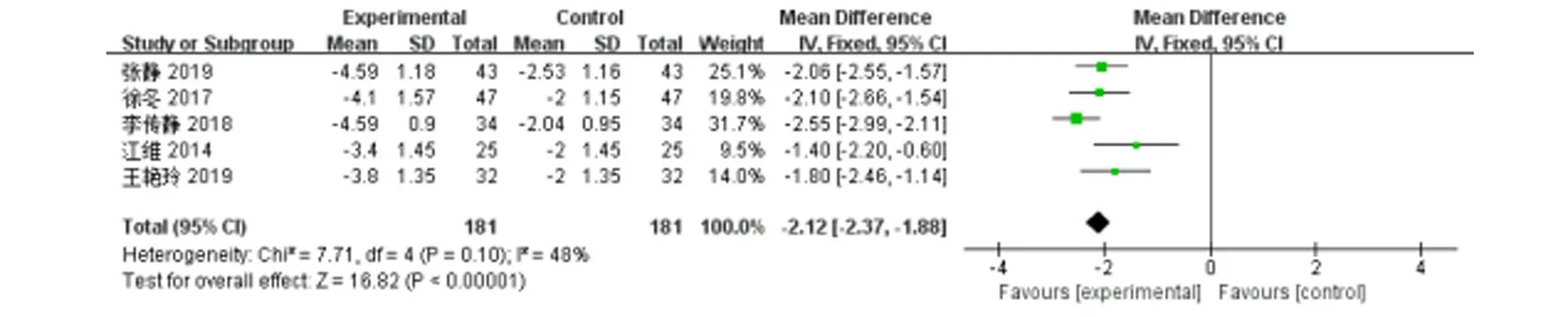
图10 试验组与对照组ESSPRI评分比较的Meta分析
2.3.3.2 ESSDAI评分 4篇文献[6-7,9-10]报道了ESSDAI评分在治疗前后的变化,共纳入394例原发性干燥综合征患者。异质性检验P<0.1,I2=56%,表明研究间存在统计学异质性,采用随机效应模型分析,结果显示,试验组降低ESSDAI评分优于对照组,差异有统计学意义[MD=-2.38,95%CI(-3.08,-1.68),P<0.000 01](图11)。

图11 试验组与对照组ESSDAI评分比较的Meta分析
2.3.4 总有效率 6 篇文献[6-7,9-10,12-13]报道了总有效率,共纳入442 例原发性干燥综合征患者。异质性检验P>0.1,I2=0%,表明纳入的研究同质,采用固定效应模型分析,结果显示,试验组总有效率高于对照组,差异具有统计学意义[RR=1.26,95%CI(1.14,1.40),P<0.000 01](图12)。
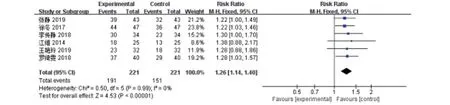
图12 试验组与对照组总有效率比较的Meta分析
2.3.5 不良反应发生率 7 篇文献[6-10,12-13]报道了不良反应发生率,共纳入502 例原发性干燥综合征患者。异质性检验P>0.1,I2=0%,表明纳入的研究同质,采用固定效应模型分析,结果显示,两组间在不良反应发生率上没有统计学差异[RR=0.91, 95%CI(0.63,1.33),P=0.63](图13)。

图13 试验组与对照组不良反应发生率比较的Meta分析
3 讨论
pSS 一般会影响患者生活质量,增加疾病相关成本[15]。目前还缺乏一种专门针对pSS 的治疗方法,目前主要有局部治疗(人工泪滴、M 胆碱受体激动剂)和全身治疗(包括非甾体抗炎药,糖皮质激素,改善病情的抗风湿药物和生物制剂),全身治疗一般针对具有严重外分泌腺炎症或腺外系统受累的情况。其中传统的改善病情的抗风湿药物治疗pSS的疗效受限于缺乏大型RCT验证,然而,专家意见、非对照研究和日常临床实践支持使用它们[16-18]。根据建议,羟氯喹是治疗具有肌肉骨骼系统炎症性表现的一线药物。小剂量/短疗程的糖皮质激素可用于腮腺肿大、关节炎和皮肤血管炎,环磷酰胺和硫唑嘌呤是治疗严重血管炎或中枢神经系统受累的有效药物,利妥昔单抗用于治疗pSS相关淋巴瘤。但由于非甾体抗炎药糖皮质激素不良反应较多以及生物制剂价格昂贵的原因,改善病情的抗风湿药物被寄予厚望,其中鉴于艾拉莫德抗炎抗免疫作用及抑制COX-2酶活性作用,表现出良好的抗风湿及不影响胃黏膜前列腺素生成的作用。但是,许多有关艾拉莫德治疗pSS疗效及安全性的临床研究仍缺乏系统的评价及分析,因此,我们对此进行了系统的定量合成分析。
本次Meta分析总共纳入了9项RCT,分析结果显示,在治疗原发性干燥综合征时,与对照组比较,艾拉莫德试验组能够明显改善临床症状(降低了血沉、类风湿因子及血清IgG、提升了血小板计数、降低了ESSPRI 评分和ESSDAI 评分);改善泪腺和唾液腺分泌功能(升高了Schirmer试验结果和唾液流率)。其中异质性检验发现血清IgG和Schirmer试验均存在高度异质性(两者均>75%),仔细阅读纳入的RCT,发现干预措施不完全相同,可能是异质性的来源,故均对其进行亚组分析及敏感性分析(逐篇剔除法),结果提示试验组血清IgG 和Schirmer 试验结果均优于对照组,且结果较稳定。另外,我们通过定量的方法检验发表偏倚,结果Pegger's 均大于0.05,表明研究不存在发表偏倚。
在药物不良反应发生率方面,本次荟萃分析结果显示,艾拉莫德试验组的不良反应发生率较对照组低,但两者差异较小,且差异无统计学意义,表明艾拉莫德不增加不良反应率,安全性较好。
需要指出的是,本次荟萃分析存在一定的局限性:①未纳入其他语种的文献;②各研究的方法学质量不均一;③地区、人种较为局限。因此,仍需未来更多高质量、大样本量、多中心的RCT研究加以验证。

