气相色谱质谱法测定鱼油胶囊壳中22种邻苯二甲酸酯类含量及迁移量
邓 龙,周 思,张瑞瑞,刘 苗
(1.广东食品药品职业学院,广东广州 510520;2.广州市疾病预防控制中心,广东广州 510440;3.广州检验检测认证集团有限公司,广东广州 511447)
邻苯二甲酸酯类(PAEs)是一种常见的高分子材料助剂,可用于改善材料的可塑性和柔韧性,在食品包装材料、医疗用品等方面使用广泛。PAEs与塑料单体间相互作用为氢键和范德华力,键合强度弱,容易造成PAEs迁移,随着PAEs的大量生产和广泛应用,PAEs逐渐遍布每一个角落,研究表明,在大气、水体、生物乃至人体等各类环境中均有PAEs存在[1-3]。PAEs作为一种环境激素,可通过多种途径影响机体内分泌系统的正常功能,危害人体健康[4-6]。早在1995年,世界卫生组织就将PAEs列为必须控制的一类扰乱内分泌的化学物质。我国卫生部公告2011年第16号将邻苯二甲酸二(2-乙基)己酯等17种PAEs列为可能违法添加的非食用物质[7]。2017年实施的食品安全国家标准GB 9685-2016将食品接触材料中允许使用的PAEs减少至邻苯二甲酸二丁酯、邻苯二甲酸二(2-乙基)己酯、邻苯二甲酸二异壬酯、邻苯二甲酸二烯丙酯4种,且明确不得用于接触脂肪性食品[8]。鱼油作为大众接受度极高的一类营养补充剂,是较为特殊的脂肪性食品,受原料、提取、精炼、包装工艺等因素的影响,PAEs富集、迁移、溶入风险较高,鱼油胶囊壳不论是直接食用或仅作为包装材料,都将直接影响鱼油保健品中PAEs的含量水平,鱼油胶囊壳中PAEs残留水平和迁移量的检测未见相关报道。
目前,报道的PAEs检测方法包括气相色谱法(GC)[9-10]、液相色谱法(LC)[11]、气相色谱-质谱法(GC-MS)[12-13]、气相色谱-串联质谱法(GC-MS/MS)[14-15]、液相色谱-串联质谱法(LC-MS/MS)[16-17]等。其中,质谱法因灵敏度高、抗干扰能力强等优势,在PAEs的检测中应用广泛。本文选取22种常见PAEs为目标物,结合GC-MS在易挥发化合物定性定量方面的优良性能,通过优化样品前处理方法、色谱条件,建立鱼油胶囊壳及食品模拟物中22种PAEs的GC-MS检测方法,研究市售鱼油胶囊壳中PAEs的残留现状及正常储存条件下的迁移水平,可为鱼油胶囊类保健食品的质量监控提供技术支撑和数据支持。
1 材料与方法
1.1 材料与仪器
鱼油胶囊15款 购自采芝林和大叁林药房;脂肪性食品模拟物、精制玉米油 购自家乐福超市,气相色谱测试满足GB 5009.156要求[18];22种邻苯二甲酸酯类标准品 Dr Ehrenstorfer GmbH公司,纯度均大于98%;乙腈、正己烷等试剂 德国Merck公司,均为色谱纯。
7890A-5975C气相色谱-质谱联用仪 美国安捷伦公司;Milli-Q去离子水发生器 美国Millipore公司;MS3漩涡混合器 德国IKA公司;SIGMA 3-18K离心机 德国Sigma公司;固相萃取装置 美国Waters公司。
1.2 实验方法
1.2.1 标准溶液的配制 目标物用乙腈配制成浓度为500 mg/L的单标储备液,于-20 ℃冰箱保存。分别吸取适量的单标储备液,用乙腈稀释成浓度为5.00 mg/L混合标准溶液,于-20 ℃冰箱保存。使用时,用乙腈逐级稀释成浓度为5、10、20、50、100、200、500 μg/L的系列标准工作溶液。
1.2.2 鱼油胶囊壳中PAEs的提取 准确称取碎胶囊壳1.0 g(精确至0.01 g)于50 mL具塞离心管中,加入60 ℃热水5 mL,涡旋至溶解,待冷却,加入10 mL正己烷,涡旋2 min,超声20 min,经4000 r/min离心2 min,吸取上清液至25 mL氮吹管中,残渣加入10 mL正己烷重复萃取,合并清液,40 ℃氮吹至1 mL供测试。
1.2.3 气相色谱条件 色谱柱:Agilent Select PAH(30 m×0.25 mm×0.15 μm);载气:高纯氦气,流速1.0 mL/min;升温程序:初始温度60 ℃,20 ℃/min升至160 ℃,保持1 min,15 ℃/min升至220 ℃,4 ℃/min升至280 ℃,保持4 min,20 ℃/min升至320 ℃,保持1 min,进样口温度:280 ℃;进样量:1 μL,不分流进样;溶剂延迟6 min。
1.2.4 质谱条件 离子源:EI,70 eV;离子源温度250 ℃;四极杆温度150 ℃;传输线温度:300 ℃;选择离子监测(SIM)模式;保留时间和特征离子见表1。
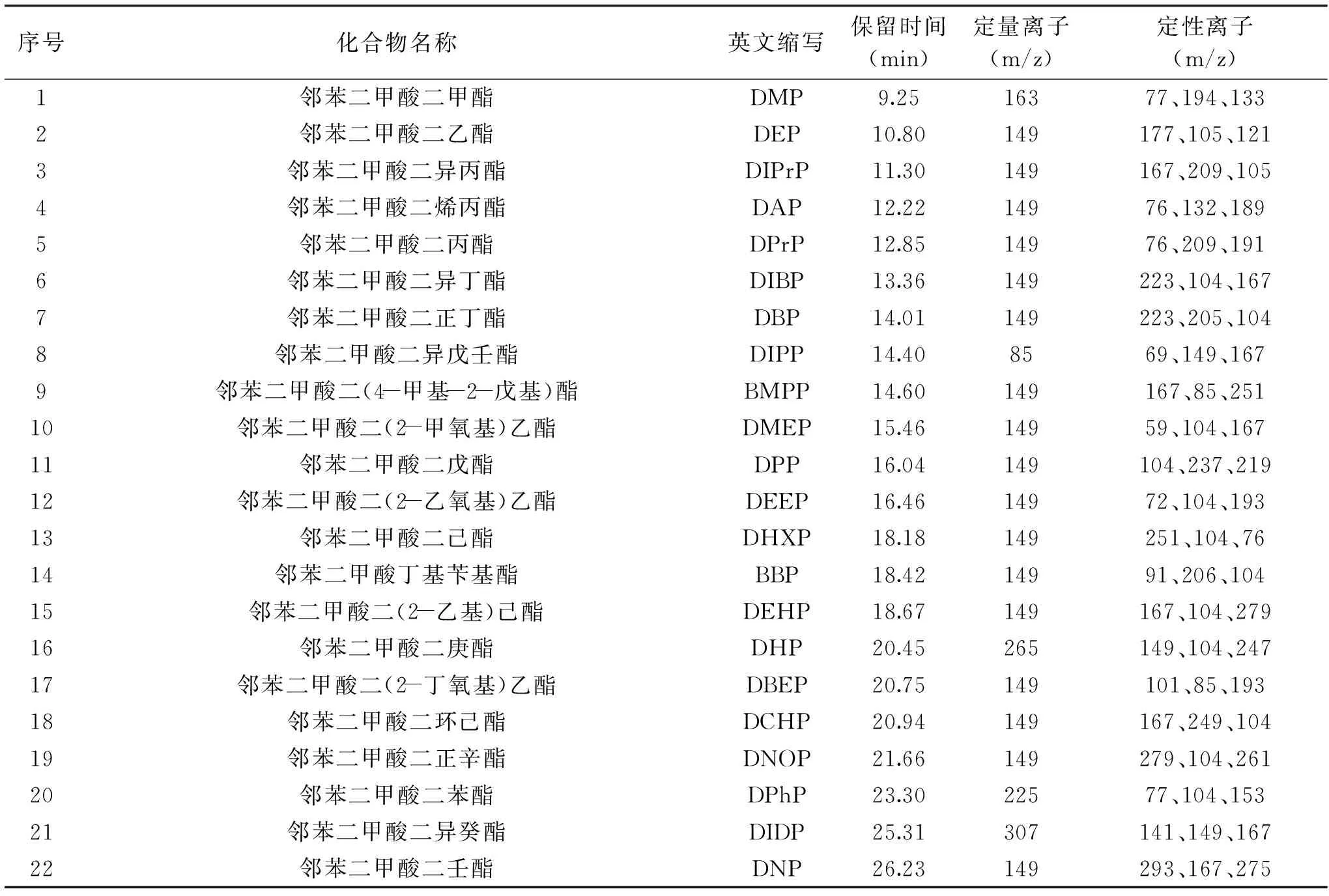
表1 邻苯二甲酸酯类化合物的质谱参数Table 1 MS parameters of PAEs
1.2.5 鱼油胶囊壳中PAEs迁移量的测定 剪取1.2 cm2胶囊壳,浸入4 mL玉米油中,25 ℃测定各时间的迁移量。食品模拟物中PAEs的测定参照GB 5009.271中植物油的前处理方法[19],准确称取1.0 g食品模拟物于具塞离心管中,加入0.2 mL正己烷和10 mL乙腈,涡旋2 min,超声20 min,吸取上清液至25 mL氮吹管中,残渣加入10 mL乙腈重复萃取1次,合并上清液,40 ℃氮吹至1 mL供测试。
1.3 数据处理
采用外标法进行定量,通过标准加入法和控制变量法优化实验条件。应用仪器配套工作站Data Analysis进行数据处理,使用Origin 8.5进行作图和分析。
2 结果与分析
2.1 样品前处理条件的优化
市售鱼油胶囊壳多以明胶为基质,加入甘油、着色剂、遮光剂等辅料制成。基于明胶的亲水性,选择以温水进行溶解以充分释放出样品中的目标物,水温过低胶囊壳溶解不充分,水温过高容易导致目标物损失,且增加后续处理时间,故选择以60 ℃热水进行溶解。目标物邻苯二甲酸酯为亲脂性化合物,根据相似相溶的原理结合文献报道[20],本实验对比了乙腈、正己烷、石油醚3种萃取溶剂的提取效果。实验发现,石油醚中DBP和DEHP的本底值较高,其中DBP的本底值高于方法的定量限。相比之下,乙腈和正己烷的试剂空白较低,两者作为萃取溶剂目标物回收率在80%~120%之间,符合GB/T 27404标准要求[21]。使用乙腈萃取样品的同时萃取了较多的水溶性杂质,部分样品的检测产生干扰待测物的杂质峰,增加后续净化处理的难度,而正己烷对于水溶性杂质的溶解性较差,样品基质干扰少,因此,选择正己烷作为萃取溶剂。
鱼油是从鲭鱼、鲱鱼等多脂鱼类中提取的油脂,按照食品安全国家标准GB 31604。选择精制玉米油作为食品模拟物[22]。根据GB 5009.156标准要求迁移实验食品接触材料的面积(S)与食品模拟物的体积(V)应反映实际的使用情形[18],由于不同品牌的鱼油胶囊规格、形状各异,接触面积值难以估算,加之胶囊壳体积小、材质均一,统一按每6 dm2食品接触材料对应1 L食品模拟物的比例采用全浸没法进行迁移实验。查看15款鱼油胶囊的产品信息,保质期为9~24个月不等,产品储藏方法多描述为置阴凉干燥处、常温保存,按特定迁移实验条件的选择原则,可选择60 ℃,10 d条件开展加速实验[22]。实验发现,明胶在此条件下会发生变黑、软化等理化性质的改变。考虑鱼油胶囊壳可直接食用或仅作为包装材料,是一类特殊的食品接触材料,且本文侧重考察正常储存情况下鱼油胶囊壳中的PAEs的迁移情况。最终确定实验条件为:剪取1.2 cm2的胶囊壳,浸入4 mL玉米油中,25 ℃下测定各个时间的迁移量。
2.3 仪器条件的优化
2.3.1 质谱条件的优化 将配制好的浓度为50.0 μg/L的PAEs单标溶液进行全扫描采集,通过NIST谱库查询功能结合文献报道,确定22种目标物的定性定量离子,并采用选择离子(SIM)扫描方式分段检测不同保留时间的待测物,以提高样品检测的灵敏度并消除部分杂质干扰。参照欧盟2002/657/EC决议中有关质谱分析方法不少于4分的规定,每个待测物选取4个离子为质谱采集参数[23]。22种待测化合物的监测条件如表1所示。
2.3.2 色谱柱的选择 本次测定的邻苯类化合物共22种,存在多种结构相似物和同分异构体,碎片离子相似度高,采用邻苯类化合物测定中常用的DB-5MS色谱柱进行测试[24],DIPP和BMPP、DHP和DEHP等化合物分离效果不佳,且离子碎片相似,不易实现单独定量。为了实现各目标物的分离,需要精细程序升温条件,导致分析时间过长,不利于检测工作的开展。实际工作中发现,PAH专用柱通过修饰固定相,优化膜厚,可提高柱效,改善色谱峰型,有效地增大了目标物的分离度。选择Agilent Select PAH色谱柱对22种PAEs进行分析,在27 min内所有目标物全部出峰,达到基线分离,目标物峰型尖锐,半峰宽窄,检测灵敏度和分离度得到大幅提高。本方法检出限与国家标准GB 31604.30-2016相比[25]低2~3个数量级。22种PAEs的总离子流色谱图如图1所示。
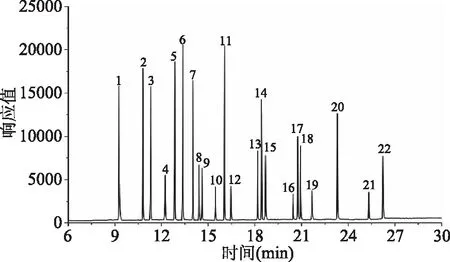
图1 PAEs混标溶液总离子流色谱图Fig.1 Total ion chromatogram of mixed standard solution注:序号对应表1相应化合物。
在优化条件下,测试1.2.1节的混合标准溶液,以目标物的质量浓度(x,μg/L)为横坐标,定量离子的峰面积(y)为纵坐标作图,得到22种PAEs的线性方程如表2所示。由表可知,22种目标物在一定浓度范围内线性关系良好,相关系数均大于0.9987。以3倍信噪比(S/N=3)计算检出限,以10倍信噪比(S/N=10)计算定量限,结合样品前处理过程得到方法检出限为3.1~9.8 μg/kg,定量限为10~29 μg/kg,表明本方法具有较高的灵敏度。

表2 化合物的线性方程、相关系数、线性范围、方法检出限和方法定量限Table 2 Linear equations,linear ranges,correlation coefficients,detection limits and quantification limits of PAEs
2.5 回收率与精密度
为考察样品处理的可靠性,进行加标回收率试验。选取阴性样品参照GB/T 27404[21]选取1倍、2倍和10倍方法测定低限进行3水平加标回收实验,每个水平平行测试6次,实验结果见表3。由表可知,在加标浓度范围内,22种待测物的平均回收率为82.1%~112.1%,相对标准偏差(RSD,n=6)为2.1%~7.7%,说明方法具有良好的回收率与精密度。
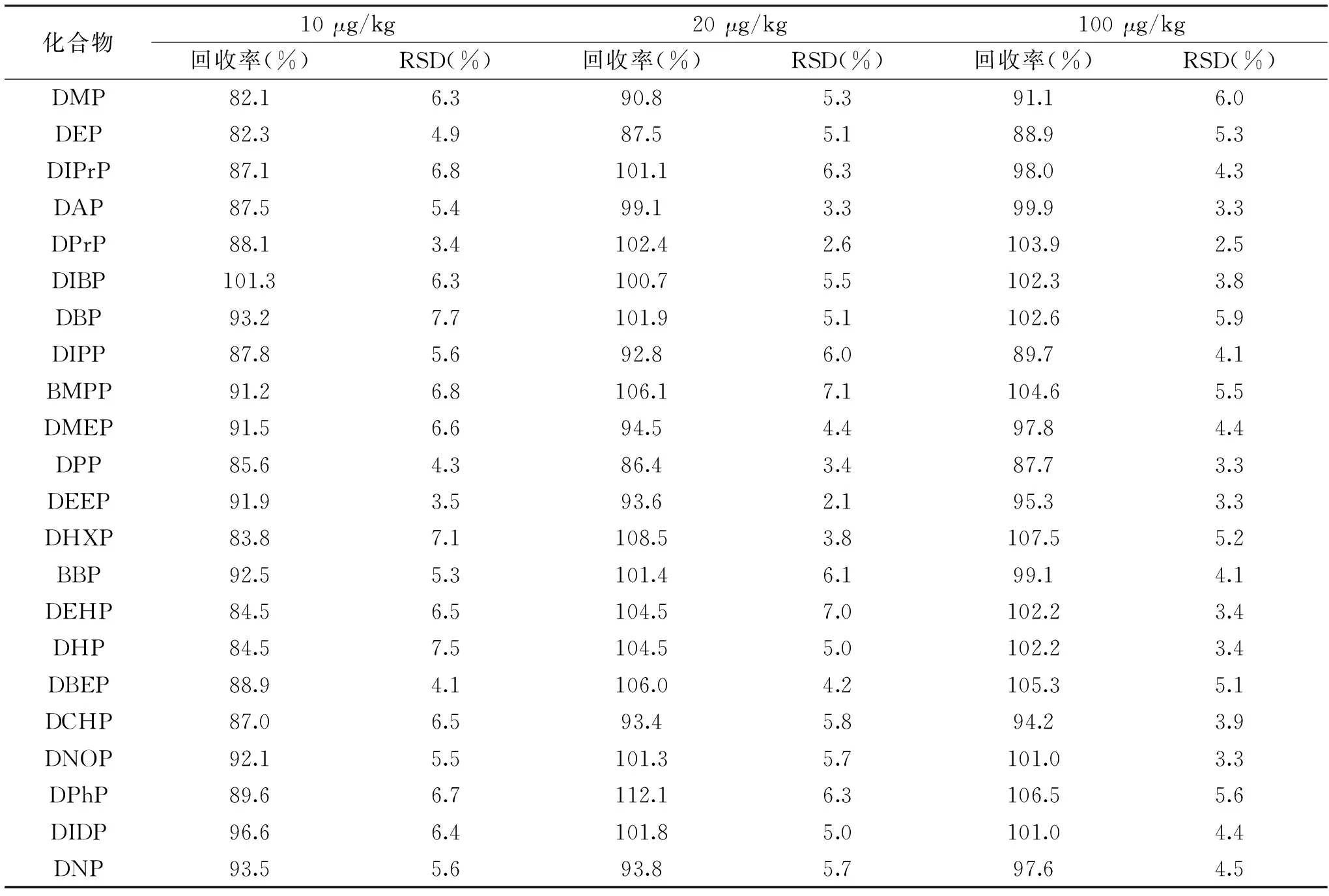
表3 加标回收和精密度实际测定结果(n=6)Table 3 Determination results of recovery and precision(n=6)
2.6 实际样品的检测
利用建立的分析方法检测15个市售鱼油样品胶囊壳。结果表明,有5个胶囊壳检出少量PAEs,检出种类包括DEP、DBP、DIBP、DEHP,含量水平在0.14~0.78 mg/kg之间。鉴于含量较低,排除在生产过程中故意添加的可能性;此外,有1个胶囊壳检出较高水平的PAEs,DEHP含量为4.51 mg/kg,DBP含量为1.13 mg/kg。GB 9685规定DEHP、DBP作为食品接触材料及制品用添加剂不得用于接触脂肪性食品,最大残留限量分别是1.5、0.3 mg/kg,此样品中的胶囊壳作为包装材料,最大残留限量不符合GB 9685标准要求[8]。需进行溯源,排查含量过高的原因。阳性样品稀释25倍后测定的总离子流色谱图见图2。

图2 阳性样品总离子流色谱图Fig.2 Total ion chromatogram of positive sample
2.7 鱼油胶囊壳中PAEs的迁移量
以精制玉米油为食品模拟物,考察25 ℃下鱼油胶囊壳中PAEs的迁移情况。鉴于DEHP是报道污染较为严重的化合物,且市售鱼油胶囊样品检出较高水平的DEHP,故选择DEHP作为迁移实验的研究对象,考察浸泡时间为1、2、5、10、20、30、40 d迁移量的变化,DEHP迁移量随时间的变化趋势如图3所示。由图3可知,胶囊壳中的PAEs存在明显的迁移现象,随着时间增加,DEHP的迁移量不断增加,增加幅度逐渐减小,20 d后迁移量增加值逐渐变缓。卫办监督函[2011]551号规定严禁在食品、食品添加剂中人为添加增塑剂,DEHP在食品和食品添加剂中的最大残留量1.5 mg/kg[26]。该样品在40 d时食品模拟中DEHP的含量为0.49 mg/kg,未超过最大限量要求。实际样品中鱼油与胶囊壳的接触面积之比(S/V)远小于1∶6,迁移量水平更高,存在潜在风险。因此,鱼油胶囊壳不论是直接食用还是仅作为包装材料,都将直接影响鱼油产品中PAEs的含量水平,生产过程除考虑鱼油的品质外,还应关注胶囊壳的质量安全。
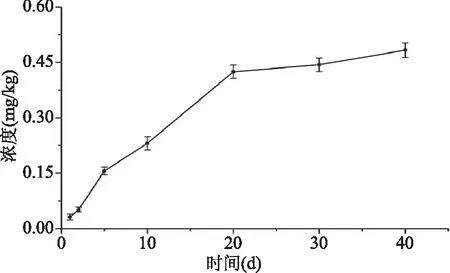
图3 DEHP迁移量随着时间的变化趋势图Fig.3 Migration of DEHP from fishoilcapsule shells for different time
3 结论
本文建立了气相色谱-质谱同时检测鱼油胶囊壳及食品模拟物中22种邻苯二甲酸酯类化合物的检测方法。通过优化样品前处理方法,选择PAH专用柱进行分析,通过优化色谱条件和质谱参数,实现了22种目标物的有效分离,22种邻苯二甲酸酯类化合物在10~500 μg/L浓度范围内线性关系良好,定量限在10~29 μg/kg之间。本方法具有操作简便、检出限低,选择性好、精密度高等特点,方法学结果符合GB/T 27404中理化检测质量控制相关技术要求,适用于鱼油胶囊壳及食品模拟物中邻苯二甲酸酯类的测定。

