温度敏感型淀粉基聚合物载体的制备、表征及性能分析
寇宗亮,关 欣,蓝丽红,张金彦,李湘静,黄思颖,蓝 平
(广西民族大学化学化工学院,广西多糖材料及改性重点实验室,广西高校化学与生物转化过程新技术重点实验室,广西南宁 530006)
淀粉是一种天然多糖,具有无毒性、相容性良好、非免疫原性和低抗原性等特点[1-3],作为一种无毒和生物可降解的聚合物材料已被广泛地用于制备生物纳米载体[4]。其有大量可被修饰的官能团,当释放功能性物质后可降解为寡糖且易吸收,不会导致炎症发生[5]。由于天然淀粉存在水溶性差、糊化液易老化[6]等缺点,使其应用受到限制。
为了拓宽木薯淀粉的应用范围,研究者们通过物理[7-8]、化学、生物[9]等改性方法对淀粉进行功能化修饰,使其广泛应用于食品、医药[10-11]、化工等各个领域。由于化学改性可以通过在淀粉分子的羟基上引入功能性基团使其获得其他功能特性,近年来受到人们的追捧[12]。通过淀粉分子上的羟基与其他基团进行反应,可以制备各种功能性物质载体[13-14]。然而在食品包装部和各种抗性食品的应用中,多为玉米淀粉[15],木薯淀粉的应用较为鲜见。
胶束作为功能性载体的一种,近年来因体内循环稳定性好,常被用作传递介质,受到的关注程度越来越高[16]。两亲性聚合物的亲水片段和疏水片段在浓度较低时,聚合物分子以单分子的形式存在;当聚合物浓度达到某一数值后,聚合物分子能够自组装形成聚合物胶束[17-18]。
为了改善木薯淀粉诸多缺点限制,拓宽其在食品医药领域的应用,本研究利用木薯淀粉作为基材,首先以异丙基缩水甘油醚作为温度敏感的疏水基团,接枝于淀粉分子骨架上将淀粉分子功能化。然后接枝生物相容性的聚乙二醇(mPEG)作为亲水基团。利用傅里叶红外变换光谱(FTIR)、核磁共振(1H-NMR)对其化学结构进行表征,验证木薯淀粉基聚合物是否成功合成。然后利用透射电镜(TEM)、荧光分子探针和马尔文激光纳米粒度散射仪对其形貌和粒径进行表征。最后以姜黄素作为药物模型,进一步探究其在不同温度环境中的释放行为。为制备新型温度敏感型淀粉基胶束提供了理论依据,进一步拓宽了木薯淀粉的应用范围。
1 材料与方法
1.1 材料与仪器
木薯淀粉 工业级,广西武鸣安宁淀粉有限公司;聚乙二醇(PEG,Mn=4000) 分析纯,广东光华化学厂有限公司;羧基封端聚乙二醇 根据参考文献步骤合成[20];丁二酸酐(SA) 分析纯,阿拉丁;姜黄素、N-(3-二甲基氨丙基)-N-乙基碳二亚胺(EDC)、4-二甲基氨基吡啶(DMAP) 分析纯,麦克林。
DF-101集热式恒温加热磁力搅拌器 巩义市予华仪器有限责任公司;MAGNA-1R550傅里叶变换红外光谱仪(FTIR) 美国Thermo 公司;Cary100紫外-可见分光光度计 Agilent Technologies;冷冻干燥机 埃朗科技国际贸易(上海)有限公司;600 MHZ核磁共振波谱仪(1H-NMR)、透射电子显微镜(TEM) Hitachi日立;F-7000荧光分光光度计 日本株式会社日立高新技术。
1.2 实验方法
1.2.1 疏水淀粉(St-R)的制备 首先对木薯淀粉进行降解处理[19],将原淀粉25 g,无水甲醇100 mL加入三口瓶中,然后滴加浓盐酸4 mL,0.5 h后,加热至50 ℃反应5 h,冷却至室温后,先用碳酸钠进行中和,然后抽滤,用甲醇洗涤,干燥备用。
疏水化处理参照杨锦东[19]的方法,在装有10 mL去离子水的三口瓶中加入5 g降解淀粉,搅拌条件下加入0.5 g的氢氧化钠,随后升温至70 ℃,碱化反应1 h。然后缓慢滴加12 g疏水醚化剂,继续反应5 h。待反应结束后,冷却到室温,并用冰醋酸中和至中性,过滤。产物用50%丙酮反复洗涤数次,将析出的产品干燥后称重保存以备后用。
1.2.2 疏水淀粉(St-R)接枝聚乙二醇共聚物的制备(R-St-mPEG)
1.2.2.1 羧基封端聚乙二醇的制备 参照文献[20]中的方法,称取3.8 g聚乙二醇(mPEG)、0.6 g丁二酸酐(SA)和0.01 g4-二甲氨基吡啶(DMAP)溶解在100 mL 的二氯甲烷中,在25 ℃下搅拌48 h。旋蒸除去大量的二氯甲烷之后,反应物用四氢呋喃溶解,然后用乙醚在分液漏斗中多次洗涤、沉降。最后真空干燥,得到羧基封端的聚合物mPEG-COOH。
1.2.2.2 疏水淀粉接枝聚乙二醇接枝的制备 参照文献方法[21],将1 g疏水淀粉(St-R)和9.4 g羧基封端的聚乙二醇溶解在装有60 mL二甲亚砜(DMSO)溶剂的反应瓶中,在搅拌的条件下加入N-(3-二甲基氨丙基)-N′-乙基碳二亚胺(EDC)0.72 g和4-二甲基氨基吡啶(DMAP)0.023 g,反应在常温下反应。随后,溶剂和未反应的反应物通过透析除去。然后将溶液过滤,冷冻干燥即得烷基淀粉接枝聚乙二醇共聚物R-St-mPEG。
1.2.3 胶束溶液的制备 取1.2.2.2制备的聚合物100 mg于装有100 mL PBS缓冲溶液的100 mL容量瓶中,室温振摇48 h,100 W超声10 min,使得聚合物在水溶液中充分分散。0.45 μm滤膜过滤,得澄清的胶束溶液。
1.2.4 测试及表征
1.2.4.1 傅里叶红外变换光谱分析 取1~2 mg干燥的聚合物样品,与50~100 mg干燥的KBr粉末混合,置于玛瑙研钵中充分研磨,将研磨好的混合物粉末放入压模中,在10 kPa的压力下压制成透明薄片,然后小心地将压片取出,放入红外光谱仪进行测试,4000~5000 cm-1波长范围内扫描。
1.2.4.2 核磁共振分析 称取30~50 mg的聚合物,用DMSO-d6为溶剂在样品管中溶解,为了使得样品充分溶解,用超声清洗器在100 W的功率条件下超声10 min。最后将溶解好的样品装入核磁管,在室温下检测聚合物的氢谱。
1.2.4.3 临界胶束浓度(CMC)测定 临界胶束浓度的测定采用芘的荧光探针法分析。荧光探针芘标准贮备溶液的配制(6×10-6mol/L):用分析天平准确地称取芘0.0012 g,烧杯中用适量丙酮溶解后转入1 L容量瓶中,用丙酮定容并摇匀,配制得到浓度为6×10-6mol/L的芘丙酮贮备溶液,使用时在胶束水溶液中保持6×10-7mol/L的最终浓度。
胶束系列标准工作溶液的配制:分别取1 mL配制的芘丙酮溶液于几个烧瓶中,让其完全挥发备用。再称取100 mg冻干材料粉末两份分别于100 mL容量瓶中,加不同pH缓冲溶液溶解定容,取不同量上述胶束溶液进行稀释,配制成1~1×10-4mol/L不同浓度系列的胶束溶液。将不同浓度的胶束水溶液分别取10 mL,分别加入上述含芘的烧瓶中。
1.2.4.4 透射电镜观察 取1.2.3制备的胶束溶液滴于铺有三百目铜筛的碳膜上,用滤纸除去多余水分,在自然条件下干燥,然后用加速电压为80 kV扫描。
1.2.4.5 粒径表征 采用激光纳米粒度分析仪测定,用PBS缓冲溶液制备浓度为1.0 mg/mL的胶束溶液,取适量样品加入比色皿中,参数设置为检测器位置:173 °,温度:25 ℃,淀粉折射率:1.53,缓冲溶液折射率:1.33。
1.2.5 负载性能的探究
1.2.5.1 负载胶束的制备 精确称取25 mg姜黄素,将其置于烧杯中,用DMSO溶解后,将姜黄素的DMSO溶液移到250 mL容量瓶中,再用DMSO进行定容,得到100 μg/mL的储备液。精密移取2、3、4、5、6 mL 100 μg/mL的储备液,将其分别移到100 mL的容量瓶中,用DMSO进行定容,即制成2~6 μg/mL系列标准溶液。用DMSO做空白对照液,分别在427 nm处测定其吸光度。W浓度(C,μg/mL)为横坐标,吸光度(A)为纵坐标,绘制姜黄素在DMSO中的标准曲线。称取8~16 mg姜黄素溶于4 mL DMSO,另称取100 mg 聚合物,溶于6 mL DMSO中,磁力搅拌使其完全溶解;在剧烈搅拌下,将4 mL姜黄素DMSO溶液缓慢滴入聚合物溶液中,室温避光搅拌5 min,混合均匀,将混匀后液体转移至透析袋内(透析膜截留分子量为3500 Da),对蒸馏水透析24 h,开始每隔12 h换水1次除去有机溶剂,5000 r/min离心除去药物沉淀,得上清液,即为载姜黄素纳米胶束。选取不同总投药量(8、10、12、14、16 mg),固定材料每次用量为100 mg,以考察最大负载量。

式(1)
1.2.5.2 温度响应条件的研究 精确称取25 mg姜黄素,用PBS缓冲液溶解,转移到250 mL容量瓶中,用PBS缓冲液定容,即得到100 μg/mL的药物溶液,精密移取2、3、4、5、6 mL的药物溶液到100 mL容量瓶定容,即制得浓度为2~6 μg/mL系列标准溶液。用PBS做空白对照液,427 nm处测定吸收波长。绘制得到姜黄素在PBS中的标准曲线。称取一定量的负载胶束,将其溶解在不同温度的PBS缓冲溶液中(含0.5%吐温80),使其浓度为1 mg/mL。量取5 mL的上述胶束溶液,装入预先处理好的透析袋,再放置于30 mL的PBS缓冲溶液中,分别于25、37 ℃下恒温振荡(120 r/min)。间隔多次取样,每次取样4 mL,然后再补充4 mL新鲜的PBS缓冲溶液。用紫外分光光度计测定427 nm处的吸收波长,再根据姜黄素在PBS缓冲溶液中的标准曲线计算姜黄素在不同时间下的释放量。累计释放量可根据式(2)计算:
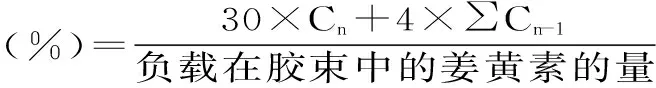
式(2)
式中,Cn:第n次取样时的浓度;Cn-1:第n-1次取样时的浓度。
1.3 数据处理
每组数据均采用三组平行试验得出平均值,采用Excel 2018进行数据计算与处理,并用软件Origin 8.5进行作图。
2 结果与分析
2.1 聚合物(R-St-mPEG)的制备
木薯淀粉作为天然淀粉的一种,溶解性也相对较差,所以在制备木薯淀粉基聚合物胶束时,选用二甲基亚砜作为反应溶剂。由木薯淀粉制备聚合物胶束,为避免多基团之间的相互反应,首先需要在淀粉分子骨架上引入疏水性基团。异丙基缩水甘油醚不仅是良好的疏水化试剂,同时也是温度敏感性的功能基团,可以使得聚合物形成疏水性内核的同时使得淀粉基聚合物获得温度敏感性。反应在碱催化下遵循亲核取代机理进行,淀粉在碱的催化下产生氧负离子,产生的氧负离子越多,亲核取代也就越容易发生。其次,胶束的亲水性外壳需要具有良好的生物相容性,聚乙二醇由于其突出的物化和生物性质(无毒、无抗原性和无免疫原性)使其在制备两亲性聚合物时常常被作为一种可溶性的聚合物改性剂,用其所制得的聚合物有很高的两亲性,生物相容性和生物可降解性。聚乙二醇的特性满足作为负载胶束亲水外壳这一要求。根据酯化反应机理,用羧基封端的聚乙二醇对淀粉进行亲水基的修饰。最终得到产物R-St-mPEG。合成过程如图1所示。
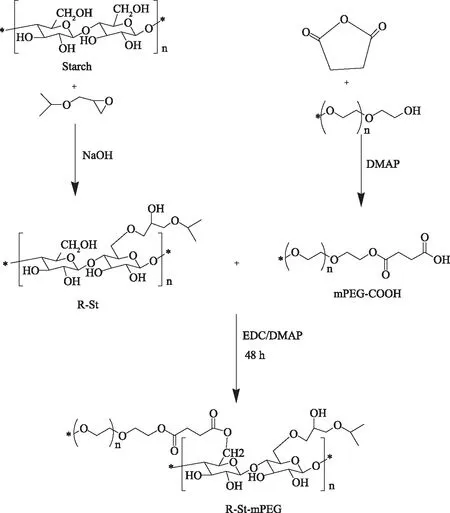
图1 淀粉基聚合物(R-St-mPEG)的合成路线图Fig.1 The synthetise of starch based polymer(R-St-mPEG)
2.2 聚合物结构表征
2.2.1 傅里叶红外变换光谱(FTIR)结果分析 聚合物红外光谱如图2所示,由图2中可以得知,与原淀粉(St)红外图相比,疏水淀粉(St-R)谱图发生了新的变化。在1014~1160 cm-1出现新的宽强峰,这是缩水甘油醚接枝淀粉后的醚键的特征吸收峰[21]。1646和1465 cm-1两处的吸收峰属于C-H的弯曲振动[19]。3444 cm-1处的峰变强变宽,这是因为在淀粉分子链上引入缩水甘油醚后新增加的羟基所引起的。而与淀粉接枝缩水甘油醚(St-R)相比,疏水淀粉接枝聚乙二醇(R-St-mPEG)的红外谱图也出现了新的变化。1735 cm-1出现了羰基的特征吸收峰,这是羧基封端聚乙二醇接枝到淀粉上的重要标志。还有1110 cm-1处出现了明显的酯键吸收峰[21]。此外,图中2881~2977 cm-1之间的峰在不断变宽变强,这是由于淀粉分子上引入了烷基类基团所导致的。这些证据都在一定程度上证明淀粉接枝聚合物(R-St-mPEG)的成功合成。核磁共振氢谱和红外变换光谱相辅才能进一步证明聚合物的成功合成。
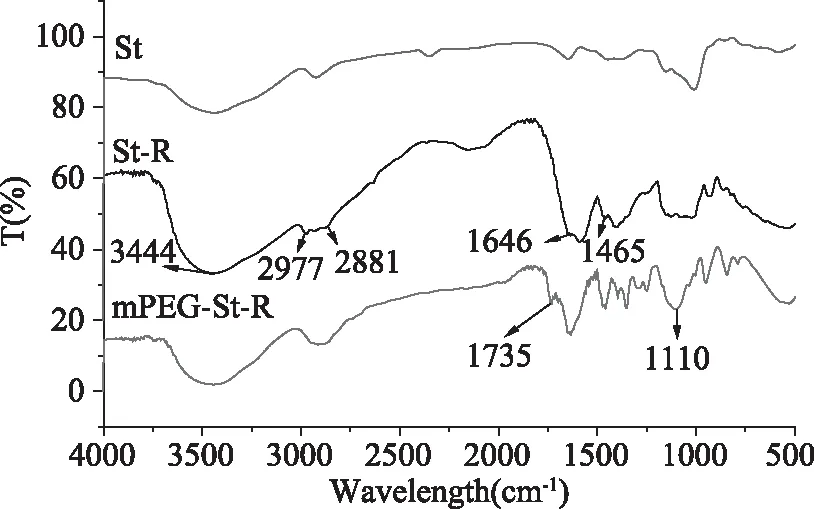
图2 淀粉基聚合物(R-St、R-St-mPEG)及原淀粉(St)红外光谱图(FTIR)Fig.2 The infrared spectrum(FTIR)of starch-based polymer(R-St,R-St-mPEG)and starch(St)
2.2.2 核磁共振氢谱(1H-NMR)结果 利用核磁共振氢谱对聚合物的结构进行进一步表征,如图3为淀粉基聚合物的核磁共振氢谱图。由图中则可以看出淀粉葡萄糖环(AGU)上各氢的质子峰都可以被明显的观察到,分别是5.6 ppm(20)、5.3 ppm(19)以及5.1 ppm(1)位置处的三个质子峰。除此之外,出现在化学位移δ=3.51和3.23 ppm处的质子峰分别归属于mPEG上的亚甲基和末端甲基,这些结果与文献对照一致[22]。淀粉分子骨架上除了亲水性的聚乙二醇(mPEG)之外,还引入了疏水性的缩水甘油醚,根据文献可知[21,23],异丙基缩水甘油醚亚甲基中(H14,H15)的各质子峰出现在3.0~3.8 ppm之间,H17、H18出现在0.75 ppm附近,以及1.4和1.5 ppm附近的H16。这些证据都证明聚合物中接枝的各个基团都出现在了产物中,与红外光谱中特征官能团的谱图共同证明了聚合物(R-St-mPEG)的成功合成。
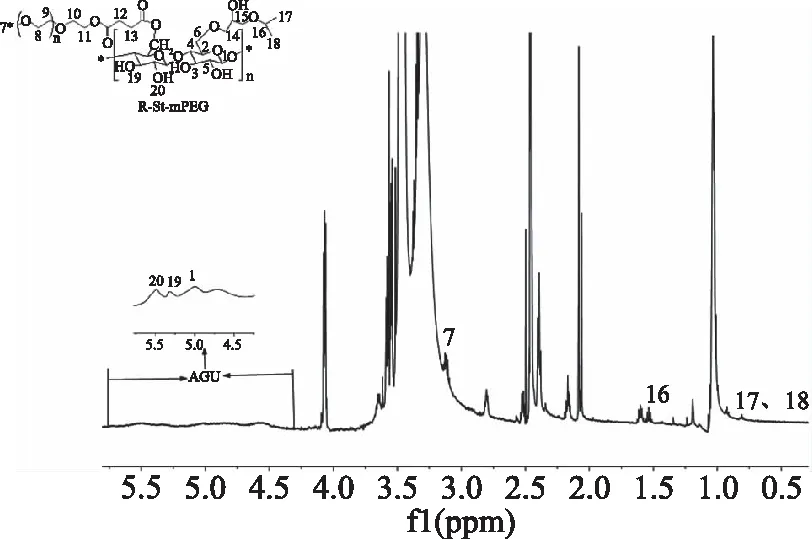
图3 淀粉基聚合物(R-St-mPEG)的核磁共振氢谱图(1H-NMR)Fig.3 Nuclear magnetic resonance spectrum ofstarch-based polymer(R-St-mPEG)
2.3 临界胶束浓度(CMC)测定结果
临界胶束浓度是证明胶束自组装行为发生的重要参数,同时也能够说明药物载体在体内长效循环中的稳定性[24]。以芘做荧光探针,当芘从亲水环境转移到疏水环境的过程中,当聚合物浓度达到某个值的时候芘的荧光强度发生突变,这个浓度被定义为临界胶束浓度(CMC)。如图4所示,以芘的荧光强度比值(I318/I332)和聚合物浓度的对数(Log C)作图,图中拐点所示即为聚合物R-St-mPEG的临界胶束浓度。拐点所对应的浓度为0.339 mg/mL。说明当聚合物胶束在溶液中的浓度达到0.339 mg/mL时,聚合物便能发生自组装行为。疏水性基团向内卷曲形成疏水内核,亲水性基团向外部排列形成亲水性外壳。此外,临界胶束浓度(CMC)的测定为聚合物胶束负载功能性物质提供了理论基础,当胶束发生自组装行为时,可以与姜黄素溶液混合,将姜黄素分子成功包裹进胶束的疏水内核中。
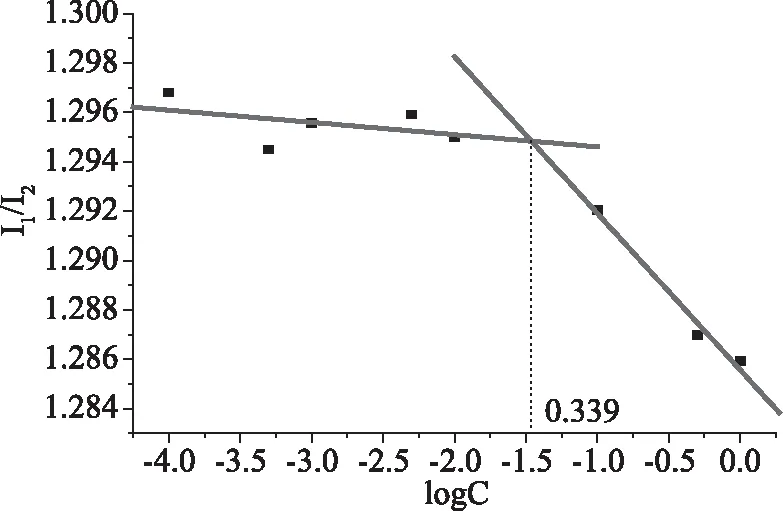
图4 芘的荧光强度比值与胶束浓度对数图Fig.4 Pyrene fluorescence intensity ratioand micelle concentration logarithm plot
2.4 聚合物(R-St-mPEG)透射电镜(TEM)结果表征
透射电镜可以对胶束的形貌进行表征,由于人体正常组织环境pH为7.4,所以为了保证胶束负载后进入体内能够稳定输送药物,选用在pH7.4的磷酸缓冲液中对胶束分散后观察其形貌。图5所示为胶束在pH=7.4 PBS缓冲溶液中50 h后的形貌图。由图中可以看到,胶束呈现球形和椭球型结构,粒径不均一。胶束在存放50 h后仍旧能够保持球形结构,结构没有发生坍塌或者破裂,这为后续胶束的负载提供了有利的稳定环境。负载胶束在进入人体后若是发生结构的坍塌或者破裂,将导致提前释放和削弱胶束的缓释效果。此外,透射电镜结果也表明了通过自组装行为形成了球形结构。

图5 聚合物胶束的透射电镜(TEM)图Fig.5 TEM of polymer micelles
2.5 聚合物粒度分析
聚合物胶束作为药物载体,其粒径小于200 nm时,胶束能够显示出较好增强渗透性和滞留(EPR)效应[27]。通过马尔文激光纳米粒度散射仪可以测量聚合物胶束在溶液中粒径,图6所示为聚合物胶束在pH=7.4的缓冲溶液中的粒径分布图。粒径集中分布在28和122 nm附近。粒径分布不均一主要是聚合物基材淀粉的性质所导致的,淀粉本身粘度大,淀粉之间容易发生粘连[28],当淀粉分子之间发生粘连时,势必会造成粒径测量结果较大。此外,胶束的粒径分布不均一与透射电镜结果也相符,这也证明了实验结果的正确性。
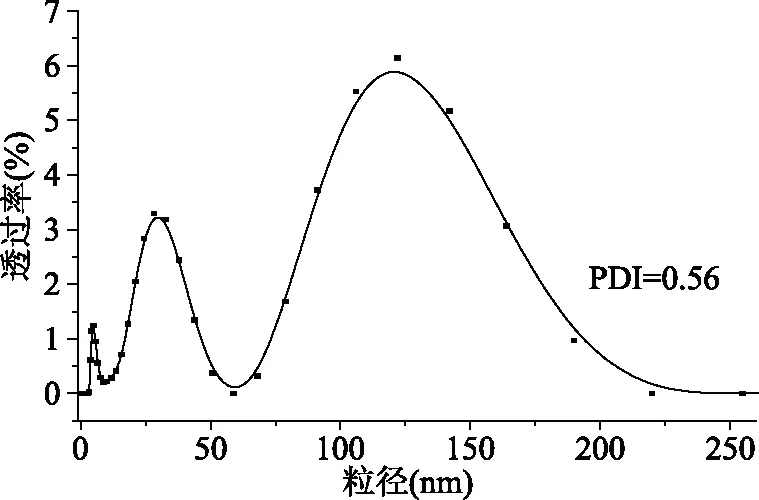
图6 胶束的粒径分布图Fig.6 Particle size distribution of micelles
2.6 负载性能分析
为了获得负载胶束中姜黄素的载药量(DLC),称取一定量负载有姜黄素的负载胶束溶解在DMSO中,利用紫外可见分光光度计测定波长在427 nm处的吸光强度,然后再通过姜黄素的标准曲线进行计算浓度,姜黄素在DMSO中标准曲线如图7所示,标准曲线线性拟合良好。如图8所示为不同投药量胶束的载药量,根据1.2.5.1中的式1计算可得,当材料投入100 mg,姜黄素投入量为14 mg时,胶束有最大负载量,负载量为18.47%。聚合物的投入量与药物浓度之间有着密切的联系,当药物浓度较小时,胶束在形成时,药物不能完全占据胶束的内核空间,导致负载量不能达到饱和。当逐步增大药物浓度时,负载量呈现先增大后减小的趋势,这是由于姜黄素在水中的稳定性较差[25],随着DMSO不断透析被除去,聚合物还未在水溶液中形成核-壳结构的胶束时,姜黄素便已经结晶析出,姜黄素发生聚集,导致负载量也随着姜黄素浓度的增大而出现减小趋势。所以聚合物材料的投加与药物浓度之间需要有合适的比例。
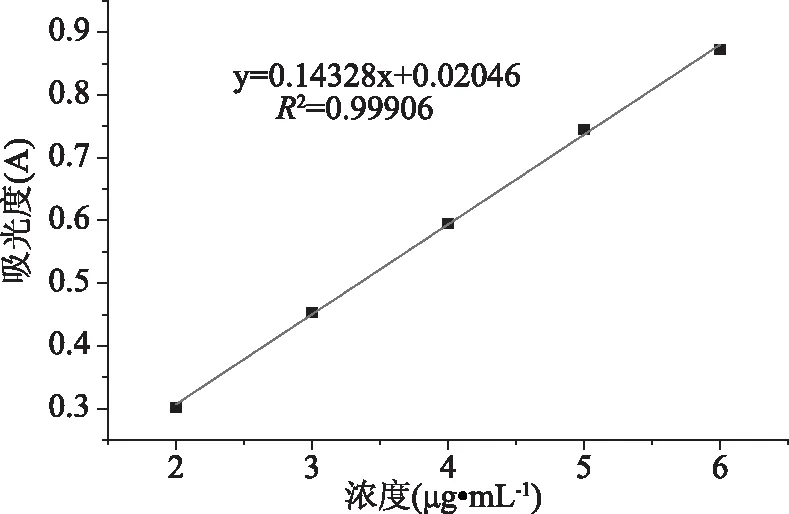
图7 姜黄素在DMSO中的标准曲线Fig.7 Standard curve of curcumin in DMSO
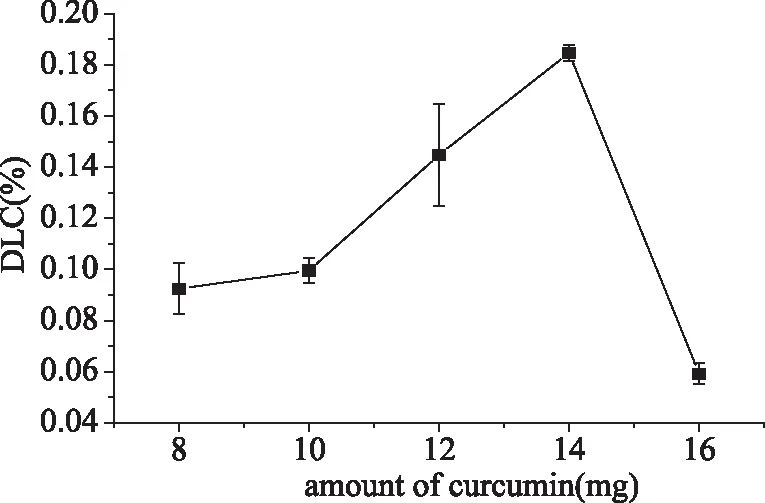
图8 不同投药量下的胶束负载量Fig.8 Micelle loads at different dosages
2.7 聚合物胶束的温敏性能考察
人体内各组织之间的温度也会存在一定的差异,肿瘤组织的温度明显高于人体正常体温,这也为开发温度敏感型的负载胶束提供了先决条件。温度敏感型聚合物胶束的释放机理主要与外界环境的温度有关,当温度高于聚合物的临界温度时,聚合物的结构和性质发生改变,导致胶束的核-壳结构收缩从而释放。当温度对于临界温度时,聚合物胶束分子上的羟基、氧、烷氧基等与溶液中的水分子形成氢键,胶束的核壳结构也会更加稳定,功能性物质姜黄素通过扩散和渗透作用[26]从胶束中进行释放。根据上述机理,采用常温和人体外环境温度两个条件下考察淀粉基聚合物R-St-mPEG的温度敏感性和缓释性能。首先绘制了姜黄素在磷酸缓冲液(PBS)中的标准曲线(如图9),线性拟合度良好。间隔不用时间取样,然后测定溶液的吸光度,根据式2计算负载胶束的累计释放量,并以时间为横坐标作图(如图10)。由图中可以看出33 h以前,25 ℃环境中的胶束累计释放量大于37 ℃环境中的累计释放量,这是由于37 ℃环境中的负载胶束会经历胶束球形结构收缩的过程,胶束更加紧密,导致药物通过扩散和渗透方式释放变慢。30~52 h之间,37 ℃环境中的胶束大于收缩更加紧密胶束中的药物通过“挤出”方式释放,产生突释效应,累计释放量变大。而25 ℃环境中的胶束一直处于平稳的释放阶段,没有突释阶段,这也符合胶束通过扩散和渗透作用逐步释放的机理。60 h内37 ℃环境中的胶束累计释放量达到了43.9%,25 ℃环境中的负载胶束累计释放量只有34.7%。负载胶束的累计释放结果表明淀粉基聚合物R-St-mPEG具备温度敏感性能,随着温度的升高释放量也会不断增加。
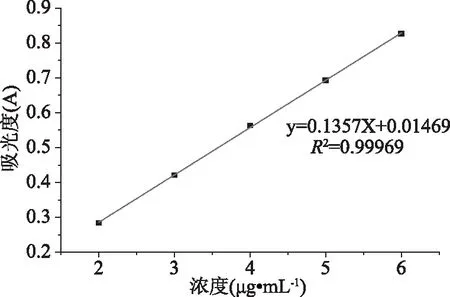
图9 姜黄素在PBS缓冲液中的标准曲线Fig.9 Standard curve of curcumin in PBS buffer
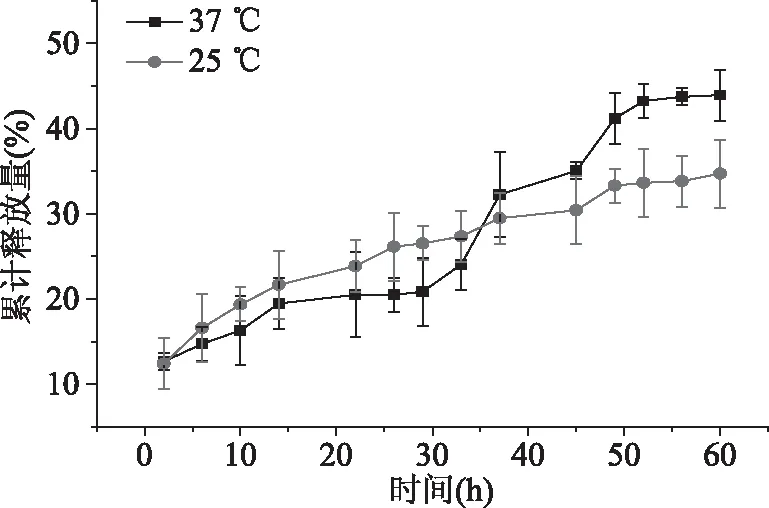
图10 负载胶束在不同环境中的释放曲线Fig.10 Release curves of loadedmicelles in different environments
3 结论
本研究首先用异丙基缩水甘油醚改性木薯淀粉制备了疏水化淀粉R-St,然后用生物相容性好的亲水性基团mPEG进行修饰,得到了一种新型两亲性的淀粉基聚合物R-St-mPEG。利用芘的荧光探针法表征了聚合物的自组装行为,当聚合物胶束浓度达到0.339 mg/mL时,胶束能够发生自组装行为。利用透射电镜进一步表征胶束的形貌,发现胶束结构呈现球形和椭球形。为了探明胶束的粒径,利用马尔文激光纳米粒度散射仪对胶束粒径进行测定,胶束粒径集中分布在两个区域,28和122 nm,与透射电镜结果相符。此外,通过负载抗癌药物姜黄素考察了胶束的负载性能,胶束与姜黄素之间需要合适的比例才能够达到最大负载量,当胶束投加量为100 mg,姜黄素投加量为14 mg时,聚合物胶束具有最大负载量为18.47%。体外释放结果表明聚合物胶束(R-St-mPEG)释放是一个缓慢而稳定的过程,在温度较高的条件下,聚合物胶束的释放速度明显较快,37 ℃环境中,胶束60 h内累计释放量为43.9%,而在25 ℃环境中,60 h内胶束的累计释放量为34.7%。证明聚合物胶束具有温度响应性。本研究证明两亲性聚合R-St-mPEG胶束能够有效包裹和释放药物,能够成为有效的药物载体。

