碳包覆纳米SnSb合金作为高性能钠离子电池负极材料
李海霞,王纪伟,焦丽芳,陶占良,梁静
南开大学化学学院,先进能源材料化学教育部重点实验室,天津 300071
1 引言
钠离子电池具有和锂离子电池类似的电化学反应原理,且钠资源储量丰富、分布广泛、成本低廉。在锂离子电池的大规模发展可能受到锂资源短缺的瓶颈制约情况下,钠离子电池有望在规模储能系统中得到应用,因而受到科研界和工业界的广泛关注1-4。但是由于钠离子半径较大且质量较重5-7,造成钠离子在电极材料中的动力学缓慢8,9,使得钠离子电池实用化进程受阻,因此寻找合适的正负极材料,特别是性能优异的负极材料成为钠离子电池领域的研究重点10,11。目前,高容量的负极材料主要集中于金属氧化物/硫化物材料、合金类材料等。其中,合金类负极材料由于具有较高的理论比容量而广受关注,例如锡锑合金、锡磷化合物和SnGeSb三元合金等12-14。SnSb合金理论比容量高达853 mAh·g-1,是一种非常有潜力的钠离子电池负极材料,但其在充放电过程中体积膨胀造成材料粉化进而导致电池性能迅速衰减15。目前常用的改进方法是纳米化和碳包覆16。Liu等17使用球磨方法制备SnSb/C复合材料,保持Sn和Sb比例在1 : 1,首周比容量为544 mAh·g-1,循环50周之后,容量保持在400 mAh·g-1左右,但球磨法制备的材料尺寸较大,反应活性位点少,材料整体利用率低。Bhattacharyya等18使用静电纺丝法制备多孔碳-SnSb复合材料,在0.2C下,循环200圈之后可逆容量在345-350 mAh·g-1,但材料含碳量达到40%,没有充分发挥SnSb材料的优势。
喷雾热解技术是将原料在溶液状态下混合,粉末由悬浮在气氛中的液滴干燥而来,具有组分均匀、过程简单、高效可控等优点,适合制备多组分复合纳米材料。因此,本文使用气溶胶喷雾热解技术制备碳包覆纳米SnSb复合材料,通过优化合成温度,改变合成条件,实现了对纳米颗粒尺寸及含量的可控制备,并探讨了SnSb/C复合材料的电化学储钠性能。
2 实验部分
2.1 材料制备
首先将3.76 g SnCl2·2H2O (0.05 mol·L-1)与3.8 g SbCl3(0.05 mol·L-1)、3.85 g间苯二酚与5 mL甲醛分别溶解在295 ml的无水乙醇中,形成稳定的溶液。然后将两份溶液混合,搅拌1 h,制得均匀白色前驱体溶液。在0.2 MPa氩气气压下,使用喷雾雾化器将前驱体溶液恒定雾化喷出,吹入到内径为2.5 cm、长度为80 cm的炉管中,然后小液滴在高温下(700、800、900 °C)迅速发生热解反应。在反应过程中,SnCl2和SbCl3在氩气气氛下分解反应生成SnSb,金属Sn、Sb又可作为催化剂来促进酚醛树脂的碳化19,生成的碳基质以及快速的反应时间都有利于限制SnSb粒子的长大,因此便合成了纳米SnSb颗粒与碳的复合材料。在炉管尾端安装内径为2.5 cm、长度为2.0 cm的小石英管用来收集反应产物,根据SnSb纳米颗粒尺寸,将产物命名为10-SnSb/C。通过调整前驱液Sn离子和Sb离子浓度,SnCl2·2H2O和SbCl3分别调整到7.52 g (0.1 mol·L-1)与7.6 g (0.1 mol·L-1),方法同前制得20-SnSb/C。
2.2 材料表征

图1 不同温度下合成SnSb/C复合材料的FESEM图Fig. 1 FESEM images of SnSb/C prepared by different temperatures.
用X射线粉末衍射仪(XRD,MiniFLex600,日本Rigaku公司)和拉曼光谱仪(Raman,DXR型,美国Thermo Fisher公司)进行物相和结构分析;用场发射扫描电子显微镜(FESEM,JEOL JSM-7500F,日本电子株式会社)和透射电子显微镜(TEM,Philips Tecnai F20,美国FEI公司)观察微观形貌;用同步热分析仪(TGA,STA449F3,德国耐驰)测定样品的碳含量;用X射线光电子能谱仪(XPS,PHI 1600 ESCA,美国Perkin Elemer公司)来测定复合材料中Sn、Sb、C的价态;用化学吸附仪(BET,Belsorpmini II,日本拜尔有限公司)进行N2吸脱附测试,测定样品的比表面积、孔分布等信息;用CT2001电池测试系统(武汉市蓝电电子股份有限公司)和Zahner IM6e电化学工作站(德国Zahner公司)进行循环倍率性能测试和循环伏安测试。
2.3 电池组装
将SnSb/C复合材料,碳黑,羧甲基纤维素钠(CMC-Na)以8 : 1 : 1的质量比,加水充分研磨成浆料,然后均匀涂抹在预处理的铜箔上。在真空80 °C下烘干,压片机压制为10 mm的小圆片作为测试电池的正极,金属钠片作为对电极,玻璃纤维为隔膜,1 mol·L-1NaClO4/PC + 5% C3H3FO3(体积分数)溶液为电解液,在高纯氩气手套箱中组装成CR2032型半电池。
3 结果与讨论
3.1 不同温度合成SnSb/C复合材料的形貌和物相分析
对不同热解温度下(700、800、900 °C)合成的10-SnSb/C复合材料进行了SEM和XRD表征,结果如图1、2所示。图1a为700 °C下合成的产物,块状形貌较多,形貌不均一。图1b为800 °C下形成的三维碳球分级结构,由大球和小球堆叠而成,与均匀球形貌相比,具有较高的堆积密度20。图1c中900 °C下制备的样品,形貌同样不均一,碳球之间粘连较为严重,表面有片状和块状物质。这主要是因为反应温度升高使干燥时间缩短,热解后的液滴未及时充分分散便在高温下快速变干团聚,从而导致片状和块状不均一形貌的出现21。从图2的XRD图中可以看出,700 °C下不能合成纯相SnSb/C,800和900 °C温度下能够合成纯相SnSb/C复合材料。而800 °C下合成的复合材料碳球表面较为光滑,碳球包覆的比较完整,900 °C球形度欠佳,团聚现象严重,因此选定800 °C作为反应温度。

图2 不同温度下合成SnSb/C复合材料的XRD谱图Fig. 2 XRD patterns of SnSb/C composites prepared by different temperatures.
3.2 不同尺寸SnSb/C复合材料的形貌及结构组成分析
为了考察离子浓度对形貌和粒子尺寸的影响,在设计实验时选择了两种不同离子浓度的Sn源和Sb源。通过调控不同金属前驱体浓度,制得了不同尺寸的SnSb/C复合材料。对其进行FESEM和TEM表征,结果如图3所示。图3a,b分别为20-SnSb/C和10-SnSb/C的FESEM图,图中可以看出SnSb/C复合材料呈球状堆积,直径在100 nm-1 μm,呈三维分级分布,错落有致。但是由于20-SnSb/C的Sn离子和Sb离子浓度较高,高温下合成的SnSb颗粒不能及时被碳包裹,容易导致部分SnSb合金块状物质出现19(图3a)。从20-SnSb/C的TEM图中(图3c)可以看出,因为Sn离子和Sb离子浓度较高,在高温下形成的碳没有及时包裹住SnSb纳米颗粒,造成SnSb颗粒比较大,与碳包覆不均匀。而10-SnSb/C复合材料中SnSb纳米颗粒(黑色小颗粒)均匀分布,且为碳均匀包覆,总体形成球状分级结构(图3d)。使用Nano-measure软件统计SnSb纳米颗粒大小分布,计算出10-SnSb/C样品中SnSb纳米颗粒为10 nm左右,高倍TEM测定SnSb纳米颗粒晶格间距为0.307 nm,对应SnSb(202)晶面。碳的完整包覆可以有效缓冲SnSb纳米颗粒在脱嵌钠过程中的体积膨胀,提高材料的电化学稳定性能。

图3 SnSb/C复合材料的FESEM和TEM图Fig. 3 FESEM and TEM images of SnSb/C composites.

图4 10-SnSb/C和20-SnSb/C复合材料的XRD(a)和Raman(b)谱图Fig. 4 XRD (a) and Raman (b) spectra of 10-SnSb/C and 20-SnSb/C.
对合成的样品分别进行XRD和拉曼表征,结果如图4所示。从图4a的XRD图可以看出10-SnSb/C和20-SnSb/C能够与SbSn标准PDF卡片(JCPDS No. 33-0118)很好的对应,无杂峰出现,同时XRD中也没有观察到明显的金属Sn或Sb的峰,说明经高温反应后SnSb形成了合金17。从拉曼表征中可以看出,在1339和1582 cm-1处存在碳的D(disorder)带和G (graphenic)带特征峰,且两个样品出峰位置基本吻合21。
使用XPS进一步研究SnSb/C复合材料中C,Sn,Sb价态,XPS测试的结合能以C 1s图谱(284.8 eV)进行校正,如图5a,b,c所示。C 1s峰在283.8 eV处的特征峰对应于sp2杂化石墨型碳,284.8 eV处的特征峰对应于sp3杂化石墨型碳,288.2 eV处的微弱峰可归结为C与O的相互作用22,23。Sn元素在495.3和486.9 eV处的两个峰,分别对应合金SnSb的Sn 3d3/2和Sn 3d5/2轨道24。Sb元素在540.6和531.2 eV处的两个峰,分别对应合金SnSb的Sb 3d3/2和Sb 3d5/2轨道25。10-SnSb/C和20-SnSb/C的碳含量通过热重测定,如图5d所示。SnSb/C复合材料在350 °C时质量有一个上升的过程,对应于SnSb合金的氧化过程(生成SnO2和Sb2O3),造成质量增加。随后继续升温(≥ 400 °C),碳被氧化为二氧化碳并流失到空气中,表现为材料的失重过程。由此计算10-SnSb/C的含碳量为22.6%,20-SnSb/C的含碳量为12.1%21,26。
采用BET进行N2吸脱附测试,研究样品的比表面积、孔分布等信息,结果如图6所示。SnSb/C纳米复合材料的吸脱附曲线为典型的IV型曲线,高相对气压处有一个陡升的趋势,表明SnSb/C纳米复合材料为介孔材料。SnSb/C形成介孔的原因与SnS/C复合材料相同,酚醛树脂、SnCl2·2H2O和SbCl3热解产生的大量气体蒸发促使介孔生成。进一步对吸脱附曲线进行拟合,计算出10-SnSb/C和20-SnSb/C比表面积分别为157、107 m2·g-1,10-SnSb/C具有较高的比表面积得益于SnSb纳米颗粒的小尺寸及在碳球中的均匀分布。较高的比表面积可以有效增加电极材料与Na+的接触位点,提高材料利用率,增加储钠性能。

图5 10-SnSb/C复合材料的XPS图谱和10-SnSb/C与20-SnSb/C复合材料的TG图Fig. 5 XPS spectra of 10-SnSb/C and the TG curves of 10-SnSb/C and 20-SnSb/C.
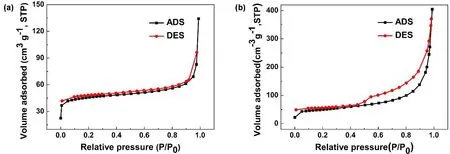
图6 SnSb/C的氮气吸脱附曲线Fig. 6 N2 adsorption/desorption isotherms of SnSb/C.
3.3 SnSb/C复合材料的电化学测试及机理分析

图7 SnSb/C复合材料的CV曲线、充放电曲线和倍率性能图Fig. 7 CV profiles, discharge/charge curves, and cycling performance of SnSb/C composites.
为研究SnSb/C的电化学特征,将SnSb/C复合材料组装成扣式电池并进行循环伏安及充放电测试,如图7所示。值得说明的是,文中比容量的计算是以SnSb/C复合材料整体计算,没有减掉碳的质量。考虑到碳对电化学容量的贡献,将该合成条件下生成的碳材料组装成半电池进行测试,结果表明,在100 mA·g-1下首圈放电容量为133.8 mAh·g-1,循环50周后可逆容量仅为45.2mAh·g-1。由于SnSb/C复合材料中C含量较低,因此喷雾热解制备的碳在SnSb/C复合材料中贡献的比容量非常有限。图7a为10-SnSb/C在0.05 mV·s-1扫速下的循环伏安曲线,阴极扫描过程中,首圈在0.3 V左右的还原峰对应于SEI膜及NaxSn和NaxSb合金的生成,随后扫描在0.3和0.6 V处出现两个峰,0.3 V处对应Sn和Na发生合金化反应生成Na15Sn4,0.6 V处对应Sb和Na发生合金化反应生成Na3Sb。在阳极扫描过程中,位于0.22、0.6、0.82 V的特征峰分别对应Na15Sn4和Na3Sb的去合金化过程,其中0.22 V对应Na15Sn4去合金化,0.6和0.82 V对应Na3Sb去合金化过程。以上反应过程与文献报道相吻合27。从10-SnSb/C的充放电曲线可以看出(如图7b所示),首圈放电容量达到722.1 mAh·g-1,首圈库仑效率达到86.3%,30圈之后容量保持在610.0 mAh·g-1。而20-SnSb/C充放电测试(如图7c所示)首圈放电容量达到738.7 mAh·g-1,但是30圈之后容量仅剩387.5 mAh·g-1。继续对10-SnSb/C和20-SnSb/C进行大电流密度放电,测试电极材料的倍率性能(如图7d所示)。10-SnSb/C复合材料在100、1000、3000 mA·g-1下比容量分别达到607.7、645.4、452.2 mAh·g-1;而20-SnSb/C在100、1000、3000 mA·g-1下比容量分别为586.5、328.5、201.2 mAh·g-1。20-SnSb/C相较于10-SnSb/C,充放电容量衰减迅速、倍率性能较差,这主要是由于20-SnSb没有被碳球全部包裹住,体积膨胀严重,表面SnSb纳米颗粒没有得到较好的保护。
接下来对10-SnSb/C、20-SnSb/C及纯SnSb在1 A·g-1电流密度下进行长循环测试,如图8所示。10-SnSb/C循环200周之后容量保持率为95%,可逆容量达到623 mAh·g-1,从10-SnSb/C的库仑效率可以看出SnSb/C复合材料在循环过程中电化学性能比较稳定。20-SnSb/C循环200周之后可逆容量仅为476 mAh·g-1。纯SnSb合金循环30圈之后比容量为248 mAh·g-1,容量衰减最为严重。
对10-SnSb/C和20-SnSb/C进行EIS阻抗分析(图9),10-SnSb/C欧姆电阻(Rs)为2.3 Ω,电荷转移阻抗(Rct)为11.9 Ω,20-SnSb/C欧姆电阻(Rs)和电荷转移阻抗(Rct)分别为5.1和380.2 Ω,两个值均大于10-SnSb/C,这表明10-SnSb/C中碳的均匀包覆,以及超小SnSb纳米粒子更有利于钠离子快速脱嵌。

图8 10-SnSb/C, 20-SnSb/C以及纯SnSb在1 A·g-1下的循环性能对比,以及10-SnSb/C的库仑效率图Fig. 8 Cycling performance of 10-SnSb/C,20-SnSb/C and pure SnSb at 1 A·g-1, and the coulombic efficiency of 10-SnSb/C.
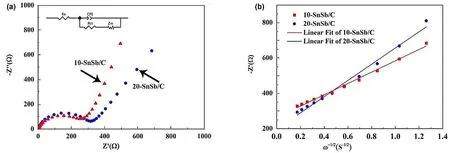
图9 10-SnSb/C和20-SnSb/C阻抗分析图Fig. 9 Impedance analysis diagrams of 10-SnSb/C and 20-SnSb/C.
4 结论
通过喷雾热解法合成了SnSb/C复合材料,优化了合成条件,对比了10-SnSb/C、20-SnSb/C、纯SnSb的电化学储钠性能。测试结果表明,10-SnSb/C复合材料首圈放电达到722.1 mAh·g-1,首圈库仑效率达到86.3%,在100、1000、3000 mA·g-1下,比容量分别为607.7、645.4、452.2 mAh·g-1,在1000 mA·g-1电流下循环200周之后容量保持率为95%,可逆容量达到623 mAh·g-1。10-SnSb/C纳米复合材料优越的电化学性能得益于于以下两个方面:首先,超小的SnSb纳米颗粒(10 nm)可以显著减小活性物质在脱嵌钠过程中产生的形变应力,并提高其反应利用率;其次,碳均匀包覆后形成的多孔球形分级结构可以促进离子电子的传导,并能有效缓冲SnSb纳米粒子在循环过程中的体积变化,从而有效抑制粉化与团聚。本文采用的喷雾热解法具有快速、连续、可工业化应用的优点,结合SnSb的高比容量和碳的高导电性,进一步提高了材料的循环和倍率性能,为以后SnSb钠离子电池负极材料的应用奠定了基础。

