CDK1 磷酸化修饰对驱动蛋白Kif18A 的ATP 酶活性的影响
苏春玉,周之春,朱长军
(1.天津师范大学生命科学学院,天津300387;2.天津师范大学天津市动植物抗性重点实验室,天津300387;3.天津师范大学分子细胞系统生物学重点实验室,天津300387)
驱动蛋白分子(kinesins)是以细胞内微管为轨道的动力蛋白,与细胞内细胞器的移动、细胞有丝分裂及减数分裂、组织器官的生长发育以及神经元的发育及信号传导等密切相关[1].Kif18A 是Kinesin-8 家族中的一员.研究表明,Kif18A 对有丝分裂过程中的纺锤体微管动力学和染色体振幅起着重要调控作用[2-3].与其他驱动蛋白分子相同,Kif18A 蛋白由3个功能域组成:N 端的马达结构域(motor domain)、中央卷曲螺旋杆状结构域(stalk domain)和C 端货物分子结合结构域(tail domain).Kif18A 利用水解ATP 释放的能量可以沿着微管向正极末端移动,由于其C 末端存在另一个微管结合位点,因此Kif18A 能够稳定运动到微管正极末端并聚集,进而抑制微管的动态不稳定性[4-7],通过降低染色体的振荡速率限制其振荡幅度[8-10].有丝分裂关键蛋白激酶CDK1 可对Kif18A 的S674 和S684 氨基酸位点进行磷酸化修饰,使得Kif18A 无法到达动粒微管的末端并聚集,因此Kif18A 无法发挥其降低微管动态不稳定性的功能,使得动粒振幅增大[11].据推测这可能是因为CDK1 的磷酸化修饰影响了Kif18A 的ATP 酶活性,使Kif18A 无法到达微管正极末端.
本研究构建了Kif18A 突变体的杆状病毒Kif18AAA(S674A/S684A)和Kif18A-EE(S674E/S684E),利用SF9 细胞表达这2 种杆状病毒蛋白,通过纯化获得Kif18A-AA 和Kif18A-EE 蛋白,检测其ATP 酶活性,进而分析CDK1 磷酸化修饰对Kif18A 蛋白ATP 酶活性的影响,为深入理解Kif18A 在细胞有丝分裂期的功能提供体外实验依据.
1 材料与方法
1.1 材料
昆虫细胞SF9,本实验室自存;pFastBac-HTa、pEGFP-Flag-Kif18A-EE、pEGFP-Flag-Kif18A-AA 质粒为本实验室前期构建;TransT1、DH10Bac 感受态细胞、Kif18A 抗体、Kif18A 磷酸化抗体均为实验室自制.
1.2 试剂
ATPase/GTPase ELIPA Biochem Kit(Catalog number:BK051/52)、Tubulin 和488 Labeled Tubulin,美国Cytoskeleton 公司;琼脂糖凝胶回收试剂盒,北京康为世纪生物科技有限公司;EcoRⅠ和SalⅠ工具酶、SuperFectin 试剂,美国Thermo Scientific 公司;T4 连接酶,日本Takara 公司;SIM SF 培养基,北京义翘神州生物技术有限公司;鼠抗Flag 抗体、Flag Beads 和3×Flag Peptide,美国Sigma 公司.
1.3 方法
1.3.1 DH10Bac 感受态细胞转化
从-80 ℃冰箱中取出DH10Bac 感受态细胞,冰上融化后,加入10 ng pFastBac-Flag-Kif18A-EE 或pFast-Bac-Flag-Kif18A-AA 质粒,冰上孵育30 min 后,42 ℃水浴锅中热激45 s,迅速置于冰上2 min,加入900 μL SOC液体培养基.37 ℃条件下225 r/min 摇菌6 h,之后取100 μL 涂平板(50 μg/mL Kan+,7 μg/mL Gen+,10 μg/mL Tet+,0.1 mol/L IPTG,2%X-gal),将平板倒置放于37 ℃培养箱中培养72 h.挑取3个白色克隆转接到LB 液体培养基(含50 μg/mL Kan+、7 μg/mL Gen+和10 μg/mL Tet+)中,37 ℃过夜培养,提取杆状病毒基因组.
1.3.2 杆状病毒基因组提取
将菌液转移到1.5 mL 离心管中,14000 r/min 离心1 min,真空吸干上清,加入0.3 mL 的Buffer P1(含有RNase A)重悬沉淀,混匀后加入0.3 mL 的Buffer P2,室温孵育5min.加入0.3mL 醋酸钾(浓度为3 mol/L,pH 值为5.5),轻轻混匀,蛋白形成白色沉淀. 冰上放置10 min后14000 r/min 离心10 min,将上清转移到含有0.8 mL 异丙醇的离心管中.混匀,冰上放置10 min.室温下14000 r/min 离心15 min,弃去上清后加入0.5 mL 70%的乙醇,室温下14000 r/min 离心5 min.室温放置10 min 风干沉淀,加入40 μL pH 值为8.0 的1×TE Buffer 重新溶解DNA 沉淀.-20 ℃储存.
1.3.3 PCR 验证杆状病毒基因组
1.3.2 中得到的杆状病毒基因组须进行PCR 验证,确定其是否为发生转座的重组基因组. 引物序列:M13F(5′-CCCAGTCACGACGTTGTAAAACG-3′),Kif18A-R(5′-CTAATGCCATCTCCCTTGAAAG-3′).PCR体系:93 ℃预变性3 min;94 ℃变性45 s,55 ℃退火45 s,72 ℃延伸5 min,30个循环;72 ℃终延伸7 min,4 ℃保存. 取5 μL PCR 产物进行琼脂糖凝胶电泳,110 V 恒压45 min.
1.3.4 重组杆状病毒基因组感染SF9 细胞
在60 cm 平板中接种3×106个SF9 细胞,27 ℃下培养30 min,使细胞贴壁生长.吸弃培养基,加入3 mL新鲜培养基,加入转染试剂(1 μg 病毒基因组DNA,15 μL SuperFectin 转染试剂),边滴加边摇匀,27 ℃条件下培养72 h.
1.3.5 杆状病毒的收取、扩增及滴度的测定
转染72 h 后,收集上清为第一代杆状病毒,避光保存在4 ℃冰箱中.由于转染所得到的病毒滴度较低,不能高效表达目的蛋白,因此要进行杆状病毒扩增,以增加病毒的滴度.用第一代杆状病毒分别在10 cm平皿和50 mL 培养瓶中继续感染SF9 细胞,扩增杆状病毒,使其滴度逐步提高. 但过高的感染浓度可能会产生不完整的目的蛋白,因此通过调整感染比例(1 ∶100、1 ∶500、1 ∶1000、1 ∶5000)和感染时间(36、48、60、72 h)得到病毒表达蛋白的最佳条件.
1.3.6 Kif18A 突变体蛋白的表达和纯化
在50 mL 锥形瓶中接种SF9 细胞,细胞密度为1×106mL-1,以杆状病毒最佳感染浓度感染SF9 细胞,27 ℃条件下悬浮培养,在病毒表达蛋白的最佳时间收取细胞并将细胞沉淀冻存于-80 ℃冰箱中.
由于Kif18A 突变体蛋白在SF9 细胞中进行表达,因此蛋白要进行纯化. 通过对融合到目的蛋白中的Flag 标签蛋白进行纯化,就可以得到目的蛋白.向50 mL SF9 细胞沉淀中加入2 mL 裂解液(0.3 mol/L NaCl,20 mmol/L pH 值为7.5 的Tris-Cl,1%NP-40,1 mmol/L PMSF,1 mmol/L DTT,10 mmol/L β-ME,0.5 mmol/L ATPNa,1μg/mL Approtinin,1×Cocktail,50 μmol/L Na3VO4),将细胞沉淀重悬后,冰上裂解60 min,将液体转移至2 mL 离心管中.4 ℃下14000 r/min 离心30 min,转移上清到2 mL 离心管中. 加入25 μL Flag Beads,4 ℃下旋转孵育2 h 后收集上清,用洗液(0.3 mol/L NaCl,20 mmol/L pH 值为7.5 的Tris-Cl,1 mmol/L PMSF,1 mmol/L DTT,10 mmol/L β-ME,0.5 mmol/L ATP-Na,1μg/mL Approtinin,1×Cocktail,50 μmol/L Na3VO4)清洗Beads 3 次,加入洗脱液(3×Flag Peptide,稀释比例为1 ∶20)4 ℃下洗脱2 h,收集第1 次洗脱样品.再次加入洗脱液,4 ℃下过夜,洗脱后收集第2 次洗脱样品.将2 次所得的纯化蛋白进行聚丙烯酰胺凝胶电泳,考马斯亮蓝染色1 h 后进行脱色,观察蛋白纯化的效果.
1.3.7 体外微管合成
根据微管合成试剂盒(Cat.#TL488M)说明书合成微管. 取1 份分装好的微管蛋白(Tubulin 和488 Labeled Tubulin 体积比为5 ∶1),迅速加入等量General Tubulin Buffer(80 mmol/L PIPES,2 mmol/L MgCl2,0.5 mmol/L EGTA,1 mmol/L GTP,1 mmol/L DTT,20 μmol/L Taxol).37 ℃水浴合成2 h 后,取0.5 μL 滴片,镜下观察微管合成情况,室温保存合成的微管.
1.3.8 Kif18A 突变体蛋白的ATP 酶活性测定
首先根据ATPase/GTPase ELIPA Biochem Kit 说明书绘制磷酸根标准曲线. 将1mL ELIPA 反应溶液、12.5 μL ELIPA 试剂2、240 μL ELIPA 试剂1、80 μL合成微管和10 μL Taxol(2 mmol/L)混和后,按每孔147.5 μL 混合液的量在96 孔板中分装,向每孔中加入1 μg 纯化的Kif18A-EE 或Kif18A-AA 蛋白,每种蛋白设置3个重复. 以不加目的蛋白为空白对照,用洗脱液补齐.设置好分光光度计参数,在加入ATP 前预先测定2 组吸光度值.用排枪移液器同时向混合液中加入10 μL ATP 溶液,立刻置于分光光度计中测定不同孔的360 nm 处的吸光度值(OD360),每1 min 测1 次,连续测量1 h.处理数据,绘制ATP 酶活性曲线.
1.4 数据处理
将测得的3 组OD360取平均值,用目的蛋白的OD360减去空白对照的OD360,根据磷酸根标准曲线计算出差值对应的磷酸根的物质的量.用加入ATP 后的磷酸根物质的量减去加入ATP 前的数值,得到目的蛋白水解ATP 产生的磷酸根物质的量,分别根据2 种蛋白对应的磷酸根物质的量绘制ATP 酶活性曲线.
2 结果与分析
2.1 质粒pFastBac-Kif18A-EE 和pFastBac-Kif18AAA 的构建与鉴定
用EcoRⅠ和SalⅠ双酶切pEGFP-Flag-Kif18AEE、pEGFP-Flag-Kif18A-AA、pFastBac-HTa 质粒后进行琼脂糖凝胶电泳,结果如图1 所示.pEGFP 空质粒大约为4800 bp,Kif18A cDNA 长度为2697 bp,因此电泳前面的条带为Flag-Kif18A-EE 和Flag-Kif18A-AA.pFastBac-HTa 质粒长度为4855 bp,与DNA marker 进行比对,位置正确.

图1 酶切3 种质粒后的琼脂糖凝胶电泳检测Fig.1 Electrophoresis of agarose gel of three kinds of plasmid after digestion
通过琼脂糖凝胶回收试剂盒得到Flag-Kif18AEE、Flag-Kif18A-AA 和pFastBac-HTa 的线性DNA,电泳结果如图2 所示.
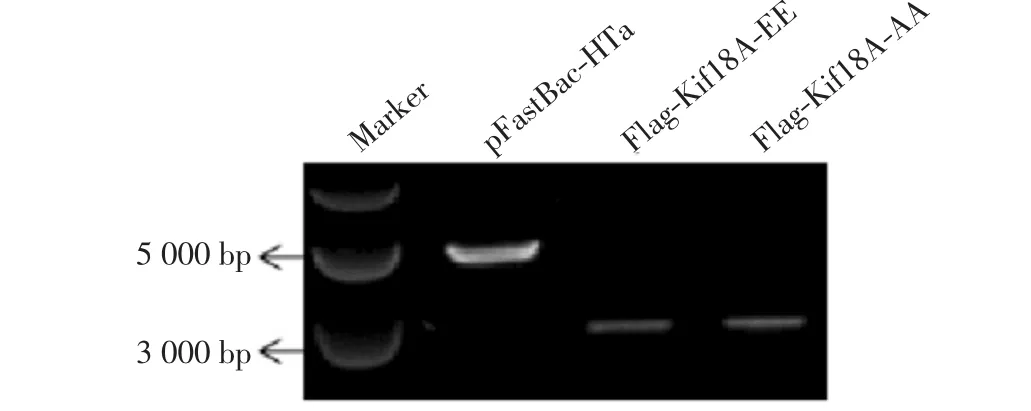
图2 胶回收后3 种质粒的琼脂糖凝胶电泳图Fig.2 Electrophoresis of agarose gel of three kinds of plasmid after gel extraction
通过T4 连接酶16 ℃过夜连接,连接产物全部转化TransT1 感受态细胞,过夜培养,挑取阳性克隆,液体培养. 通过小提质粒试剂盒提取pFastBac-Kif18AEE、pFastBac-Kif18A-AA 质粒. 质粒经过测序后与NCBI 公布的序列进行比对验证.
2.2 杆状病毒基因组的制备及验证
将pFastBac-Kif18A-EE、pFastBac-Kif18A-AA 质粒分别转化至DH10 Bac 感受态细胞中,挑取白色克隆过夜培养,提取杆状病毒基因组.当目的基因插入到杆状病毒基因组中,如图3 所示,会得到含有目的基因的重组杆状病毒基因组. 使用转座位点上游存在的M13 上游引物和目的片段中设计的下游引物进行PCR,可得到大小为3707 bp 的DNA 片段.对PCR 产物进行琼脂糖凝胶电泳,条带大小与理论值相符,证明确实发生了转座,获得了重组杆状病毒的基因组.

图3 重组杆状病毒基因组的验证Fig.3 Verification of recombinant baculovirus genome
2.3 杆状病毒的扩增及蛋白表达条件优化
将重组的杆状病毒基因组转染SF9 细胞后,杆状病毒在SF9 细胞中进行组装和增殖.当SF9 细胞中的病毒过多时,杆状病毒就会从SF9 细胞中释放,进一步感染其他的SF9 细胞.但病毒扩增到一定程度后,可能会表达不完整的Kif18A 蛋白,因此需要优化Kif18A突变体蛋白表达的病毒感染条件.以Kif18A-EE 杆状病毒为例进行优化过程的描述.通过设置连续梯度的感染比例(1 ∶100,1 ∶500,1 ∶1000,1 ∶5000)感染SF9细胞进行蛋白表达,在表达时间(72 h)一致的情况下,可以得到杆状病毒的最佳感染比例为1 ∶5000,如图4(a)所示,在此感染比例下未出现杂蛋白. 如果无论何种感染比例都出现很多杂蛋白,则用1 ∶5000 的感染比例感染SF9 细胞,分别在36、48、60、72 h 收取细胞,通过Weatern Blot 验证,得到蛋白的最佳表达时间为72 h,如图4(b)所示.最终得到Kif18A-AA 的最佳感染比例为1 ∶20000,Kif18A-EE 的最佳感染比例为1 ∶5000,最佳表达时间均为72 h.
2.4 蛋白质的表达及纯化
按照2 种杆状病毒表达目的蛋白的最优条件感染SF9 细胞,收取细胞后通过蛋白印迹杂交实验验证所感染的SF9 细胞大量表达了目的蛋白,结果如图5所示.
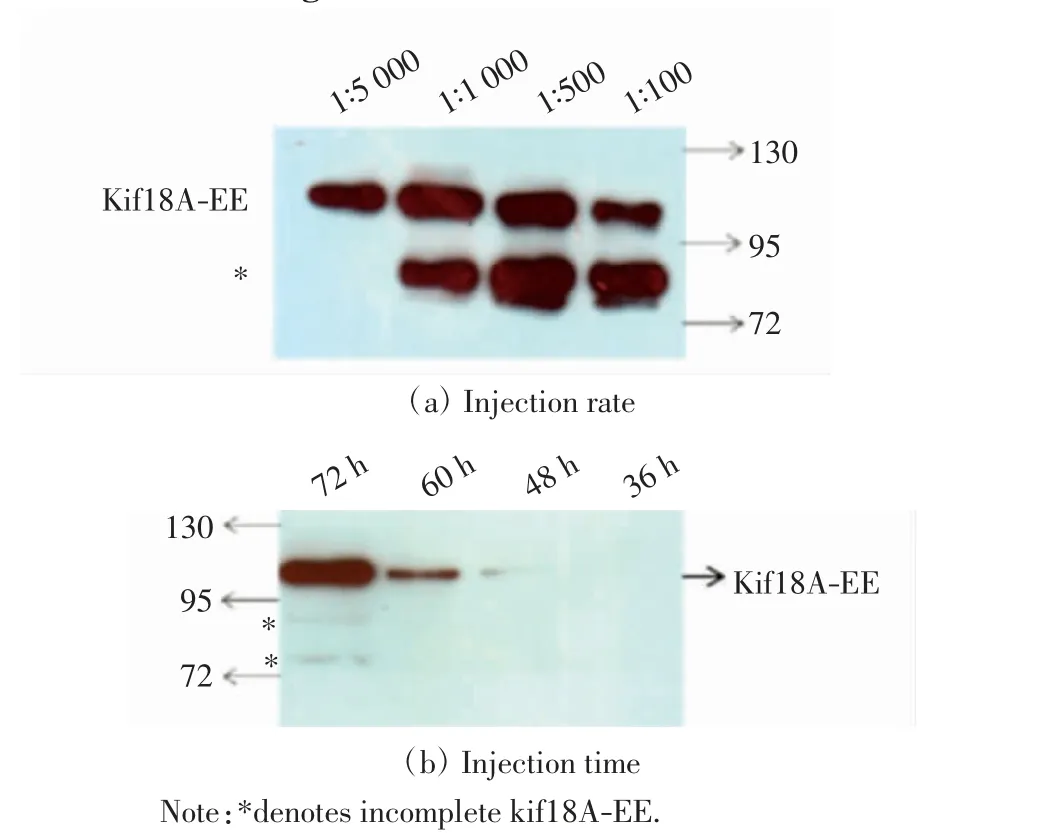
图4 Kif18A-EE 杆状病毒条件优化Fig.4 Condition optimization of Kif18A-EE baculovirus

图5 杆状病毒表达蛋白的鉴定Fig.5 Identification of baculovirus-expressed proteins
由图5 可以看出,SF9 细胞表达的蛋白可以被特异性鼠抗Flag 和兔抗Kif18A 抗体识别,Kif18A-EE 蛋白可以被特异性抗Kif18A-S674 和S684 位点磷酸化的抗体所识别,Kif18A-AA 蛋白不能被这些磷酸化抗体识别.表明Kif18A-EE 蛋白可以很好地模拟磷酸化的Kif18A 蛋白,而Kif18A-AA 蛋白模拟了非磷酸化的Kif18A 蛋白.
随后利用Flag Beads 纯化上述蛋白,纯化后进行聚丙烯酰胺凝胶电泳,考马斯亮蓝染色后脱色,观察目的蛋白的纯化效果,结果如图6 所示.纯化得到的Kif18A-EE 和Kif18A-AA 蛋白浓度分别为0.12 μg/μL和0.10 μg/μL.
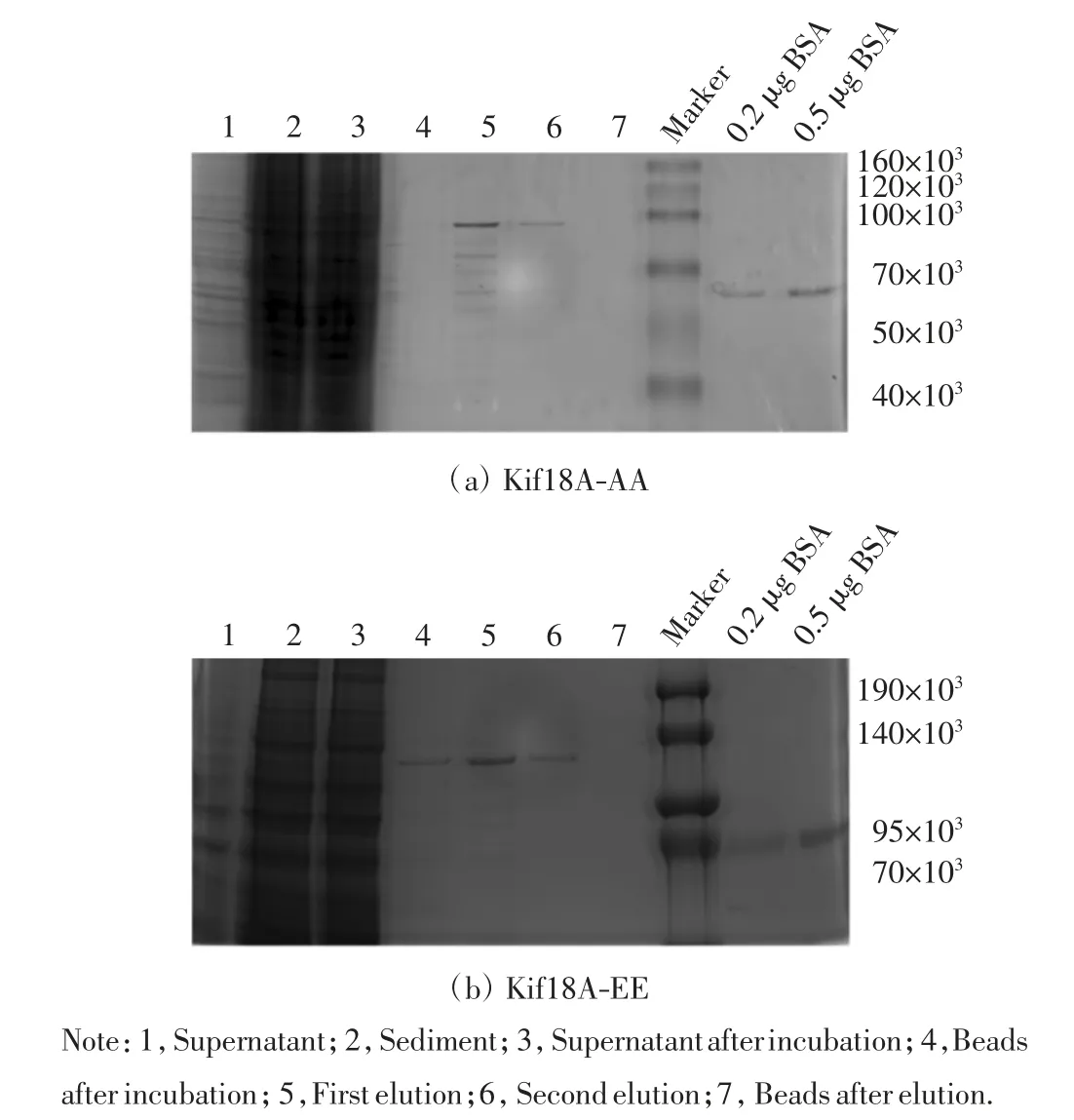
图6 Kif18A-AA 和Kif18A-EE 的蛋白纯化Fig.6 Purification of Kif18A-AA and Kif18A-EE
2.5 微管体外合成
Kif18A 作为一种驱动蛋白,能够利用水解ATP 释放的能量沿着微管向正极末端移动. Kif18A 要发挥ATP 酶活性,需要微管参与,因此必须进行体外微管合成.微管蛋白在GTP 存在下倾向于聚合,但聚合的微管并不稳定,所以在合成微管的过程中加入Taxol.微管蛋白通过聚合,合成了相对独立的微管,如图7所示,在荧光显微镜下观察,可以看到发出绿色荧光的微管.
2.6 ATP 酶活性检测
Kif18A 沿微管向正极移动会水解ATP,形成ADP和磷酸根,且每水解一分子ATP 会生成一分子磷酸根,因此通过磷酸根的量可以得出被水解ATP 的量,即被水解的ATP 的量反映Kif18A 的ATP 酶活性.磷酸根在360 nm 处有自己的吸收峰,因此可以利用分光光度计测量360 nm 处的吸光度值从而得到磷酸根的量.通过磷酸根的物质的量及其对应的吸光度值,得到磷酸根的标准曲线,如图8 所示.
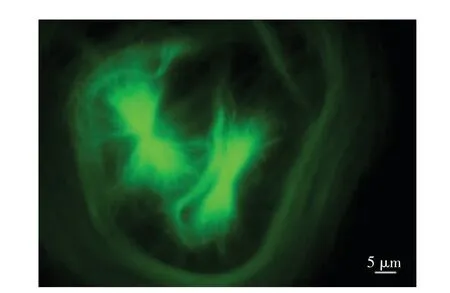
图7 微管体外合成Fig.7 Microtubule synthesis in vitro

图8 磷酸根标准曲线Fig.8 Standard curve of phosphate
利用纯化得到的目的蛋白和体外合成的微管,进行ATP 酶活性检测.根据加入目的蛋白后磷酸根的吸光度值,由磷酸根标准曲线计算出Kif18A 突变体蛋白水解ATP 的量,得到Kif18A 突变体蛋白的ATP 酶活性,结果如图9 所示.

图9 Kif18A-AA 和Kif18A-EE 的ATP 酶活性检测Fig.9 Detection of ATPase activities of Kif18A-AA and Kif18A-EE
由图9 可以看出,非磷酸化的Kif18A(Kif18A-AA)的ATP 酶活性进入平台期后数值均为3.47 nmol Pi,模拟CDK1 磷酸化后Kif18A(Kif18A-EE)的ATP 酶活性平台期数值约为2.72 nmol Pi,即Kif18A-EE 蛋白的ATP 酶活性低于Kif18A-AA 蛋白的ATP 酶活性,表明CDK1 对Kif18A 的磷酸化修饰降低了Kif18A 的ATP酶活性.
3 讨论与结论
Kinesin-8 家族在整个真核细胞有丝分裂过程中对于微管长度的控制具有重要作用. Kif18A 作为Kinesin-8 家族中的一员,在微管正极末端的作用存在争议:体外实验发现Kif18A 能够作为微管解聚酶使微管的稳定结构解聚[12],但也有研究表明,Kif18A 不具有内在的解聚酶活性,而是通过阻止微管蛋白加到微管末端,进而阻止了微管的聚合和解聚[2].Kif18A 对细胞周期中的染色体整列有很大的影响.染色体整列包括中板集合与形成最薄中期板(thinnest metaphase plate)2个过程.有研究[11]报道,Kif18A 在细胞有丝分裂早期被有丝分裂蛋白激酶CDK1 磷酸化,这种修饰可以被磷酸酶PP1 去磷酸化,当Kif18A 无法被PP1 去磷酸化时,细胞有丝分裂过程就无法形成最薄中期板.这可能是因为磷酸化的Kif18A 无法到达微管正极末端,从而无法降低微管的动态不稳定性.同时Kif18A 被磷酸化后不影响中板集合的时间,但会延迟最薄中期板形成的时间,这可能是因为CDK1 的磷酸化修饰影响了Kif18A 的运动能力.虽然Häfner 等[11]应用细菌表达的Kif18A 进行了ATP 酶活性的测定,但是由于原核细胞表达的蛋白可能不具有正常的蛋白构象[13],因而实验结果仍需进一步验证.本研究利用杆状病毒昆虫细胞表达系统获得了目的蛋白,这种真核表达系统能够使目的蛋白的免疫原性、ATP 酶活性等与天然蛋白的生物活性基本相同.体外实验结果显示Kif18A-EE 蛋白的ATP 酶活性低于Kif18A-AA 蛋白的ATP 酶活性,表明CDK1 对Kif18A 的磷酸化修饰降低了它的ATP 酶活性.这一结果预示着CDK1 的磷酸化修饰作用通过影响Kif18A 的ATP 酶活性,进而影响其在微管上的运动能力,使其无法及时到达微管末端并控制最薄中期板形成的时间. CDK1 磷酸化修饰调节Kif18A 的ATP 酶活性的机制仍不清楚,是通过影响Kif18A 的结构还是与其他蛋白的结合能力,仍需继续深入探索.

