LC-HR-MS/MS法鉴定头孢丙烯干混悬剂中的未知杂质
肖颖 袁晓 林顺权

中图分类号 R927 文献标志码 A 文章编号 1001-0408(2020)10-1217-06
DOI 10.6039/j.issn.1001-0408.2020.10.12
摘 要 目的:检测头孢丙烯干混悬剂中的未知杂质,并对其进行结构鉴定。方法:采用高效液相色谱-串联高分辨质谱法检测并鉴定头孢丙烯干混悬剂中的未知杂质。色谱柱为Thermo HyPURITYTM C18,流动相为乙腈-0.013%甲酸水溶液(梯度洗脱),检测波长为230 nm,流速为1.0 mL/min,柱温为40 ℃,进样量为20 μL;以电喷雾离子源行正离子全扫描,扫描范围为质荷比(m/z)100~1 500,喷雾电压为3.8 kV,金属毛细管温度为320 ℃,鞘气压力为60 Arb,辅助气压力为10 Arb,喷雾温度为280 ℃。结果:在该色谱条件下,杂质K的检测限为0.202 μg/mL,精密度、重复性试验的RSD均小于4%。杂质K附近发现3个未知杂质,且互为异构体,离子保留时间为17.83~19.31 min,二级母离子均为m/z 436.150 0[M+H]+,可能为头孢丙烯开环、脱水后的产物。结论:本方法检测出头孢丙烯干混悬剂中杂质K附近的3个未知杂质。
关键词 高效液相色谱-串联高分辨质谱法;头孢丙烯干混悬剂;杂质K;未知杂质
Identification of Unknown Impurities in Cefprozil Suspension by LC-HR-MS/MS
XIAO Ying1,YUAN Xiao2,LIN Shunquan2(1.Baiyunshan Pharmaceutical General Factory, Guangzhou Baiyunshan Pharmaceutical Holdings Co., Ltd., Guangzhou 510515, China;2.Guangzhou PI & PI Biotechnology Co., Ltd., Guangzhou 510530, China)
ABSTRACT OBJECTIVE: To determine unknown impurities in Cefprozil suspension, and to identify its structure. METHODS: LC-HR-MS/MS method was used to detect and identify unknown impurities in Cefprozil suspension. The determination was performed on Thermo HyPURITYTM C18 with mobile phase consisted of acetonitrile-0.013% formic acid solution (gradient elution) at the flow rate of 1.0 mL/min. The detection wavelength was set at 230 nm, and column temperature was 40 ℃. The sample size was 20 μL. ESI+ full scanning was carried out with electrospray ion source scanning range was mass-charge ratio (m/z) 100-1 500 with spray voltage of 3.8 kV, metal capillary temperature of 320 ℃, sheath gas pressure of 60 Arb, auxiliary gas pressure of 10 Arb, spray temperature of 280 ℃. RESULTS: Under this condition, the detection limit of impurity K was 0.202 μg/mL. RSDs of precision and reproducibility tests were both lower than 4%. Three unknown impurities were found around impurity K, which were isomers of each other. The retention time of ions were 17.83-19.31 min, and the secondary parent ion were all m/z 436.150 0[M+H]+, which may be the product of ring opening and dehydration of cefpropene. CONCLUSIONS: Three unknown impurities near impurity K in Cefprozil suspension were detected by this method.
KEYWORDS LC-HR-MS/MS; Determination; Cefprozil suspension; Impurity K; Unknown impurities
頭孢丙烯是由美国Bristol-Myers Squibb公司于1983年开发的第2代头孢菌素口服制剂[1-2],于1992年以“Cefzil”的商品名在美国首次上市,其对革兰氏阳性菌和革兰氏阴性菌均表现出良好的抑制活性,且安全性高、毒副作用小[3]。头孢丙烯对细菌感染的疗效与阿莫西林克拉维酸、红霉素、头孢克肟相似且优于或等于同为第2代头孢菌素的头孢克洛和头孢呋辛酯[4]。
头孢丙烯是美国FDA批准的第1个可用于治疗儿童中耳炎和鼻窦炎的口服头孢菌素类抗生素,目前该药已知的特定杂质包括杂质A(α-对羟基苯甘氨酸)、杂质B(头孢羟氨苄)、杂质D、 杂质G、杂质H、杂质I、杂质M,其他非特定杂质C、杂质E、杂质F、杂质J、杂质K、杂质L、杂质N[5]。有研究报道,头孢丙烯结构中含有β-内酰胺环,所以其在水或酸性溶液等情况下易发生水解开环而失去抗菌活性[6]。
头孢丙烯干混悬剂为儿童用药剂型,加入的辅料相较片剂更多,制剂受辅料影响也较大,因而制剂中仍有一些未知的杂质。笔者前期研究发现,在某厂生产的头孢丙烯干混悬剂中,在杂质K色谱峰附近还有其他未知的杂质,且这些杂质在贮存过程中还会逐渐增加。
目前,液质联用技术(LC-MS)[7]在各类药物的杂质分析中已被广泛应用[8-12],尤其是抗生素类如β-内酰胺类、氨基糖苷类、四环素类、大环内酯类、喹诺酮类等药物的杂质分析[13]。本文采用高效液相色谱-串联高分辨质谱法(LC-HR-MS/MS)定性研究了头孢丙烯干混悬剂中杂质K附近的未知杂质,并进行结构鉴定,旨在为头孢丙烯干混悬剂生产中的杂质控制提供参考。
1 材料
1.1 仪器
Q-Exactive Focus型高分辨质谱仪、Dionex UltiMate 3000 RS型超高效液相色谱(UPLC)仪(包括四元泵洗脱系统、自动进样器、柱温箱、二极管阵列检测器)均购自美国Thermo Fisher Scientific公司;1260型HPLC仪(美国Agbilent公司);AR2140型分析天平(上海奥豪斯仪器有限公司)。
1.2 药品与试剂
头孢丙烯干混悬剂(批号:02180802,规格:0.125 g)及其空白辅料均由广州白云山医药集团股份有限公司白云山制药总厂提供;头孢丙烯杂质K标准品[广州牌牌生物科技有限公司,批号:PITBBX-K-EP-20181017-01,纯度:96.64%(以4个异构体的总和计)];乙腈、甲酸均为质谱纯,磷酸二氢铵为分析纯,其余试剂均为分析纯,水为自制纯水。
2 方法与结果
2.1 溶液的制备
2.1.1 杂质K对照品溶液 精密称取头孢丙烯杂质K标准品适量,用水配制成质量浓度为0.02 mg/mL的对照品溶液。
2.1.2 供试品溶液 精密称取头孢丙烯干混悬剂100 mg,溶于水5 mL中,超声(功率:360 W,频率:40 kHz,下同)使溶解,滤过,取滤液,即得。
2.1.3 空白辅料溶液 精密称取头孢丙烯干混悬剂空白辅料1.97 g,溶于水5 mL中,超声使溶解,滤过,即得。
2.2 色谱与质谱条件
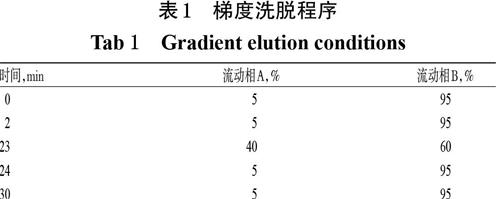
2.2.1 色谱条件 色谱柱:Thermo HyPURITYTM C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.013%甲酸水溶液(B),梯度洗脱(洗脱程序见表1);检测波长:230 nm;流速:1.0 mL/min;柱温:40 ℃;进样量:20 μL。
2.2.2 质谱条件 离子源:电喷雾离子源(ESI),正离子扫描;扫描模式:全扫描;扫描范围:质荷比(m/z)100~1 500;喷雾电压:3.8 kV;金属毛细管温度:320 ℃;鞘气压力:60 Arb;辅助气压力:10 Arb;喷雾温度:280 ℃;相对碰撞能(NCE):10、20、30。
2.3 方法学考察
2.3.1 专属性试验 精密量取“2.1”项下杂质K对照品溶液、空白辅料溶液和供试品溶液各20 μL,按“2.2”项下条件进样测定,记录色谱图。另对头孢丙烯干混悬剂进行高温(以水溶解,60 ℃水浴2 h)、酸(以0.1 mol/L盐酸溶液溶解,60 ℃水浴6 h)、碱(以0.08 mol/L氢氧化钠溶液溶解,室温静置1 h)、氧化(以1%过氧化氢溶液溶解,室温静置1 h)、光照(以水溶解,4 500 lx光照18 h)破坏后,按“2.1.2”项下方法制备成供试品溶液,再按“2.2”项下条件进样测定,记录色谱图。结果显示,空白辅料对头孢丙烯2个主峰(异构体Z、E)测定均无干扰;头孢丙烯干混懸剂经高温、酸、碱、氧化、光照破坏后也均无明显降解。色谱图见图1(图中,1~6号峰依次为头孢丙烯异构体Z、头孢丙烯异构体E、杂质K1、杂质K2、杂质K3、杂质K4,下同)。
2.3.2 检测限考察 精密称取头孢丙烯杂质K标准品适量,用流动相A配制成质量浓度为500 μg/mL的贮备液;将上述贮备液用流动相A逐级稀释,按“2.2”项下条件分别进样测定,计算能被检测出的杂质K的最低质量浓度,即为检测限。结果,当信噪比为3.1 ∶ 1时得杂质K的检测限为0.202 μg/mL。
2.3.3 精密度试验 按“2.1.2”项下方法制备供试品溶液6份,使用不同的仪器于2日内,按“2.2”项下条件进样测定,记录峰面积。结果,12次测得的峰面积的RSD为3.90%,表明本方法精密度良好。
2.3.4 重复性试验 按“2.1.2”项下方法制备供试品溶液6份,按“2.2”项下条件进样测定,记录峰面积,按外标法计算杂质K的含量。结果,含量的RSD为3.70%(n=6),表明本方法重复性良好。
2.3.5 稳定性试验 将杂质K对照品溶液分别在室温放置0、1、2、4、6、8 h时按“2.2”项下条件进样测定,记录峰面积。结果,各时间点峰面积的RSD为0.98%~1.02%(n=6)。
2.4 未知杂质的结构鉴定
2.4.1 LC-HR-MS检测 分别取杂质K对照品溶液、供试品溶液,以及供试品溶液与杂质K对照品溶液的混合溶液(混合体积比约为20 ∶ 1),按“2.2”项下条件进行LC-HR- MS测定,结果见表2~表4,LC-HR-MS图见图2~图4(图中,7~9号峰依次为杂质Z1、杂质Z2、杂质Z3,下同)。
通过对比LC-HR-MS检测结果发现,头孢丙烯杂质K对照品(4个异构体,分别命名为K1、K2、K3、K4)与供试品中4个未知杂质保留时间和准分子离子基本一致。另外,供试品中还发现了3个未知杂质,保留时间分别为17.75、18.60、19.23 min,其准分子离子基本相同,推测其互为异构体,统称为杂质Z(分别命名为Z1、Z2、Z3);再根据准分子离子,推测杂质Z可能为头孢丙烯开环乙酯。
2.4.2 LC-HR-MS/MS二级裂解检测 为进一步确认杂质K和杂质Z的结构,按“2.2”项下条件对供试品溶液进行LC-HR-MS/MS二级裂解,杂质Z1、Z2、Z3的LC-HR-MS/MS图见图5,杂质K和杂质Z1、Z2、Z3的LC-HR-MS/MS检测结果见表5,分析结果见表6。
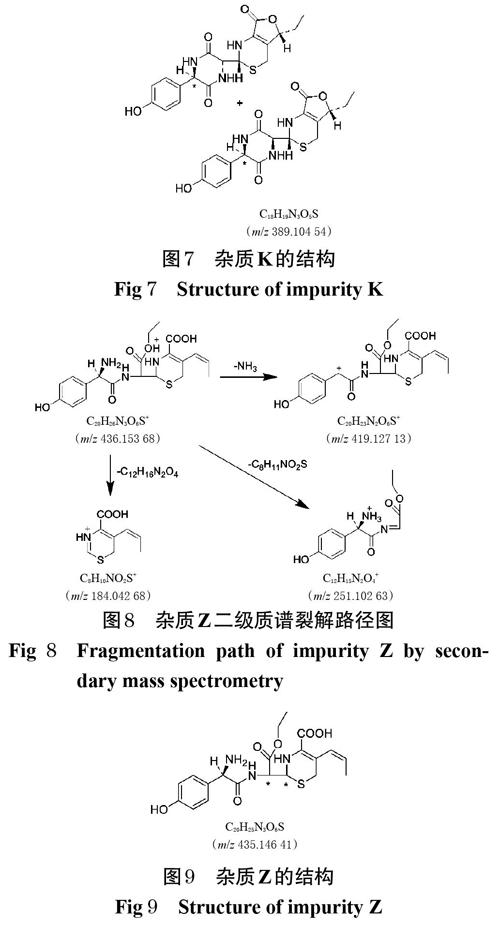
“2.2”项条件下,杂质K的二级母离子m/z约为 390[M+H]+,故其相对分子量为389,与头孢丙烯相同,提示两者可能互为异构体,推测杂质K为头孢丙烯四元环水解再与7位侧链氨基脱水合环,3位侧链双键发生水合与2位羧基脱水酯化后所得的化合物,其实测准分子离子与理论准分子离子误差小于5 ppm,结合二级质谱碎片信息,确定杂质K结构。杂质K二级质谱裂解途径见图6,结构见图7。
在“2.2”项条件下,杂质Z的二级母离子m/z约为436[M+H]+,故其相对分子量为435,与头孢丙烯分子量差46,多1个乙醇分子量,推测杂质Z为头孢丙烯四元环水解开环与乙醇发生酯化所得的化合物,其实测准分子离子与理论准分子离子误差小于5 ppm,结合二级质谱碎片信息,确定杂质Z结构。杂质Z二级质谱裂解路径见图8,结构见图9。
3 讨论
本研究以头孢丙烯杂质K为对象,采用LC-HR- MS/MS法对头孢丙烯干混悬剂中的杂质K及其附近的未知杂質进行了定性研究,并进行了方法学验证。结果显示,这些杂质为杂质Z,包含Z1、Z2、Z3,互为异构体。本文前期研究结果显示,杂质K(含K1、K2、K3、K4,互为异构体)为头孢丙烯干混悬剂在长期贮存条件下降解产生,杂质Z(含Z1、Z2、Z3)推测为头孢丙烯干混悬剂中头孢丙烯受辅料的影响,在放置过程中头孢丙烯开环并脱水所得。干混悬剂及混悬剂由于加入的辅料种类比较多,因此这一类剂型设计处方时,应充分考虑辅料与原料的相容性,了解并考察在产品的放置过程中其杂质的降解与产生过程,合理设计处方。
综上所述,本文定性研究了头孢丙烯干混悬剂中的杂质K、杂质Z,可为头孢丙烯干混悬剂生产中的杂质控制提供参考。
参考文献
[ 1 ] 余红,余蔚蔚,侯仲轲.头孢药物及中间体研发趋势及市场动 态[J].精细化工中间体,2009,39(3):7-14.
[ 2 ] 张雯,刘晓琰,董世波,等.析因设计筛选头孢丙烯干混悬剂处方[J].中国药师,2018,21(4):635-639.
[ 3 ] 邱家军,王宗利,胡琳娜,等.头孢丙烯中一个未知杂质的合成与确认[J].精细化工中间体,2016,46(1):53-56.
[ 4 ] 张明发.头孢丙烯的抗菌药理与临床[J].上海医药,2005,26(3):111-117.
[ 5 ] European Pharmacopoeia Supplement. European Pharmacopoeia:9.0[S]. 2017 edition. Strasbourg:the European Directorate for the Quality of Medicines & HealthCare of the Council of Europe,2017:1992.
[ 6 ] 陈兆坤,胡昌勤.头孢菌素类抗生素的降解机制[J].国外医药抗生素分册,2004,25(6):249-252.
[ 7 ] 国家药典委员会.中国人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:49.
[ 8 ] 李丹凤,朱健萍,卢日刚.药物杂质结构鉴定的研究进展[J].广西科学院学报,2019,35(4):1-2.
[ 9 ] 吴文杰,周伟娥,张元,等. LC-MS/MS技术在中药化学成分分析中的应用[J].时珍国医国药,2016,27(11):2735-2737.
[10] 张元元,王晨,张斗胜,等. LC-MS/MS法测定犬血浆中阿莫西林的浓度及其药动学研究[J].中国药房,2018,29(23):3193-3197.
[11] 杨大龙,孔蓉,柏植政,等.阿齐沙坦有关物质的LC-MS/MS测定与鉴定[J].药物分析杂志,2018,38(7):1231- 1237.
[12] 李瑶瑶,余飞,薛英,等. LC-MS/MS法测定曲普瑞林微球的酰化杂质[J].烟台大学学报(自然科学与工程版),2018,31(4):304-309.
[13] 孙艳文,高明珠,伍乔,等.液质联用技术在样品剖析中的应用[J].信息记录材料,2018,19(12):100-101.
(收稿日期:2019-12-10 修回日期:2020-03-20)
(编辑:邹丽娟)

