去乙酰转移酶ZmHDA101 与TPL/TPRs 蛋白的互作研究
于 璐,白 华,庞 茜,朱 岩,张 康,邢继红,董金皋
(1.河北农业大学 河北省植物生理与分子病理学重点实验室/真菌毒素与植物分子病理学实验室,河北 保定 071000; 2.河北省农药发展与应用协会,河北 石家庄 050031)
表观遗传学是近年来植物发育中的研究热点,其中组蛋白修饰调控是表观遗传学研究的重要领域之一,主要包括磷酸化(Phosphorylation)、甲基化(Methylation)、泛素化(Ubiquitylation)和乙酰化(Acetylation)等。组蛋白乙酰化是由组蛋白乙酰转移酶和去乙酰转移酶共同完成的,其中组蛋白去乙酰化是其赖氨酸残基的乙酰基被去乙酰化酶(HDACs)清除,使组蛋白恢复正电荷与带负电的DNA 紧密结合,松弛的核小体变得紧密,从而抑制了调控元件和DNA 的结合,进而抑制基因的转录。HDA19 是拟南芥组蛋白去乙酰化酶RPD3/HDA1 超家族中的一员。研究已明确,HDA19 参与调控植物生长发育、响应生物和非生物胁迫反应等过程[1]。拟南芥AtHDA19 的反义表达会增加组蛋白H4 的乙酰化水平,使转基因植株表现出早期衰老、锯齿花环、空中花环结构、开花延期等发育变态型[2-4]。AtHDA19 可通过抑制WRKY38 和WRKY62 的活性来调控PR1 的表达,参与SA 介导的植物防御反应,在植物抵抗细菌病原体侵染过程中发挥重要作用[5]。
TPL/TPRs 蛋 白(TOPLESS/TOPLESS-related proteins)是植物Grocho/Tup1 辅助抑制子家族成员,与酵母中Tup1 转录辅抑制因子同源,在多种生物途径中作为通用辅助抑制因子[10]。TPL/TPRs 蛋白可以稳定的与特异性的转录抑制因子相互作用,抑制目标基因的表达,参与植物生理过程的调控[6]。TPL/TPRs 基因家族成员通过与乙烯反应因子相关的反应抑制基序(EAR 基序)相互作用,广泛参与植物细胞周期调控、应激反应以及信号通路调节等生命进程[7]。拟南芥TPL/TPRs 有5 个家族成员,分别与TPL、TPR1、TPR2、TPR3 和TPR4,TPL/TPRs 家族成员之间存在一定的功能冗余和互补现象[8]。有研究报道,TPL/TPRs 和HDACs 一般以复合体的形式参与植物信号转导途径,共同参与调控植物的生长发育[9-10]。研究发现,AtHDA19 与TPL-1 相互作用,参与调控拟南芥茎端的正常生长[11]。APETALA(AP2)通过招募TPL 和AtHDA19 来调控花发育中花器官相关基因的表达,影响花形态的建成[12]。
本实验室前期研究发现,ZmHDA101 与AtHDA19一致性最高且保守性较好。ZmHDA101 属于RPD3/HDA1 型的,通过组蛋白修饰的序列特异性调控参与基因转录和植物生长。ZmHDA101 调控了玉米籽粒大小,是在整个发芽过程中都进行表达,对维持传递细胞特异基因在种子发育早期表达模式等植物生理发育方面十分重要[13-14]。目前,玉米ZmHDA101 与TPL/TPRs 之间的互作关系尚未见相关报道。本研究利用酵母双杂交(Yeast two-hybrid, Y2H)技术,对ZmHDA101 与TPL/TPRs 之间的互作关系进行深入研究,为阐明ZmHDA101 在玉米生长发育和抵抗生物/非生物胁迫中的功能及其调控机制奠定基础。
1 材料和方法
1.1 试验材料
酵母双杂交载体PGADT7(AD)、PGBKT7(BD),酵母转化菌株AH109、玉米自交系B73和拟南芥野生型Col-0 等,均由河北农业大学真菌毒素与植物分子病理学实验室提供和保存。
1.2 ZmHDA101 的酵母双杂交载体的构建
利用OMEGA 植物RNA 提取试剂盒,提取玉米自交系B73 的总RNA,使用TaKaRa 反转录合成试剂盒,进行玉米cDNA 的合成。利用ZmHDA101基因的特异性上、下游引物(表1),以自交系B73 的cDNA 为模板,扩增ZmHDA101 基因全长。将ZmHDA101 与入门载体pBM27 连接,构建该基因的入门载体pBM27-ZmHDA101,将测序正确的pCR8-ZmHDA101 与终载体AD、BD 进行LR 重组反应,构建ZmHDA101 基因的酵母双杂交载体ADZmHDA101、BD-ZmHDA101。
1.3 TPL/TPRs 的酵母双杂交载体的构建
利用OMEGA 植物RNA 提取试剂盒,提取拟南芥野生型Col-0 的总RNA,使用TaKaRa 反转录合成试剂盒,进行拟南芥的cDNA 的合成。利用TPL/TPRs 的特异性上、下游引物(表1),扩增TPL/TPRs 的基因序列,并将其分别与入门载体pBM27 进行连接,转化克隆测序后,获得TPL/TPRs 的入门载体pBM27-TPL/TPRs;利用LR 重组试剂盒,将pBM27-TPL/TPRs 分别与AD、BD 进行重组反应,经菌落PCR 和测序鉴定后,获得TPL/TPRs 的酵母双杂交载体AD-AtTPL、AD-AtTPR1、AD-AtTPR2、AD-AtTPR3、AD-AtTPR4 和BDAtTPL、BD-AtTPR1、BD-AtTPR2、BD-AtTPR3、BD-AtTPR4。

表1 试验中所用引物Table 1 Primers used in this study
1.4 ZmHDA101 和TPL/TPRs 的酵母自激活活性 检测
取 预 冷 的BD-ZmHDA101、BD-AtTPL、BDAtTPR1、BD-AtTPR2、BD-AtTPR3、BD-AtTPR4和空BD 载体5 μL 分别转化酵母感受态AH109,于SD/-Trp 固体培养基涂布,30 ℃下培养96 h 后,分别挑取单克隆接种于5 mL 的-Trp 液体培养基, 30 ℃ 200 r/min 震荡培养24 h,测OD600约等于0.7,稀释到OD600为0.2,分别定量点于-Trp、-Trp/-His和-Trp/-His/+x-α-gal 培养基上,30 ℃下培养48 h。根据菌落生长情况,确定ZmHDA101、TPL/TPRs的自激活活性。
1.5 ZmHDA101 与TPL/TPR 的酵母双杂交试验
按 质 粒 浓 度 比1∶1 将AD-ZmHDA101 分 别与BD-AtTPL、BD-AtTPR1、BD-AtTPR2、BDAtTPR3 和BD-AtTPR4 质 粒 混 合, 同 时 将BDZMHDA101 分 别 与AD-AtTPL、AD-AtTPR1、AD-AtTPR2、AD-AtTPR3 和AD-AtTPR4 的 质 粒混合。同时设置对照组合AD-ZmHDA101+BD、AD+BD-AtTPL、AD+BD-AtTPR1、AD+BDAtTPR2、AD+BD-AtTPR3、AD+BD-AtTPR4、BD-ZmHDA101+AD、BD+AD-AtTPL、BD+ADAtTPR1、BD+AD-AtTPR2、BD+AD-AtTPR3、BD+AD-AtTPR4 和AD+BD,将各个组合的质粒分别转化酵母感受态细胞,于-Leu/-Trp 二缺固体培养基上,30 ℃培养96 h 至长出酵母单克隆菌落,挑取单克隆置于-Leu/-Trp 二缺液体培养基内,30 ℃ 200 r/min 震荡培养至OD600为0.2 时,然后将菌液梯度稀释10 倍和100 倍,分别吸取5 µL 点于-Leu/-Trp二缺、-Leu/-Trp/-His 三缺和-Leu/-Trp/-His+3-AT 固体培养基上,30 ℃培养48 h,观察酵母生长情况。
2 结果与分析
2.1 ZmHDA101 酵母双杂交载体的构建
使用ZmHDA101 基因的特异性引物扩增获得ZmHDA101(1 554 bp)的基因片段(图1A),回收目的片段后将其与入门载体pBM27 连接,转化大肠杆菌感受态细胞,菌落PCR 鉴定获得与目的片段大小一致的单一条带(图1B),进一步测序鉴定后获得ZmHDA101 基因的入门载体pBM27-ZmHDA101。利用LR 重组试剂盒,将pBM27-ZmHDA101 分别与目标载体PGBKT7 和PGADT7进行重组反应,菌落PCR 鉴定均获得了目的条带(图1C)。经测序鉴定后获得目的载体ADZmHDA101、BD-ZmHDA101。
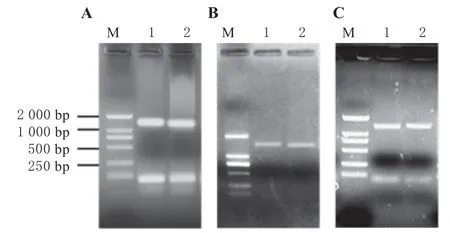
图1 ZmHDA101 基因的酵母双杂交载体构建Fig.1 Yeast two-hybrid vector construction of ZmHDA101 gene
2.2 TPL/TPRs 酵母双杂交载体的构建
利用TPL/TPRs 的特异性上下游引物扩增获得TPL/TPRs 的 目 的 片 段:AtTPL(1 032 bp)、AtTPR1(1 029 bp)、AtTPR2(1 005 bp)、AtTPR3(1 005 bp)和AtTPR4(1 032 bp),回收目的片段后分别进行克隆、测序,获得TPL/TPRs 的入门载 体AtTPL-pBM27、AtTPR1-pBM27、AtTPR2-pBM27、AtTPR3-pBM27 和AtTPR4-pBM27(图略)。将这些基因的入门载体分别与目标载体PGADT7和PGBKT7 进行LR 重组反应,菌落PCR 鉴定均获得了目的条带(图2)。经测序鉴定后获得TPL/TPRs 的酵母双杂交载体AD-AtTPL、BD-AtTPL、AD-AtTPR1、BD-AtTPR1、AD-AtTPR2、BDAtTPR2、AD-AtTPR3、BD-AtTPR3、AD-AtTPR4和BD-AtTPR4。

图2 TPL/TPRs 的的酵母双杂交载体构建Fig.2 Yeast two-hybrid vector construction of TPL/TPRs
2.3 ZmHDA101、TPL/TPRs 的自激活活性检测
对ZmHDA101、TPL/TPRs 的自激活活性进行检测,结果发现,转化了BD-ZmHDA101、BDAtTPL、BD-AtTPR1、BD-AtTPR2、BD-AtTPR3、BD-AtTPR4 和空载体BD 的酵母均能够在-Trp 培养基上生长良好,表明酵母转化成功;转化了BDAtTPR2 和BD-AtTPR4 的酵母均能够在-Trp/-His和-Trp/-His+x-α-gal 的培养基上生长良好,且在-Trp/-His+x-α-gal 的培养基上显蓝色(见图3),表明AtTPR2 和AtTPR4 具有自激活活性。

图3 ZmHDA101、TPL/TPRs 的自激活活性检测Fig.3 Self-activation activity of ZmHDA101 and TPL/TPRs
2.4 ZmHDA101 与TPL/TPRs 的酵母双杂交互作鉴定
利用酵母双杂交技术,检测ZmHDA101 与TPL/TPRs 蛋白之间的互作关系,结果发现,共同 转 化 了ZmHDA101 与TPL/TPRs 组 合(ADZmHDA101+BD-AtTPL、BD-ZmHDA101+ADAtTPL、AD-ZmHDA101+BD-AtTPR1、BDZmHDA101+AD-AtTPR1、AD-ZmHDA101+BDAtTPR2、BD-ZmHDA101+AD-AtTPR2、ADZmHDA101+BD-AtTPR3、BD-ZmHDA101+ADAtTPR3、AD-ZmHDA101+BD-AtTPR4、BDZmHDA101+AD-AtTPR4) 的 酵 母 均 能 在-Leu/-Trp、-Leu/-Trp/-His 和-Leu/-Trp/-His+3-AT 培 养基上正常生长(图4A),而转化了对照组合的酵母 不能在-Leu/-Trp/-His 或-Leu/-Trp/-His+3-AT 培养基上正常生长(图4B)。表明ZmHDA101 与AtTPL、AtTPR1、AtTPR2、AtTPR3 和AtTPR4 在酵母细胞中均能够直接互作。

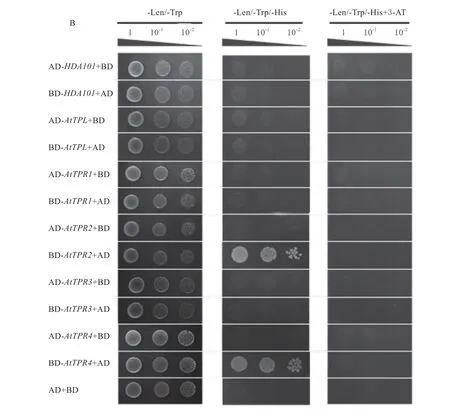
图4 ZmHDA101 与TPL/TPRs 的酵母双杂交结果Fig.4 Yeast two-hybrid results of ZmHDA101 and TPL/TPRs
3 结论与讨论
有研究报道,去乙酰转移酶在抵抗生物、非生物胁迫过程中发挥重要作用[1,5]。AtHAD6 是病原体防御反应的普遍抑制因子,在抑制和调控致病菌应答基因的表达中起着重要的作用[20]。组蛋白去乙酰化酶HDA19 参与了抑制水杨酸(SA)介导的拟南芥防御反应,AtHDA19 活性的丧失增加了SA 积累所需的一组基因的表达,通过将染色质修饰成抑制状态,可以确保防御基因的低基础表 达[15]。过表达的AtHDA19 有效地消除了WRKY38和WRKY62 的转录激活活性,组蛋白脱乙酰酶催化从组蛋白尾中去除乙酰基,并通过减少转录因子对DNA 的访问来抑制基因的转录,AtHDA19 可能通过物理作用而降低转录因子WRKY38 和WRKY62在植物细胞中的转录调节活性[16]。AtHDA19 在调控植物生长发育、对非生物胁迫的响应、对植物病原物侵染胁迫的应答等方面均有重要功能[17]。拟南芥AtHDA19 参与拟南芥的生长发育和抵抗生物、非生物胁迫过程[2-5]。已有研究发现,AtHDA19 能与TPL 蛋白互作,参与调控拟南芥茎端生长和花形态的建成[11]。玉米ZmHDA101 与AtHDA19 同源,在玉米生长发育和抵抗生物、非生物胁迫中的功能及其调控机制尚未见相关报道。本研究利用酵母双杂交技术,对ZmHDA101 与TPL/TPRs 之间的互作关系进行研究,确定了ZmHDA101 与TPL/TPRs 家族成员TPL、TPR1、TPR2、TPR3 和TPR4 均能在酵母细胞中直接互作,研究结果为阐明ZmHDA101在玉米生长发育和抵抗生物/非生物胁迫中的功能及其调控机制奠定了基础。
研究表明,植物转录辅助抑制因子TPL/TPRs蛋白在植物信号通路中发挥着中心位置作用。TPL/TPR 与生长素信号通路组分之间的相互作用,主要与含有抑制区(RD)序列的转录因子相互作用,是植物基因转录的通用抑制因子[18-19]。TPL/TPRs与HDACs 一般以复合体的形式参与到信号转导途径中,共同参与调控植物生长发育的[9-10]。水稻TPL/TPRs TPD 蛋白与核小体存在相互作用,TPD蛋白可以与组蛋白H3、H4 尾部多肽相互作用[4]。玉米ZmHDAC101 高度受到冷胁迫的诱导,与H3和H4 发生局部的去乙酰化现象[20]。本研究确定了ZmHDA101 与TPL/TPRs 之间的相互作用,推测ZmHDA101 与TPL/TPRs 形成复合体影响组蛋白H3、H4 的去乙酰化水平,抑制相关基因的表达,参与玉米生长发育以及响应生物和非生物胁迫过程。研究将进一步对ZmHDA101 调控的基因及其参与调控的植物抗病信号通路进行深入研究,为阐明ZmHDA101 在玉米生长发育和抵抗生物/非生物胁迫中的功能及其调控机制奠定基础。

