血管介入治疗移植肾动脉狭窄的疗效分析
李树欣,赵永恒,陈文忠,胡伟,周允冲,宋永琳,马寅锐,孙洵(.昆明 市第一人民医院泌尿外科,云南 昆明 650000;.昆明市第一人民医院介入科,云南 昆明 650000)
同种异体肾移植术是治疗终末期肾病的方法之一,也是目前唯一能够有效改善肾脏病患者肾功能的方法。移植肾动脉狭窄(tranplant renal artery stenosis,TRAS)是肾移植术后常见的血管并发症之一,占肾移植术后血管并发症的75%[1],可引起顽固性高血压、移植肾功能减退甚至移植肾失功,因此,早期诊断及积极有效的治疗对移植肾长期存活具有重要意义。本中心自2012 年1 月—2019 年10 月共完成同种异体肾移植术513 例,其中有9 例 患者术后出现移植肾动脉狭窄,均行血管介入治疗,现将此9 例患者临床资料进行回顾性分析,探讨血管介入治疗移植肾动脉狭窄的疗效。
1 材料和方法
1.1 研究对象:回顾性分析本中心2012 年1 月—2019 年10 月完成的513 例肾移植患者中出现TRAS 的9 例患者的临床资料,男性7 例,女性2 例,平均年龄为(33.6±6.3)岁;原发病中慢性肾小球肾炎6 例,糖尿病肾病2 例,IgA 肾病1 例;均为首次尸体供肾肾移植,其中2 例供肾为婴幼儿供肾(1 例为8 个月,1 例为3 岁),其余7 位患者均为成人供肾;1 例供肾为2 支动脉1 支静脉,其余 8 例为单支动静脉;术前供受者均血型相同,人类白细胞抗原(human leukocyte antigen,HLA)配型有0 ~3 个抗原错配,术前群体反应性抗体(panel reactive antibody,PRA)及淋巴细胞交叉配型实验(complement dependentcytotoxicity,CDC)均为阴性; 其中1 例患者手术方式为机器人辅助腹腔镜下肾移植术,其余8 例为传统开放肾移植术,9 例患者术中均采用肾动脉与髂外动脉端侧吻合。免疫诱导方案:兔抗人胸腺细胞免疫球蛋白(rabbit Antihuman thymocyte immunoglobulin,ATG)或巴利昔单抗联合甲强龙,术后免疫维持方案:他克莫司联合吗替麦考酚酯及泼尼松三联抗排斥反应方案。高血压表现者4 例,血肌酐升高表现者6 例,尿量减少表现者2 例,三种临床表现都有者3 例。
1.2 TRAS 的诊断及治疗:对肾移植术后患者出现以下一种或多种症状时怀疑TRAS:① 不明原因的高血压,且口服药物效果欠佳者;② 不明原因的肾功能减退,肌酐升高者;③ 不明原因尿量减少者。对怀疑TRAS 患者首选移植肾彩色多普勒血流显像(color doppler flow imaging,CDFI)检查,若出现狭窄处彩色血流束变细变窄,动脉收缩期峰值流速 (peak systolic velocity,PSV)>200 cm/s,叶间动脉阻力指数 (resistive index,RI)<0.55,移植肾血供不丰富者,安排行MRA 检查进一步明确病因,随后行数字减影血管造影(digital substraction angiography,DSA)检查确诊。于股动脉置入6F血管鞘,导丝引导下插入5F 直头多侧孔造影导管,于移植肾动脉吻合口处经多角度造影,显示肾动脉狭窄位置、长度及狭窄程度。根据术中情况,若狭窄程度>50%,选用合适快速交换球囊沿导丝送入狭窄处,在压力泵的作用下对狭窄段进行逐级扩张,或沿导丝置入支架,并再次造影观察狭窄段改善程度。术后患者皮下注射低分子肝素100 U/kg,12 h 一次,共3 d,并长期口服拜阿司匹林100 mg/d 或硫酸氢氯吡格雷片75 mg/d 预防血栓形成。术后监测患者血压、肌酐变化情况,并复查移植肾超声观察移植肾血流情况。
1.3 伦理学:本研究符合医学伦理学标准,得到医院伦理委员会审批(2020-01)。
1.4 统计学分析:采用IBM SPSS 20 统计软件对数据进行处理,计量资料采用均数±标准差(±s)表示,比较采用两独立样本t 检验,P <0.05 表示差异有统计学意义。
2 结 果
2.1 2012 年1 月—2019 年10 月 本 中 心 共 完 成DCD 同种异体肾移植例数513 例,其中9 例患者确诊TRAS,TRAS 发生率为1.75%(9/513),诊断时间为肾移植术后(10.6±1.3)个月。临床表现:血压升高且口服降压药效果欠佳者4 例,血肌酐缓慢爬升者6 例,尿量减少者2 例,三者症状均有者3 例,无任何临床表现者2 例。动脉狭窄部位:吻合口处5 例(55.6%,5/9),肾动脉主干局限性狭窄4 例(44.4%,4/9)。
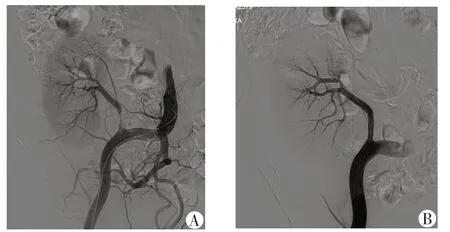
9 例患者经过CDFI 初筛,行MRA 进一步明确诊断后,均安排行DSA 检查,轻度狭窄患者(狭窄 程度0%~49%)2 例,中度狭窄患者(狭窄程度50%~74%)2 例,重度狭窄患者(狭窄程度75%~100%)5 例。行DSA 检查确诊后给予球囊扩张和(或)支架植入(图1)。9 例患者治疗均成功,其中8 例患者单纯行球囊扩张术,1 例患者行球囊扩张术后置入支架。8 例球囊扩张术的患者有3 例在术后2 个月内再次出现狭窄,随后再次给予球囊扩张均成功,二次狭窄发生率为33.3%(3/9)。随访6 个月,无再发狭窄,其中1 例患者球囊扩张术后4 个月由于肺部感染死亡,其余8 例患者均在本院门诊规律复查。治疗前患者血肌酐 为 (142.3±59.6) μmol/L, 治疗后1 周、1 个月、3 个 月、6 个月血肌酐为(133.5±57.2) μmol/L、 (131.8± 35.6) μmol/L、(127.0±29.9)μmol/L、(125.7± 37.1) μmol/L,与术前相比,无统计学差异,但较术前,治疗后肌酐有下降趋势。治疗前患者收缩压为(149.7±19.3)mmHg(1 mmHg =0.133 kPa),治疗后1 周、1 个月、3 个月、6 个月为 (131.3± 4.1)mmHg、(136.2±7.9)mmHg、(128.5±6.6)mmHg、 (127.1±3.6)mmHg,与术前相比,收缩压明显降低,具有统计学差异(P <0.05)。治疗前患者移植肾PSV 为(297.2±105.3) cm/s,治疗后1 周、1 个月、 3 个月、6 个月分别为为 (171±56.3) cm/s、(185.8± 64.8) cm/s、(197.5±69.1) cm/s、(178.8±75.4) cm/s,与术前相比,差异均具有统计学差异(P <0.05)。同时还观察治疗前,治疗后1 周、1 个月、3 个月、6 个月的叶间PSV、叶间动脉RI 等指标,与术前相比,无统计学差异,见表1。
3 讨 论
TRAS 是肾移植术后常见的血管并发症,同时也是导致移植肾功能损伤及术后顽固性高血压的重要因素之一,早期文献报道其发生率为1%~ 23%[2],但随着移植技术的日趋完善,近年来国内文献报道发病率为0.5%~9.0%[3-4],本中心的发病率为1.75%(9/513)。 TRAS 可发生于肾移植术后的任何时间,最常发生在肾移植术后3 个月~ 2 年[5],本中心9 例患者中绝大多数发生在肾移植术后6 个月内,说明其发生与手术中血管吻合技术、早期动脉内膜损伤等因素密切相关。近期研究发现TRAS 发生因素有很多,包括外科手术中血管的处理技术、DGF、排斥反应、巨细胞病毒感染、 钙调磷酸酶抑制剂的应用、扩大标准供肾及动脉粥样硬化等因素[6]。由于TRAS 临床表现不典型, 常表现为难治性高血压、血肌酐升高、尿量减少,临床上容易漏诊及误诊,最终导致移植肾丢失, 因此TRAS 的早期诊断及治疗至关重要。
彩色多普勒超声检查被列为肾移植术后常规的复查项目,具有无创、简便、廉价、动态连续性监测等特点,通过监测移植肾动脉血流参数,能够敏感的判断是否存在狭窄及狭窄的程度[7], 目前为诊断TRAS 的初步筛查手段。CT 血管造影 (CT angiography,CTA)能够更加客观、清晰的重建血管形态,直观的反映血管的狭窄部位及程度,并通过影像学的测算,明确狭窄的长度及血管内径,为后续的介入治疗提供数据支持,但缺点是需要使用碘造影剂,其肾毒性可能进一步损伤移植肾功能。磁共振血管造影(magnetic resonance angiography,MRA)同时具备了无创、无肾毒性的特点,也能够客观的反映移植肾动脉狭窄的部位及程度,缺点是价格昂贵[8]。目前DSA仍然是诊断TRAS的金标准,不仅能够确诊,同时还兼顾了治疗,但存在造影剂肾毒性及手术并发症等风险。在本中心确诊的9 例患者均为门诊彩色多普勒超声动态监测存在血流参数异常,行MRA 进一步明确诊断后,给予行DSA确诊并同时行经皮血管腔内成形术(percutaneous transluminal angioplasty,PTA)和(或)支架置入治疗,术中选用的造影剂为小分子物质的碘克沙醇,它能够透过肾小球基底膜,肾毒性较小,减少了对移植肾功能的进一步损伤[9]。
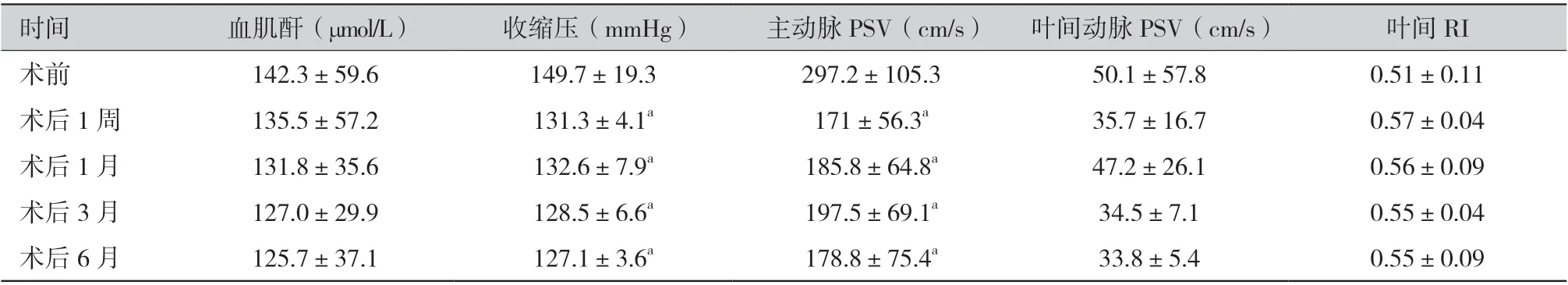
时间 血肌酐(μmol/L) 收缩压(mmHg) 主动脉PSV(cm/s) 叶间动脉PSV(cm/s) 叶间RI术前142.3±59.6149.7±19.3297.2±105.350.1±57.80.51±0.11术后1 周135.5±57.2131.3±4.1a171±56.3a35.7±16.70.57±0.04术后1 月131.8±35.6132.6±7.9a185.8±64.8a47.2±26.10.56±0.09术后3 月127.0±29.9128.5±6.6a197.5±69.1a34.5±7.10.55±0.04术后6 月125.7±37.1127.1±3.6a178.8±75.4a33.8±5.40.55±0.09
目前TRAS 的治疗方法有保守治疗(抗高血压治疗)、外科手术治疗及介入治疗,对于移植肾功能稳定,CDFI 显示狭窄并未严重影响移植肾血流动力学,如主动脉PSV<180 cm/s,阻力指数>0.75, 移植肾动脉狭窄<60%,可采取保守治疗,应用ACEI 和ARB 类药物[10],同时抗高血压治疗也常作为手术治疗后的辅助手段。外科手术治疗包括主动脉-肾动脉搭桥术、血管旁路移植术、 肾动脉内膜剥脱术等,手术难度高、成功率低, 且存在创伤大、出血、术后再狭窄等并发症[11]。目前主要用于无法行介入治疗或多次介入治疗后失败的患者。1978 年,Gruntzig 等[12]首次报道了肾动脉狭窄的经皮肾动脉成形术,自此介入治疗成为了治疗TRAS 的主要方式,具有创伤小、恢复快、效果确切及可重复治疗的优势。主要方式有PTA 和支架植入术,均可有效的解除动脉狭窄及改善移植肾功能[13]。术后再狭窄是介入治疗后的最常见问题,单纯性经皮球囊扩张术,成功率可达70%~90%,但术后再狭窄的发生率10%~33%,常发生在治疗后6 ~9 个月,可以再次行PTA 或行支架置入[14]。本组9 例患者,8 例行单纯经皮球囊扩张术,1 例行球囊扩张术+支架置入术,与治 疗前相比,治疗后患者收缩压、肌酐、主动脉PSV均有不同程度下降,效果确切,9 例患者手术均成功,治疗过程中无相关并发症。8 例单纯球囊扩张治疗的患者有3 例术后2 个月时再发狭窄,复发率为33.3%,给予再次行球囊扩张术,手术均成功,在随后随访的6 个月里9 例患者无再发狭窄,其中包括扩张术后4 个月因肺部感染死亡的患者。目前有部分学者认为经皮球囊扩张后+支架置入可明显降低术后再狭窄的发生率[15],但是另一部分学者认为支架置入虽然在一定时期内可以改善患者的临床症状,但是研究显示血管内膜可延支架的网孔增生,厚度可达1 ~1.5 mm,再次狭窄的发生率为15%[16]。本次研究由于存在样本量小、观察时间短等局限,对于TRAS 患者单纯行球囊扩张或是球囊扩张联合支架置入的长期获益问题,以及支架置入术后需长期口服抗凝药导致出血风险等问题研究还需要进一步增加样本量,延长随访时间。就本中心而言,考虑PTA 的疗效确切、可重复治疗等优点,对于TRAS 患者的初次治疗,建议PTA 作为首选,而支架置入可作为PTA 的补充治疗或PTA 治疗后再狭窄的替代方案。

