即抛型氧化石墨烯/血红蛋白传感器的制备及其对H2O2的测定
樊 璨, 裴新月, 周 亮, 黎夏彤, 舒 婷, 吴 诗, 闵 清, 王 诗*
(湖北科技学院药学院,湖北咸宁 437100)
血红蛋白(Hb)在生命活动和生物代谢过程中起着重要的作用,由于其结构明确、分布广泛,常作为研究血红素蛋白质及其它氧化还原蛋白质的直接电化学以及生物传感的理想研究对象。但Hb直接固定在电极上时,很容易吸附而导致变性失活,且其电活性中心包埋在多肽结构内部,导致电极表面的电子转移速率很低。近年来,研究者利用各种材料修饰在电极上固载Hb,用以保持Hb的生物活性并加速Hb活性中心与电极之间的电子转移,如在玻碳电极上修饰功能化多壁碳纳米管[1]、介孔氧化铝[2]、氧化镝-氧化石墨烯[3]、SnO2纳米纤维-聚苯胺[4]、碳纳米管-MnO2纳米线[5]、磁性纳米微球[6]、纳米磷酸钬[7]等材料。还有研究者尝试对其他电极进行修饰,如纳米粒修饰多晶金电极[8]、石墨烯修饰碳纤维微电极[9]、石墨烯-硫化铜纳米修饰离子液体碳糊电极[10]等。但上述这些方法多为柱状玻碳电极或其他固体电极,使用后需要重新制备或进行繁琐的预处理,不利于样品的批量及连续测定,在一定程度上限制了其应用。与上述电极不同,丝网印刷传感器以丝网印版作模具,将工作电极、辅助电极和参比电极印制在一张基材上。丝网印刷传感器可批量生产,使用前无需繁琐的预处理过程,用完即可抛弃无需再生,使电化学测定更为简单。
本研究采用丝网印刷技术制备传感器(SPE),然后将制备好的氧化石墨烯(GO)修饰于传感器表面,利用GO良好的导电性和生物相容性固载Hb,制备Hb/GO/SPE。配合实验室自制的反应池,将Hb/GO/SPE用于H2O2的测定。Hb/GO/SPE与反应池的组合在减少检测溶液体积的情况下,满足测定所需的通氮除氧需求,测定完成后Hb/GO/SPE即可抛弃,使用方便快捷。
1 实验部分
1.1 主要仪器及试剂
CHI660E电化学工作站(上海辰华);实验室用多功能丝网印刷设备(珠海凯为);Quanta 250扫描电镜(美国,FEI);UV-8000紫外分光光度计(日本,岛津);SPM-9700原子力显微镜(日本,岛津);JEM-2010FEF透射电子显微镜(日本,JEOL);XRD-6000X射线衍射(日本,岛津);JB-2磁力搅拌器(上海雷磁);KQ-100E超声波清洗器(昆山舒美)。
丝印碳油墨(ED 423SS)、银油墨(ED 427SS)、Ag/AgCl油墨(CNC-01)及绝缘油墨(ED 452SS BLUE)购于美国Acheson;PVC片材(上海新立);石墨粉(国药);猪血红蛋白(上海源叶);30% H2O2(Sigma),不同浓度H2O2溶液每次实验前都重新配制;0.1 mol/L磷酸盐缓冲溶液(PBS)由NaH2PO4和Na2HPO4配制。其他试剂均为分析纯,实验用水均为超纯水。
1.2 实验方法
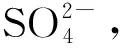
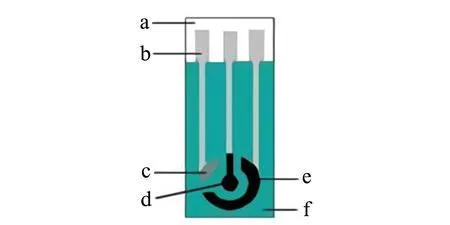
图1 丝网印刷传感器结构图Fig.1 Structure of screen printed sensora-PVC sheet;b-Ag leads;c- Ag/AgCl reference electrode;d-working electrode;e-auxiliary electrode;f-insulation layer.
1.2.2 修饰传感器的制备参考前期工作制备丝网印刷传感器(SPE)[12]:于基材表面逐层套印导电银轨、工作电极、辅助电极、Ag/AgCl参比电极,置70 ℃烘箱中烘干,最后印刷绝缘层,紫外烘干。为保证SPE的一致性及重现性,在同一批次制备和不同批次制备的SPE中分别随机抽取5片进行检验:SPE经水洗涤氮气吹干后,在5.0×10-3mol/L K3[Fe(CN)6]的溶液中进行循环伏安分析(0.5~-0.1 V,0.05 V/s)。5次循环伏安扫描所得氧化还原峰基本重合,变异系数小于5%的批次的SPE才可进行下一步实验。传感器结构见图1。
GO混悬液(50 mg/mL)由GO和水混合超声3 h制备,每次使用前超声5 min。SPE用水清洗,氮气吹干后备用。吸取5 μL的GO混悬液滴涂在SPE的工作电极表面,室温放置干燥后,再取5 μL Hb溶液(5 mg/mL)修饰于工作电极表面,在4 ℃下干燥,制得GO/Hb/SPE,于4 ℃下保存备用。用同样的方法制备GO/SPE和Hb/SPE,以作对照。
1.2.3 反应池的制备及使用反应池由上下两个模块组成,模块1由聚二甲基硅氧烷凝固态的方体和外包有环氧树脂的固化态外壳组成,其中聚二甲基硅氧方体的中间开有适应传感器反应区域的圆柱体孔洞,进气孔道满足待测溶液的通氮气需求;模块2由环氧树脂固化态组成,用于放置传感器。上下两部分的组合连接由角码和螺丝组成。

图2 自制反应池Fig.2 Laboratory-constructed cell
使用时将SPE放置于模块2的表面,然后覆盖上模块1,调整传感器的位置使其反应区域(包含工作电极、参比电极及对电极)同时处于模块1的圆柱体孔洞中;然后对准角码并使用螺丝和螺母紧密固定。最后将传感器与电化学工作站相连接,即可开始测试。在圆柱体孔洞底部的O型弹性密封圈的作用下,圆柱体孔洞可作为反应池在检测中不会出现漏液的情况。
1.2.4 电化学测定方法循环伏安法(CV)和电流-时间(i-t)响应实验在电化学工作站上进行,所有溶液在使用前通高纯氮气除氧20 min,并且在氮气氛围下进行实验。CV实验在静止体系中进行,扫描范围-1.0~0.2 V。i-t实验在搅拌体系中进行,工作电位为-0.46 V,先获得稳定的背景电流,然后再逐次加入H2O2溶液,间隔时间为50 s。
2 结果与讨论
2.1 氧化石墨烯(GO)的表征
原子力扫描电镜(AFM)图显示GO在云母片表面均呈现出均匀分散的片状结构,通过高度变化图可以计算GO的平均片层高度为1.63 nm,高于单原子层1 nm的厚度,可能是因为在干燥的过程中有少量GO片层堆叠(图3(A))。
由图3(B)的扫描电镜(SEM)图可见制备得到的GO为不规则的半透明薄片状结构,片层上可以看出有明显的褶皱。图3(C)X射线衍射(XRD)图显示,在2θ=11.3°附近出现很强的衍射峰,这与文献报道GO的衍射峰一致[13]。
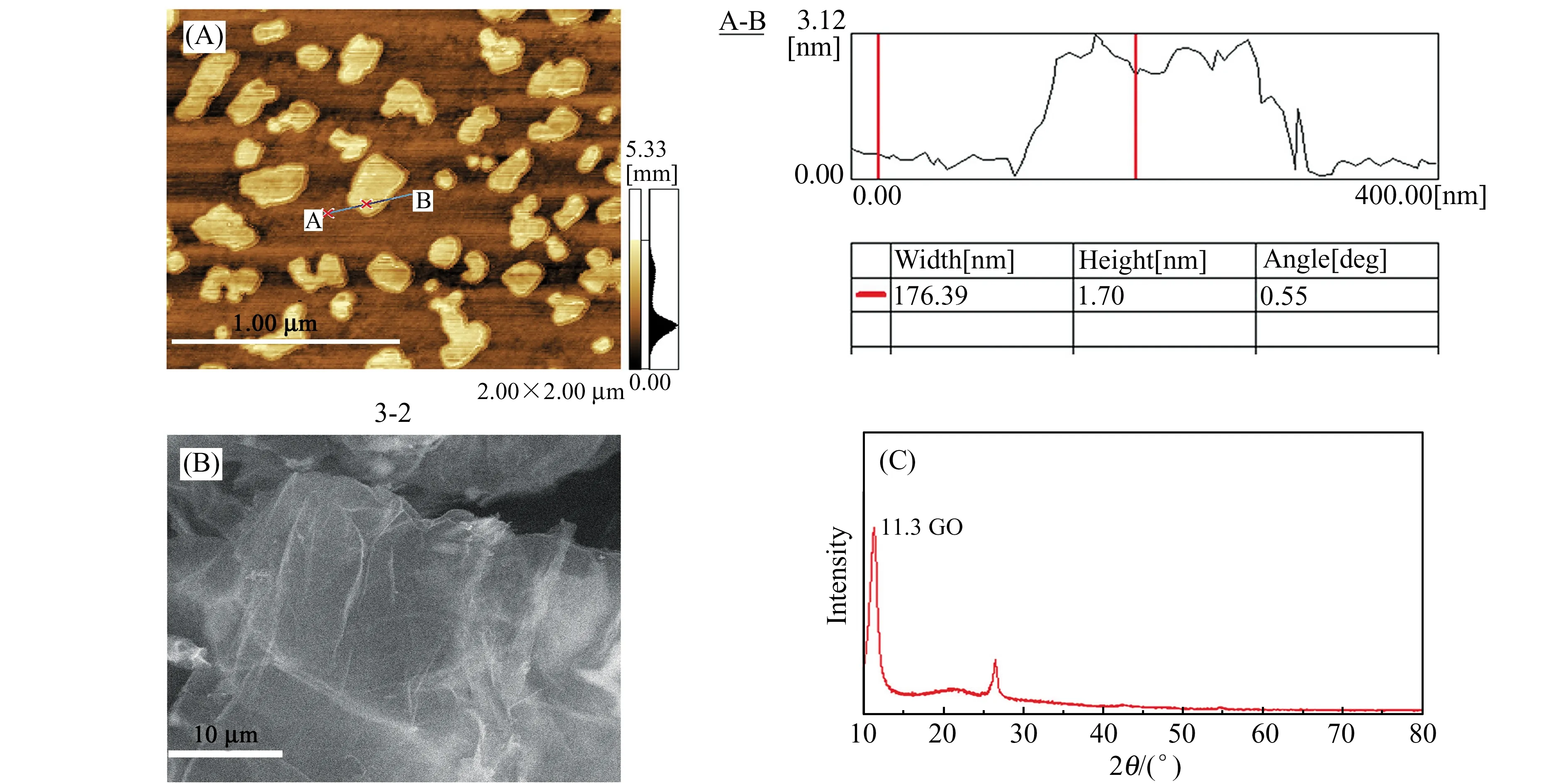
图3 GO的原子力显微镜(AFM)(A)、扫描电镜(SEM)(B)及X射线衍射(XRD)(C)图Fig.3 AFM image(A ),SEM image(B ) and XRD patterns(C) of GO
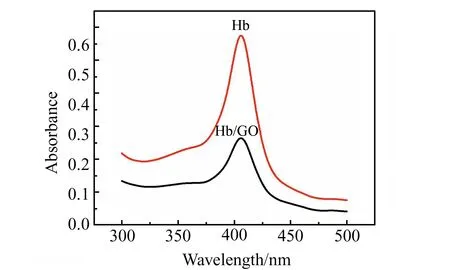
图4 Hb和Hb/GO混合液的紫外-可见(UV-Vis)吸收光谱Fig.4 UV-Vis absorption spectra of Hb and Hb/GO in water
2.2 紫外-可见吸收光谱
利用紫外-可见(UV-Vis)吸收光谱吸收带的位置和形状可以观察Hb的活性中心血红素是否变性,一旦血红素蛋白质变性Soret吸收带就会消失。如图4所示,Hb/GO混合物溶液在405 nm处有一个明显的吸收峰,与溶液中天然态Hb分子的Soret吸收带一致,表明Hb/GO混合物中的Hb仍保持其自然构象而不变性。
2.3 传感器的表征
通过SEM分别对未修饰的传感器(bare SPE)和GO修饰的传感器(GO/SPE)进行表征。未修饰的传感器工作电极表面粗糙,凹凸不平,含有大量碳墨颗粒团簇,整体结构疏松,分布不均匀(图5(A));而GO修饰的传感器的工作电极表面可以很清晰地看到GO的片层结构,使得电极表面更为平整,并增大了电极的反应表面积(图5(B))。

图5 未修饰传感器(A)和GO修饰传感器(B)的扫描电镜(SEM)图Fig.5 SEM images of the bare SPE(A) and GO modified SPE(B)
2.4 传感器的电化学特性
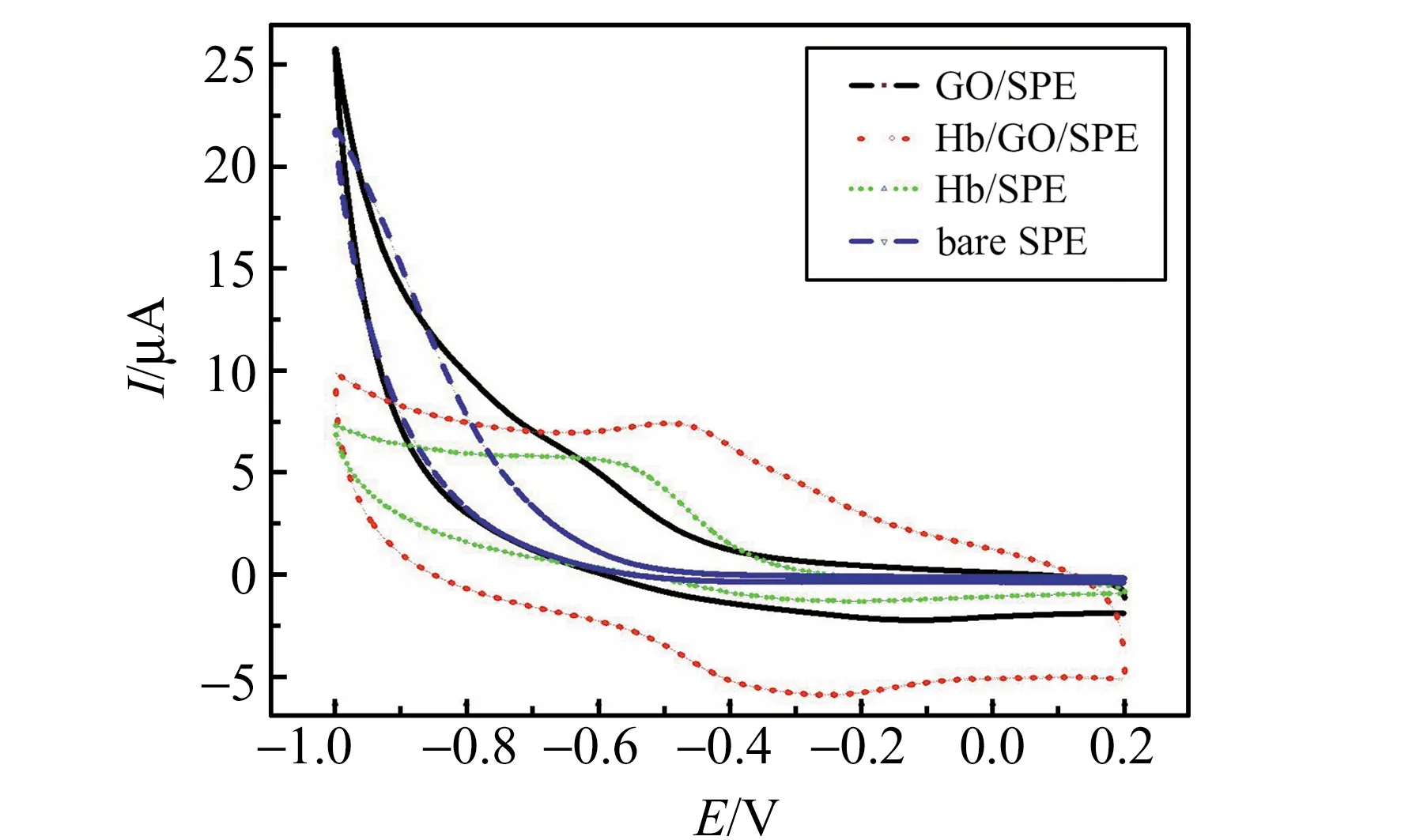
图6 未修饰传感器(bare SPE)、GO修饰传感器(GO/SPE)、Hb修饰传感器(Hb/SPE)和Hb/GO修饰传感器(Hb/GO/SPE)在0.1 mol/L PBS中的循环伏安图Fig.6 Cyclic voltammograms of bare SPE,GO/SPE,Hb/SPE and Hb/GO/SPE in 0.1 mol/L PBS solutionscan rate:100 mV/s.
不同传感器的循环伏安(CV)曲线如图6所示,在0.1 mol/L磷酸盐缓冲溶液(PBS,pH=8.0)中,GO修饰传感器(GO/SPE)与未修饰传感器(bare SPE)相比背景电流增大,说明GO具有良好的导电性,并且具有大的比表面积。血红蛋白修饰传感器(Hb/SPE)只在电位-0.58 V出现还原峰,没有对应的氧化峰。但在相同条件下,Hb/GO/SPE在-0.28 V和-0.46 V呈现出了一对氧化还原峰,对应于Hb血红素中心Fe(Ⅲ)/Fe(Ⅱ)的特征峰。与Hb/SPE相比,Hb/GO/SPE还原峰峰电位正移,峰电流更大,表明GO不但生物相容性好,能保持Hb的活性,同时具有良好的导电性,能实现并加速Hb的直接电子转移。通过公式:Q=nFAΓ*,计算得Hb在Hb/GO/SPE上的表观覆盖量(Γ*)为8.97×10-11mol/cm2,有电活性的Hb约为滴加到电极表面Hb总量(3.68×10-9mol/cm2)的2.44%,并大于血红蛋白理论单层覆盖量1.89×10-11mol/cm2[14],说明电极表面GO固载了多层Hb参加了反应。
图7显示了扫描速率对Hb/GO/SPE电化学响应的影响。随着扫描速率的增加,氧化还原峰电流也相应地增加,并且氧化还原峰电位差也在逐渐增大。扫描速率在20~300 mV/s范围内,峰电流与扫描速度成正比。说明本体系所涉及的电极过程是表面控制过程。
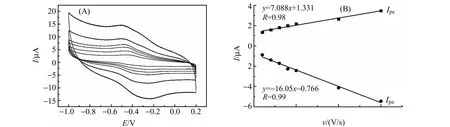
图7 (A)Hb/GO/SPE在0.1 mol/L PBS中于不同扫描速率下的循环伏安曲线(内→外:扫描速度分别为20,40,60,80,100,200,300 mV/s);(B)峰电流(Ip)与扫描速度的线性关系Fig.7 (A) Cyclic voltammograms of Hb/GO/SPE in 0.1 mol/L PBS solution at different scan rate(Inner→Outer:20,40,60,80,100,150,200,and 300 mV/s,respectively);(B) The relationships of Ip vs scan rate
通过改变PBS的pH值研究Hb/GO/SPE的电化学行为,随着pH值在6.0~10.0增加,Hb的氧化还原峰的峰形几乎不变,但其氧化峰电位和还原峰电位均发生负移,表明有质子参与了反应。当pH值为8时,峰电流最大,灵敏度最高。故选择pH值为8的0.1 mol/L PBS为测定介质。
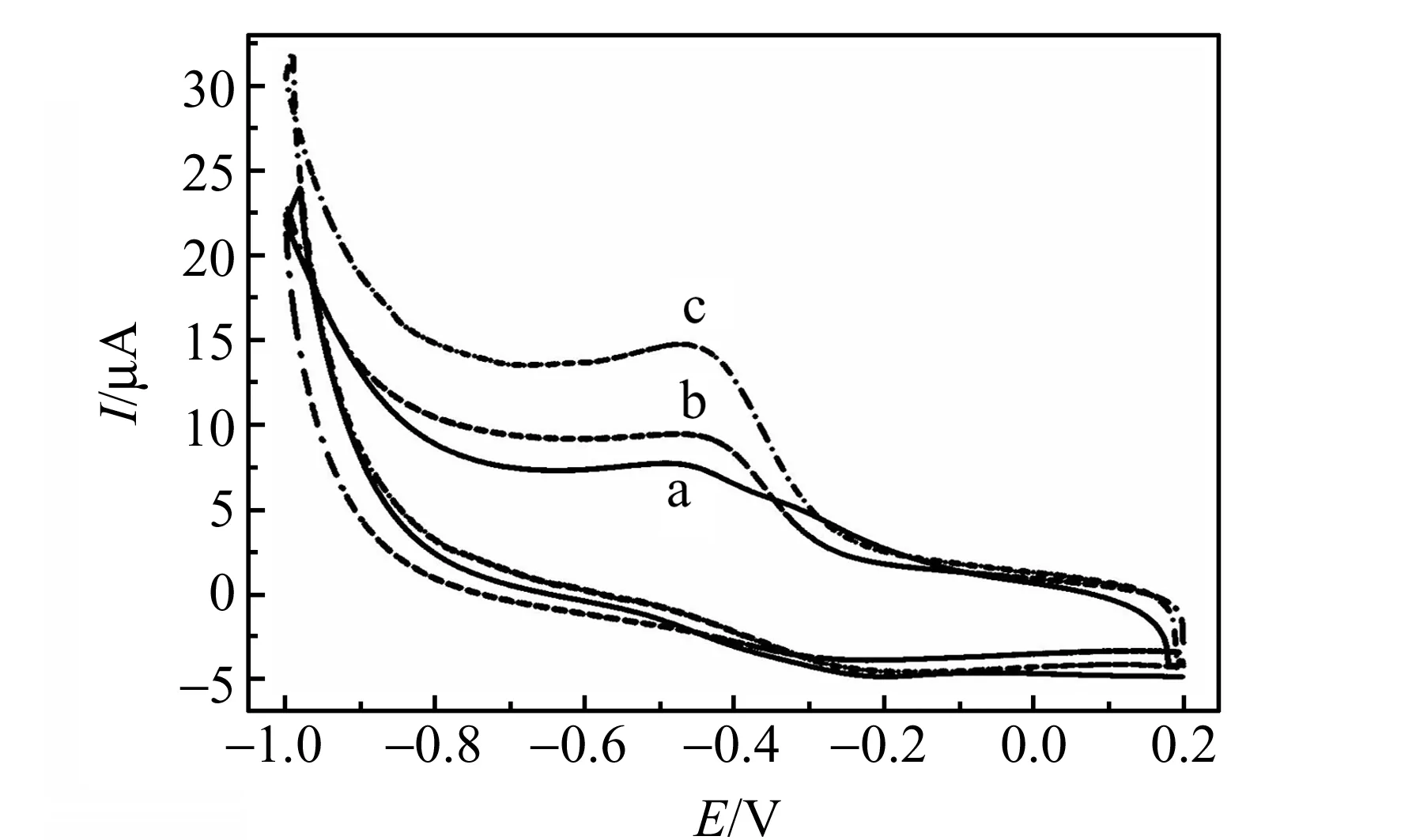
图8 Hb/GO/SPE在含有不同浓度H2O2的PBS溶液中的循环伏安图(a→c:H2O2浓度依次为0.00,6×10-6 mol/L,6×10-5 mol/L mol/L)Fig.8 Cyclic voltammograms of Hb/GO/SPE in 0.1 mol/L PBS containing different concentrations of H2O2(a→c:0.00,6×10-6 mol/L,6×10-5 mol/L)scan rate:100 mV/s.
2.5 Hb/GO/SPE对H2O2的检测
2.5.1 循环伏安行为Hb/GO/SPE对H2O2电催化还原循环伏安曲线如图8所示,向溶液中加入H2O2后,可以观察到Hb的还原峰电流电流增加,同时伴随着氧化峰电流的减小,这是典型的电催化还原H2O2的过程。
2.5.2 线性关系及检测限实验在恒定电位-0.46 V的条件下,采用电流-时间(i-t)曲线观察Hb/GO/SPE对H2O2的响应。结果表明,在6.0×10-6~2.0×10-2mol/L的浓度范围内,还原峰电流Ip与H2O2的浓度c呈线性关系,线性方程式为:Ip=0.001c(10-6mol/L)+8.702,相关系数R=0.997,检测限(S/N=3)为3.5×10-6mol/L。
2.5.3 干扰实验i-t曲线在最佳电位-0.46 V条件下,以葡萄糖、抗坏血酸、尿酸、多巴胺、Na+、K+、Ca2+、Mg2+作为H2O2检测的干扰物质进行干扰实验。固定H2O2的浓度为6.0×10-6mol/L,同等浓度的葡萄糖、Na+、K+、Ca2+、Mg2+对H2O2浓度的测定基本不产生影响。同等浓度的抗坏血酸、多巴胺和尿酸对H2O2(6.0×10-6mol/L)的检测存在一定程度的干扰,但H2O2的测定误差<5%。
2.5.4 Hb/GO/SPE的稳定性和重现性随机抽取同一批次与不同批次制备SPE进行修饰得到Hb/GO/SPE,分别测定6.0×10-6mol/L和3.0×10-4mol/L的H2O2。同一批次制备的Hb/GO/SPE的相对标准偏差(RSD,n=5)分别为4.52%和4.93%;不同批次制备的Hb/GO/SPE的RSD(n=5)分别为5.36%和6.51%。将制备好的Hb/GO/SPE置于干燥无尘的塑料袋中,4 ℃干燥保存,两周后进行测定,H2O2的测定基本不受影响(误差<5%),一个月后进行测定,H2O2的测定误差<10%,具有较好的稳定性。
3 结论
本实验合成了GO用以固定Hb,构建了Hb/GO/SPE,实现了Hb活性中心与电极之间的直接电子传递,并研究了Hb/GO/SPE对H2O2的催化作用。实验结果表明,GO具有良好的生物相容性与导电性,Hb在GO中能保持其生物活性和催化作用。
Hb/GO/SPE对H2O2的还原具有良好的电催化活性,检测范围宽、稳定性和重现性较好。Hb/GO/SPE与自制反应池的组合为传感器的构建提供了一种新的思路和方法,与常用电极相比,无需繁琐的预处理过程,使用后即可抛弃,极大提高了测定速度,且采样量少,易于制成便携式设备,有望成为一个通用型的检测平台。

