吡咯并[3,2-b]吡啶骨架构建的合成新法
范 威
(滁州城市职业学院 医学系,安徽 滁州 239000)

图1 多样的吡咯并吡啶骨架Fig.1 Diverse pyrrolopyridine skeletons

图2 含有吡咯并吡啶骨架的生物碱Fig.2 Alkaloids containing pyrrolopyridine skeleton
吡咯并吡啶骨架按照吡咯和吡啶组合形式的不同,可分为吡咯并[3,2-b]吡啶、吡咯并[3,4-b]吡啶、吡咯并[2,3-b]吡啶等6种不同的结构(图1).该类衍生物存在于ASP3627[1]、Mappicine[2]、Vemurafenib[3]等生物碱中(图2),可用作LRRK2抑制剂[4]、MPS1抑制剂[5]、JAK1抑制剂[6]、Met激酶抑制剂[7]等.该骨架的构建得到了化学工作者的持续研究.
Xu P等[8]用锰催化3-异氰基-[1,1′-联苯]-2-腈和芳基硼酸,通过自由基加成反应,构建了吡咯并[3,4-b]吡啶骨架(图3a).Zhu Y等[9]从2-氨基-3-碘吡啶和活化的炔烃出发,通过共轭加成和铜催化的分子内丙烯酸化,构建了吡咯并[2,3-b]吡啶骨架(图3b).Jarugu等[10]从(3-碘吡啶-4-基)氨基甲酸叔丁酯和((丙-2-炔-1-基氧基)甲基)苯出发,经两步反应,合成了吡咯并[3,2-c]吡啶衍生物(图3c).Westhuyzen等[11]用酰胺和吡咯-2,5-二酮反应,以三氟乙酸(TFA)为催化剂,二氯乙烷(DCE)为溶剂,回流3 d,构建了吡咯并[3,4-c]吡啶骨架(图3d).Men Y等[12]报道了甲亚胺叶立德的双环化反应,合成了高度功能化的吡咯并[2,3-c]吡啶衍生物(图3e).
在众多吡咯并吡啶骨架中,吡咯并[3,2-b]吡啶衍生物具有多样的药理活性,可用作选择性GluN2B负变构调节剂[13]、酪蛋白激酶I-Epsilon抑制剂[14]、5-HT1F受体激动剂[15]等,故备受瞩目.关于该类衍生物的合成,得到了广泛报道.
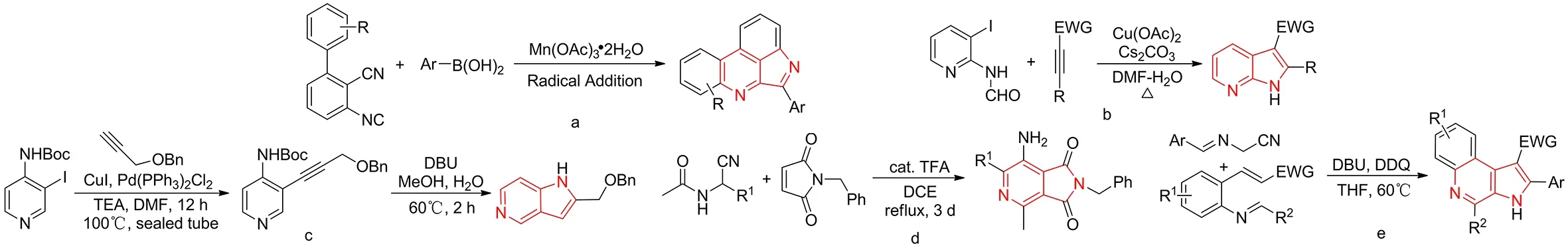
图3 吡咯并吡啶骨架的构建Fig.3 Construction of pyrrolopyridine skeleton
Xiao D等[16]在钯炭催化下,用镍(镭)加氢还原硝基,伴随着Cbz基团的消除,最终合成了吡咯并[3,2-b]吡啶衍生物.该反应的缺点是反应需要两步,不能一步完成(图4a).Lin Y等[17]用三氟化硼乙醚作催化剂,室温条件下合成了吡咯并[3,2-b]吡啶衍生物.该反应耗时8~12 h,时间太长(图4b).Liu D Y等[18]以α,γ-二氨基乙缩醛为原料,在三氯化铁催化下,构建了吡咯并[3,2-b]吡啶骨架.该反应用金属催化,后处理不便(图4c).
本研究描述了一种新型的α,β-环氧酮类化合物参与的串联反应,以α,β-环氧酮类化合物1和吡咯酮2为原料,在叔丁醇锂(t-BuOLi)促进下,高区域选择性和高立体选择性地构建了吡咯并[3,2-b]吡啶骨架3(图4d).

图4 吡咯并[3,2-b]吡啶骨架的构建Fig.4 Construction of pyrrolo[3,2-b]pyridine skeleton
1 材料与方法
1.1 材料与试剂
制备原料1[19]:以1-芳基-3-(叔丁基过氧)-3-苯基丙-1-酮为原料,奎宁衍生的硫脲为催化剂,均三甲苯为溶剂,25 ℃条件下合成了α,β-环氧酮类化合物1(图5).
制备原料2[20]:从4-羟基-1H-吡咯-2(5H)-酮和芳胺出发,以醋酸和乙醇为混合溶剂,反应1.5 h后得到了吡咯酮2(图6).

1.2 仪器与设备
熔点仪(美国SRS仪器公司),红外光谱仪(德国布鲁克公司),质谱仪(英国质谱仪器公司),核磁共振仪(德国布鲁克公司),单晶衍射仪(德国布鲁克公司).
1.3 合成化合物3的通法
在微波合成仪容器中放入α,β-环氧酮类化合物1(1.0 mmol)、吡咯酮2(1.0 mmol)、叔丁醇锂(1.0 mmol)、N,N-二甲基甲酰胺(2.0 mL).设置微波合成仪温度为60 ℃,反应充分后取出冷却.将反应物倒入水中搅拌,减压抽滤,重结晶,得到吡咯并[3,2-b]吡啶衍生物3.
1.4 表征数据
①红外光谱操作:用溴化钾(KBr)做背景,将样品和溴化钾以1∶100的比例混合,研磨均匀做成压片,放进红外光谱仪中测试.分析谱图,导出数据.②核磁共振谱操作:将样品溶入氘代试剂(DMSO-d6),装入样品管中4 cm的高度.之后将样品放入磁体,设置采样参数,经历锁场、自动调谐探头、自动匀场等过程,得到测试谱图.分析谱图,导出数据.③质谱操作:将样品用标准溶剂(50%水,50%乙腈或甲醇,0.1%甲酸)溶解,将配好的样品吸入进样器,将进样器放置于进样泵中,将进样器与离子源连接,设置基本参数.分析测试样品,得到数据.化合物3a~3f数据表征如下.
3a红外光谱:1 492,1 637,3 072,3 551 cm-1;氢谱 (400 MHz,DMSO-d6):4.43 (dd,J1=2.0 Hz,J2=2.0 Hz,1H),5.12(s,1H),5.23 (s,1H),6.41(d,J=7.2 Hz,1H),7.15~7.28(m,4H),7.36(t,J=7.6 Hz,2H),7.40 (d,J=7.2 Hz,2H),7.47~7.50(m,3H),7.68(d,J=2.0 Hz,1H),9.51(s,1H);质谱(APCI-TOF):m/z calcd for C25H17BrCl2N2NaO2548.974 8[M+Na]+;found:548.973 6.
3b红外:1 491,1 684,3 057,3 554 cm-1;氢谱 (400 MHz,DMSO-d6):4.44(dd,J1=2.0 Hz,J2=2.0 Hz,1H),5.14(s,1H),5.31(s,1H),6.41(d,J=7.2 Hz,1H),7.17~7.27(m,4H),7.35~7.37(m,2H),7.38~7.46(m,3H),7.49 (d,J=8.8 Hz,2H),7.60(d,J=6.8 Hz,1H),9.50(s,1H);质谱(APCI-TOF):m/z calcd for C25H17BrCl2N2NaO2548.974 8[M+Na]+;found:548.973 9.
3c红外:1 026,1 638,3 026,3 516 cm-1;氢谱 (400 MHz,DMSO-d6):2.28(s,3H),4.41(d,J=7.2 Hz,1H),5.00(s,1H),5.20(s,1H),6.41 (d,J=7.2 Hz,1H),7.12 (d,J=8.4 Hz,2H),7.16 (d,J=2.4 Hz,1H),7.25~7.28 (m,3H),7.32~7.44 (m,5H),7.70 (d,J=8.8 Hz,1H),9.44 (s,1H);质谱 (APCI-TOF):m/z calcd for C26H20BrClN2NaO2529.029 4 [M+Na]+;found:529.029 9.
3d红外:1 671,1 748,2 866,2 910,3 048 cm-1;氢谱 (400 MHz,DMSO-d6):4.51 (dd,J1=2.4 Hz,J2=2.0 Hz,1H),5.03(s,1H),5.16(d,J=1.2 Hz,1H),6.08(d,J=7.2 Hz,1H),7.22~7.28(m,3H),7.29~7.36 (m,7H),7.41~7.45(m,4H),9.37(s,1H);质谱(APCI-TOF):m/z calcd for C25H19FN2NaO2421.132 8[M+Na]+;found:421.131 6.
3e红外:1 675,1 741,2 878,2 918,3 045 cm-1;氢谱(400 MHz,DMSO-d6):4.52(dd,J1=2.4 Hz,J2=2.0 Hz,1H),5.03(s,1H),5.15 (d,J=1.2 Hz,1H),6.06(d,J=7.2 Hz,1H),7.17~7.25(m,3H),7.26~7.36(m,7H),7.38~7.44(m,2H),7.54~7.60(m,2H),9.38(s,1H);质谱(APCI-TOF):m/z calcd for C25H19ClN2NaO2437.103 3[M+Na]+;found:437.102 6.
3f红外:1 673,1 743,2 877,2 916,3 041 cm-1;氢谱(400 MHz,DMSO-d6):4.52(dd,J1=2.0 Hz,J2=2.0 Hz,1H),5.05(s,1H),5.14(d,J=1.6 Hz,1H),6.07(d,J=7.2 Hz,1H),7.16~7.23(m,3H),7.25~7.35(m,7H),7.38~7.44(m,2H),7.54~7.60(m,2H),9.38(s,1H);质谱(APCI-TOF):m/z calcd for C25H19BrN2NaO2481.052 8[M+Na]+;found:481.053 1.
2 结果与分析
当吡咯酮2中Ar2为对溴苯基时,叔丁醇锂(t-BuOLi)促进下,考查α,β-环氧酮类化合物1中Ar1的多样性.图7中的结果表明,α,β-环氧酮类化合物1中Ar1的取代基不影响吡咯并[3,2-b]吡啶骨架的构建.
当α,β-环氧酮类化合物1中Ar1为苯基时,叔丁醇锂(t-BuOLi)促进下,考查吡咯酮2中Ar2的多样性.吡咯酮2中Ar2由对氟苯基拓展为间氯苯基和邻溴苯基时,都能给出良好的结果(图8).

图7 拓展1中Ar1的多样性 图8 拓展2中Ar2的多样性Fig.7 Diversity of Ar1 in expansion 1 Fig.8 Diversity of Ar2 in expansion 2
3 结论
以α,β-环氧酮类化合物和吡咯酮为起始原料,在叔丁醇锂(t-BuOLi)作用下,高区域选择性和高立体选择性地构建了呋喃并[3,2-b]吡啶骨架,发展了新型的α,β-环氧酮类化合物参与的串联反应.

