非痴呆性血管性认知功能障碍的影响因素分析
刘 岩,万京桦
非痴呆性血管性认知功能障碍(vascular cognitive impairment not dementia,VCIND)是临床较为常见、被国内外学者广泛关注的一类医学现象,表现为执行功能障碍,伴行动迟缓、情感淡漠、情绪不稳等异常,对病人身心有较多不利影响,具有一定可逆性,如不加控制,50%以上病人可在5年内进展为血管性痴呆,不仅丧失临床干预价值,而且可明显增加家庭、社会负担[1-4]。受限于发病机制尚不十分明了,VCIND疗效较为有限,预防是其医学领域首选及主要推崇的应对策略[1-4]。本研究筛选VCIND的影响因素,为开展针对性防治提供参考。
1 资料与方法
1.1 一般资料 选取2015年2月—2017年10月就诊于武汉科技大学医学院的VCIND病人95例,设为观察组;同期于体检中心选取95名认知功能正常者,设为对照组。观察组,男63例,女32例;年龄62~82(73.63±5.21)岁;文化程度:文盲2例,小学5例,初中及以上88例。对照组,男63名,女32名;年龄61~84(74.04±5.54)岁;文化程度:文盲2名,小学5名,初中及以上88名。
1.2 诊断标准 VCIND诊断参照《血管性认知功能损害的专家共识》[5]中的诊断标准:①无法确诊为痴呆;②认知异常由血管引起,有斑片状认知异常、阶梯样病程、突然起病等证据;③有影像学、局灶体征、动脉粥样硬化证据;④存在血管类危险因素,仅有血管性危险因素无缺血、梗死体征者除外。
1.3 认知功能评定标准
1.3.1 蒙特利尔认知评估量表(Montreal Cognitive Assessment,MoCA)[6]从计算和定向力、抽象思维、视空间技能、语言、记忆、执行功能、注意与集中等方面评定(受教育时间≤12年则加1分),总积分30分。26~30分为正常,<26分为认知功能障碍,该量表用于初筛。
1.3.2 简明精神状态检查(Mini-Mental State Examination,MMSE)[7]共20个问题(30项),答对1项计1分,不知道或答错计0分,总积分30分。测验成绩与文化程度密切相关,文化程度初中及以上<24分、小学<20分、文盲<17分均为痴呆;<27分为认知功能障碍。该量表用于认知功能最终判定。
1.4 病例选择标准 纳入标准:观察组为VCIND病人,对照组认知功能正常者,年龄≥18岁;临床资料完整,对本研究知情并签署知情同意书。排除标准:无法按照文化程度、性别相同,年龄相近(±3岁)进行1∶1配对者或血管以外其他因素所致认知功能障碍;合并恶性肿瘤、先天畸形等严重危及生命基础疾病者,或孕妇、哺乳期妇女、意识障碍、失语等无法研究者;合并癫痫、颅内肿瘤、脑积水等疾病或近期行激素、免疫剂治疗,酗酒等可能影响检测指标者。
1.5 资料收集 通过Excel表格建立本研究数据库,采用双人双录的方式收集受试者姓名、性别、年龄、体质指数(body mass index,BMI)、文化程度、基础疾病(高血压、糖尿病、冠心病、卒中史)、烟酒史、血脂、同型半胱氨酸(homocysteine,Hcy)、血尿酸、脑白质稀疏等,之后派专人核对,数据更新后及时备份。BMI=身高/身高2(kg/m2)。高血压:已服用降压药,或者两次测量(非同日,安静1h以上)收缩压≥140mmHg(1 mmHg=0.133 kPa)和(或)舒张压≥90 mmHg。冠心病:接受冠状动脉旁路移植术,或既往心绞痛、心肌梗死病史者。糖尿病:两次以上(非同日)随机血糖≥11.1 mmol/L或空腹血糖≥7.0 mmol/L,或者需应用降糖药、胰岛素控制血糖者。卒中史:非外伤性缺血性、出血性卒中等脑不良事件。吸烟指数≥400者为有吸烟史[4]。每周至少饮酒3次,每次≥100 g(折合为白酒),每年持续时间超过6个月者为有饮酒史。采集安静半小时、空腹8 h以上外周静脉血约5 mL,离心后(3 500 r/min,15 min)将血清保存于-70 ℃的冰箱中备用。经AU5400全自动生化分析仪(美国贝克曼库尔特有限公司)检测。Hcy正常值上限为15 μmol/L,高尿酸血症(hyperuricemia,HUA)诊断标准:男性>420 μmol/L,女性>360 μmol/L;高脂血症:总胆固醇>5.72 mmol/L和(或)三酰甘油>1.70 mmol/L。脑白质稀疏诊断标准:磁共振成像(MRI)T1、T2加权像分别为低信号或等信号、高信号,CT显示低密度影。
1.6 统计学处理 应用SPSS20.0统计软件分析,χ2检验筛选VCIND的可疑影响因素,然后将是否具有VCIND设为因变量,可疑因素设为自变量,赋值后用多因素(逐步回归法,α入=0.05,α出=0.10)Logistic模型筛选影响VCIND的独立因素。以P<0.05为差异有统计学意义。
2 结 果
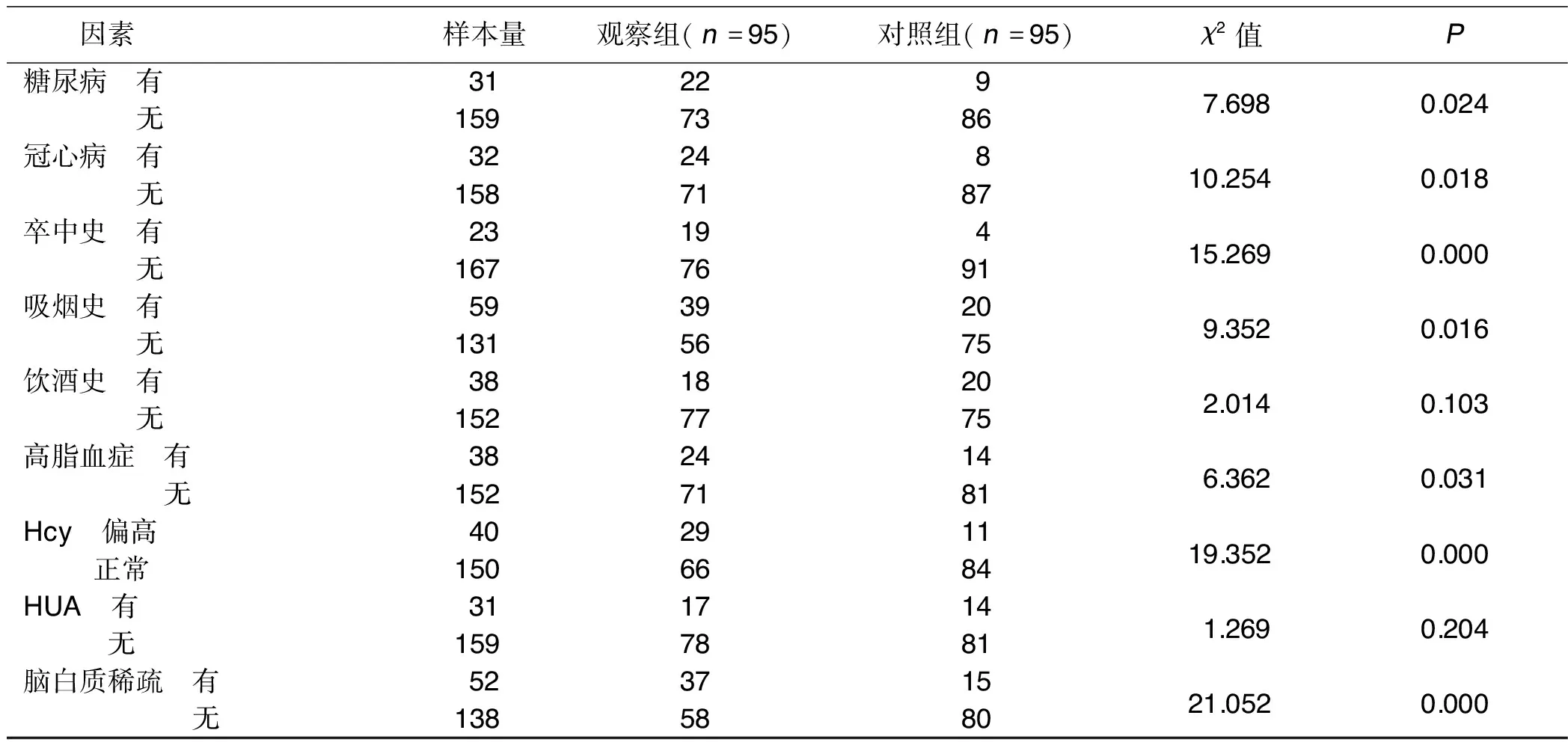
2.1 VCIND可疑影响因素筛选情况 BMI、糖尿病、冠心病、卒中史、吸烟史、高脂血症、Hcy、脑白质稀疏是VCIND的可疑影响因素(P<0.05),而高血压、饮酒史、HUA尚不能判定为VCIND的影响因素(P>0.05)。详见表1。

表1 VCIND可疑影响因素筛选情况 单位:例
(续表)
因素样本量观察组(n=95)对照组(n=95)χ2值P糖尿病 有312297.6980.024 无159 7386冠心病 有3224810.2540.018 无158 7187卒中史 有2319415.2690.000 无167 7691吸烟史 有5939209.3520.016 无131 5675饮酒史 有3818202.0140.103 无152 7775高脂血症 有3824146.3620.031 无152 7181Hcy 偏高40291119.3520.000 正常150 6684HUA 有3117141.2690.204 无159 7881脑白质稀疏 有52371521.0520.000 无138 5880
2.2 VCIND独立影响因素筛选情况 多因素Logistic回归显示,糖尿病、冠心病、卒中史、吸烟史、Hcy、脑白质稀疏是VCIND的独立影响因素(P<0.05),而BMI、高脂血症尚不能判定为VCIND的独立影响因素(P>0.05)。详见表3。

表3 VCIND独立影响因素筛选情况
3 讨 论
VCIND影响因素不单一。首先,卒中对认知功能的影响已得到共识,脑梗死时大脑动脉闭塞或狭窄,组织灌注减少,神经元兴奋性、代谢降低,当病人出现边缘皮质梗死或多发梗死灶、皮质-皮质下环路破坏、白质受损,或者累及灰质、幕下、海马与内侧颞叶、纹状体环路、前额皮质、Papez回路时,可使思维减慢、认知功能降低。另外,脑白质稀疏作为影像学术语在认知功能研究领域正逐渐得到重视,该病变主要指脑室周围深部白质受损,其发生与年龄、高血压、糖尿病、高脂血症、一氧化碳中毒等所致的脑血管异常有关。本研究中,相比于认知功能正常者,合并卒中史者发生VCIND的危险度增加了7倍,脑白质稀疏者发生VCIND的危险度增加了3倍,与既往报道[8-9]一致,临床中应加以重视。
糖尿病是VCIND重要影响因素,其干预机制主要包括[10-11]:①糖尿病又称之为糖脂症,血糖波动明显,长期高血糖一方面可使毛细血管基底膜增厚,血管腔狭窄,加之脂代谢紊乱,血黏度增高,脑血流减少;另一方面,提高血-脑脊液屏障,炎性分子、自由基因通透性提高而增加对脑细胞损害。另外,糖尿病脂代谢紊乱形成的自由基可导致剧烈氧化应激反应,减弱机体抗氧化系统功能,从而使血管平滑肌被纤维化,形成血管病变,引发脑白质缺血缺氧、脱髓鞘改变。②低血糖不仅可直接引发认知功能异常(低于3.0 mmol/L可迅速出现),而且可通过引发抑郁、焦虑、恐惧等负面情绪,影响血糖控制,反复的血糖波动可降低机体敏感性,从而使认知损害不断加重。③糖代谢异常可使糖基化终末产物大量蓄积,可通过直接细胞毒性促进神经元凋亡,与受体结合增加氧自由基含量,修饰β淀粉样蛋白和Tau蛋白,沉积于血管壁损害血管内皮等路径损害机体认知功能。④中枢胰岛素受体组成单元α、β亚基可与胰岛素样生长因子-1受体形成复合体,从而营养脑神经,胰岛素量及活性异常可直接损害脑细胞功能。⑤糖尿病病人钙离子通道兴奋性高,大量内流可阻断线粒体电子传递、激活磷脂酶、促进自由基释放。在钙离子超负荷状态,凋亡诱导因子和细胞色素C进入胞内活化Caspase-3,从而激活多聚二磷酸腺苷核糖聚合酶,增加三磷酸腺苷水解,抑制其合成,最终促进脑细胞凋亡、死亡。本研究中,高脂血症是VCIND的可疑影响因素,糖尿病者VCIND的发生风险约是无糖尿病者的3.5倍,与以上观点吻合,因此,应严格控制血糖以减轻糖尿病病人认知功能损害。
冠心病对VCIND的影响不容忽视,35%~46%冠心病病人会发生VCIND,其发生机制包括[12-14]:①冠心病病人脑小血管异常,血脑屏障功能受损,使β淀粉样蛋白沉积增多。②冠心病内皮细胞功能紊乱、血小板高度激活,后者通过与P选择素、Ⅱb/Ⅲa受体发生结合反应,进而诱发脑内血管旁炎症。③冠心病病人炎症反应活跃,胆固醇-25-羟化酶介导的免疫炎症损害脑细胞功能。另外,研究表明,冠心病与认知功能障碍多见于抑郁、焦虑、D型人格者,且ApoE4基因、KIAAl462和内皮素转换酶基因C-338A多态性与二者紧密相关[13-14]。本研究中,冠心病病人发生VCIND的危险度约是非冠心病病人的2.6倍,与以上观点相仿,故而应积极干预。
Hcy同样可导致VCIND,其可能机制包括[15-17]:①Hcy被脑细胞摄取后因缺乏排出途径而易导致大量蓄积,可使一氧化氮生物利用度、谷胱甘肽过氧化物酶活性降低,维生素E、C、A水平下降,过氧化氢、超氧化物增多,机体氧化反应增加、抗氧化力降低,脑组织氧化受损。②卒中时Hcy含量明显增加,其作为兴奋氨基酸可兴奋Ⅰ型亲代谢性谷氨酸盐受体、N-甲基-D-天冬氨酸(N-methyl-D-aspartate,NMDA)受体、甘氨酸受体,从而直接刺激被暴露的神经元,激活蛋白激酶C、提高胞内三磷酸肌醇,使胞内钙离子大量释放至胞浆,钙离子超载,从而引发对神经元的兴奋毒性效应。③Hcy浓度偏高可抑制S-腺苷高半胱氨的分解,后者可强烈抑制甲基转移酶活性,使神经组织内甲基化减慢,DNA断裂。类似的促进细胞凋亡的途径还有增加核转移因子-κB活性而提高神经元内氧化应激反应、提高非伴侣蛋白及伴侣分子表达、激活caspase-3凋亡途经等。④Hcy偏高可增加局部非对称性二甲基精氨酸含量、抑制内源性组织型血纤维蛋白溶酶激活剂活性,导致血管内皮损伤、平滑肌增殖。Hcy还可刺激单核巨噬细胞、淋巴细胞氧化应激,分泌趋化蛋白1、白介素8,使二者与血小板在血管壁聚集,与载脂蛋白形成复合物,被巨噬细胞吞噬,这既可形成血管壁活跃炎症反应,又可导致脂肪大量堆积于血管壁,促进动脉粥样硬化,损害认知功能。⑤神经元长时间暴露于高浓度Hcy中可导致海马信号、视空间能力、神经可塑性改变,锥体束细胞发生毒性反应,抑制神经传导功能。本研究中Hcy偏高者VCIND发生率是Hcy正常者的1.5倍,与以上观点并不矛盾,但通过调节Hcy代谢能否有效防治VCIND,仍需有效的临床研究进一步证实。

