锂离子电池正极材料LiVOPO4的制备及其长循环稳定性*
周小荣,李东林,张 巍,李童心,孔祥泽,王子匀,贺 欣
(长安大学 材料科学与工程学院,能源材料与器件研究所,西安710064)
0 引 言
锂离子电池具有工作电压高、能量密度大和循环寿命长等优点,成为目前便携式电子设备和电动车辆最重要的能量储存工具[1-3]。锂离子电池的性能与正极材料密切相关,层状LiCoO2在可逆性、放电容量及电压稳定性等方面综合性能好,已经被商业化,但钴资源有限,价格昂贵,对环境不友好,从而限制了其应用[4-6]。因此需要寻找其他性能优异的正极材料。橄榄石型磷酸盐基正极材料LiMPO4(M=Fe、Mn)相对于LiCoO2层状正极材料具有结构稳定、成本低廉和环境友好等优点[7-8]。LiFePO4具有170mAh/g的理论容量和3.5V左右的对锂充放电平台,用作正极材料热稳定性好,循环性能优良,但其能量密度很难满足新一代高能量电池的需要。与铁(Fe)相比,过渡金属钒(V)价态高、化学性质活泼,它既可以与锂和磷酸根等结合生成聚阴离子型化合物,也可先与氧结合,再以钒氧离子的形式与锂和磷酸根等结合[9-10]。目前研究发现,钒(V)的聚阴离子型化合物电极材料主要有LiVPO4F[11-13]、Li3V2(PO4)3[14-16]、LiVOPO4[17-22]等。研究者们发现LiVOPO4[17]理论容量(158mAh/g) 与LiFePO4(170mAh/g)相差不大,但具有更高的工作电压(3.9 V)和理论能量密度(616 Wh/Kg),有望成为锂离子电池中高压正极材料的替代品。
目前研究表明,限制LiVOPO4应用的主要问题在于其电子导电性和循环性能差,通过适当的方式改善其导电性和循环稳定性是实现LiVOPO4在锂离子电池领域应用的关键。由于(PO4)3-离子与多价钒离子可形成多种化合物,材料合成时组分难以控制,不易得到目标产物。目前制备LiVOPO4的方法主要有高温固相法[23]、化学还原法[24]、溶剂热法[25]、和溶胶凝胶法[17,26]等。Nagamine[23]等用玻璃-陶瓷法,把原料高温熔融后,再经过1 000 ℃以上的高温热处理得到β-LiVOPO4,由于在高温加热条件下,磷元素很容易挥发,难于控制材料化学组分,且P元素挥发还造成环境污染。溶胶凝胶法具有原料混合均匀、合成温度低等优点,可极大地减少磷元素的污染,易于控制材料的化学组分,提高材料纯度,是合成磷酸盐材料的有效方法[27-29]。另一方面,磷酸氧矾锂电极材料的长循环性能较差,这可能与材料合成的纯度有关,而这是该材料能否应用的关键,对其能否用实际应用任然存在着疑问。因此,需要探索新的合成方法克服上述困难,在这篇文章中,我们采用溶胶凝胶法合成了LiVOPO4正极材料,研究了合成工艺对其电化学性能的影响,所合成的LiVOPO4正极材料表现出非常稳定的长循环充放电性能。
1 实验部分
1.1 材料的制备
采用溶胶凝胶法制备LiVOPO4正极材料。按一定化学计量比将草酸加入去离子水中,室温下搅拌,溶解后加入V2O5,移至设定70 ℃水浴锅中加热搅拌,30 min后变为蓝色透明溶液,再加入LiNO3与NH4H2PO4,直至蒸干溶剂得到绿色粘稠前驱体,在100 ℃烘箱中干燥12 h,于马弗炉中300 ℃下保温4 h,研磨成均匀粉末后在500 ℃空气中热处理4 h,自然冷却,得到草绿色粉末,即为LiVOPO4。
1.2 材料的表征
采用德国的Bruker AXS D8A型X射线衍射仪对所得样品进行晶体结构分析,样品的测试条件为:Cu-Kα辐射(λ=0.15406 nm),管电流40 mA,管电压40 kV,扫描2θ角度15°~80°。用日本Hitachi S-4800型扫描电子显微镜(SEM)对样品形貌进行分析。通过Versa STAT3型号的电化学工作站,在室温下进行恒定电流充放电测试,电压范围在3.0~4.5 V。
1.3 电化学性能测试
导电碳SuperP为导电剂,聚偏二氟乙烯(PVDF)为粘结剂,N-甲基丙咯烷酮(NMP)为分散剂,将制备好的电极活性材料与导电剂(SuperP)和粘结剂(PVDF)按质量比7∶2∶1的比例混合,研磨均匀后,于密封环境下溶于分散剂(NMP)中,经搅拌均匀后涂布于铝箔上,Ar气气氛下100 ℃干燥15 h,即得到待用电极片。在充满高纯惰性气体的手套箱中进行扣式电池的组装,以金属锂片为对电极,1.0 mol/L LiPF6的碳酸乙烯酯(EC)-碳酸二甲脂(DMC)混合溶液(质量比1∶1)为电解液,聚丙烯微孔膜(Celgard2400)为隔膜,将之组装完成后移出手套箱,通过油压封装机加压密封,即得到待测扣式电池,并对其进行电化学性能测试。
2 结果与讨论
2.1 XRD分析
溶胶凝胶合成工艺的一个重要特点是原料在液相状态下达到分子级别混合,有利于降低晶相的形成温度,但是,如果溶胶凝胶合成工艺过程中不能均匀地混合原料,例如形成沉淀物,则在随后的煅烧过程中,晶相形成温度提高,对于磷酸盐材料,则不易控制P元素,易形成杂相,在实验中,先把V2O5溶解为透明溶液,再与LiNO3和NH4H2PO4混合搅拌,形成蓝色透明溶液,干燥过程中均匀反应形成物质溶胶,从前驱体透明性上看,达到了均匀混合,经热处理后,在400~500 ℃形成LiVOPO4晶相,这种低温制备的材料在本文中称为LiVOPO4-1。作为对比,采用NH4VO3作为钒源,在合成溶胶过程中,容易发生沉淀,显然,很难形成均匀溶胶和凝胶;将一定计量比的H2C2O4、NH4VO3、LiNO3及NH4H2PO4加水在80 ℃的水浴锅加热混合搅拌,蒸干溶剂得到绿色前驱体,于100 ℃烘箱干燥12 h,在600 ℃空气中退火12 h,得到目标产物,记为LiVOPO4-2;以柠檬酸、NH4VO3、LiNO3及NH4H2PO4为原料,经溶胶凝胶得到前驱体在650 ℃空气中保温6h,所得样品记为LiVOPO4-3。
图1为不同温度下制备的LiVOPO4样品的XRD图谱,测试角度从15°到80°。可看出采用溶胶凝胶法制备的LiVOPO4均具有明显的(011),(201)和(020)衍射峰,与LiVOPO4(PDF#85-2438)标准图谱对比,得到样品的衍射峰与标准衍射峰的峰位吻合,证明均合成出β-LiVOPO4相,其结构为正交晶系,属于Pnma空间群。由图可知600 ℃温度下合成的产物中含有Li2VPO6、V4O9和三斜晶系α-LiVOPO4等杂质相,650 ℃合成的材料中含有V4O9杂质相,而500 ℃下的反应产物所有的XRD衍射峰均对应于β-LiVOPO4相,没有杂质峰出现,表明该温度下的反应产物是纯相的β-LiVOPO4,我们推测LiVOPO4-2和LiVOPO4-3产生杂相原因是VO2+的存在, NH4VO3实际结构是(NH4)4V4O12,与H2C2O4反应生成络合物(NH4)2[(VO)2(C2O4)][30],VO2+在酸性介质中是一种还原剂, LiNO3加入酸性溶液中是一种氧化剂,发生氧化还原反应,少量V4+变为V5+,故而存在杂质Li2VPO6和V4O9;另一方面,LiVOPO4-2和LiVOPO4-3样品在溶胶凝胶工艺过程中发生沉淀,产生了不均匀凝胶,LiVOPO4晶体的形成温度提高,而在较高的煅烧温度下,P元素烧损增大,使V元素提供了形成钒化合物杂相的化学配比条件,与此同时,在共气氛中相对高的煅烧温度又促进V4+变为V5+,这些因素都有利于V4O9杂相的生成。与LiVOPO4-2和LiVOPO4-3相比,LiVOPO4-1在制备过程中形成了均匀透明溶胶,使得材料在分子水平上被均匀混合,较低的煅烧温度就能使LiVOPO4晶体结晶析出,得到纯相β-LiVOPO4,其氧化还原反应可通过以下途径进行:
V2O5+3H2C2O4→2VOC2O4+3H2O+2CO2↑
(1)
VOC2O4+LiNO3+NH4H2PO4→LiVOPO4+2CO↑+2NO↑+3H2O
(2)
NH4H2PO4属于正磷酸,在酸性条件下,水溶的磷酸是主要存在方式, 在261 ℃P元素开始挥发,而LiVOPO4-1热处理温度较低,在很大程度上可减少磷的挥发。
2.2 形貌分析
LiVOPO4样品形貌对锂离子电池性能有着非常重要的影响。图2为3个样品的扫描电镜图。由图2(a)、(b)、(c)可知,所有样品均由不规则的多面体组成,且存在颗粒团聚现象。从图2(d)可看出,LiVOPO4-1颗粒尺寸平均在1 μm左右,表面均匀光滑,部分颗粒存在微孔,图2(e)、(f)分别为LiVOPO4-2和LiVOPO4-3的扫描电镜图(SEM),存在很多尺寸较小的二次团聚颗粒,大颗粒尺寸达4 μm以上。可能是因为LiVOPO4-1煅烧温度较低,颗粒尺寸较小,存在微孔,这种结构有利于电解液渗透到多边形结构的内部,缩短锂离子在材料内部扩散距离,提高材料的电化学性能。
2.3 电化学性能分析
对制备的电极材料进行恒流充放电测试,测试电压范围在3.0~4.5V。图3为样品在10 mA/g电流密度下的首次充放电曲线。可看出LiVOPO4-1、LiVOPO4-2、LiVOPO4-3的首次放电比容量分别为129.2、 117.8、90.7 mAh/g,充放电平台在3.9 V左右。充电过程中,电压逐渐上升至3.9V,LiVOPO4中的Li+脱出,相应的V4+被氧化成V5+。LiVOPO4-1的首圈放电比容量明显高于其他温度所制备的电极材料,进一步研究其CV特性,图4为LiVOPO4-1材料的循环伏安(CV)特性曲线,分别测0.05、0.1、0.2、0.3、0.4、0.5 mV/s扫描速率下CV曲线,介于3.0 V和4.5 V之间。其中Li的嵌入与脱出是以V4+/V5+的变价实现电荷平衡。从图中可明显观察到,峰值电流随扫描速率的增加而增加,氧化峰转移到更高的电位,相应的还原峰电位降低,从而导致极化强度增加。图5为 LiVOPO4-1材料在0.2 mV/s扫描速率下的循环伏安图(CV),材料循环两周后曲线的重叠性较好,还原峰与氧化峰的面积相差不大,表明材料的脱锂/嵌锂的可逆性良好,内部结构较为稳定,氧化还原电位一致,故具有良好的循环可逆性。
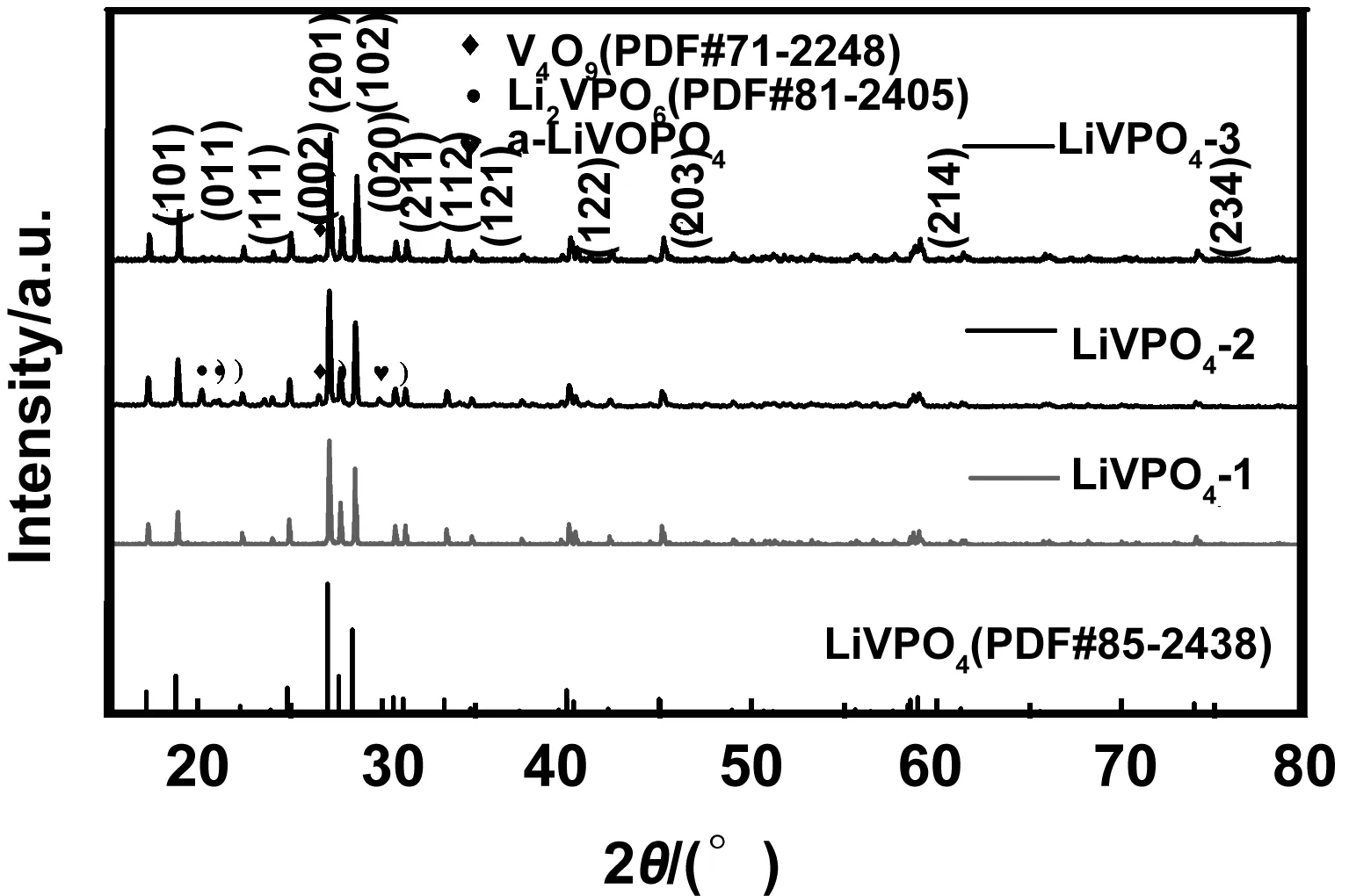
图1 LiVOPO4正极材料的XRD衍射图谱Fig 1 XRD patterns of LiVOPO4 and LiVOPO4-1/2/3

图2 (a)、(d)为LiVOPO4-1的SEM图,(b)、(e)为 LiVOPO4-2的SEM图,(c)、(f) 为LiVOPO4-3的SEM图Fig 2 SEM images of LiVOPO4-1(a,d), LiVOPO4-2(b,e) and LiVOPO4-1(c,f)

图3 LiVOPO4-1, LiVOPO4-2,and LiVOPO4-3 首圈充放电曲线Fig 3 Initial charge-discharge curves of LiVOPO4-1, LiVOPO4-2 and LiVOPO4-3 samples

图4 LiVOPO4-1循环伏安Fig 4 Cyclic voltammograms of LiVOPO4-1
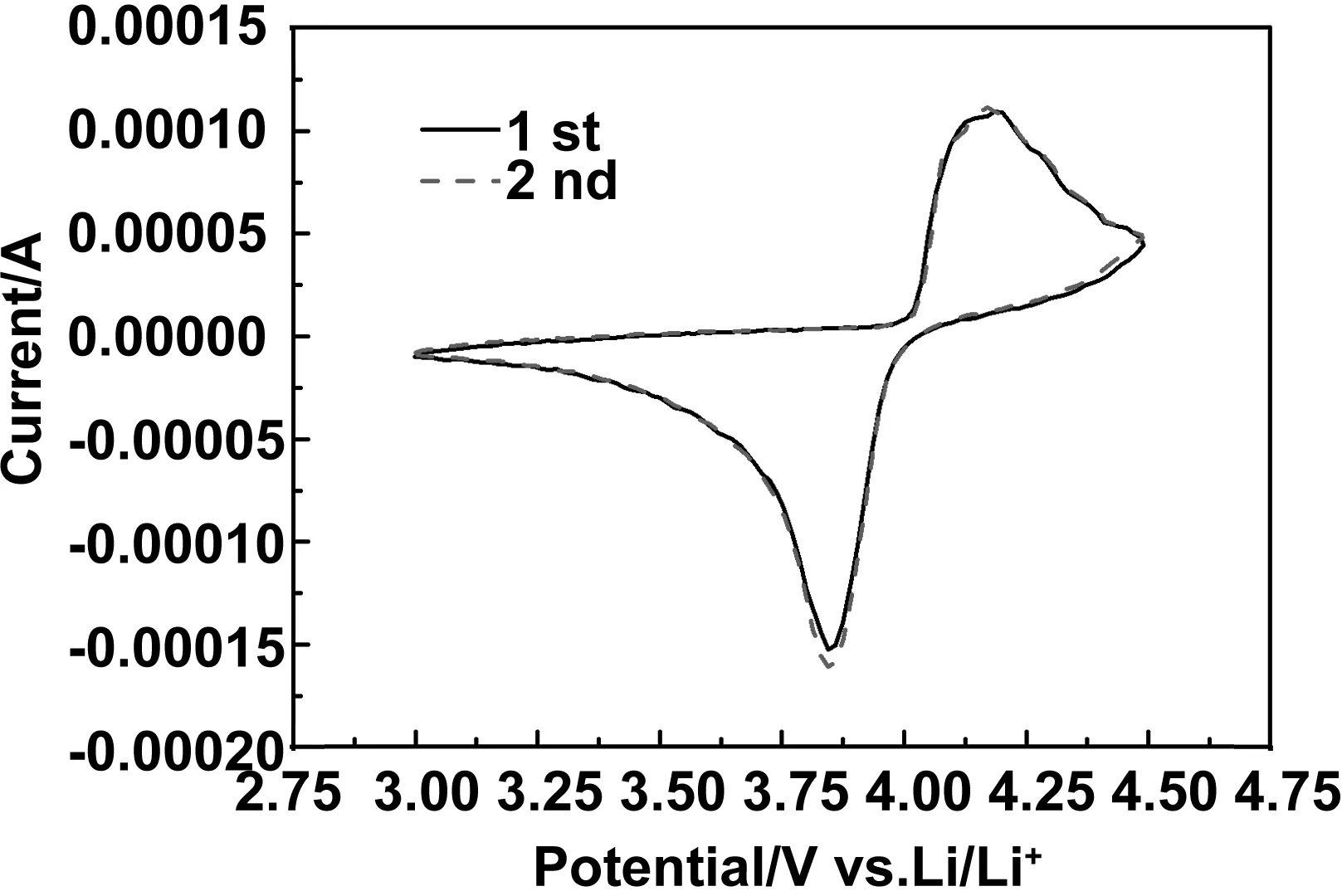
图5 LiVOPO4-1不同圈数循环伏安曲线图Fig 5 Cyclic voltammograms of LiVOPO4-1 after different cycles
图6为样品在20 mA/g的电流密度下循环300次的循环次数与放电比容量关系图, LVOPO4-1循环300次后,放电比容量无任何衰减,LiVOPO4-2在相同的循环条件下放电比容量保持率只有73.7%, LiVOPO4-3的比容量保持率虽为100%,但其初始放电比容量相比LiVOPO4-1要低38.5mAh/g。导致LiVOPO4-2的循环性差和LiVOPO4-3容量低的原因可能是由于V4O9及Li2VPO6杂相的生成,且存在尺寸较小的二次团聚颗粒,阻碍了电解液的渗透;LiVOPO4-1材料颗粒尺寸小,缩短了Li+嵌入和脱嵌过程中离子扩散路径,有利于载流子的传输,部分微孔的存在利于锂离子扩散进材料内部,提高材料的电化学性能。图7为LiVOPO4-1在10 mA/g电流密度下不同循环中的充放电曲线。循环300次后比容量和平台无任何衰减,比容量维持在150 mAh/g 以上 ,可能是因为合成的相纯,且存在微孔;为了验证高倍率下材料的循环性能,在100 mA/g电流密度下对 LiVOPO4-1进行循环性能测试,如图8所示。经1 000次充放电循环后放电比容量保持率达100%;。这些结果说明LiVOPO4-1不管在20 mA/g还是100 mA/g的电流密度下都具有良好的电化学循环稳定性。
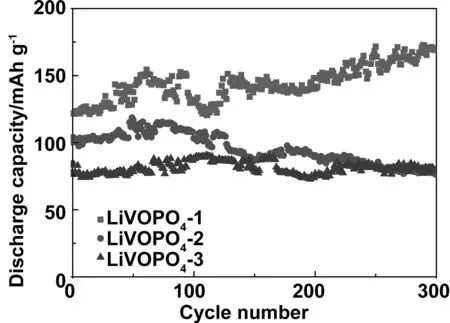
图6 LiVOPO4-1,LiVOPO4-2,and LiVOPO4-3循环性能图Fig 6 Cycle performance of LiVOPO4-1, LiVOPO4-2 and LiVOPO4-3

图7 LiVOPO4-1在不同循环中的充放电曲线Fig 7 Charge-discharge profiles of LiVOPO4-1
SHEN C[31]等以溶胶-凝胶法制备出β- LiVOPO4,在24和160 mA/g下,初始放电比容量分别为116和73.6 mAh/g,且放电比容量随循环次数的增加而衰减,循环30次后比容量保持率分别为96.7% 和73.6%,而LiVOPO4-1在20 mA/g下循环300次比容量不衰减,在100 mA/g下循环1 000次放电比容量保持率达100%,都表现出优秀的循环稳定性。我们推测可能是因为LiVOPO4-1采用溶胶凝胶法使材料在分子水平上混合均匀,热处理温度低,合成的相纯,故具有非常稳定的结构和良好的可逆电极反应特性。
3 结 论
采用溶胶-凝胶法制备出的LiVOPO4正极材料,由于控制了均匀透明溶胶的形成过程,产生均质凝胶,可有效地降低形成LiVOPO4-1晶相的热处理温度,在500 ℃形成了结晶完好的纯LiVOPO4晶相,与有杂相的LiVOPO4相比,纯LiVOPO4材料具有高的比容量和稳定的长循环性能,在10 mA/g的电流密度下循环300 次,其放电比容量无衰减,维持在150 mAh/g以上,且在100mA/g的电流密度下循环1000圈比容量保持率为100%。

