一道高考实验题的赏析与研究
徐明奎

摘要:2018年北京高考理科综合第12题以考查学生化学核心素养申的“证据推理”和“科学探究”为主旨,具有情境选取贴近课堂、题干呈现新颖精炼、立意关注学科素养和功能导向课程改革的特点。通过对“牺牲阳极的阴极保护法”的研究,证实在一定条件下,以Zn为阳极,Fe片可以被氧化,Zn对Fe存在不完全保护现象。
关键词:牺牲阳极的阴极保护法,核心素养,试题研究
文章编号:1008-0546(2020)05-0080-03 中图分类号:G632.41 文献标识码:B
doi:10.3969/j.issn.1008-0546.2020.05.021
高考化学试题由学科专家精心命制和打磨而成,新课程改革后的高考化学试题在题型总体保持稳定的基础上,突出了对于化学学科核心素养的考查,一些具有创新性和示范性的高考试题值得我们深入学习和研究。本文所要赏析和研究的是2018年北京高考理科综合第12题。
一、原题呈现
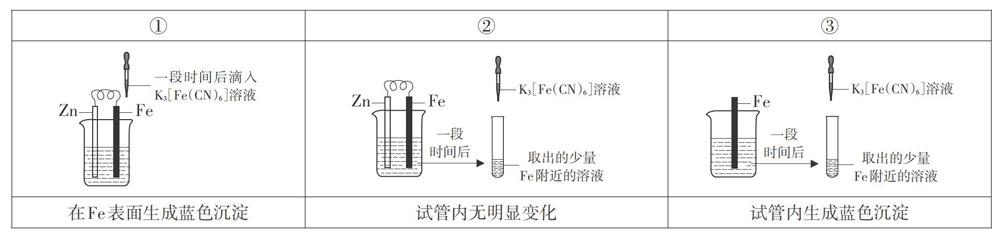
验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)
下列说法不正确的是
A.对比②③,可以判定Zn保护了Fe
B.对比①②,K3[Fe(CN)6]可能将Fe氧化
C.验证Zn保护Fe时不能用①的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
二、试题赏析
1.情境选取贴近课堂
情境是试题命制的载体,情境的真实性是试题科学性的保证。高考试题一直坚持以真实的工业生产、科学研究、化学实验等为情境,这对培养学生应用所学知识分析解决实际问题的能力和认识化学学习的意义具有重要作用。与大多数试题情境虽然真实,但离学生的课堂学习太远不同,本题的情境源自真实的课堂实验,是人教版教材选修4《金属的腐蚀与防护》一节中一个科学探究实验。除缺少电压表外,试题实验中所用试剂和装置与教材相同。试题所展示的实验过程和结果并不是课堂实验的原景再现,而是一次课堂实验的“异常”及后续探究。如果课堂中没有做过该实验,仅是理论分析,学生能得出的实验现象是“溶液中没有蓝色沉淀生成”,因为锌比铁活泼,电子由锌流向铁,可以防止铁被腐蚀。高考试题命制时选取值得探究的教材实验作为情境,能引导教师重视实验教学,能为学生课堂上进行真实的实验探究提供表现机会。
2.题干呈现新颖精炼
试题中包含的实验情境有“课本实验操作时出现异常现象”“对异常现象发生原因的探究”,如果用文字方式来描述实验情境,再用普通实验探究题的格式来命制本道试题,试题题干必将包含大量的文字阅读信息,与一般选择题的体量不符。命题者创造性的用三幅图示的形式完整地表示了实验探究的全过程,还特别引导学生注意加入K3[Fe(CN)6]的位置这一细节,图示的形式不仅丰富了化学试卷的呈现形式,还把信息呈现由抽象间接变为了形象直接,非常有利于学生快速提取和分析信息。刘芳等认为:“对于学生而言,仅从大段的文字中提取有效信息是相对困难的,适当配以图或表反而有利于学生更好地理解题意。
3.立意關注学科素养
作为一道实验探究题,试题立意重在考查学生化学核心素养中的“证据推理”和“科学探究”,作为一道“非典型”形式的实验探究题,学生需要具备“科学探究”素养中的“水平4”才能完全理解试题中三幅图在探究过程中的顺序和作用。第一幅图展示了课本实验“验证牺牲阳极的阴极保护法”的实验过程和现象,预期的现象是“Fe片表面没有蓝色沉淀生成”,而“异常”现象是在Fe表面生成蓝色沉淀。因为蓝色沉淀的产生需要有Fe2+,由此引发两个猜想:猜想1是“Fe片被H+或O2氧化生成Fe2+”;猜想2是“Fe片被K3[Fe(CN)6]氧化生成Fe2+”。作出“猜想2”的依据是K3[Fe(CN)6]中F。元素的化合价是+3价,可能将0价Fe氧化到+2价。为验证“猜想1”是否成立,设计第二幅图所示实验,根据现象可知,Fe片未被H+或O2氧化。由此得出试题中的结论“对比①②,K3[F3(CN)6]可能将Fe氧化”。第二幅图所示实验还有一个作用,就是说明Zn对Fe片有保护作用,因为如果没有Z。片,Fe片会被H+或O2氧化,为验证这一作用的存在,补充进行了第三幅图所示实验。命题者还利用选项C和D考查了学生“科学探究”素养中实验方案设计的水平,要求学生能对实验方案的科学性作出判断。
4.功能导向课程改革
化学实验是认识和学习化学的重要方法,实验探究是学生综合运用所学化学知识和技能、分析问题、设计方案、解决问题的实践活动,是化学学科核心素养的构成要素之一。核心素养的培养不仅需要在课堂教学中持续关注,也需要在考试中进行有效评价。《普通高中化学课程标准(2017年版)》在“学业水平考试命题建议”中提出如图1所示的命题框架:
赏析本题不难发现,试题命制时遵循了课程标准的命题框架,以真实的“验证牺牲阳极的阴极保护法”的实验情境为测试载体,以探究和解释实验中的异常现象为测试任务,以考查学生的证据推理与科学探究素养为测试宗旨。这样的命题必然导向高中的化学学科教学应符合课程标准的教学建议:“充分认识化学实验的独特价值,精心设计实验探究活动”和“创设真实问题情境,促进学习方式的转变”。
三、试题研究
1.提出问题
在赏析本题之余,笔者对于命题和实验产生一些疑问:
疑问1:试题所选情境为教材实验,探究的是实验中的“异常”,作为已经使用10多年的高中化学教材,以该实验为背景的试题情境选取是否会因为学生过于熟悉而使试题的效度不大?
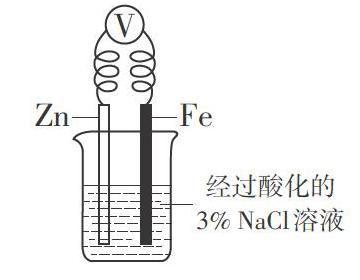
疑问2:教材中所示实验装置如图2所示,而试题中的实验装置不含电压表,电压表的省去是否是命题者有意为之,目的是什么?
疑问3:试题情境中的“异常”现象,是否已经有老师进行过研究?
疑问4:试题的实验探究是通过证明“Fe片被H+或O2氧化”不成立,从而间接证明“Fe片被K3[Fe(CN)6]氧化”成立。K3[Fe(CN)6]能氧化Fe,选择题中给出的结论是可能,如能直接氧化,为什么Zn片能保护Fe片不在酸化的3%NaCl溶液中被氧化,而不能保护Fe片被K3[Fe(CN)6]氧化?
疑问5:该实验中Zn片对Fe有没有保护作用,如果有,如何证明?
2.命题揣摩
对于疑问1和疑问2,因为无法与命题者直接交流,所以只能借助于调查和分析来揣摩命题者的想法。筆者对本地区的高中进行了调研,发现老师们在授课时没有进行该实验,都是引导学生进行了理论分析。没有进行该实验的原因是认为学生已经学习了电化学的相关知识,实验现象可以根据理论推导得出。从调研中还了解到,老师也不知道该实验现象会存在“异常”,没有进行过实验验证和探究。因此试题以该实验情境为背景来命制,情境具有陌生度,能考查学生真实的科学探究素养水平。
对于疑问2,因为实验指向的结论之一是“验证Zn保护Fe时不能用①的方法”,如装置中使用了电压表或电流表,则均可证明实验时有电子从Zn片流向了Fe片,电子的流向可以证明Zn片对Fe片具有保护作用,这与本题期待得到的结论相矛盾,猜想命题者在命题时将电压表舍去,以免引起争议。
3.已有研究
通过知网查询,有三位老师的研究与本题情境相关。朱正德用图3所示的实验装置研究发现:电压表指针偏转,往Fe电极附近滴人K3[Fe(CN)6]溶液,溶液变蓝色。朱正德认为是由于铁片含有杂质,在酸性条件下发生原电池反应有Fe2+生成所致。
杨颐钢用教材所示实验装置进行实验,研究发现,电压表所示指数随溶液酸性增强而逐渐增大,当使用高纯铁片,不会出现蓝色沉淀,使用普通铁片时,在pH=1-3时有蓝色沉淀,pH=4-6时,无明显蓝色沉淀。杨颐钢认为Fe片纯度高时,溶液的pH对实验无影响,溶液的pH低时,Fe片的纯度会影响实验。
房寿高通过理论分析和实验探究,结果均表明,K3[Fe(CN)6)溶液能将Fe氧化,生成蓝色的Fe3[Fe(CN)6]2沉淀。同时提出加入NaCl溶液能破坏Fe片表面的氧化膜,有利于Fe片的氧化。
综合上述研究,朱正德和杨颐钢认为蓝色沉淀是Fe片在酸性条件下先被H+氧化为Fe2+,后Fe2+与[Fe(CN)6]3-反应生成蓝色沉淀。而蓝色沉淀是否存在于铁片表面、以及蓝色沉淀的产生是否是K3[Fe(CN)6]将Fe氧化后所致,两位老师因未能考虑到K3[Fe(CN)6]的氧化性,所以研究未涉及。
4.实验研究
为验证试题中的实验现象及探究Zn片对Fe片是否有保护作用,笔者进行了下列实验:
实验1:连接如试题所示的装置①,其中酸化后3%NaCl溶液的pH约为2。1分钟后,在Fe片附近滴加K3[Fe(CN)6]溶液,可以观察到Fe片的边缘、划痕处出现明显的蓝色物质,蓝色物质逐渐扩散到溶液中,但蓝色物质总量不多。
实验2:连接如试题所示的装置①,其中酸化后3%NaCl溶液的pH约为1。10分钟后,在Fe片附近滴加K3[Fe(CN)6]溶液,可以观察到Fe片附近出现明显的蓝色物质。
实验3:将实验1中的Zn片从溶液中取出,Fe片表面立即有较多新的蓝色物质出现。
根据已有研究和实验1、2,可以得出结论:在3%NaCI溶液的环境中,当溶液酸性较弱时,蓝色沉淀产生于Fe片的表面,Fe2+主要来自于K3[Fe(CN)6]溶液对Fe片的氧化;当溶液酸性较强时,溶液中的H+和K3[Fe(CN)6]均能氧化Fe片。
在不使用电流表的情况下,根据实验1、3的现象对比,可以证明Zn片对Fe存在一定的保护作用,因为当将Zn片从溶液中取出,Fe片表面立刻新生成更多的蓝色物质。这一结论对“牺牲阳极的阴极保护法”的教学和实验均具有重要的意义,因为多数教师和学生均认为,只要铁与更活泼的金属相连,或铁与直流电源的负极相连,那么在电解质溶液中,铁片一定不会被腐蚀。查阅资料发现,利用电化学法保护金属不被腐蚀,金属必须达到它的最小保护电位,最小保护电位即金属达到完全保护时所需要的最低电位值。而最小保护电位值与金属的种类、腐蚀介质的条件(成分、浓度、温度等)因素相关,如果达不到最小保护电位值,金属是不能完全被保护的。本实验中,当溶液酸性过强或有K3[Fe(CN)6]存在时,Fe片达不到它的最小保护电位而被氧化。日常生活中,我们经常能发现镀锌铁管在镀层并没有完全被腐蚀的情况下,铁管局部有生锈现象,这也说明在一定的环境中,Zn不能起到完全保护的作用。
四、研究启示
在教学中,对于陌生的实验情境,我们有时会不经过实验就推导出“理想”的实验现象,或者在实验出现“异常”现象时,不经过研究就给出可能的原因,这些做法都不利于学生化学核心素养的培养。而要改变这一现状,需要教学和评价两个方面都能重视实验,尤其是贴近学生学习实际的实验。倪娟认为:真实性的试题可以纠正学生所学不科学、不完整的化学知识,教学如能围绕学生的实验、学生的研究性学习等真实的学习过程,是能增加学生对化学的学习兴趣的。
我们要培养学生科学探究的核心素养,就应该在课堂中多创设科学探究的机会。我们要培养学生科学精神的核心素养,则自己首先就要具备科学精神。

