2种术后进食方案在上消化道内镜黏膜下剥离术患者的应用效果观察
刘梅娟,周丽华,唐美云,谭文欣,刘玉萍,程凤平
(南方医科大学南方医院 消化内科,广东 广州510515)
内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)是治疗消化道隆起性病变的一种微创手术,疗效与外科手术相当,已成为消化道早癌及癌前病变的首选治疗方法[1]。快速康复理念(enhanced recovery after surgery,ERAS) 在上消化道内镜黏膜下剥离术后的应用措施主要包括:早期经口进食、早期下床活动。 快速康复理念早期经口进食已经在腹腔镜胆囊切除术、腹腔镜胃癌根治术、结肠癌手术、肝癌手术等普外科手术及喉全切除术中得到应用[2-7];在消化内镜下治疗肝硬化食管胃底静脉曲张、 早期食管癌和肠息肉中也有一些报道[8-10],取得满意效果。文献研究表明:内镜黏膜下剥离术后早期进食加速和改善患者伤口愈合,减轻患者痛苦,加速患者术后的康复,早期进食并不增加并发症发生率,反而对于狭窄的发生率有所降低[11]。 鉴于此,我院从2017年12 月—2019 年10 月,开展了内镜黏膜下剥离术后早期经口进食和术后常规饮食护理的临床对照研究,观察术后早期经口进食的效果及安全性,取得了满意效果,报道如下。
1 对象
2017 年12 月—2019 年10 月,纳入在本医院消化内镜中心行上消化道内镜黏膜下剥离术患者。 纳入标准:(1)自愿入组,沟通无障碍;(2)经超声内镜检查或相关影像学检查无器官及淋巴结转移;(3)无凝血功能异常;(4)围术期未行抗血小板、抗凝治疗;(5)无严重心、肝、肺、肾等脏器功能障碍;(6)内镜黏膜下剥离术手术时间<100 min。 排除标准:(1)术中穿孔;(2)术后留置胃管行胃肠减压;(3)术后患者私自改变饮食进程;(4) 非医嘱出院。 共纳入82 例患者,采用随机数字表法对患者进行分组,对照组和观察组各41 例, 因观察组4 例非医嘱出院而脱落,最终观察组37 例,对照组41 例,共收集病例78 例, 2组患者在性别、年龄、血浆凝血酶原时间测定、手术时间、病变性质、病变部位、合并症比较均无统计学差异(P>0.05),见表1。
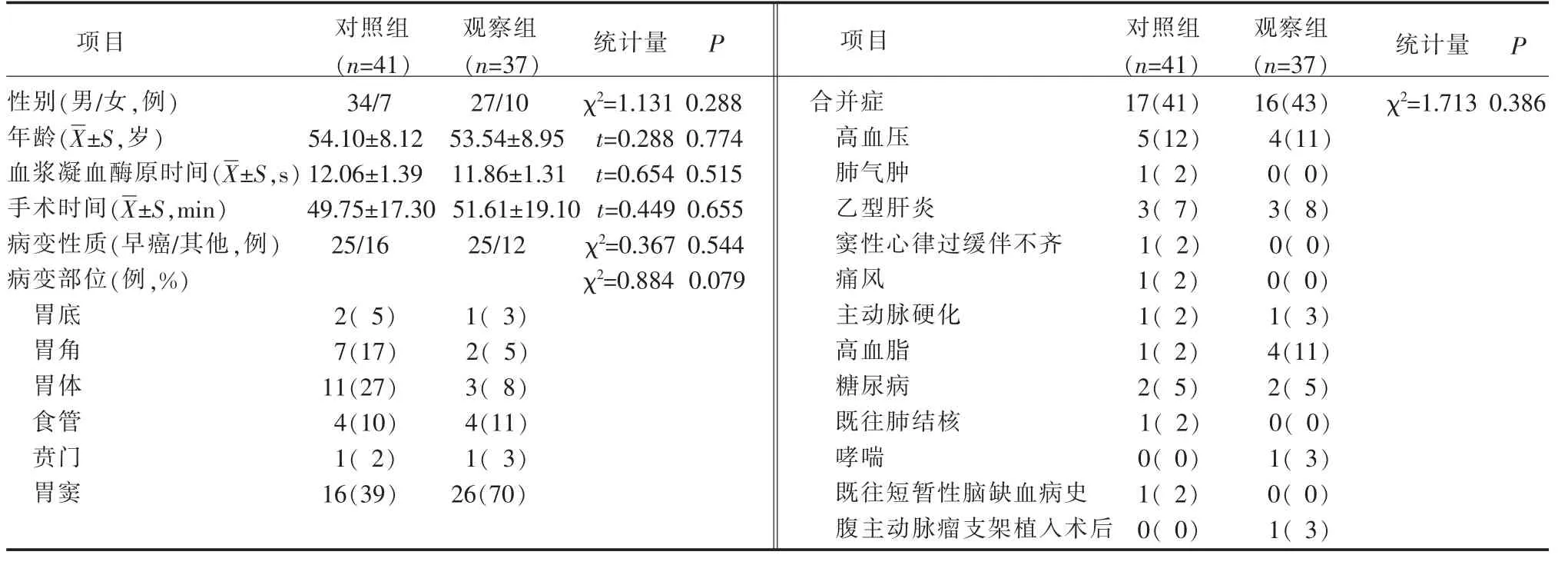
表1 2 组内镜黏膜下剥离术患者一般资料比较
2 方法
2.1 收集临床资料 包括患者基本信息 (年龄、性别等),血浆凝血酶原时间测定,手术时间,内镜下病变的临床特征(病变大小、部位),合并症,术后病理信息,术后并发症等。2 组患者均由内镜室高级职称医师进行手术,固定高级职称麻醉医师进行麻醉,同一医疗组及同一护理组进行治疗与护理。
2.2 干预方案
2.2.1 2 组的术前宣教及内镜治疗相同 (1)术前宣教,使患者对手术过程有充分了解,并向患者解释术后护理的基本流程、 可能出现的术后并发症和处理方法,尽量缓解患者紧张焦虑的心情,消除患者顾虑;(2)术前准备,所有患者术前禁食8 h,禁水4 h;(3)内镜治疗,行内镜下治疗时均取左侧卧位,以丙泊酚行静脉麻醉;术中使用Olympus 电子胃镜,按标准内镜黏膜下剥离术操作流程标记、 染色、 边缘切开、剥离、创面处理5 个步骤完成手术。(4)术后予患者一级护理,巡视1 次/h,测血压4 次/d,测体温4次/d。 关心、询问患者感受。
2.2.2 2 组的术后饮食护理方案不同 2 组患者术后进食进水时间、用药及活动情况详见表2。

表2 2 组上消化道内镜黏膜下剥离术后患者进食进水时间、用药及活动方案
表2 中,温凉水为25~38℃白开水,由责任护士用水温计测温;全流食为25~38℃米汤水,由医院食堂提供或家属自备,责任护士用水温计测温。半流食及低渣软食种类:粥类、面包、蛋糕、软米饭、面条、嫩肉、蒸蛋等,由医院食堂提供或家属自备。测温方法:责任护士取少量食物于手腕内侧试温, 感觉温凉适宜为准。
2.2.3 研究实施者 由主任护师、主管护师、护士各1 名,护师4 名组成护理研究小组。 由主任护师担任组长,负责统筹协调工作及进行研究策划,其余6 名成员负责健康教育、病情观察、进食进水监督指导、收集资料。
2.3 观察指标 分别记录2 组患者术后并发症发生率(包括腹痛、发热、出血、穿孔等)。使用数字疼痛评分量表进行疼痛评分,≥3 分为腹痛;使用水银体温计测腋温,>37.0℃为发热;观察患者大便,肉眼见黑便或柏油样便,且大便潜血阳性为术后出血。总住院费用由医护电子系统自动计算得出。
2.4 统计学分析 应用SPSS 15.0 处理数据, 计量资料以±S 表示,采用两独立样本t 检验,计数资料采用χ2检验,检验水准α=0.05。
3 结果
2 组术后并发症发生率比较:2 组均未出现术后出血、穿孔等并发症。2 组并发症发生率的差异无统计学意义(22% VS 16%,P=0.521)。 详见表3。
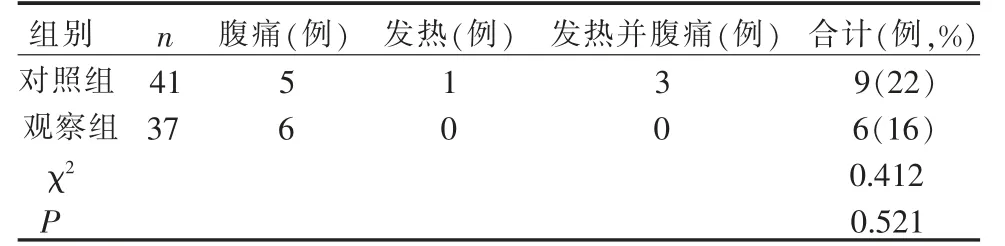
表3 2 组上消化道内镜黏膜下剥离术后并发症比较
4 讨论
常规观点认为: 内镜黏膜下剥离术后为了避免食物与创面摩擦, 一般需要禁食24~72 h 再逐步过渡到流质、半流质饮食[12],但术前的应激、睡眠及进食减少,清肠剂的服用,均可造成营养状态下降,使机体处于一种负氮平衡状态;如术后仍长时间禁食、禁水会加重上述情况,对机体产生不利影响,同时手术创伤机体消耗也影响患者伤口愈合和组织修复[11]。 在本研究中,观察组患者禁食、禁水的时间较对照组的禁食、禁水的时间有效缩短,依据是早期饮水可以缓解口干、清洁口腔、祛除口气;早期进食能提供充足营养,促进加速和改善伤口愈合,避免或降低低血糖等问题,同时减轻患者痛苦,加速术后康复[11,13-15]。 另外,术后使用艾司奥美拉唑可防止胃酸对手术创面的损伤,促进手术创面愈合,有助于上消化道内镜黏膜下剥离术后患者早期经口进食。 观察组在术后每日的输液量比对照组少, 第1 天观察组输液700 mL,对照组输液1 950 mL;第2 天,观察组输液200 mL,对照组输液1 950 mL。 观察组的输液种类比对照组少(4 种VS 2 种),可见观察组减少了静滴肠外营养液和能量合剂液体的种类、 用量及持续时间,同时,患者可以早期经口进食,减轻饥饿感,舒适感明显增加,摄取的食物营养也能促进创面愈合。从表3 可见,2 组术后并发症发生率差异无统计学意义, 表明观察组的术后早期进食方案与对照组的传统进食方案效果相同,且都具有安全性。

