血乳酸水平与休克患者肠内营养耐受性的相关性
于 晴,毛 智,陈金明,杨 彬,虎 磐,薛 超,周飞虎
肠内营养可以起到维护肠道屏障功能,促进胃肠道功能恢复并可以起到代谢调理及代谢支持的作用,早期肠内营养(enteral nutrition,EN)可以降低感染发生率[1],进而减少住院时间、住院费用及降低病死率[2],在临床起到重要作用,可以改善危重患者预后[3]。然而休克患者因为存在血流动力学不稳定,会出现胃肠道功能障碍及对EN不耐受等情况,导致反流误吸等[4]。欧洲营养指南[5]推荐只要休克可以通过液体输注及血管加压药物或正性肌力药物的使用而得到控制,尽早开始低剂量肠内营养。美国成人重症营养指南[6]同样支持在休克患者尽早启动EN。然而休克患者EN时会增加呕吐、腹泻、肠梗阻等不耐受EN的表现[8]。针对休克患者是否早期EN,指南[7]并未做明确推荐。因此,对于休克患者能够早期预测EN不耐受情况就尤为重要,然而相关危险因素研究仍存争议[9]。乳酸作为休克患者微循环灌注的有效监测指标在临床上应用广泛[10],但目前尚无研究证实乳酸水平与EN不耐受的关系。因此,本研究旨在探讨血乳酸针对休克患者EN不耐受预测作用。
1 对象与方法
1.1 病例选择 选择2015-01至2018-01解放军总医院重症医学科收治的,应用血管收缩药物同时给予肠内营养支持的休克患者,年龄≥18岁。排除标准:EN使用时间≤1 h,存在肠道梗阻,急性胰腺炎,腹膜炎以及缺血性结肠炎等,数据不全或丢失等。
1.2 调查资料
1.2.1 一般资料 患者性别、年龄、诊断、休克类型,以及急性生理和慢性健康评估(APACHEII评分)、序贯器官衰竭评分(sequential organ failure assessment,SOFA)、体重指数、营养风险评分(Nutric评分)、住院时间、ICU住院时间、机械通气及床旁血滤(continuous renal replacement therapy,CRRT)。
1.2.2 肠内营养支持相关数据 记录启动EN时间(入ICU至开始EN时间),开始EN营养时胃肠道功能状态[11],营养管放置位置,胃残留量,呕吐量,大便量及次数。休克患者第一日给予肠内营养支持时使用血管活性药物名称,剂量及时间,平均动脉压(9:00 am;9:00 pm),血乳酸(9:00 am;9:00 pm)。记录EN的能量密度;EN目标值,初始速度及平均输注速度;营养目标摄入率:平均实际EN摄入量/目标营养摄入量。
1.2.3 血管活性药物 包括名称,开始EN时血管活性药物剂量(初始剂量)、平均剂量,以及最大剂量。去甲肾上腺素等价量[12]=去甲肾上腺素(μg/min) +多巴胺[μg/(kg·min)÷2]+肾上腺素(μg/min) +去氧肾上腺素(μg/min) ÷10 +垂体后叶素 (U/h) ×8.33。
1.2.4 其他指标 记录合并应用的正性肌力药物包括多巴酚丁胺、异丙肾上腺素、米利农等,以及需记录是否使用促胃肠动力药物以及减少蠕动药物。
记录腹部CT扫描结果,以及肠管缺血、穿孔情况,病死率及主要的致死原因。
1.3 分组处理 同时使用EN及血管活性药物24 h进行评估,根据对患者EN耐受性评估将患者分为耐受组及不耐受组。EN不耐受定义为:胃残留>250 ml,呕吐,腹平片或腹部CT阳性,肠管缺血或穿孔。

2 结 果
2.1 基础情况比较 146例纳入观察研究。EN耐受组114例,EN不耐受组32例。EN耐受组与EN不耐受组的患者一般情况比较,年龄存在差异,但患者APACHEⅡ评分、SOFA评分、营养风险评分(Nutric评分)比较无统计学差异;两组患者休克类型、住院时间、ICU住院时间及机械通气时间均无统计学差异,但在机械通气应用比上,不耐受组显著高于耐受组。不耐受组患者28 d病死率高,差异有统计学意义(表1)。
2.2 EN相关指标 EN耐受组与EN不耐受组的EN开始时间,开始给予的EN能量密度、开始EN给予速度,EN营养摄入量,以及EN营养摄入率比较,差异均无统计学意义(表2)。
2.3 基础胃肠道损伤情况与EN耐受性关系 EN不耐受组患者胃肠道功能分级(AGI评分)加重比例明显高于耐受组(P<0.001),腹部疾病的比例以及幽门后喂养比例两组间差异无统计学意义(表3)。
2.4 血管活性药物剂量与EN耐受性关系 与EN耐受组比较,EN不耐受组患者MAP、NE最大剂量均无统计学差异,但EN不耐受组患者初始NE等价剂量高于耐受组,且血乳酸>2mmol/L的患者比例亦高于EN耐受组(P<0.001,表4)。
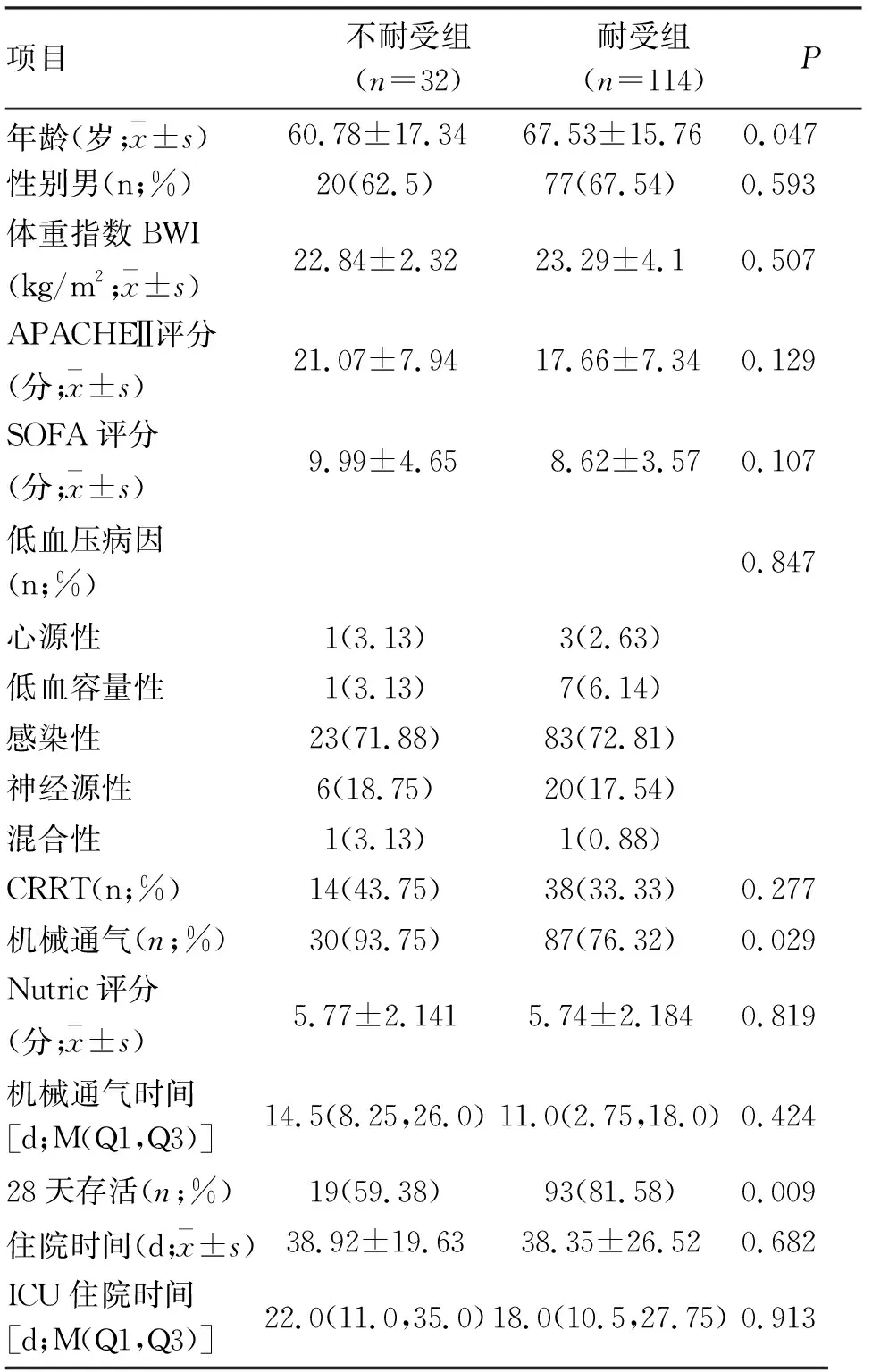
表1 休克患者两组应用血管活性药物并开始肠内营养支持治疗的一般情况


项目不耐受组(n=32)耐受组(n=114)PEN营养能量密度0.95±0.1781.07±0.4690.571EN营养摄入量(kcal/d)460.32±288.94518.41±386.930.221EN摄入速度(ml/h)32.80±24.1939.66±32.100.324EN营养摄入率0.36±0.237 0.42±0.390.236EN开始时间[d;M(Q1,Q3)]4(2.0,7.0)3.0(1.0,5.0)0.665
2.5 EN不耐受影响因素评估 多因素分析显示,年龄、AGI分级、血乳酸>2.0 mmol/L是导致休克患者EN不耐受的独立危险因素(表5)。

表3 两组休克患者应用血管活性药物并开始肠内营养支持治疗的基础胃肠道状况与EN耐受性关系比较

表4 两组休克患者应用血管活性药物并开始肠内营养支持治疗的血流动力学情况与EN耐受性关系比较
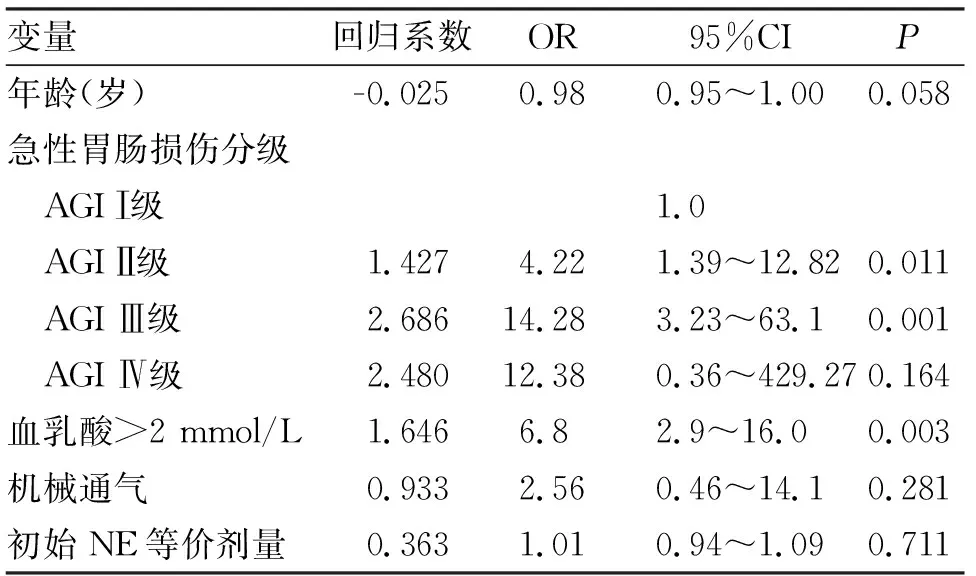
表5 休克患者EN不耐受的多因素Logistic回归分析独立危险因素
3 讨 论
休克患者启动EN的指征目前指南尚未做明确推荐。早期EN可以改善患者的临床预后[13]。然而,休克患者由于血流动力学不稳定,应用血管活性药物,可能导致胃肠道功能障碍及对EN不耐受等情况[14]。对于休克患者,使用ENChecklist可缩短EN启动时间[15]。但对于休克患者何时开始给予EN以及早期给予EN的安全性目前仍无定论[6,7]。有研究显示,合并休克的机械通气患者早期给予EN后ICU住院时间,机械通气时间均小于未给予EN 的患者[16]。但部分研究显示,机械通气的休克患者,早期给予EN与早期给予PN比较,28 d病死率与院内感染发生率无明显差别,但明显增加呕吐、腹泻、肠梗阻的发生[8]。但启动EN时血管活性药物剂量目前仍不确定。研究显示,去甲肾上腺素等价剂量12.5 μg/min时休克患者EN耐受率可达75%[17]。Merchan等[18]的研究显示,应用去甲肾上腺素等价剂量小于0.14 μg/(kg·min)的患者EN耐受率为62%。但上述研究关于休克患者出现EN不耐受相关因素未进一步分析。
血乳酸升高的休克患者给予EN时可能会出现EN不耐受性比例增大。《第三版脓毒症与感染性休克定义的国际共识(简称“脓毒症3.0”)》[19]中提出脓毒症患者,经充分液体复苏后仍存在持续性低血压,需缩血管药物维持平均动脉压(MAP)≥65 mmHg且血乳酸水平>2.0 mmol/L的患者病死率明显升高。此定义是通过大型电子病历数据集进行队列研究验证的[20]。其中感染性休克指标之一血乳酸>2.0 mmol/L。本研究亦将休克进行EN治疗的患者血乳酸是否>2.0 mmol/L进行统计。本研究显示,休克患者高血乳酸是EN不耐受的独立危险因素。
血乳酸水平升高提示组织存在缺氧表现,血流动力不稳定患者胃肠道功能障碍,进而影响EN的耐受性。有学者观察应用机械通气的休克患者EN耐受性情况,发现EN耐受组与EN不耐受组血乳酸无明显差异,但是血乳酸升高的患者比例EN耐受组低于EN不耐受组[18]。本研究显示,EN不耐受组患者血乳酸高于EN耐受组,且同时,血乳酸升高的患者比例高于EN耐受组,多因素回归分析提示血乳酸升高(Lac>2.0 mmol/L)时EN不耐受的概率升高5倍以上,是EN不耐受的独立风险因素。其原因考虑血乳酸升高提示全身组织缺血缺氧,同时胃肠道亦可能存在缺血缺氧情况,导致EN不耐受情况发生。同时血乳酸水平升高可能与患者疾病严重程度相关,但本研究两组比较APACHEⅡ评分及SOFA评分并无明显差异,需更大规模的临床研究证实。
EN不耐受的休克患者死亡率高。本研究结果显示,休克患者给予EN不耐受发生率21.9%,EN不耐受组血乳酸水平高于EN耐受组,且死亡率高于EN耐受组,这一结果可能与患者疾病严重程度有关,因为EN不耐受亦可为胃肠道衰竭表现,且组织缺氧明显导致患者病情重有关。此外,本研究结果中,EN不耐受组启动EN时初始NE等价剂量高于耐受组,与Merchan等[18]相似,但不同之处在于,EN不耐受组患者病情严重程度评分高于耐受组,提示EN不耐受休克患者,往往是病情更重的原因,对EN不耐受是否为休克患者死亡独立危险因素需进一步研究。
本研究显示,休克患者EN耐受组患者年龄在基线上高于不耐受组,年龄对于休克患者EN耐受性影响有待证实。既往研究表明,高龄患者给予肠内营养时容易合并胃排空延迟,胃残余量增加,是影响预后的独立危险因素[21]。Park 等[22]研究发现,高龄、未经过外科肠管切除手术以及非梗阻性缺血性肠病使缺血性肠病患者病死率高,预后差。Halm等[23]调查发现,高龄(年龄>80岁)是心脏外科患者发生肠内营养并发症的独立危险因素。但Rai 等[9]发现,血流动力学不稳定的患者尽管胃排空延迟,同样可以早期开始给予肠内营养。亦有部分研究显示,年龄并不是影响胃肠道疾病预后以及肠内营养并发症发生的因素[24],而与基础疾病有关。还有研究显示尽管高龄患者并存病几率高,但年龄不是影响患者急性上消化道出血内镜治疗胃肠道功能恢复以及预后的指标[25]。由此可见,高龄患者肠内营养仍存在争议,结合本研究显示表明高龄不是休克患者启动EN的禁忌,对于血乳酸值较小、血流动力学逐渐稳定的患者,亦可早期给予EN。但本研究病例数仅146例,结果可能需要更大规模的临床研究进一步证实。
综上所述,对于使用血管活性药物的休克患者早期启动肠内营养时,应评估EN不耐受风险。血乳酸值高(Lac>2.0 mmol/L)的患者发生EN不耐受风险较大,应谨慎进行肠内营养。

