疑似新型冠状病毒肺炎2例影像学表现分析
汪 茜,刘树元,王贵生,马立芝,刘亚华,王立祥
2019年12月起,由严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)感染引发的肺炎(corona virus disease 2019,COVID-19)在湖北省武汉市暴发流行,迅速波及全国31个省市。肺部HRCT检查是疑似或确诊COVID-19的重要依据。COVID-19早期大多数表现为先于临床症状的肺外带斑片状密度增高影,部分呈类磨玻璃样改变。这种磨玻璃样改变是一类非特异性的影像学表现,不易区分病因。早期如何在及时诊断的前提下减少误诊、漏诊,是临床工作的难点之一。笔者就我院在2020年2月疫情防控期间筛查的2例COVID-19疑似病例进行分析、总结,旨在对临床病例筛检提供参考。
1 病例报告
1.1 例1 患者男性,57岁,2020-02-11下午无明显诱因出现胸闷、喘憋、咳嗽,咳少量白色黏痰,无体温升高,当时未做特殊处理。12日凌晨1:30喘憋加重1 h持续不缓解,再次就诊,患者来诊时无发热,无呕吐、腹痛、腹泻等症状。查体:T36.4 ℃,BP150/90 mmHg,心率120次/min,喘息明显,听诊双肺呼吸音粗,双下肺可闻及湿啰音,局部少量干啰音,未闻及心脏杂音,双下肢不肿。既往有高血压、糖尿病、慢性肾衰竭尿毒症病史,每周一、三、五在我院肾内科规律透析。患者及家属否认COVID-19流行病学接触史。接诊后立即完善相关血液化验及肺部CT检查。化验结果:CRP18.83 mg/L,WBC8.71×109/L,NEUT6.59×109/L,比例75.6%,淋巴细胞1.3×109/L,比例14.9%,NLR(中性细胞/淋巴细胞之比)5.07;呼吸道病毒检测五联:柯萨奇病毒IgM抗体阳性;Cr1071 μmol/L,血钾5.9 mmol/L,BNP>35 000 pg/ml。肺部CT提示(图1):双肺磨玻璃样改变,双肺小叶间隔增厚,双肺病毒性肺炎,早期间质性肺水肿不除外。医院专家组会诊意见,根据COVID-19第5版诊疗指南的诊断标准,COVID-19不能完全除外,建议进行新冠病毒核酸排查,收入隔离观察病区诊治,立即抽血送检。患者于就诊当日8:00行维持性常规血液透析治疗,超滤4 kg(平素常规超滤2 kg左右),治疗后患者喘憋明显缓解,13日复查肺部CT提示右下肺索条状影,陈旧性病变,前日可疑斑片状磨玻璃样改变全部消失。13日、14日海淀CDC新冠病毒核酸检测初筛、复筛结果均阴性,修正诊断,解除隔离出院。
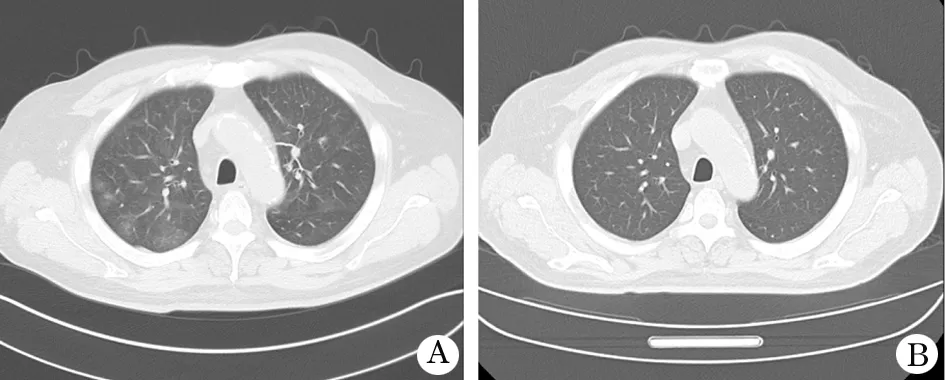
图1 疑似并新型冠状病毒肺炎患者肺部CT(男,57岁)
A. 2020.02.12双上肺见多发散在分布小斑片状磨玻璃影,边界不清,以右上肺为重;B.2020.02.13复查CT片,显示右上肺病变已经吸收
1.2 例2 患者男性,54岁,2020-02-20出现畏寒、乏力、肌肉酸痛,发热最高达39 ℃,无明显规律,伴咳嗽、咳白色黏痰,胸闷气短。21日就诊于当地医院给予化痰、平喘及退热等对症治疗,治疗后症状有好转。22日体温再次升高,达38.7 ℃,来我院就诊。患者否认COVID-19流行病学接触史。查体:血脉氧饱和度95%,心率109~120次/min,咽稍红肿,心肺腹未见其他异常。血液化验:CRP 117.88 mg/L,血常规WBC 6.37×109/L,NEUT5.2×109/L,比例81.8%,LYM 0.65×109/L,比例10.2%,NLR(中性细胞/淋巴细胞之比)8;呼吸道病毒检测五联均为阴性,甲、乙流(-)。胸部CT示(图2):右肺上叶斑片状磨玻璃影,轻微炎性病变。医院专家组会诊意见:根据COVID-19第5版诊疗指南的诊断标准,COVID-19不能完全除外,建议进行新冠病毒核酸排查,收入隔离观察病区诊治。患者来诊前曾口服布洛芬0.2 g,入院后T 36.3 ℃,P 97次/min,BP 110/80 mmHg,SpO299%。两肺听诊未见明显异常。鉴于患者心率较接诊时明显下降,血氧饱和度正常,夜间未做特殊处理。患者夜眠好,次日晨起P 76次/min,T 36.4 ℃,无明显胸闷气短,仍有轻微咳嗽、乏力,对比患者既往胸部CT发现2018-01-10在相同位置有基本相同的磨玻璃样病灶影,考虑该病灶为慢性轻度间质性增生,撤回COVID-19疑似病例申报,修正诊断,解除隔离出院。

图2 疑似并新型冠状病毒肺炎患者肺部CT(男,57岁)
C.2018-01-10检查CT片,D.2020-02-22检查CT片,右上肺后段见小斑片状密度增高影,边界不清,内见索条。2年检查影像未见明显变化
2 讨 论
我们对COVID-19的认识是逐步深入的。2020年3月1日世界卫生组织发布最新疫情报告,指出COVID-19大约80%患者症状较轻,14%左右发展为严重疾病,5%左右为重症病例,重症患者病死率超过50%。Chen等[1]报道武汉金银潭医院早期收治的99例COVID-19患者中,死亡11例,病死率为11%。COVID-19病理学特点与其他疾病有本质不同,首例患者尸检报告显示主要引起深部气道和肺泡损伤为特征的炎性反应,其肺部纤维化和实变没有SARS导致的病变严重,而渗出性反应较SARS明显[2]。
早期CT(high resolution CT,HRCT)影像具有独特性,是主要诊断手段之一,第5版《新型冠状病毒感染的肺炎诊疗方案》中“临床诊断”病例更将CT表现作为重要诊断依据[3]。早期COVID-19在HRCT表现上以斑片状磨玻璃样改变为主,是一种非特异性肺内密度改变,表现为模糊或轻度的斑片状、云雾状密度增加,但尚不能遮盖肺组织中的气管及血管纹理。肺内密度受肺内气体、体液、血液、肺组织自身等多因素影响,可见于各种炎症、水肿、出血、纤维化和肿瘤等病变,其中肺泡内含气量及肺内血管外体液量变化是肺密度改变的常见病理基础[4]。有文章报道COVID-19特异性斑片状磨玻璃样改变占55%~95.2%,出现统计数据差异主要受汇总病例病情轻重不一,病程早晚不一,病例样本数量较小等因素影响[5-7]。
早期识别对于准确诊断、隔离、治疗COVID-19患者至关重要,同样,对于容量负荷所致的急性间质性肺水肿患者的及时救治,以及避免给予慢性间质增生患者过度治疗也具有现实意义。
例1患者肺部CT可见多处斑片状毛玻璃影,同时伴有肺间质水肿,结合患者既往慢性肾衰竭尿毒症期长期规律透析病史,以及后期询问出来的近1个月患者体重较标准体重增加1 kg的线索,其实不难判断患者喘憋症状多由肺水过多所致。肾脏是调节机体体液平衡、保持机体内环境稳定的主要脏器。尿毒症引发肺改变常表现为相对独特的肺水肿,其一,尿毒症毒素本身可导致肺泡毛细血管通透性增加;其二,钠水潴留也造成体液大量滞留在组织间隙,跨膜胶体压和静水压改变,以上因素均可导致体液从肺毛细血管和小静脉外渗至肺泡和肺间质中,引发原发及继发肺水肿。而其病理则表现为渗出至肺泡及肺泡间隔内液体因富含蛋白、纤维素常呈胶冻样、易凝固,可伴有透明膜形成,这种病理改变与COVID-19患者肺泡病理改变有相通之处,但其形成病因不同,对治疗的效果反应不同。例1患者经就诊当日大量超滤后,喘憋症状明显减轻,次日复查肺部CT云雾状磨玻璃样改变基本消失,也证实单纯肺水多是本次病情变化的主因,及时的肺部CT复查明确了下一步诊疗工作的方向。对长期规律透析的患者来讲,及时排除COVID-19疑似病例诊断,极大程度减轻了患者的经济压力及心理负担。本病例提醒首诊医师应重视病史采集细节,才能提高对患者病情变化及影响因素的整体把控,提高诊治能力。
例2患者2020年2月22日肺CT发现右下肺磨玻璃样改变,与2018年1月10日肺CT相比,病灶部位、大小、密度基本一致,考虑是慢性炎伴间质纤维组织增生的影像学改变。根据国家卫健委发布的COVID-19诊疗指南要求,患者不满足COVID-19疑似病例诊断条件,解除医学隔离。这种肺组织慢性炎症,病理过程一般为进展缓慢的弥漫性肺泡炎和(或)肺泡结构紊乱,肺组织结构性改变过程可以长达数年。单次检查的肺CT斑片状磨玻璃样改变有时很难区分慢性炎伴轻度间质纤维组织增生与早期急性渗出性肺泡炎,有学者提出在没有毛细支气管扩张和蜂窝影的情况下,斑片状密度增高更倾向于表示肺泡炎[8],也有学者观察到COVID-19病例在急性期可出现类似于慢性间质性肺病影像学改变的现象[9]。所以,对于此类患者肺部CT老片与新片的对比就显得至关重要,例2患者COVID-19疑似病例的排除也主要依据其2018年的肺部CT存在右下肺磨玻璃样改变证据。本病例提醒医师在临床诊疗过程中,相比于现存在的症状、体征和辅助检查证据,更重要的是这些证据指标的动态变化,只有充分了解这些变化才能得出更准确的临床判断。
总体而言,临床诊疗工作的基础在于首诊医师工作的细致与准确。其一,在于病史采集,过去、现在、将来的全因分析是综合评价病情的基础,其二,注重临床数据、证据的动态变化,才能正确掌握、评估病情轻重及转归,做出及时、正确的处置。

