介入取出儿童右心内断裂输液港导管一例
张玉林 庞桦进
静脉输液港系统对于需长期开展静脉化疗的肿瘤患者具有非常重要的意义[1]。完全植入式静脉输液港系统并发症较少,患儿活动更安心且使用时间长久等优势[2]。主要并发症有导管静脉血栓形成、导管阻塞等。但随着留置导管时间的延长,导管移位、导管断裂等并发症相对增多,并可导致严重并发症(包括心脏心律失常、腔内栓塞及感染性心内膜炎)[3]。我科收治1 例急性淋巴细胞性白血病患儿输液港导管断裂进入右心内的病例,并成功通过血管内介入异物抓捕技术取出断裂的输液港导管,现介绍如下。
病例资料患者,男,4 岁,确诊急性淋巴细胞白血病,行右锁骨下静脉输液港置入(图1),术后导管通畅并使用正常。患儿每隔4 周返院进行输液港维护。一年后复查胸部正位片提示锁骨下区导管损伤(图2),未做特殊处理。再经过8 个月后行输液港维护时,回抽无回血,注入5 ml生理盐水,患儿锁骨下软组织肿胀、疼痛,行胸片及CT检查,发现输液港导管断裂、脱落,离断端位于右心(图3,4),患儿无明显心慌、胸闷等不适症状,为进一步治疗收住入院。
完善常规检查后,于全麻下行异物抓捕取出术。患儿仰卧于DSA 检查床,透视下可见右心内管状异物影,上端游离并摆动,位于右心房上部,下端固定,位于右心室内。穿刺右侧股静脉,留置8F 血管鞘,置入6F 抗折长鞘(Cook公司)至右心房下部。用鹅颈式抓捕器套件(Amplatz Goose Neck Snare Kit,EV3),成功套取异物游离端,确认收紧后,向后拉入抗折长鞘内并移至体外(图5)。透视心影内未见异物残留影。取出输液港底座及导管残端,检查两断端对合良好,未见缺损(图6)。
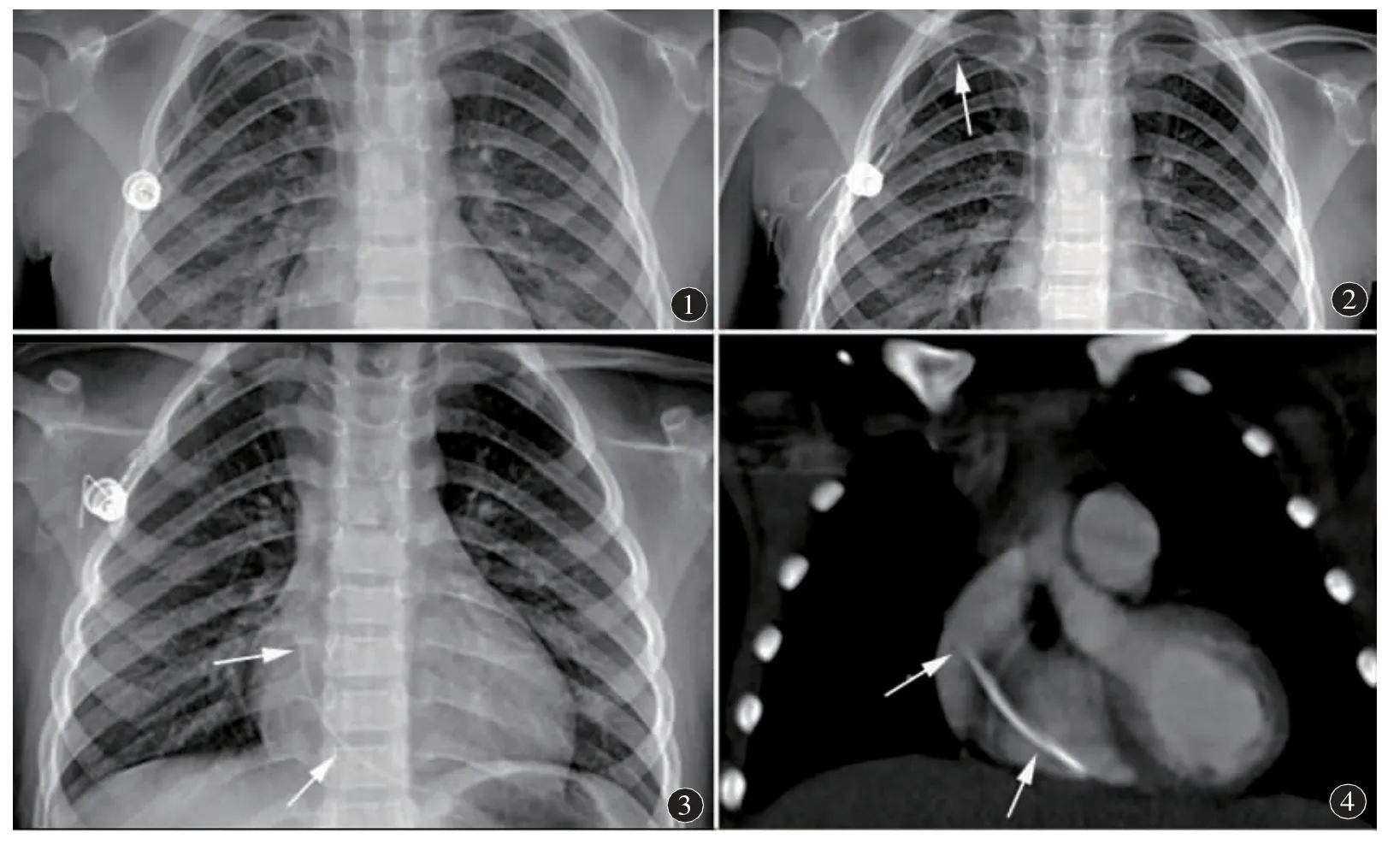
图1 胸部后前位片。右锁骨下静脉输液管导管边缘光滑,走形自然图2 胸部后前位片。输液管导管下缘与第1 前肋上缘贴合部折曲、不连续,考虑不完全断裂(箭)图3 胸部后前位片示断裂的导管位于右心(箭) 图4 CT 冠状位重组图示导管断裂、脱落,离断裂导管位于右心系统(箭)
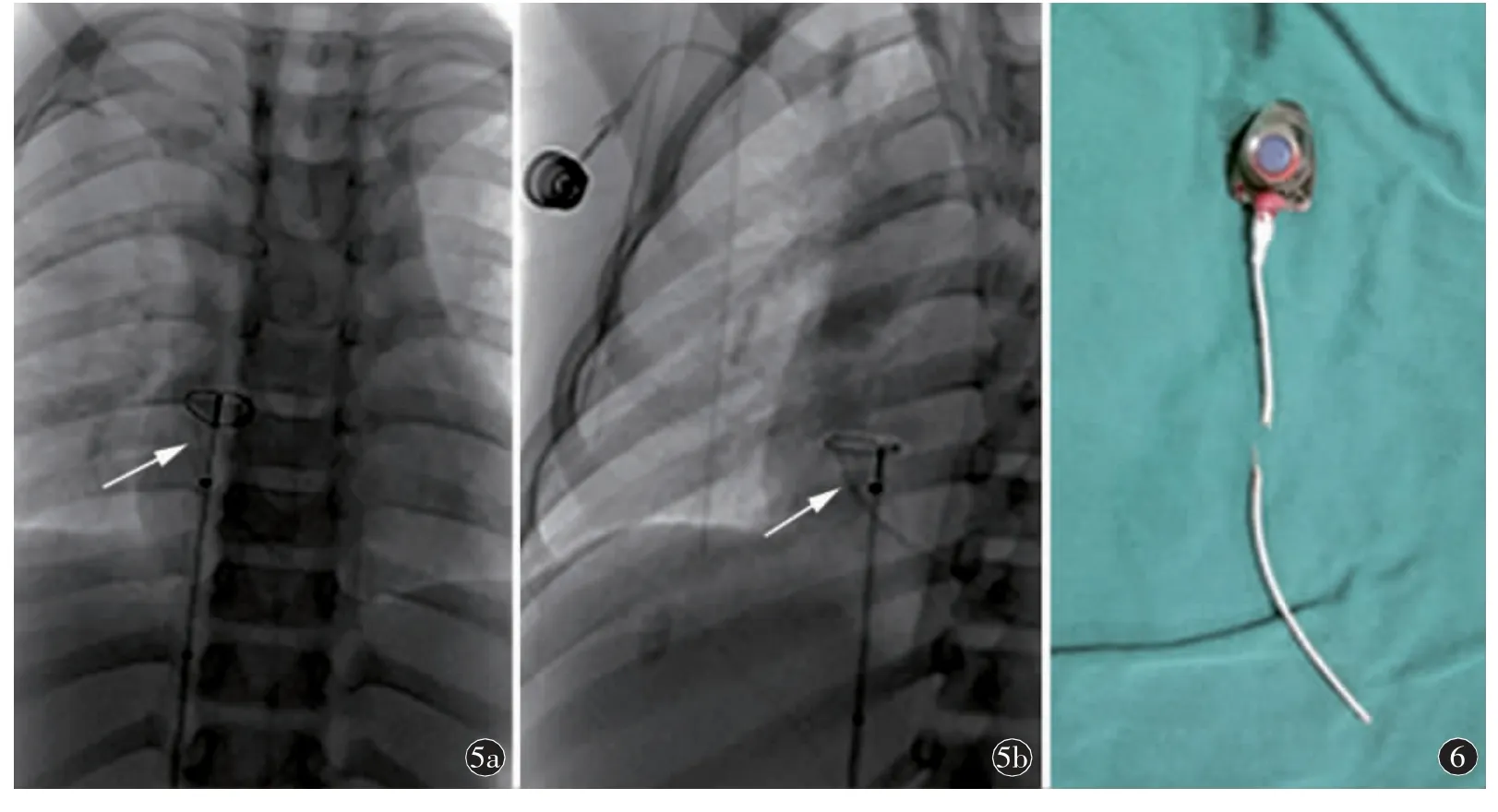
图5 DSA 多体位观察,可判断鹅颈抓捕器与异物的位置(箭) 图6 离断导管、输液管底座和导管残端取出后,对合良好,未见缺损
讨论输液港在长期开展静脉化疗的肿瘤患者中应用广泛,导管断裂是少见且严重的并发症。患者肢体活动过度、高压力注射、护理操作不规范及导管固定不正确等均可导致导管断裂[4]。回顾病史及影像资料,该患者导管断裂考虑可能与以下因素有关:(1)Pinch-off 综合征:该输液港为右锁骨下静脉入路。若静脉穿刺点位于锁骨中线以内,可能会出现输液港导管和锁骨下静脉并行通过锁骨与肋骨间的狭小间隙的情况,导致导管受到第一肋骨和锁骨挤压。长期的挤压及较长的置管时间可能会造成导管损伤或断裂[5]。(2)输液港置入时,患者身高110 cm、体重20 kg,而发现导管断裂时,身高121 cm、体重25 kg,随着身高的增长,肋骨会稍向上移,而输液港底座与导管相对固定,造成了导管与第一肋贴合更加紧密,当呼吸运动、血管搏动及肢体活动所致两者的摩擦力较置入时明显增加。(3)当导管损伤后,损伤面会变得毛糙,日常活动及生理运动导管损伤部所受的摩擦力较正常时显著增加。(4)当导管损伤至内面(即不完全断裂),输液港维护时,注入生理盐水阻力增加,操作人员会加大推注压力,或选用10 ml 以下注射器,会造成压力增大,从而会加速导管的撕裂。综上,考虑Pinch-off 综合征有可能致导管断裂,因此在儿童输液港置入时选择B 超引导下穿刺右侧颈内静脉入路或者偏外侧的锁骨下静脉入路可能是一个更佳的选择[6]。
对于此次异物抓捕,有如下体会:(1)首先应检查明确离断导管的大小、所在位置、游离端随血流摆动的方向及患者配合程度选择合适入路和手术方式。(2)如两端固定,可选择猪尾导管配合泥鳅导丝改变离断导管的位置,再用抓捕器抓捕或选用异物钳钳取异物[7]。(3)该离断导管直径为6F,选择6F 的长鞘,那么抓捕时需尽可能的选择游离段的头端,避免导管成袢后拉入长鞘失败;如若拉入长鞘失败,则后撤长鞘,异物可经8F 短鞘拉出。(4)套取异物时,适当转动球管,多角度观察抓捕器与异物位置,能显著提高抓捕效率。因此术前详细计划、术中精细操作及适时转动球管角度为异物取出的关键。

