高粱醇溶蛋白-卡拉胶复合纳米颗粒负载姜黄色素的特性研究
李兴飞 陈 斌 陈国靖 龙 杰 华欲飞
(江南大学食品学院;食品科学与技术国家重点实验室1,无锡 214122) (宣城柏维力生物工程有限公司2,宣城 242000)
高粱中含有6%~18%的蛋白质,包括球蛋白、清蛋白、醇溶谷蛋白和谷蛋白。醇溶蛋白是高粱蛋白主要存在形式,占总蛋白的77%~82%[1],主要是由α-,β-和γ-三种类型构成[2]。高粱醇溶蛋白与玉米醇溶蛋白具有很多相似的物理化学性质,例如溶解度、摩尔质量、氨基酸组成和多肽结构等[3, 4]。但是,与玉米醇溶蛋白相比,高粱醇溶蛋白的疏水性更强,消化特性更差[5]。由于高粱蛋白的消化率低,高粱主要利用其中的谷蛋白用于酿酒发酵,丢弃的残渣中含有大量的醇溶蛋白,造成资源浪费。高粱醇溶蛋白具有的较好的物理化学特性和生物相容性,可以被用来塑形成膜[6];也可以作为包埋传递活性分子的理想载体[7]。目前,有关玉米醇溶蛋白作为输送载体的相关报道十分广泛[8-10];但是,高粱醇溶蛋白的潜在应用仍然缺乏详细而系统的研究。
姜黄素是从姜黄根中提取的一种黄色化合物,经体内和体外实验证实具有抗氧化、抗癌等生物活性,是一种较为理想的食品和药品原料[11]。但是,姜黄色素水溶性很差,化学性质不稳定,易在外部环境变化条件下发生降解,从而导致其生物活性利用率低。因此,姜黄色素一般是通过生物介质传递增强其稳定性,例如微球、粒子、生物膜、纳米纤维等[12-14]。
本研究以高粱醇溶蛋白为原料,基于反溶剂法,以碳酸钠为牺牲模板制备中空高粱醇溶蛋白纳米颗粒,并根据静电吸附作用形成卡拉胶包被层,从而获得装载姜黄色素的中空纳米颗粒,增强姜黄色素的稳定性和体外释放特性,提高姜黄色素产品在食品和药品中的应用价值,同时为高粱醇溶蛋白的高值化利用提供参考。
1 材料与方法
1.1 实验材料
1.1.1 原料与试剂
白高粱粉、胃蛋白酶、胰蛋白酶、卡拉胶、姜黄色素、氢氧化钠、浓盐酸、焦亚硫酸钠、冰乙酸、Tween 20等分析纯试剂。
1.1.2 仪器与设备
Himac CR21 GⅡ型冷冻离心机;多角度粒度与高灵敏度Zeta电位分析仪;Delta 320 pH计;CR 21G Ⅱ型冷冻离心机;UV-1500型分光光度计;LGJ-18型冷冻干燥机;傅里叶红外光谱仪;Tecnai T20透射电子显微镜。
1.2 实验方法
1.2.1 高粱醇溶蛋白的提取
依照Taylor等[15]方法,略有修改。称取0.5 kg高粱粉,加入2.5 kg 70%的乙醇水溶液,然后将12.5 g偏亚硫酸氢钠和8.7 g冰醋酸加入上述混合物中,搅拌均匀并加热至70 ℃,水浴恒温震荡提取1 h。将上述悬浮物经两层滤纸真空抽滤,除去不溶物。将过滤液在50 ℃下真空抽滤,旋转蒸发挥干酒精,收集沉淀组分。将以上沉淀用去离子水冲洗3次,滤纸过滤,收集沉淀并冷冻干燥。将所提粗蛋白粉末用正己烷(1∶2 g/mL)浸泡脱脂3次,置于通风橱,挥干正己烷,-20 ℃贮存备用。
1.2.2 负载姜黄色素高粱醇溶蛋白纳米颗粒的制备
在70 ℃水浴循环下,用70%乙醇配制质量浓度为2.0%的高粱醇溶蛋白溶液,磁力搅拌1 h至完全溶解,冷却至室温,离心(6 000 r/min, 30 min)去除少量不溶性颗粒。在避光条件下,按照姜黄素/高粱醇溶蛋白(芯壁比)质量比1∶5,1∶10,1∶15,1∶20,1∶25和1∶30向上清液加入相应质量的姜黄色素,置于暗处磁力搅拌24 h,使姜黄色素完全溶解吸附。同时配制2%的碳酸钠水溶液,待用。
1.2.2.1 中空纳米材料:参考Xu等[16]方法,略有修改。将2%的碳酸钠水溶液与无水乙醇3∶7(V/V)混合,制备得到分散均匀的碳酸钠乙醇悬浮液。将以上悬浮液按照体积比1∶2加入到负载姜黄色素的高粱醇溶蛋白溶液中,磁力搅拌10 min,使其充分混合。在磁力搅拌条件下,将以上混合溶液按照体积比1∶20缓慢加入到去离子水中,使其通过反溶剂法分散形成纳米颗粒,简称HNP。
1.2.2.2 实心纳米材料:与制备中空纳米粒子不同,将负载姜黄色素的高粱醇溶蛋白溶液直接按照体积比1∶20缓慢加入到去离子水中,使其通过反溶剂法分散形成纳米颗粒。然后加入相应体积的碳酸钠乙醇悬浮液(2%的碳酸钠水溶液与无水乙醇3∶7混合),以保证实验条件与1.2.2.1一致;通过以上步骤制备的纳米颗粒简称SNP。
1.2.3 负载姜黄色素的高粱醇溶蛋白-卡拉胶复合纳米颗粒的制备
配制质量浓度为0.1%的卡拉胶溶液,按照体积比1∶5与上述1.2.2制备的中空和实心纳米溶液分别混合均匀,磁力搅拌10 min,然后用2 mol/L HCl调节混合溶液pH至4.0,使卡拉胶和高粱蛋白发生静电吸附,形成中空复合纳米颗粒和实心复合纳米颗粒,低温冷冻干燥,分别简称为C-HNP和C-SNP。
1.2.4 Zeta电位测定和粒径测定
分别取新鲜制备的纳米溶液和冻干复水后的纳米颗粒溶液,在25 ℃下,用Zetasizer Nano电位仪测定Zeta电位、粒径分布以及PDI,每个样品重复3次测定。PDI 是指多分散性系数,PDI 越小,代表体系粒径越均匀,一般认为小于0.4 较好。
1.2.5 微观结构观察
采用(FEI Tecnai T20)透射电子显微镜观察制备的复合纳米颗粒的微观结构。取18 μL样品液滴在铜网上,30 s后用滤纸吸去溶液,然后加入相同体积的固定剂,30 s后滤纸再次吸净。放大倍数30 000~50 000下观察形态结构。
1.2.6 傅里叶变换红外光谱分析
取10 mg冻干的样品颗粒与0.1 g KBr粉末于玛瑙研钵中,在红外灯照射下,研磨均匀,取适量样品置于压片槽中,经压片后进行衰减全反射傅里叶变换红外光谱分析,波数范围为400~4 000 cm-1,分辨率为4 cm-1,扫描次数为32次。
1.2.7 姜黄色素包埋率和负载率
取10 mg冻干样品用2 mL乙酸乙酯冲洗2遍,去除未吸附的姜黄素。收集上述样品,继续用80%乙醇提取姜黄色素,离心(4 000 r/min,15 min),收集上清液,并用80%乙醇稀释一定比例,用紫外分光光度计在425 nm下测定吸光度。在相同实验条件下,配制一系列浓度(0、1、2、3、4、5、6、7 μg/mL)的含有姜黄色素的80%乙醇溶液,于425 nm下测定吸光度,绘制标准曲线(y=0.077 8x+0.005 4,R2=0.998 9)。由标准曲线计算得到复合纳米颗粒中的姜黄色素含量,根据式(1)和式(2)计算复合纳米颗粒的包埋率和负载率:

(1)

(2)
1.2.8 体外模拟消化实验
体外模拟消化实验根据Xiao等[17]方法,略有修改。准确称取姜黄色素1.0 mg, 并称取相应质量的中空纳米颗粒和实心纳米颗粒粉末,使其含有相同质量的姜黄色素。分别将以上3种样品混合于18 mL的含有0.5%的吐温 20的 0.1 mol/L 盐酸溶液;在搅拌状态下37 ℃水浴10 min。然后加入15 mg/mL的胃蛋白酶溶液2 mL (0.1 mol/L 盐酸溶液配制),继续磁力搅拌,开始计时胃蛋白酶模拟消化1 h。1 h消化后,加入30 mg/mL的胰蛋白酶溶液10 mL,调节pH至 7.4,37 ℃计时搅拌2 h,模拟胰蛋白酶消化。分别在第0、30、60、90、120、150、180 min吸取250 μL溶液,离心(4 000 r/min,15 min),取上清测定姜黄色素浓度。
2 结果与讨论
2.1 负载姜黄色素高粱醇溶蛋白纳米颗粒制备的条件优化
纳米粒子的粒径及电位分布是表征纳米粒子稳定性等特性的重要指标。实验首先研究了不同芯材比例对制备的纳米粒子粒径及Zeta电势的影响,结果如表1所示。结果表明,实验制备的负载姜黄色素中空纳米颗粒平均粒径在62~77 nm,负载姜黄色素实心纳米颗粒的平均粒径约为102~123 nm,后者约为前者的2倍。Xu等[18]研究表明,通过Na2CO3作为牺牲模板自组装的玉米醇溶蛋白中空纳米颗粒相比实心纳米粒子,其平均粒径显著减小。该研究认为,70%乙醇中分散形成的Na2CO3晶体可以作为纳米颗粒生长的非均相成核位点,从而有效控制形成的纳米颗粒尺寸增长。本实验中,两种纳米颗粒制备原理的差异主要在于Na2CO3晶体是否参与蛋白质纳米颗粒的形成。在HNP制备过程中,Na2CO3晶体是与高粱蛋白分子包裹在一起的,当两者共同加入到水溶液中时,由于蛋白质的强疏水性,高粱蛋白通过反溶剂法自组装形成纳米颗粒,并且其尺寸增长受控于Na2CO3晶体;于此同时,被包裹的Na2CO3晶体由于其极强的水溶解性,快速从高粱蛋白纳米颗粒内部释放到外部的水溶液介质中,从而促使纳米颗粒形成了内部中空结构。与之相反,在SNP制备过程中,高粱醇溶蛋白首先通过反溶剂法自组装形成实心纳米颗粒, Na2CO3晶体并未参与纳米颗粒的形成,后续步骤中再次加入Na2CO3晶体未对纳米颗粒形态结构造成影响。因此,与实心蛋白纳米颗粒相比,通过Na2CO3晶体作为牺牲模板组装构建的高粱醇溶蛋白中空纳米颗粒具有更小的平均粒径。在考察的芯材比例范围内,两种纳米颗粒的Zeta电位变化范围在-35~-38 mV,这表明两种制备工艺对所形成的纳米粒子电势没有显著性影响,较高的电势绝对值可以保证制备的纳米粒子具有较高的物理稳定性。但是,由于两种纳米粒子是在Na2CO3存在的碱性环境下制备的,因此他们仅在碱性pH范围(pH 7~10)内保持稳定;当调节pH至蛋白质等电点附近时(pH 5.3),蛋白质之间的静电斥力作用较弱,颗粒因疏水相互作用而发生大量聚集沉淀。因此,纳米颗粒的酸性pH稳定性将关系到其在体内胃消化环境下的稳定特性。
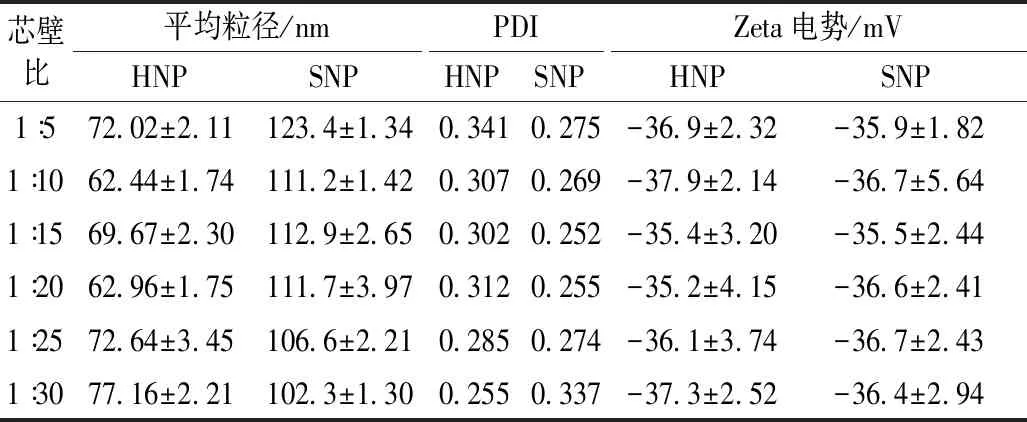
表1 负载姜黄色素的两种高粱蛋白纳米颗粒剂 的粒径、多分散性系数(PDI)及电位
注:HNP代表负载姜黄色素的中空纳米材料;SNP代表负载姜黄色素的实心纳米材料。
如表2所示,随着芯材比例的降低,两种纳米复合颗粒对姜黄色素的包埋率均在不断的降低,尤其是芯壁比条件1∶5下,包埋率相较于1∶10发生显著降低(P<0.05)。当芯壁比1∶5时,姜黄色素浓度已经达到了壁材的过饱和状态,不利于纳米颗粒的制备及姜黄色素的包埋[19]。在芯壁比1∶30~1∶5范围内,复合纳米颗粒的负载率随着姜黄色素添加量的增加而不断上升,最大负载率出现在1∶5芯壁比条件下。综合考虑包埋率和负载率效果,在芯壁比1∶10条件下所制备的复合纳米颗粒较好。
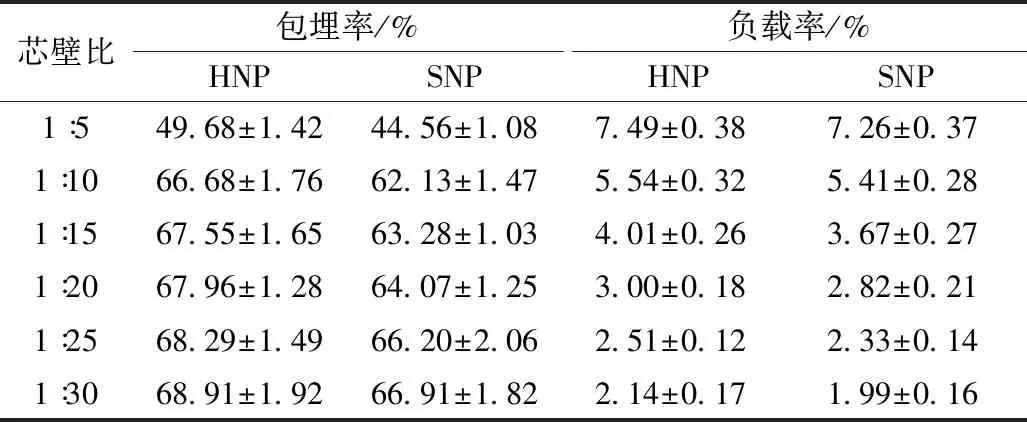
表2 芯壁比对复合纳米颗粒包埋率与负载率的影响
注:HNP代表负载姜黄色素的中空纳米颗粒;SNP代表负载姜黄色素的实心纳米颗粒。
2.2 卡拉胶包被对负载姜黄色素高粱醇溶蛋白纳米颗粒性质的影响
两种高粱醇溶蛋白纳米颗粒对姜黄色素的最大包埋率均小于70%,为了进一步提高纳米颗粒的包埋率以及酸性pH条件下的稳定性,研究多糖包被对纳米颗粒包埋效果的影响,结果见表3。结果表明,随着芯壁比的逐渐降低,两种纳米颗粒的包埋率在逐渐上升,但是当芯壁比达到1∶15时,其包埋效率上升趋势不明显,且此时负载率表现出急剧下降趋势。C-HNP和C-SNP对姜黄色素的最大包埋率均超过了90%。在相同的实验条件下,C-HNP比C-SNP具有更高的姜黄色素包埋能力,尤其是当芯壁比例较高时,例如1∶10和1∶5;这可能与中空纳米颗粒的结构有关,使得一部分被包埋分子可以进入纳米颗粒内部。综合考虑纳米颗粒的包埋率和负载率,选择1∶10芯壁比制备复合纳米颗粒的综合效果最好。
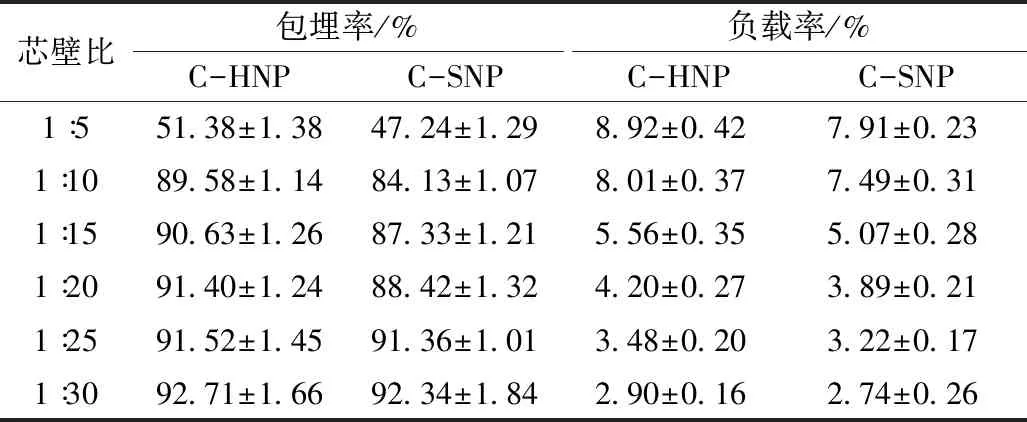
表3 卡拉胶包被对复合纳米颗粒包埋率、负载率的影响
注:C-HNP代表卡拉胶-高粱蛋白中空纳米颗粒;C-SNP代表卡拉胶-高粱蛋白实心纳米颗粒。
在最佳实验条件下,对冷冻干燥制备的卡拉胶-高粱蛋白纳米颗粒进行复水溶解,并测定其粒径和Zeta电位变化,以表征纳米颗粒的稳定性。如表4所示,在最佳芯壁比1∶10下,中空和实心卡拉胶-高粱蛋白纳米颗粒的平均粒径分别为71.35 nm和135.4 nm,PDI较小,与单一高粱蛋白纳米颗粒相比,平均粒径仅发生略微增加,这表明包被的卡拉胶分子层较薄,没有引起纳米颗粒的聚集增大或者纳米颗粒结构的坍塌导致粒径缩小问题,纳米颗粒仍然是稳定的。由于卡拉胶为强阴离子多糖,可以通过静电作用吸附于高粱蛋白表面上,形成一层稳定的负电荷层;因此形成的纳米颗粒Zeta电势主要取决于卡拉胶分子。表4结果显示,两种卡拉胶-高粱蛋白纳米颗粒的Zeta电势分布于-37~-38之间,较高的电势绝对值可以保证制备的纳米溶液具有长期的物理稳定性。
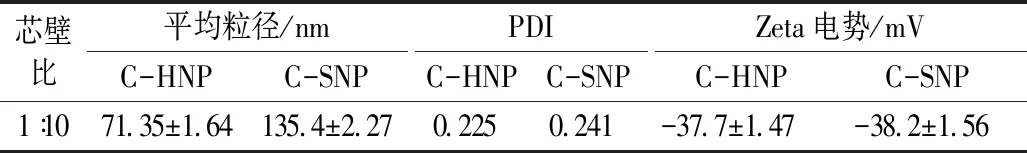
表4 最佳实验条件下卡拉胶-高粱蛋白纳米颗粒的 冻干复水后粒径、多分散性系数及电位
注:C-HNP代表卡拉胶-高粱蛋白中空纳米颗粒;C-SNP代表卡拉胶-高粱蛋白中空纳米颗粒。
2.3 透射电镜对卡拉胶-高粱蛋白复合纳米颗粒形貌观察
两种复合纳米颗粒的微观结构观察结果如图1所示。两种复合纳米颗粒呈规则的球形,粒子与粒子之间相互黏连较少。Zhang等[20]认为具有空芯结构的颗粒或胶囊经过透射电子穿透后一般会形成为内部透光度高,外部透光度低的暗环形态结构。如图1a所示,透射电镜(TEM)结果表明卡拉胶-高粱蛋白中空复合纳米颗粒同样形成了内部较亮、外部较暗的形态结构,分界线处形成了一层厚度约为几纳米的“壳”,如图1a中双箭头所示,这说明纳米颗粒内部存在一个中空的腔。相反地,实心复合纳米颗粒整体透光度均一,颜色较暗(图1b),因为实心纳米颗粒比中空纳米颗粒能阻挡更多的电子进入[16]。Xu等[16]在研究玉米醇溶蛋白中空纳米颗粒的微观结构形态时观察到其壳厚度约为2~10 nm,内部空腔直径约为20~50 nm,且粒子平均粒径为60 nm,显著性地小于实心纳米颗粒。
本实验中,卡拉胶-高粱蛋白中空复合纳米颗粒的粒径在50~60 nm之间,卡拉胶-高粱蛋白实心复合纳米颗粒的粒径在80~100 nm,这与通过Zeta纳米粒径测定的结果基本一致,证实了中空纳米粒子具有更小的平均尺寸。TEM观察到的卡拉胶-高粱蛋白实心复合纳米颗粒的粒径略小于动态光散射技术(DLS)测定值,这是因为DLS测定的是具有一定水合半径的粒子大小,而TEM需要样品观察前进行脱水干燥。两种技术观察到的粒径差异已经被广泛报道[21]。

注:放大倍数为30 000×,对应标尺为50 nm。图1 卡拉胶-高粱蛋白中空复合纳米颗粒(a)和卡拉胶- 高粱蛋白实心复合纳米颗粒(b)的透射电子显微镜图
2.4 傅里叶红外变换光谱分析

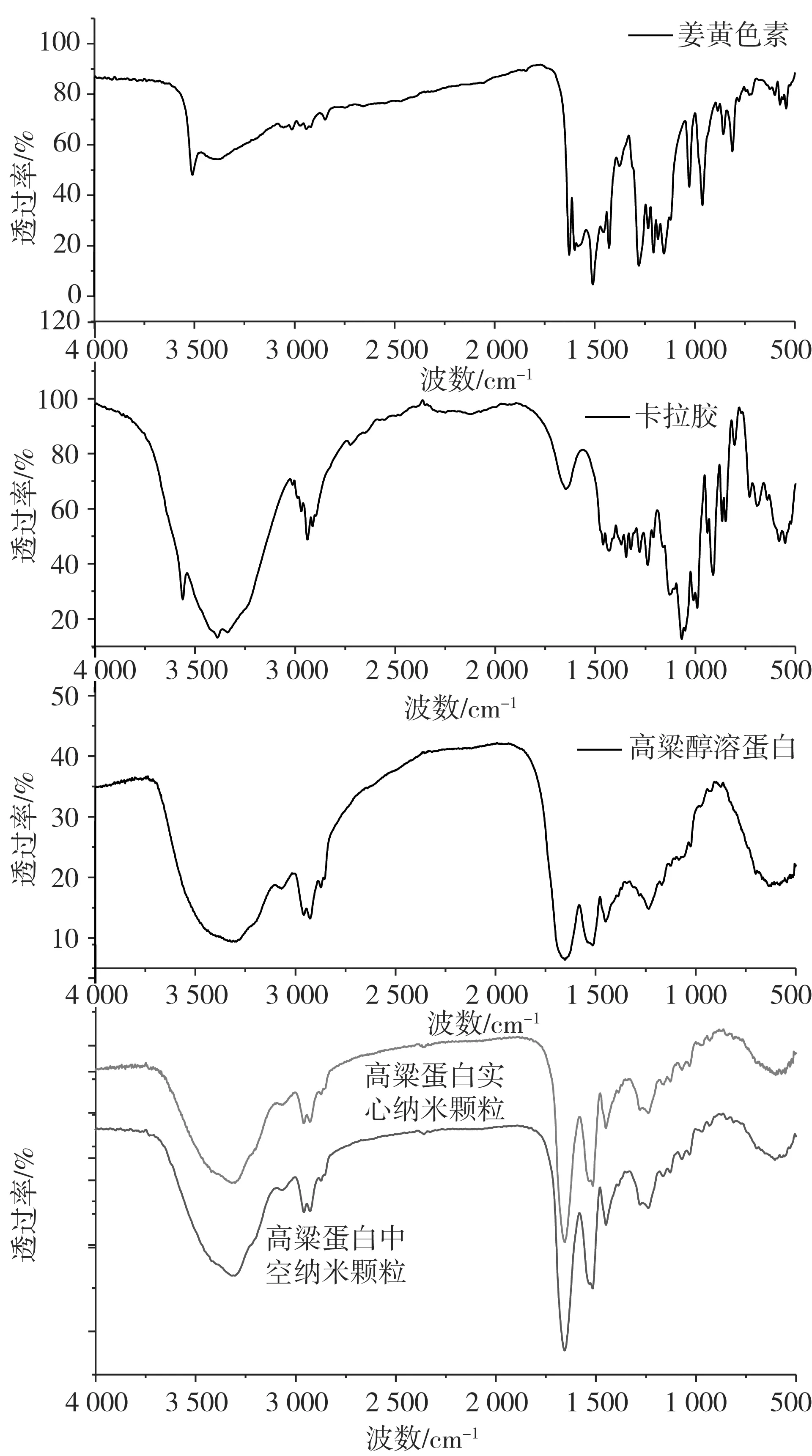
图2 姜黄色素、卡拉胶、高粱醇溶蛋白及中空和 实心纳米颗粒的傅里叶红外变换谱图
2.5 不同贮藏时间下的复合纳米颗粒稳定性
在食品的加工储藏过程中,延缓产品的腐败变质,对提高产品的货架期有重要意义,因此对制备的两种复合纳米材料进行贮藏时间实验,以观察制备纳米粒子的贮藏稳定性。如表5所示,两种复合纳米颗粒在30 d的贮藏时间内,其平均粒径略微增大,PDI值也在略微增高,但整体变化不明显,这说明两种复合纳米颗粒的贮藏稳定性较高。值得注意的是,实心纳米材料似乎相较于中空纳米材料更不稳定,表现为更高的PDI和平均粒径变化值。
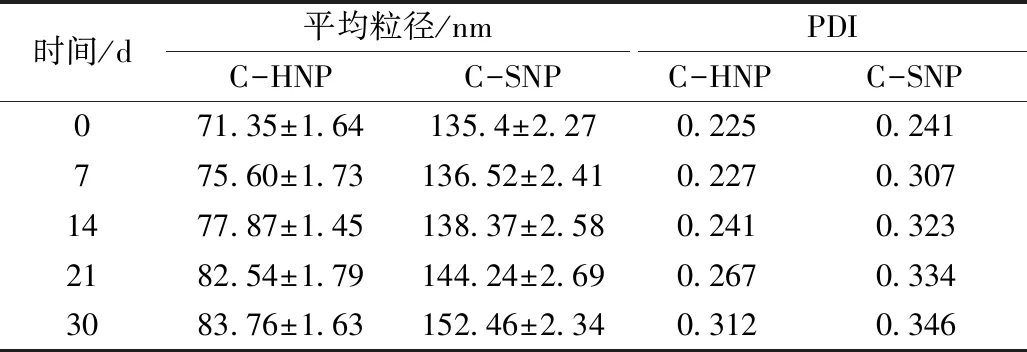
表5 储藏时间对卡拉胶-高粱蛋白复合纳米颗粒 平均粒径与多分散系数PDI的影响
注:C-HNP代表卡拉胶-高粱蛋白中空纳米颗粒;C-SNP代表卡拉胶-高粱蛋白实心纳米颗粒。
2.6 复合纳米颗粒的体外消化释放
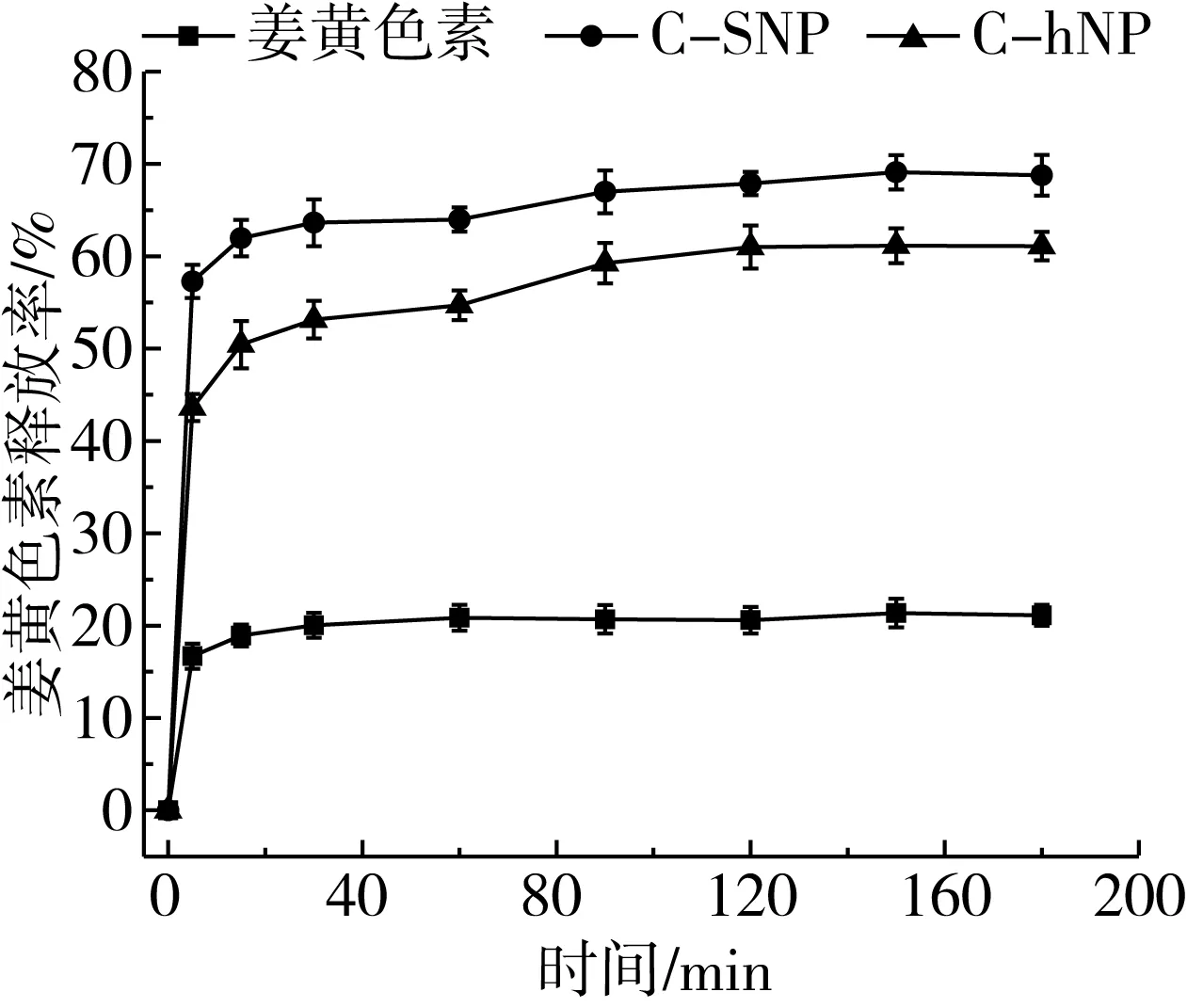
图3 体外模拟条件下姜黄色素的溶解释放特性
如图3所示,对于天然姜黄色素,在模拟胃液消化结束后,仅有约21%的姜黄素以溶解状态释放出来;在进一步模拟肠液消化过程,其溶出速率基本维持不变(P> 0.05)。由于天然姜黄色素在0.5%吐温溶剂中溶解度较低(约20%),并且在碱性pH的小肠环境中易发生降解,因此可以推断天然状态的姜黄色素生物吸收利用较低。当姜黄色素被复合纳米颗粒包埋后,其体外释放率明显增高,表明以溶解状态和分散纳米粒子状态存在的姜黄色素浓度明显增加,姜黄色素被人体胃肠道消化吸收利用的机会明显增加。在模拟肠液消化2 h后,实心和中空复合纳米颗粒的最大姜黄色素释放率分布达到69%和61%。中空纳米颗粒的姜黄色素释放率略低于实心纳米颗粒,这可能是因为部分姜黄色素分子被包埋在纳米颗粒内部,阻碍了其释放途径。这个结果还说明中空纳米颗粒相比实心纳米颗粒具有更高的药物控释能力。因此,两种复合纳米颗粒均显著地增加了姜黄色素的体外消化释放率。
3 结论
本实验采用反溶剂法,利用高粱醇溶蛋白与卡拉胶的相互作用,制备了两种类型的负载姜黄色素复合纳米颗粒。实验最佳条件为:芯壁比为1∶10,中空和实心纳米颗粒平均粒径分别为71 nm和135 nm,电位为-37.7 mV和-38.2 mV,包埋率分别为89.6%和84.1%,负载率分别为8.01%和7.49%。透射电镜显示中空复合纳米颗粒形成了内部较亮,外部较暗的形态结构;实心复合纳米颗粒整体规则,颗粒较大。红外光谱结果显示,相较于高梁醇溶蛋白,两种复合颗粒中部分波峰均发生蓝移,说明卡拉胶和姜黄素分子与蛋白质分子间有较强的静电以及疏水相互作用。两种复合纳米颗粒在30 d的贮藏时间内,平均粒径及PDI均未发生明显变化,表明稳定性较好。体外消化模拟实验结果表明,两种复合纳米颗粒均显著地增加了姜黄色素的体外消化释放率,但是中空纳米颗粒具有更高的控释能力。本研究结果为高粱及其副产物中醇溶蛋白的高附加值利用提供了一定的参考。

