实验室检测新方法的验证
张梦雪,李玉卡,王志恒,马玉涛,吴建利
(1.石家庄市畜产品质量监测中心 050000;2.新乐市农业农村局 050000;3.石家庄市鹿泉区农产品综合质检站 050000)
实验室在进行检测活动时,需要控制很多关键要素,目的都是为了保障实验结果的准确性和有效性, 检验方法的控制是其中一个关键环节。 根据RB/T 214-2017《检验检测机构资质认定能力评价 检验检测机构通用要求》 中要求:“在使用标准方法前,应进行验证”。 那么方法验证的定义是什么? 范围包括哪些?如何进行方法验证,步骤包括哪些? 验证的各项技术参数及其要求是什么? 下面我们进行一一讨论与分析。
1 方法验证的定义与范围
根据RB/T 214-2017《检验检测机构资质认定能力评价 检验检测机构通用要求》、GB/T 32465-2015《化学分析方法验证确认和内部质量控制要求》、GB/T 27404-2008《实验室质量控制规范 食品理化检测》、GB/T 27417-2017 《合格评定 化学分析方法确认和验证指南》、NY/T 1896-2010 《兽药残留实验室质量控制规范》可知,方法验证是指实验室在引入方法前,通过进行核查,提供客观有效的证据证明实验室能够满足方法规定的要求,正确地运用该方法,以确保实现所需的方法性能。 如果原方法发布机构修订了该方法,应根据需要重新进行验证。 其范围主要是标准方法,包括国际标准、国家(或区域性)标准、行业标准、地方标准、标准化主管部门备案的企业标准[1-4]。
2 方法验证的步骤
2.1 立项研讨
实验室首先应当集合技术负责人及相关技术骨干对此项目进行立项研讨,详细探讨此项目的预期用途、适用范围、开展的必要性、客户的要求等[5]。 明确项目的立项必要性,同时对此项目开展工作进行初步分工,预先准备进行人员、设备、试剂耗材及环境条件的工作。
2.2 标准方法收集
业务办公室标准查新负责人应当对确认立项项目进行标准方法收集,选择符合规定的标准方法,同时保障标准现行有效[6]。 与检测室相关人员进行沟通,根据立项目标,选择适宜的、尽可能符合目前检测条件的标准方法,经技术负责人确认后,移交相关人员。
2.3 熟悉标准
检测室、业务办公室承担本次新项目负责人应当尽快熟悉选定好的本立项标准,对标准关键点进行学习总结,同时整理需要配备的仪器设备、试剂耗材、环境保障设备。
2.4 人员培训
检测室、业务办公室承担本次新项目负责人负责对本室内人员进行培训, 保证抽样及检测人员可以满足项目标准方法需求, 确保本室内相关人员能掌握本标准方法的关键点, 可以正确、熟练使用本方法,并对方法结果进行正确评价[7]。
2.5 仪器设备及试剂耗材的配备
项目标准方法负责人负责检查各室需要的的仪器设备、试剂耗材,按照实际情况需求,检查已有仪器设备及试剂耗材能否满足项目标准方法需求, 缺少的仪器设备及试剂耗材报相关部门审核、购买。 其中仪器设备主要检查其检测器性能、精密度、检定校准情况、维护保养情况等是否满足需求;试剂耗材主要检查种类、纯度、有效期、验收情况等,其中包含标准物质的配备检查[7]。 确保本室仪器设备及试剂耗材能够满足项目标准方法正常开展使用[8]。
2.6 环境条件配置、环境保障设备
项目标准方法负责人负责检查本室内环境条件配置、 环境保障设备是否满足项目标准方法需要。 尤其是要确保满足方法中特殊需求,如样品保存过程冷鲜保存不可冷冻;检测过程因见光分解需要避光条件等。
2.7 编制检验检测规范、原始记录表格、检验检测报告格式
各室项目负责人负责分派任务,编制相应检验检测规范、原始记录表格、检验检测报告格式。
2.8 检验检测样品准备
业务办公室准备相应样品,下达技术练兵流程卡。
2.9 开展检验检测
检测室根据流程卡安排相应人员进行技术练兵, 检测项目标准方法的各技术参数,主要包括线性、检出限、定量限、准确度/回收率、精密度、选择性/特异性、稳定性、不确定度等[9-10]。 具体各项技术参数的测试要求见下文。 各项技术参数的结果直接影响本项目标准方法验证能否通过评审, 所以一般由技术骨干进行检测或技术骨干牵头检测。 检测过程中要做好原始记录的填写及各项技术参数的记录与计算,保证原始记录的真实可靠。
2.10 组织项目评审
应当组织技术负责人、 各室项目负责人及相关人员对项目各方面进行评审,包括人员、仪器设备及试剂耗材、环境保障、相关文件格式、原始记录,尤其是对检测过程中各技术参数指标是否满足项目标准方法需求,达到完成实验的目标[11]。 若各项均可达到要求,即可通过项目评审,此标准方法通过验证。 方法通过验证后,才证明实验室具备检测此方法的能力,可以申请扩项。
3 方法验证的各项参数及测试要求
3.1 线性
根据标准方法的要求, 标准物质一般使用单点校正或校正曲线校准。 如果分析方法采用校正曲线法进行分析物的定量,在方法验证中就需要进行曲线的线性测定。 可根据标准方法规定的浓度进行测定,一般含有5 个浓度点或6 个浓度点(不包括空白)。 若没有明确的浓度规定,可自行确定浓度范围,一般会覆盖一个数量级,同时保证被测浓度在校准曲线范围内。 若此标准方法为定性或半定量方法,对校正曲线的要求相对较低,其线性回归方程的相关系数不应低于0.98,若此标准方法为定量方法,则其相关系数不应低于0.99[12]。
3.2 检出限及定量限
在一般方法中,均会给出方法检出限及定量限,即可在给定的方法检出限、定量限的基础上,对方法检出限、定量限进行验证,即使用空白基质按照方法要求添加标准物质,通过前处理方法进行处理,使用仪器对添加样品进行测定,验证给定的方法检出限及定量限,根据相关国家标准GB/T 32465-2015,分析结果应在给定的方法检出限±20%范围内。
若方法没有给出方法检出限及定量限, 则需要选择适当方法自行确认,如使用信噪比法、空白标准偏差法、校准方程适用范围法等。 如信噪比法:将添加的相应浓度的试样检测出的信号值与空白基质样品同时经过方法前处理, 上机后检测出的信号值进行比较, 若比例为3∶1 时确定相应的浓度为方法检出限;若比例为10∶1 时确定相应浓度为方法定量限。
在确定方法检出限与定量限时,检出限要求低于定量限,确定最低定量限时,应当考虑本项目的国家规定的最高残留限量,根据NY/T 1896-2010 规定,国家规定的禁用药物的方法定量限尽可能的低,一般至少低于或等于1μg/kg(L);国家规定了最高残留限量的,方法定量限一般推荐如下:
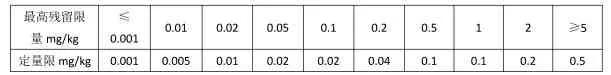
表1 方法定量限与国家规定最高残留限量关系
3.3 准确度
准确度是指待测样品按照方法处理后,上机,测量出的数值与“真值”的接近程度。 验证方法的准确度,可以通过在空白基质样品中添加适量浓度的标准物质测算回收率得到。 一般至少选取3 个添加浓度,禁用药物一般选取定量限、两倍定量限、十倍定量限3 个水平浓度, 有国家规定的最高限量值的一般选定量限、限量值、两倍限量值作为3 水平浓度,每一水平每批5 个样品,至少3 批。
回收率的建议偏差根据不同的国标有所不同, 可以根据具体需要,选择所依据的国家标准。不同标准回收率范围见表2、表3、表4。
3.4 精密度
精密度是指多个、多批的待测样品在相同的测量条件下,按照同种方法处理后,上机,测量出的数值互相的接近程度。 一般分为重复性(批内精密度)及再现性(批间精密度)。 重复性(批内精密度)是指在相同人员、时间、地点的实验条件下对同个试样测得的精密度;再现性(批间精密度)是指在不同地点、不同时间、不同人员对同个试样得的精密度。 一般精密度以相对标准偏差(变异系数)表示。
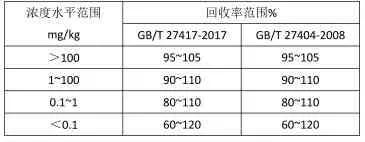
表2 GB/T 27417-2017 与GB/T 27404-2008 规定的回收率偏差范围

表3 GB/T 32465-2015 规定的回收率偏差范围

表4 NY/T 1896-2010 回收率偏差范围
在验证方法的重复性,即批内相对标准偏差时,同样采取同一空白基质样品添加一定浓度水平标准物质的方法, 禁用药物一般选取定量限、两倍定量限、十倍定量限3 个水平浓度,有国家规定的最高限量值的一般选定量限、限量值、一个合适的浓度作为3 水平浓度,每个浓度至少重复6 次,计算其变异系数[13]。验证重现性(批间相对标准偏差) 时,同样使用上述浓度,每个浓度至少重复6 次,至少进行3 批次实验,计算变异系数。 变异系数应当符合相关国家标准,表5 为NY/T 1896-2010 规定的批内变异系数及批间变异系数。
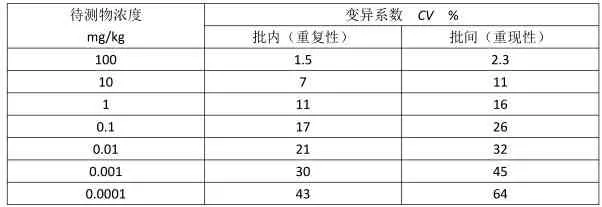
表5 不同待测浓度的协同试验精密度要求
3.5 其他
其他需要测定的参数如选择性/特异性、稳定性、不确定度、基质效应、测量区间等,具体项目根据实际情况进行验证。

