臭氧联合射频治疗腰椎术后疼痛综合征下肢痛的临床疗效*
闫芍药,黎巧玲,原伟莉,王锁良
西安交通大学第一附属医院 疼痛科(西安 710061)
腰椎术后疼痛综合征(failed back surgery syndrome, FBSS)多指因腰椎间盘突出症、腰椎管狭窄等引起的腰及下肢痛,经手术治疗后出现持续性或反复发作的慢性疼痛[1]。该病病因较复杂,临床表现也因人而异,如持续疼痛、功能障碍等[2]。FBSS患者通常会长期伴随疼痛状态,严重影响患者日常生活,降低患者生存质量[3]。目前,临床上对FBSS的治疗方法主要包括保守治疗、外科手术治疗及介入治疗[4]。尽管保守治疗可在一定程度缓解患者症状,但对临床症状较重的患者效果欠佳,通常作为一种辅助治疗手段。有研究[5]表明,手术治疗虽能松解瘢痕、黏连,但远期疗效欠佳,术后易复发瘢痕、黏连,引发下肢放射性疼痛等。因此,介入疗法因其具有安全、有效等优势渐渐得到广泛应用。有研究[6]表明,臭氧疗法可以有效缓解患者疼痛,安全性较高,但单一使用效果不理想;射频治疗作为一种新兴技术,可与臭氧治疗达到协同作用,提高临床疗效。为寻找治疗FBSS的有效手段,本研究选取了48例FBSS患者,分别采取单纯臭氧治疗及臭氧联合射频治疗,比较两组临床疗效,为临床提供资料。现报道如下。
1 资料与方法
1.1 临床资料
选取2018年4月至2019年2月西安交通大学第一附属医院收治的以下肢痛为主的FBSS患者共48例,以随机数字表法将其分为臭氧组和联合组,每组各24例。臭氧组男15例,女9例,年龄41~78(60.78±5.88)岁,平均病程(8.14±2.35)月;联合组男14例,女10例,年龄40~79(59.97±6.13)岁,平均病程(8.46±2.41)月。两组患者在性别、年龄、病程等比较,差异无统计学意义(P>0.05),具有可比性。纳入标准[7]:1)经腰椎CT或MRI确诊有腰椎间盘突出神经根压迫的症状,有腰椎手术病史;2)直腿抬高试验阳性;3)经常规保守治疗无效或效果不佳者;4)配合治疗,治疗期间未私自接受其他禁忌治疗;5)经本院伦理委员会批准,患者及病人家属同意并知悉本研究用途。排除标准:1)经X射线提示脊柱不稳、骨性椎管狭窄或椎间盘高度低于正常的40%;2)脊柱畸形、肿瘤、感染者;3)臭氧过敏者;4)严重内脏功能障碍或凝血功能障碍者;5)精神心理障碍等方面疾病者;6)中途退出治疗者。
1.2 治疗方法
给予两组FBSS患者常规检查,如血常规、生化、胸片等,经确认无明显介入手术禁忌。患者取仰卧位,CT定位椎间盘穿刺点,常规消毒、铺巾,1%利多卡因局部浸润麻醉后穿刺。臭氧组:15 mL臭氧(50 μg/L)缓慢注入,经CT观察臭氧均匀分布后拔针,局部按压止血,无菌胶布外贴穿刺点。联合组:15 mL臭氧(50 μg/L)缓慢注入,CT下臭氧均匀分布后,再患者观察10~15 min,若无异常情况,将穿刺针退至靶点,接入Baylis射频治疗仪,依次行阻抗测试、感觉神经刺激、运动神经刺激,确诊针尖周围无神经后可行射频治疗,分别设定70、75、80、85、90 ℃,各温度档治疗时间为20、40、60、120、180 s,术毕退出穿刺针,无菌胶布外贴穿刺点。所有患者均卧床休息3 d,3个月内禁止腰部负重及剧烈运动。
1.3 观察指标
疗效评价标准[8]:于患者治疗后7 d和治疗后1、3个月,以改良后的MacNab腰腿疼痛手术评价标准评估临床疗效,将临床疗效划分为4个等级:1)优:经治疗后临床症状及体征完全消失,恢复原来的工作和生活;2)良:经治疗后仍有轻微症状,活动轻度受限,无需镇痛药物,基本恢复工作和生活;3)可:经治疗后症状减轻,但活动受限,需服用NSAIDs药物,正常工作和生活受影响;4)差:治疗后临床症状及体征无改善,需服用镇痛药物,无法正常工作和生活。优良率=(优+良)例数/总例数。疼痛水平评价[8]:分别记录患者治疗前、治疗后7 d和治疗后1、3个月未服用镇痛药物时的视觉模拟评分(visual analogue scale,VAS)。VAS标准如下:1)1~3分为轻度疼痛;2)4~6分为中度疼痛;3)7~10分为重度疼痛。功能改善情况评价:分别于患者治疗前、治疗后7 d和治疗后1、3个月,采用Oswestry功能障碍指数法(Oswestry disability index,ODI)评价患者功能障碍程度[9],共有10个条目,每个条目0~5分,分数越高代表功能障碍程度越重,将10个项目得分累加,计算其占总分(50分)的百分比,即ODI值。记录两组患者治疗前、最后回访时的日本骨科学会评分(Japanese orthopaedic associatio,JOA),治疗期间不良反应发生情况,包括消化道不良反应、术后并发症等。
1.4 统计学方法
2 结果
2.1 两组治疗前后VAS评分比较
治疗时间和方法对患者VAS评分存在交互作用(P<0.05),治疗时间对患者VAS评分的影响差异有统计学意义(P<0.05),两组VAS评分呈现波动变化(P<0.05),联合组低于臭氧组(P<0.05)(表1)。

表1 两组患者治疗前后VAS评分比较(分,
2.2 两组治疗前后ODI评分比较
治疗时间和方法对患者ODI评分存在交互作用(P<0.05),治疗时间对患者ODI评分的影响差异有统计学意义(P<0.05),两组ODI评分呈现波动变化(P<0.05),联合组治疗后1、3个月的ODI评分明显低于臭氧组(P<0.05)(表2)。

表2 两组患者治疗前后ODI评分比较(分,
2.3 两组治疗前后JOA评分比较
治疗后两组患者的JOA均明显上升,且联合组治疗后3个月的JOA评分明显高于臭氧组(P<0.05)(表3)。

表3 两组患者治疗前后JOA评分比较(分,
2.4 两组治疗效果比较
联合组治疗后7 d、治疗后1个月的优良率与臭氧组同期相比差异无统计学意义(P>0.05),但联合组治疗后3个月的优良率明显高于臭氧组(P<0.05)(表4)。
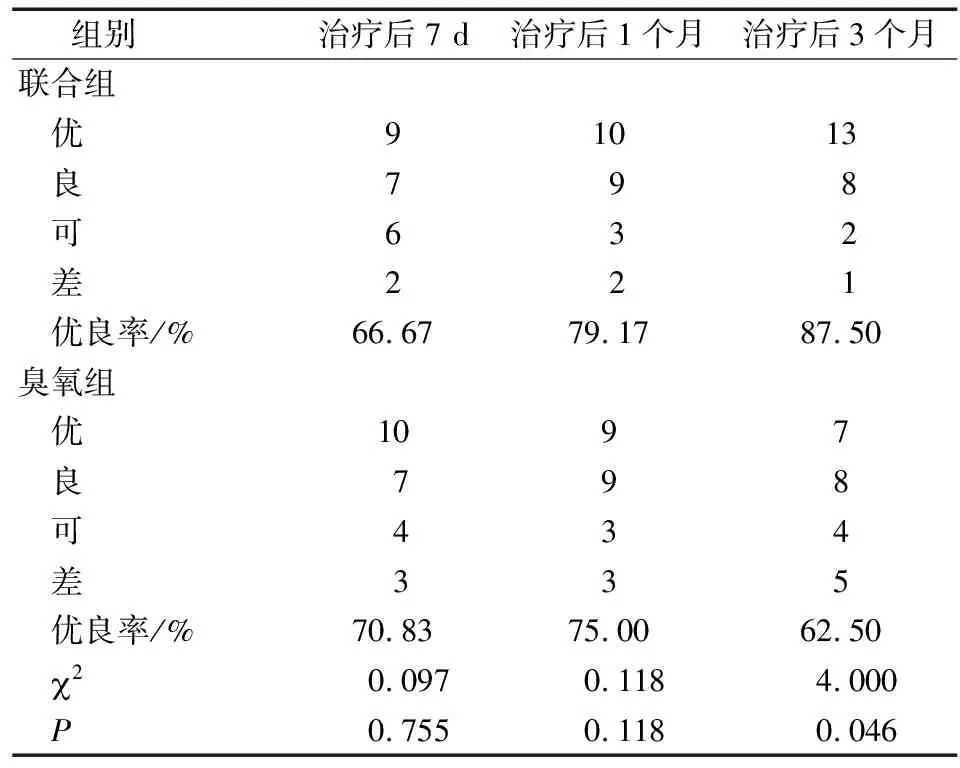
表4 两组患者治疗效果比较(n=24)
2.5 不良反应情况
治疗期间,两组患者均未出现消化道反应、感染、臭氧进入血管等严重不良反应情况。
3 讨论
近几十年来,越来越多的患者接受了开放腰椎手术,但部分患者仍在术后伴随腰或下肢疼痛症状,临床上将其归类为FBSS。有文献[10]报道,该病发病率5%~40%。FBSS病因较多,包含术中操作缺陷、突出复发、瘢痕组织硬化、自身排异反应等。下肢疼痛多由突出复发及瘢痕组织硬化引起[11]。由于患者通常伴随持续性疼痛,严重影响日常生活和工作,故优化FBSS治疗方案、改善FBSS患者生活质量不容忽视[12]。
本研究发现,采用单纯臭氧治疗或臭氧联合射频治疗以下肢痛为主的FBSS患者均有一定疗效,在术后短期(治疗后7 d、治疗后1个月),臭氧联合射频治疗与单纯臭氧治疗的优良率比较差异无统计学意义(P>0.05),但臭氧联合射频治疗的中期疗效(治疗后3个月)明显更好。臭氧治疗的原理是利用其强氧化性,使得髓核蛋白多糖发生氧化反应而变性,髓核组织坏死萎缩,从而减轻神经根压迫;同时利用其抗炎作用,减少炎性递质及其他致病物的产生、分解,消除无菌性炎症;此外,臭氧还有镇痛、促进关节软骨修复等作用[13]。李健辉等[14]研究显示,臭氧注射治疗腰椎间盘突出症患者后,患者椎间盘突出较术前明显改善,且治疗期间无不良反应,与本研究相符。提示臭氧疗法操作简单、创伤小、对腰椎间盘突出有良好的治疗作用。射频治疗的原理则是利用射频仪产生的高频率无线电波,作用于患者椎间盘组织,使其内部水分子共振产生热能,从而促使突出物内的胶原纤维成分收缩、气化,达到降低神经压迫、改善局部血液循环和缓解疼痛症状的目的[15]。云晨等[16]研究显示,脊柱内镜术后椎间盘源性脊神经后支疼痛患者经射频消融治疗后,疼痛情况、功能障碍改善明显,未见感染及并发症,论证了射频消融治疗是治疗脊柱术后椎间盘源性腰神经痛的有效治疗方法,操作安全,与本研究相符,提示射频治疗也是一种安全有效的介入手段。此外,王元等[17]研究显示,单纯臭氧注射治疗短期内改善外侧型腰椎间盘突出症患者的临床症状效果明显,但臭氧联合射频消融治疗的中远期优良率明显更优,与本研究结论一致,提示臭氧治疗与射频治疗可协同作用,提高以下肢痛为主的FBSS临床长期疗效。本研究对比了经联合疗法或单一臭氧疗法后患者VAS、ODI评分,结果表明,两组患者VAS、ODI评分呈现不同程度的波动变化(P<0.05),联合组治疗后1、3个月的VAS、ODI值较臭氧组同期下降更明显;治疗期间,未见严重不良反应。邵新军等[5]对FBSS患者行射频热凝联合臭氧盘内外注射治疗,结果显示,术后患者VAS、ODI值较术前明显下降,且无严重并发症发生,与本研究结论一致,提示臭氧联合射频治疗操作安全,且二者具有叠加作用,可有效缓解患者疼痛,改善运动障碍情况,是治疗以下肢痛为主的FBSS有效方法。此外,本研究显示,最后随访时(治疗后3个月),两组患者的JOA评分较治疗前均升高,且联合组的JOA评分高于臭氧组(P<0.05)。董俊球等[18]对下腰痛患者行椎管外射频热凝结合臭氧治疗,并随访患者治疗后3个月的恢复情况,结果表明,各类型患者的JOA 评分均较治疗前上升,与本研究结论一致,进一步证实了臭氧联合射频治疗对以下肢痛为主的FBSS治疗效果良好。
综上所述,臭氧联合射频治疗方案创伤小、操作安全,对以下肢痛为主的FBSS疗效明确。但本研究中存在样本量较少、随访时间短等不足,其远期疗效有待进一步考察。

