化学的空间思维及其教学
李梦雪 吴俊明


摘要:化学空间思维对了解物质的基本结构单元的空间关系及空间效应,包括基本结构单元间相互作用、基本结构单元对物质宏观性质的影响,以及宏观层面的晶体形状等问题有重要作用。界定了空间、空间思维、化学的空间思维,研究了化学空间思维发展的历史脉络,分析了化学教材中涉及化学空间的内容分布情况,讨论了化学空间思维的教学策略思路、化学空间思维的测量及训练方法。
关键词:空间思维;化学空间思维;化学空间思维教学
1 空间
1.1 作为科学名词的空间
作为科学名词的空间,是与时间相对的一種物质客观存在形式,两者密不可分。按照宇宙大爆炸理论,宇宙从奇点爆炸之后,宇宙的状态由初始的“一”分裂开来,从而有了不同的存在形式、运动状态等差异,物与物的位置差异度量称之为“空间”,位置的变化则由“时间”度量。空间由长度、宽度、高度、大小表现出来[1]。
空间是具体事物的组成部分,是具体事物具有的一般规定。眼睛可以看到、手可以触到的具体事物,都是处在一定空间位置中的具体事物,都具有空间的具体规定,没有空间规定的具体事物是根本不存在的[2]。
空间没有边界并且永远存在,即“空间无界永在”,被称为“空间公理”。
从经典物理学的角度看,物体存在运动的(有限或无限的)场所,即三维区域,称为(三维)空间。任何空间点都必然出现在当前时刻,是空间与时间的基本关系。根据狭义相对论中的四维时空概念,时空间隔是不变量,即时间和空间之间没有间隔,“空间永现于当前时刻”。
空间使事物具有了变化性:因为空间的存在,所以事物才可以发生变化。
从数学的角度看,空间是指一种具有特殊性质及一些额外结构的集合。具体地说,空间是“点”(即元素)的集合或具有某种几何结构的集合,例如n维空间、黎曼空间等等。
1.2 各种各样的空间
宇宙空间、物理空间、数学空间等等,都属于“作为科学名词的空间”的范畴。
通常所说的宇宙空间(Space),是指地球大气以外的空间,又称为外层空间或外太空,简称太空,一般定义为大约距离地球表面1000千米之外的空间。
物理空间是客观存在的真实的空间,有一定尺度的几何空间,可以客观测量。据说有十个维度,其中有七维空间卷曲在三维空间内部,是我们观察不到的。
数学中不存在单称为“空间”的数学对象,常见的空间类型有仿射空间、拓扑空间、一致空间、向量空间(或称线性空间)、度量空间、欧几里得空间、希尔伯特空间、射影空间、函数空间、样本空间、概率空间等等。在初等数学或中学数学中,空间通常指三维空间,常常涉及位置关系和度量问题。
空间概念引申到网络、信息学、思维学等领域,产生了网络空间、信息空间、思维空间等概念,它们代表目标事物的概念范围。事物的抽象概念是参照于空间存在的[3]。但是,这类“空间”(例如“情的空间”“知的空间”)跟作为科学名词的空间有所不同,要注意区分[4]。与此有关,所谓空间思维也有类似的情况:一类是指关于三维空间的思维,另一类是引申意义的,是指跳出点、线、面的限制去思考问题的思维方式,例如“多元思维”“全方位思维”“整体思维”或“多维型思维”等等。
在中药学与西方现代药学中,要通过对每一个分子计算一系列的分子描述符,用这些描述符来刻画其性质,并用这些数值作为一个个点构成多维空间,将化合物映射到多维空间中的一个点,通过判断多维空间中两点之间的距离来对比分子的相似性,进而推测两个化合物性质的相似性。通过一些特定选择的描述符来描述化合物的性质,所形成的多维描述符空间被称为化学空间[5]。显然,这里的“化学空间”也是引申性的,在其他领域未见采用。
2 空间思维
所谓空间思维,是指基于空间的属性和特点,着眼于事物的空间,在脑内进行的、对空间事物进行的一系列分析与判断、认知与操作的思维过程,包括确定物体的形状(空间分布)、位置、空间关系、动静态关系,通过想象和视觉化形成新的形状、位置、空间关系表象等等,是指向目标事物跟空间有关问题解决的间接和概括的意识活动。简单地说,空间思维是人脑中指向空间问题解决的间接和概括的认知活动。
跟对象形状、位置、空间关系有关的问题,空间概念及空间表征,对象的空间变换规则和变化规律是空间思维的基本内容。
空间思维能力涉及对空间的意义理解和表征,涉及形成空间内外结构与动静关系的表象,涉及形成有关问题,形成分析、解决问题的方案并获得答案。
3 化学的空间思维
化学的空间思维主要解决涉及微观层面的微粒空间分布/堆积情况和相互作用、对宏观性质的影响(寻找规律,如键长的影响、键角的影响)以及宏观层面的晶体形状等问题。为解决涉及微观层面的微粒空间分布/堆积情况的问题,常常需要建立模型,进行分析、模拟、旋转、透视、转换、匹配、表征等活动。为解决涉及微粒相互作用、对宏观性质的影响和宏观对称性问题,需要寻找有关规律,确定某些规则。
关于基本结构单元(组成微粒)空间关系及空间效应的思维,即化学的空间思维,以及关于基本结构单元(组成微粒)的思维、关于基本结构单元(组成微粒)之间相互作用的思维,都是化学物质结构思维的三大基本内容之一[6]。中学化学中空间思维的主要问题及解析过程如表1所示。
化学空间思维含旋转、透视、转换、匹配,寻找对称元素、定位、想象—寻找有关联系、表征等思维操作,以及空间信息的化学问题解决策略。
4 化学空间思维发展的历史追溯
对化学空间的研究最先开始于原子内部空间的研究。道尔顿(J. John Dalton,1766~1844)创立原子学说以后,很长时间内人们都认为原子就像一个小得不能再小的实心球。1869年发现阴极射线以后,汤姆生(Joseph John Thomson,1856~1940)发现了电子的存在,提出了原子的葡萄干面包模型。随后,原子放射性的发现促使卢瑟福(Ernest Rutherford,1871~1937)提出了原子行星模型。玻尔(Niels Henrik David Bohr,1885~1962)则在卢瑟福模型的基础上,提出了电子在核外的量子化轨道。
1811年阿伏伽德罗(Avogadro A.,1776~1856)提出分子概念后,化学家对分子的空间开始感兴趣,发现分子空间的研究涉及原子在空间中的位置,并与原子在分子中的成键情形与空间排列有关系。
分子空间的研究最先从分子内部相邻原子间联结的方式和次序的研究开始。原子间联结方式和次序的研究开始于分子结构式和化学键的研究。19世纪初,弗兰克兰(Frankland Edward,1825~1899)提出在分子中原子间按“化合价”结合,且这种“化学价”无正负之分。20世纪初,美国化学家路易斯(Gilbert Newton Lewis,1875~1946)提出“化學价”实质上是原子能够用来形成共用电子对的电子数,分子中除键合电子外,还经常存在未用于形成共价键的非键合电子(孤对电子)[7]。共价键的提出促进了溶液中、金属中原子间空间思维的发展,产生了离子键、金属键概念。
虽然分子结构式和化学键能够反映分子内或晶体内相邻两个或多个原子(或离子)间的联结,却是侧重于平面维度的联结,未能反映分子或晶体单独的、整体的形状分布。
随着贝采利乌斯(Jns Jakob Berzelius,1779~1848)于1830年发现了同分异构现象,人们开始逐渐意识到不同分子或晶体的空间形状不同,组成相同的分子可能具有不同的空间形状。不过此时大部分人都认为分子或晶体形状都是平面形的,即分子内或晶体内所有原子都处在同一个平面内。直到19世纪中叶至19世纪末,巴斯德(Louis Pasteur,1822~1895)、威利森努斯(Johannes Wislicenus,1835~1902)等人发现酒石酸、乳酸等有机化合物存在旋光异构现象,凯库勒(FriedrichA·Kekule,1829~1896)提出了碳四价的特殊性、有机物碳链结构、苯的环状结构……才将人们对分子内原子间的排列次序的注意力转移到了分子的立体形状。范特霍夫(Jacobus Henricus vant Hoff,1852~1911)针对有机物异构体现象在理论与实际中的不统一提出设想,把碳原子的价键看成直接指向一个四面体的各个角,碳原子位于四面体的中心。这样就把分子空间分布由平面推向立体,解释了许多由于原子的空间排列不同而引起的立体异构现象,为立体化学的形成奠定了基础[8]。之后,随着观察、实验方法的进步,发现大部分的化合物并非是平面结构,不同分子的构造不同;对于由成千上万个C—C单键所组成的高分子链,由于每个单键可以做不同程度的内旋转,分子内原子在空间的排布方式随之不断地变更而取不同的构象。
总体来看,人们逐步发现,原子内部呈现一定的空间结构;分子或晶体中原子不是杂乱无章排列在一起,而是按照一定规律结合,从而使分子或晶体在空间呈现出一定的几何形状,相同分子内原子的排列可能不同。
早期人类探索化学空间的思维过程有如下特点:
由经验归纳到假设检验再到实验论证。
从线式、平面的维度到立体的维度。
从构造(原子间的联结方式和次序)到构型(分子的空间形状)再到构象(有机化合物分子中,由C—C单键旋转而产生的原子或基团在空间排列的无数特定的形象)。
化学空间思维主要依赖于想象、模型、观察、实验、逻辑论证的手段和方法。
5 现代化学空间思维的发展与深化
早期化学空间思维更多地从定性分析的角度探讨微观层面的微粒空间分布和相互作用,虽然有实验事实作为观点的依据和支撑,但是缺乏严谨的理论依据和科学的定量分析手段。随着科学的进步与科学方法的发展,化学空间思维得以发展和深化。尤其是物理测量方法、量子力学、数学方法和计算机的运用,促使化学空间思维向着多元化、抽象化、理性化的方向发展。
例如,20世纪中叶,多种物理测量方法如X射线技术、电子衍射技术、分子吸收光谱、分子偶极运动、核磁共振等进入化学结构的研究领域,人们开始认识到化学空间是可以直接观察和测量的,通过这些物理测量方法可以比化学分析方法更快确定化学空间的形状和细节。威廉·亨利·布拉格(Sir William Henry Bragg,1862~1942)就利用X射线观察金刚石晶体中的原子排列,发现金刚石晶体中,每个碳原子与相邻的四个碳原子紧密结合,形成致密的三角锥结构,呈现一个正四面体的形状。化学家们还通过电子衍射法验证了环己烷的非平面结构,发现了直立键和平伏键的差异。
同时,量子力学的运用也加深了人们对化学空间的认识。薛定谔方程以及波函数的运用,揭示了原子结构、共价键和双原子分子结构的本质,以及原子轨道、分子轨道成键的过程。人们逐渐认识到微粒的空间分布、微粒间相互作用、晶体的形状等空间问题可以通过理论推演得出。化学家们推演出了用来判定分子空间分布的几何构型的理论。海特勒(Heitter,W.)、伦敦(London,F.)、鲍林(Pauling,L.)等人把量子力学理论应用到分子结构中,建立了现代价键理论;1932年,密立根(Mulliken)和洪特(Hund)从分子中电子空间状态的角度提出了分子轨道理论;后来,为了更好地解释分子的实际空间构型和稳定性,鲍林(Pauling,L.)在“电子配对”假设的基础上又提出了“轨道杂化理论”[9]。
几何方法、图论等数学方法的运用,促使化学空间思维改进了早期主要依靠几何想象推理的思维方式,如早期范特霍夫完全依靠几何推理,提出分子存在立体的空间分布。数学方法在化学空间思维发展中的运用,主要是借鉴其思维方式和分析解决问题的过程和方法。具体表现在以下两个方面。
首先是几何思维(对称、平移、空间坐标系等)的应用,其中应用较为广泛的是对称思维。在研究分子内部相同原子原子团的等效性、原子轨道成键过程中原子间总是尽可能沿着原子轨道最大重叠的方向成键[10]等问题时,可以用轴对称思维加以解释;在研究不同液体“相似相溶”现象以及分子极性时,可以用中心对称思维确定分子中的对称元素是否只交于一点(偶极矩是否为零)、分子中正负电荷中心是否重合,即分子是否有极性[11]。化学中还存在特殊的对称思维,如手性实际上涉及分子内是否有任意次映轴Sn等对称元素的对称性,可以用来解释分子的旋光性。对称思维对化学空间思维的启示和发展不仅局限于研究物质的静态性质,也可以用来解释分子在反应过程中的机理,从理论上分析,当一个化学反应的反应物和产物的分子轨道对称性一致时,反应就易于发生,不一致时,反应就难以进行。除对称思维外,还可以运用平移思维和坐标系思维研究晶体的空间结构,晶体是由完全等同的晶胞无缝平移堆积而成,晶胞具有相同的顶角、相同的平行面和相同的平行棱;可以用空间坐标系的方法来标注晶胞中原子的位置,用来判断平均每个晶胞中原子个数。
其次是图论思维的应用。化学中一直以来就常用图(式)来表示空间分布:从早期分子结构式到路易斯结构式,再到后来分子的空间构型、构象,晶体的空间点阵式。用图(式)不仅可以反映不同分子或晶体、相同分子间的空间形式、形状及细节,也可以表述反应步骤的复杂序列(如玻恩图)。
以上种种方法运用在化学空间研究中,使得化学空间思维逐步细致和丰富。但是,由于不同微粒具有不同的质量、体积以及电荷、变形等性质,化学空间研究不能单纯地只应用几何思维和物理测量等方法,还需要考虑到化学中特有的一些空间效应,如空间位阻、诱导、共轭,才能更完美地解释化学空间分布现象。
总的来看,现代化学空间思维的发展和深化表现出以下特点:
逐渐放弃了盲目性较大的猜想—验证的思维方式,测量—推演逐渐成为主导的思维方式。
由片面的思维方式逐步走向整体的思维方式。早期对物质空间接结构的认识比较片面,往往停留在想象层面,后来结合一些测量方法、数学方法、量子力学等,才逐渐认识到物质空间结构是内外相互作用、丰富的、具体的。
6 中学化学中的化学空间思维
现行中学化学教材中有关化学空间的内容分布情况如表2、表3[12]所示。大体上包含的内容有:
原子内部电子的空间排布。
分子的空间结构特点,包括原子间连接顺序、成键方式和空间排布。
化学键的类型、形成、与空间结构判断的关系。
晶体中构成微粒的空间排布方式。
有机化合物中存在的同分异构现象。
有机化合物基团之间的空间影响。
3.1 原子结构与元素周期律
认识原子结构,了解原子核外排布。能画出1~20号元素原子的原子结构示意图。教学中应注重运用实验事实、数据等证据素材,帮助学生转变偏差认识。
3.2 化学键
认识构成物质的微粒之间存在相互作用,结合典型实例认识离子键和共价键的形成,建立化学键概念。知道分子存在一定的空间结构。能判断离子化合物和共价化合物中的化学键类型。注重组织学生开展概括关联、比较说明、推论预测、设计论证等活动。
4.1 有机化合物的结构特点
知道有机化合物分子是有空间结构的,以甲烷、乙烯、乙炔、苯为例认识碳原子的成键特点。能辨识常见有机化合物分子中的碳骨架和官能团。能搭建甲烷和乙烷的立体模型。通过模型拼插等活动引导学生认识有机化合物中碳原子的成键特点、价键类型和简单分子的空间结构。
4.1 有机化合物的结构特点
知道有机化合物存在同分异构现象。能写出丁烷和戊烷的同分异构体。通過模型拼插等活动引导学生认识有机化合物中碳原子的成键特点、价键类型和简单分子的空间结构。
模块2 物质结构与性质1.1 原子核外电子的运动状态
了解有关核外电子运用模型的历史发展过程。知道电子的运动状态(空间分布及能量)可通过原子轨道和电子云模型来描述。能说明微粒粒子的运动状态与宏观物体运动特点的差异。
能结合能量最低原理、泡利不相容原理、洪特规则书写1~36号元素基态原子的核外电子排布式和轨道表示式,并说明含义。引导学生反思已有理论模型的局限,建立新的原子结构模型。借助科学史的故事和素材多角度展示人类对微观结构的认识过程,促进学生对科学本质的理解。
2.2 共价键本质和特征
认识原子间通过原子轨道重叠形成共价键,了解共价键具有饱和性和方向性。知道原子轨道的重叠方式,共价键可分为σ键和π键等类型;共价键的键能、键长和键角可以用来描述键的强弱和分子的空间结构。能根据共价分子的结构特点说明简单分子的某些性质。借助事物模型、计算机软件模型、视频等多种直观手段,充分发挥学生搭建分子结构、晶体结构模型等活动的作用,降低教学内容抽象性,促进学生对相关内容的理解和认识。
2.3 分子的空间结构
结合实例了解共价分子具有特定的空间结构,并可运用相关理论和模型进行解释和预测。知道分子的结构可以通过波谱、晶体X射线衍射技术进行测定。知道分子极性与键的极性、分子的空间结构密切相关。能根据给定的信息分析常见分子空间结构,能利用相关理论解释简单的共价分子的空间结构。借助事物模型、计算机软件模型、视频等多种直观手段,充分发挥学生搭建分子结构、晶体结构模型等活动的作用,降低教学内容抽象性,促进学生对相关内容的理解和认识。
2.4 晶体和聚集状态
了解晶体中微粒的空间排布存在周期性,认识简单的晶胞。能从微粒的空间排布及其相互作用的角度对生产、生活、科学研究中的简单案例进行分析。借助事物模型、计算机软件模型、视频等多种直观手段,充分发挥学生搭建分子结构、晶体结构模型等活动的作用,降低教学内容抽象性,促进学生对相关内容的理解和认识。
3.2 认识物质的空间结构可以借助某些实验手段来测定。通过这些手段所获得的信息为建立物质结构模型或相关理论提供支撑。能说明原子光谱、分子光谱、聚集态等不同尺度上结构特点对物质性质的影响。选取与现实生活与科学前沿密切相关的案例,促使学生认识研究物质结构的价值。通过查阅文献、听专家讲座、观看化学影视资料等多种途径开展教学,开阔学生的视野,激发学生探索物质结构奥秘的热情。
模块3 有机化学基础1.1 有机化合物的分子结构
认识有机化合物分子结构决定于原子间连接顺序、成键方式和空间排布,认识有机化合物存在构造异构和立体异构等同分异构现象。能辨识有机化合物分子中的官能团。能辨识同分异构现象,能写出符合特定条件的同分异构体,能举例说明立体异构现象。通过模型拼插或动画模拟建立对有机化合物分子结构的直观认识,利用物质结构的有关理论帮助学生理解有机化合物分子结构的特点,碳原子结构特征及其成键特征和分子空间结构的决定作用。
1.3 有机化合物中的化学键
认识有机化合物分子中共价键的类型、极性及其与有机反应的关系,知道有机化合物分子中基团之间的相互影响会导致键的极性发生改变,从化学键角度认识官能团与有机化合物之间是如何相互转化的。判断有机化合物分子中碳原子的饱和程度、键的类型,分析键的极性;能根据有机化合物分子的结构特征分析简单化合物的某些化学性质。通过对有机化合物性质的分析解释活动,引导学生体会官能团、碳原子的饱和性和化学键的极性的有机化合物性质的决定作用;结合典型案例认识有机化合物分子中基团间存在相互影响,并适当开展基于结构分析预测性质和反应的学习活动。
中学化学教学中如何培养化学空间思维
对化学课程标准中规定的空间思维内容及要求,要分别选择不同的教学策略和思路。具体地说,思路主要有三个:
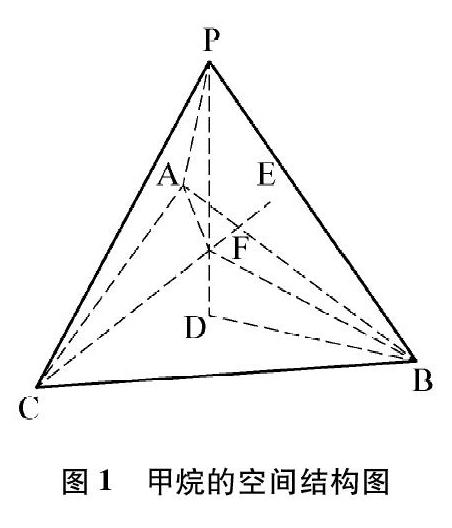
第一个思路是模型观察—想象—定位,主要应用于分子和晶体的空间构型、化学键的本质和形成,用实物模型、计算机虚拟图形、动画、分析模型等手段,展示分子的空间分布与排布。根据对模型不同角度的观察综合成对分子空间状态的完整想象,根据宏观模型的拼插定位分子内相邻原子的连接顺序,建立宏观模型与微观空间结构的联系,促使学生的思维脱离具体模型。以甲烷空间构型教学为例,给定一个甲烷的空间模型图(见图1),学生先观察各原子对应的位置,P、 A、 B、 C为氢原子位置,F为碳原子位置,先后通过点P作
第二个思路是经验归纳—假设检验—证据验证,主要应用于原子的空间分布上,根据先行认知经验作出假设,用实验事实、数据、科学史料等证据来验证,开展比较说明与逻辑推理。
第三个思路是测量—推断—表征,主要应用于同分异构体的空间排布,通过电子衍射法等技术手段判断有机化合物同分异构类型,用数学方法推断可能的同分异构体,并以一定表征方式如结构式体现。
空间思维对化学学习非常重要。
学生化学空间思维能力的高低可以通过一些工具来测量。Oliver-Hoyo和Sloan编制了“化学空间思维能力测试卷”,包含33个测试问题,认为化学空间思维能力包含视觉空间技能、多个视角、与记忆能力相关三个方面的主要因素[14]。Bodner和McMillen通过普渡旋转视觉化测试、寻找形状拼图测试等来测量《普通化学》课程中的空间能力[15]。谷进娟联系高中化学学习从空间知觉、空间定位、空间想象三个方面编制了相应的测试题目[16],可供教学时参考。
如何促进不同水平学生化学空间思维的提高和发展?笔者认为,首先要开发和使用相应的视觉化工具,如實物模型、虚拟图形、动画、分析模型等,促进学生对微粒整体空间分布/堆积情况和相互作用的想象,形成空间形象或空间印象;第二要借助结构示意图、二维和三维的结构表征,引导学生通过定位、心理旋转、透视、转换等思维操作理解空间伸展方向、原子的共面与共线等深度的空间信息;第三要结合物理测量方法、数学方法、信息技术(如虚拟现实技术)的应用来辅助学生提高空间分析技巧和空间思维的能力;第四要注意化学空间思维从平面到立体、从相互作用到空间分布、从构造到构型再到构象、从猜想验证到测量推理的发展顺序。
参考文献:
[1][4]https://baike.baidu.com/item/空间/55280?fr=aladdin.
[2]https://baijiahao.baidu.com/s?id=1611312621367609063&wfr=spider&for=pc.
[3]《数学辞海》委员会. 数学辞海·第6卷[M]. 太原:山西教育出版社,2002.
[5]https://baike.baidu.com/item/化学空间/6899746?fr=aladdin.
[6]吴俊明,钱秋萍. 化学的物质结构思维与教学[J]. 化学教学,2018,(11): 7~16.
[7]北京师范大学无机化学教研室等. 无机化学(上册)(第四版)[M]. 北京:高等教育出版社,2002:67.
[8]陈英成,蔡昆,冯光瑛. 立体化学研究的思维方式和科学方法[J]. 西安建筑科技大学学报(社会科学版),2000,(1):63~66.
[9]https://baike.baidu.com/reference/22176193/d455LEtne
Px5J6SXFqyPt6pHXfRVv5slCmhXwO-XwbKJLq2gIwxkZqO4aPni
8YObKBqtqV5RcigGtnw-dwsarVidJMAMjM0S5wz7-tZLQ6BKoeq_SQ.
[10]https://baike.baidu.com/item/最大重叠原理/9021045.
[11]陈年友. 对称性在基础化学中的作用[J]. 黄冈师专学报,1988,(3):67~70.
[12]中华人民共和国教育部定制. 普通高中化学课程标准(2017年版)[S]. 北京:人民教育出版社,2018.
[13]赵金和,兰翠玲,陈华妮. 从简单分子键角计算谈空间想象能力的培养[J]. 广东化工,2011,38(10):188+196.
[14][15]魏钊,王后雄. 化学学习中的空间能力研究[J]. 化学教学,2018,(3):12~17.
[16]谷进娟. 高中生化学空间思维能力的性别差异研究[D]. 武汉:华中师范大学硕士学位论文,2012.

