HPLC 法同时测定筋骨伤喷雾剂中7 种成分
李佳蔚,王 娇,徐家怡,程吉祥,刘 青,伍 庆∗
(1.贵州师范大学,贵州省山地环境信息系统与生态环境保护重点实验室,贵州 贵阳 550001;2.贵州远程制药有限责任公司,贵州 贵阳 550018)
筋骨伤喷雾剂是以贵州苗药赤胫散为主,配以地龙、赤芍、淫羊藿、制草乌、薄荷脑,55%乙醇浸制而成,具有消肿止痛、活血化瘀的作用,用于摔伤、扭伤等软组织损伤,方中君药赤胫散为蓼科植物赤胫散Polygonum runcinatumBuch.-Ham.ex D.Don var.sinenseHemsl.的干燥根茎,分布于四川、贵州、云南等地,其性寒,味苦、涩,无毒,具有活血舒筋、清热解毒之功效,主治劳伤腰痛、跌打损伤等[1-4],主要含有酚酸、挥发油[5-7],其中鞣花酸是一种有效的凝血剂[8],对多种细菌、病毒都有很好的抑制作用[9],能保护创面免受细菌侵入,防止感染,抑制溃疡[10];赤芍主要成分芍药苷具有广泛的抗炎作用[11-14],并且表现出明显镇痛活性[15];淫羊藿主要包括黄酮、生物碱、多糖等多种活性成分,其中淫羊藿苷、宝藿苷Ⅰ、朝藿定A、朝藿定B、朝藿定C 是黄酮类代表成分,具有促进骨骼发育的作用,可提高骨密度,增加骨强度[16],上述7 种成分药效均与筋骨伤喷雾剂功能主治一致。
然而,现行筋骨伤喷雾剂质量标准对君药赤胫散仅有TLC 定性鉴别[17],而定量指标仅为赤芍中芍药苷[3],过于简单,难以有效控制产品质量。为了进一步发挥中药多组分的协同作用,保证产品质量均一、稳定、可控[18-20]。本实验建立HPLC 法同时测定筋骨伤喷雾剂中芍药苷、鞣花酸、朝藿定A、朝藿定B、朝藿定C、淫羊藿苷、宝藿苷Ⅰ的含有量,以期为该制剂质量标准建立提供理论依据和数据支撑。
1 材料
1.1 仪器 Agilent 1100 高效液相色谱仪(配置在线脱气机、四元泵、自动进样器、DAD 检测器)、Agilent 色谱工作站(美国Agilent 公司);CH-250超声波清洗机(北京创新德超声电子研究所);HH-4 数显恒温水浴锅(邦西仪器科技有限公司);XS-105 电子天平(瑞士梅特勒-托利多公司);移液枪(20~200、100~1 000 μL,德国Eppendorf公司)。
1.2 试剂与药物 芍药苷(批号wkq18032104)、鞣花酸(批号wkq18020502)、朝藿定A(批号wkq17040509)、朝藿定B(批号wkq17032809)、朝藿定C(批号wkq17040701)、宝藿苷Ⅰ(批号wkq16081303)对照品均购于四川维克奇生物科技有限公司;淫羊藿苷(批号110737-200414)对照品购于中国食品药品检定研究院。筋骨伤喷雾剂(100 mL/瓶,贵州远程制药有限责任公司,批号20181003)。乙腈、甲醇为色谱纯;甲醇、正丁醇、磷酸二氢钾为分析纯;水为超纯水(自制)。
2 方法与结果
2.1 色谱条件 Agilent C18色谱柱(150 mm×4.6 mm,5 μm);流动相乙腈(A)-0.05 mol/L 磷酸二氢钾(B)-甲醇(C),梯度洗脱,程序见表1;体积流量1.0 mL/min;检测波长0~23 min 时230 nm,23~54 min 时254 nm,54~137 min 时270 nm;柱温35 ℃;进样量10 μL。
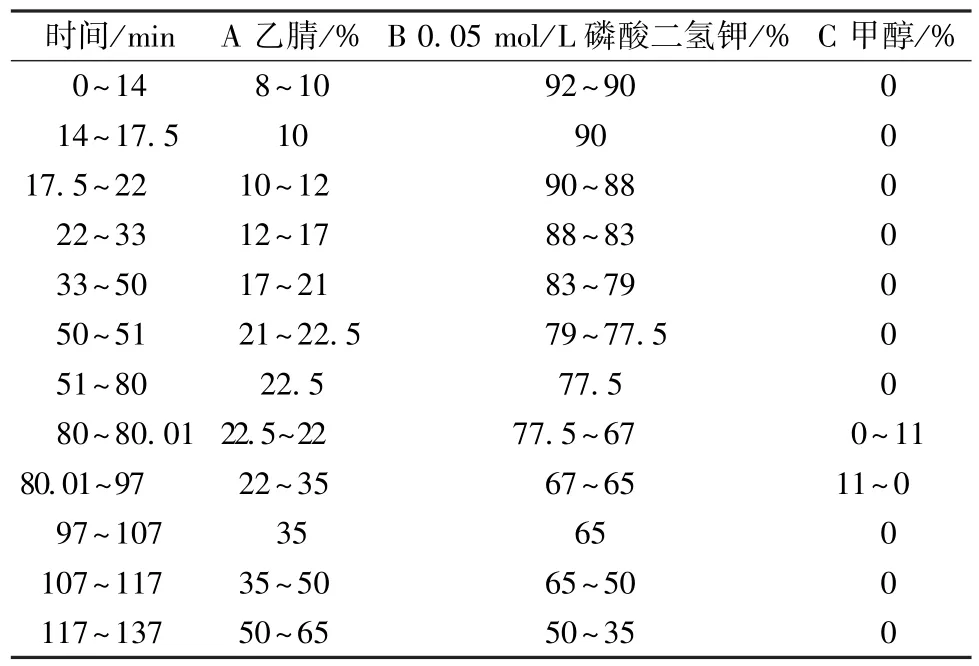
表1 梯度洗脱程序Tab.1 Gradient elution programs
2.2 溶液制备
2.2.1 对照品溶液 精密称取芍药苷、鞣花酸、朝藿定A、朝藿定B、朝藿定C、淫羊藿苷、宝藿苷Ⅰ对照品适量,甲醇溶解制得质量浓度分别为4.000、2.400、1.500、1.200、0.900、1.180、0.900 mg/mL,精密量取适量,甲醇稀释,即得(质量浓度分别为0.529、0.322、0.034、0.022、0.050、0.056、0.029 mg/mL)。
2.2.2 供试品溶液 精密吸取本品5 mL,置于蒸发皿中蒸干,精密加入5 mL 水溶解,溶解液转移至分液漏斗中,10 mL 水饱和正丁醇溶液萃取2次,取上层澄清液置于蒸发皿中蒸干,甲醇溶解后定容至10 mL 量瓶中,滤过,取续滤液,即得。
2.2.3 阴性样品溶液 按照本品处方及生产工艺,分别制备缺赤胫散、赤芍、淫羊藿的阴性样品,按“2.2.2”项下方法制备,即得。
2.3 方法学考察
2.3.1 系统适用性试验 精密吸取对照品、供试品、阴性样品溶液各10 μL,在“2.1”项色谱条件下进样测定,结果见图1。由此可知,各成分色谱峰与相邻色谱峰的分离度均大于1.5,理论塔板数均大于5 000。
2.3.2 线性关系考察 精密吸取“2.2.1”项下鞣花酸对照品溶液0.134、0.335、0.671、1.010、1.340、1.675 mL,置于5 个5 mL 量瓶中,分别加入芍药苷对照品溶液0.132、0.331、0.661、0.992、1.322、1.653 mL,朝藿定A 对照品溶液275、220、165、110、55、22 μL,朝藿定B 对照品溶液225、180、135、90、45、18 μL,朝藿定C对照品溶液700、560、420、280、140、56 μL,淫羊藿苷对照品溶液600、480、360、240、120、48 μL,宝藿苷Ⅰ对照品溶液400、320、240、160、80、32 μL,甲醇定容,摇匀,在“2.1”项色谱条件下各进样10 μL 测定。以峰面积为纵坐标(Y),溶液质量浓度为横坐标(X)进行回归,结果见表2,可知各成分在各自范围内线性关系良好。

图1 各成分HPLC 色谱图Fig.1 HPLC chromatograms of various constituents
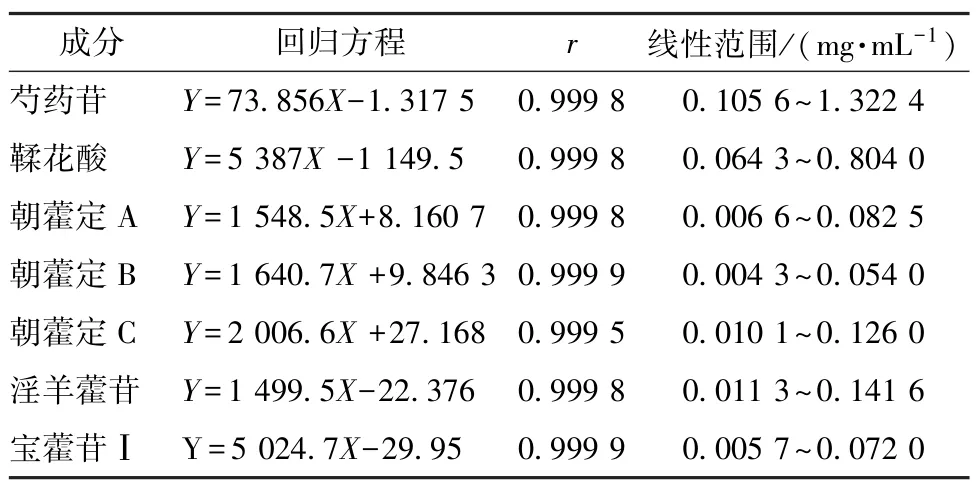
表2 各成分线性关系Tab.2 Linear relationships of various constituents
2.3.3 精密度试验 精密吸取“2.2.1”项下对照品溶液10 μL,在“2.1”项色谱条件下进样测定6 次,测得芍药苷、鞣花酸、朝藿定A、朝藿定B、朝藿定C、淫羊藿苷、宝藿苷Ⅰ峰面积RSD 分别为2.1%、2.9%、0.8%、1.6%、0.7%、0.6%、0.7%,表明仪器精密度良好。
2.3.4 重复性试验 取同一批本品(批号20181003),按“2.2.2”项下方法平行制备6 份供试品溶液,在“2.1”项色谱条件下进样测定,测得芍药苷、鞣花酸、朝藿定A、朝藿定B、朝藿定C、淫羊藿苷、宝藿苷Ⅰ含有量RSD 分别为1.4%、2.3%、2.8%、2.4%、2.4%、2.3%、2.3%,表明该方法重复性良好。
2.3.5 稳定性试验 取“2.3.4”项下供试品溶液,分别于0、2、4、8、12、24 h,在“2.1”项色谱条件下进样测定,测得芍药苷、鞣花酸、朝藿定A、朝藿定B、朝藿定C、淫羊藿苷、宝藿苷Ⅰ峰面积RSD 分别为2.2%、2.7%、2.5%、1.8%、2.2%、1.6%、0.9%,表明供试品溶液在24 h 内稳定性良好。
2.3.6 加样回收率试验 精密量取含有量已知的本品(批号20181003)9 份,每份2.5 mL,置于100 mL 蒸发皿中,精密加入适量芍药苷(0.500 mg/mL)、鞣花酸(0.448 mg/mL)、朝藿定A(0.024 mg/mL)、朝藿定B(0.037 mg/mL)、朝藿定 C(0.023 mg/mL )、淫羊藿 苷(0.152 mg/mL)、宝藿苷Ⅰ(0.011 mg/mL)对照品溶液,使高、中、低质量浓度对照品加入量与供试品中待测定成分量之比分别在0.5∶1、1∶1、1.5∶1 左右,按“2.2.2”项下方法制备供试品溶液,每种质量浓度3 份,在“2.1”项色谱条件下进样测定,计算回收率。测得芍药苷、鞣花酸、朝藿定A、朝藿定B、朝藿定C、淫羊藿苷、宝藿苷Ⅰ平均加样回收率分别为95.6%、96.0%、97.8%、94.5%、93.5%、96.7%、99.6%,RSD 分别为1.4%、1.8%、2.3%、1.5%、2.7%、2.4%、1.9%。
2.4 样品含有量测定 取3 批本品,按“2.2.2”项下方法制备供试品溶液,每批3 份,在“2.1”项色谱条件下进样测定,计算含有量,结果见表3。
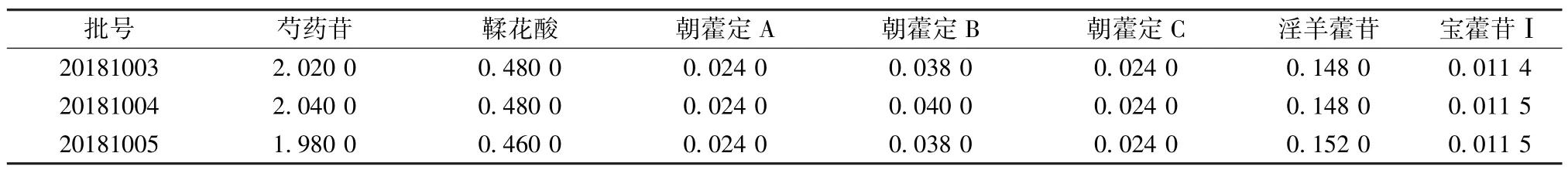
表3 各成分含有量测定结果(mg/mL,n=3)Tab.3 Results of content determination of various constituents(mg/mL,n=3)
3 讨论
3.1 供试品溶液制备方法选择 本实验考察了水饱和正丁醇、乙酸乙酯对各成分提取率的影响,发现后者萃取后不能检测出朝藿定A,故选择前者作为萃取剂。然后,又对萃取时pH 值(酸性、中性、碱性)、萃取次数(1、2、3 次)进行了考察,最终确定供试品溶液制备方法为中性纯净水加入10 mL 水饱和正丁醇萃取2 次。
3.2 色谱条件优化 本实验考察了流动相甲醇-水、乙腈-甲醇-水、乙腈-甲醇-0.05 mol/L 磷酸二氢钾,确定乙腈-0.05 mol/L 磷酸二氢钾-甲醇,此时各色谱峰分离效果最佳。再考察了检测波长,发现芍药苷、鞣花酸、淫羊藿苷最大吸收波长分别为230、254、270 nm,并且0~23 min 时230 nm、23~54 min 时254 nm、54~137 min 时270 nm 下各成分响应值较高,峰形良好,分离度理想。
4 结论
本实验建立HPLC 法同时测定筋骨伤喷雾剂中芍药苷、鞣花酸、朝藿定A、朝藿定B、朝藿定C、淫羊藿苷、宝藿苷Ⅰ的含有量,该方法准确可靠,可用于该制剂的质量控制。