淫羊藿苷不同给药途径对小鼠的急性毒性试验研究
陶荣品,姚文慧,丁选胜
(中国药科大学 基础医学与临床药学学院,江苏 南京 211198)
淫羊藿苷(Icariin,ICA)属于黄酮类化合物,是淫羊藿的主要活性成分之一,主要从小檗科植物淫羊藿、箭叶淫羊藿、巫山淫羊藿、柔毛淫羊藿或朝鲜淫羊藿的干燥茎叶中提取得到[1]。现代药理学研究表明,淫羊藿苷具有广泛的生物活性,包括调节机体免疫功能[2]、抗炎[3]、延缓衰老[4]、抗肿瘤[5]等,可以改善阿尔兹海默病、帕金森、抑郁症、骨质疏松、脑缺血、动脉粥样硬化、风湿病等多种疾病[6-8]。
目前关于淫羊藿苷药理学研究中给药方式有灌胃给药[9]及注射给药[10]两种,然而关于这两种给药方式的安全性评价研究尚不足。《中药、天然药物急性毒性研究技术指导原则》指出为尽可能观察到动物的急性毒性反应,可采用不同给药途径进行急性毒性试验[11]。因此,本研究参照急性毒性试验方法[11-13],开展淫羊藿苷灌胃及静脉给药急性毒性试验,以评价淫羊藿苷不同给药途径的急性毒性安全性评价。
1 材料
1.1 动物
淫羊藿苷灌胃给药急性毒性试验所用SPF 级ICR小鼠共20 只,雌雄各半,体质量为18 ~ 22 g,由扬州大学比较医学中心提供,许可证号:SCXK(苏)2017-0007,合格证编号为No.202008319。淫羊藿苷静脉给药急性毒性预试验所用SPF 级ICR 小鼠共40 只,雌雄各半,体质量为18 ~ 22 g,由扬州大学比较医学中心提供,许可证号:SCXK(苏)2017-0007,合格证编号为No.202008319。淫羊藿苷静脉给药急性毒性正式试验所用SPF 级ICR 小鼠共80 只,雌雄各半,体质量为18 ~ 22 g,由浙江省医学科学院提供,许可证号:SCXK(浙)2019-0002,合格证编号为No.20200803Abzz0118000188。
1.2 试验材料与仪器
淫羊藿苷(98%,HPLC,批号:18102102)购自扬子江药业集团有限公司;羧甲基纤维素钠(CMCNa,批号:F20111021)、聚乙二醇(批号:20200331)、二甲基亚砜(批号:20191112)均购自国药集团化学试剂有限公司;Tween 80(批号:180104064D)购自南京化学试剂股份有限公司;0.9%氯化钠注射液(批号:1806134)购自安徽双鹤药业有限责任公司;BS124S型电子天平(北京赛多利斯仪器系统有限公司)。
2 方法
2.1 淫羊藿苷灌胃给药急性毒性试验
取SPF级健康ICR小鼠20只,体质量为18 ~ 22 g,随机分为空白组、灌胃给药组,每组10 只,雌雄各半。《药物单次给药毒性研究技术指导原则》指出由于大多数中药的急性毒性可能相对较低,中药常常采用最大给药量法进行急性毒性研究[12],因此淫羊藿苷灌胃给药采用最大给药量法[13]。根据指导原则可知小鼠单次灌胃给药的最大体积是1 mL/20 g,由前期试验可知淫羊藿苷药物在羧甲基纤维素钠中的最大配制浓度是0.36 g/mL,早、中、晚各给药1 次,因此,小鼠淫羊藿苷灌胃给药的最大给药量为54 g/kg。
2.2 淫羊藿苷静脉给药急性毒性预试验
静脉给药急性毒性预试验正常组小鼠与灌胃给药急性毒性试验正常组小鼠共用。再取SPF 级健康ICR小鼠40 只,体质量为18 ~ 22 g,随机分为淫羊藿苷A 组(0 mg/kg,iv)、淫羊藿苷B 组(50 mg/kg,iv)、淫 羊 藿 苷C 组(100 mg/kg,iv)、淫 羊 藿 苷D 组(200 mg/kg,iv)。淫羊藿苷溶于5%的二甲基亚砜后,再依次加入40%聚乙二醇、5%聚山梨酯-80 和50%生理盐水,采用最大给药体积0.5 mL/20 g[13]。给药前,动物禁食12 h,给药后,观察14 d,根据各组小鼠毒性反应情况确定淫羊藿苷静脉给药最大非致死剂量(LD0)与绝对致死剂量(LD100)。
2.3 淫羊藿苷静脉给药急性毒性正式试验
根据预试验结果,可以初步确定50 mg/kg 为淫羊藿苷静脉给药LD0,200 mg/kg 为淫羊藿苷静脉给药LD100。按下式求算组间距(i值),确定正式试验的具体分组方案[12-13]。

经过计算,i= 0.120 412。求得的i值加上LD0对应剂量的对数值即得次低剂量组(第2 组)剂量的对数值,依次类推至最高剂量组(第n组)。计算得出正式试验各组给药剂量分别为50、66、87、115、152、200 mg/kg。
取健康ICR 小鼠80 只,体质量为18 ~ 22 g,随机分为空白组,尾静脉注射溶媒组,淫羊藿苷A 组(50 mg/kg,iv),淫羊藿苷B 组(66 mg/kg,iv),淫羊藿苷C 组(87 mg/kg,iv),淫羊藿苷D 组(115 mg/kg,iv),淫羊藿苷E 组(152 mg/kg,iv),淫羊藿苷F 组(200 mg/kg,iv),每组10 只,雌雄各半。将淫羊藿苷溶于5%的二甲基亚砜,再依次加入40%聚乙二醇、5%聚山梨酯-80 和50%生理盐水,采用最大给药体积0.5 mL/20 g。给药前,动物禁食12 h,给药后,观察14 d。
2.4 观察指标
给药后立即观察动物的毒性反应情况,包括外观体征、行为活动、精神状态、食欲、大小便及颜色、皮毛、肤色、呼吸以及鼻、眼、口腔、生殖器等有无异常分泌物。
记录每组动物死亡数量,按照孙氏改良寇氏法[14]计算淫羊藿苷静脉给药LD50,并对死亡动物进行解剖,观察小鼠的心、肝、脾、肺、肾等重要脏器的大小、形状、色状、色泽、质地,称取脏器重量,计算脏器系数。
2.5 统计学方法
用SPSS 22.0 软件进行数据分析,计量资料用均数 ± 标准差(±s)表示,两组间比较采用独立样本t检验,多组间比较采用单因素方差分析。以P<0.05 为差异具有统计学意义。
3 结果
3.1 淫羊藿苷灌胃给药急性毒性试验结果
3.1.1 灌胃给药对小鼠死亡率的影响 小鼠灌胃给予淫羊藿苷,采用最大给药量法,观察到给药后正常组小鼠与淫羊藿苷灌胃给药组小鼠活动正常,未出现痉挛、竖毛、震颤、呼吸抑制等中毒症状,且14 d内动物活动正常,均未出现死亡。
3.1.2 灌胃给药对小鼠体质量的影响 淫羊藿苷灌胃给药后,各组小鼠的体质量变化,见图1。与正常组相比较,淫羊藿苷灌胃给药后14 d 内,小鼠饮食饮水活动正常,体质量变化差异无统计学意义(P> 0.05),说明淫羊藿苷灌胃给药对小鼠体质量增长无影响。
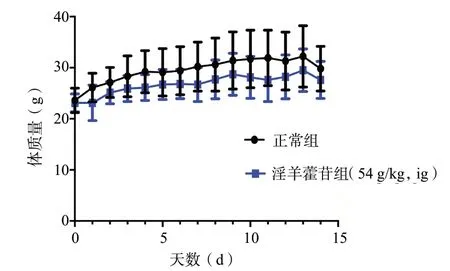
图1 给药后动物体质量变化图Fig.1 Change of animal body mass after administration
3.1.3 灌胃给药对小鼠脏器系数的影响 采用最大给药量法灌胃给予小鼠淫羊藿苷,14 d 后处死小鼠并进行解剖,观察正常组小鼠与灌胃给药组小鼠的心、肝、脾、肺、肾等重要脏器大小、形状、色状、色泽、质地等均无明显改变。各组小鼠的各脏器系数见表1,与正常组相比,小鼠的心、肝、脾、肺、肾的脏器系数差异无统计学意义(P> 0.05)。说明淫羊藿苷灌胃给药无急性毒性作用。
表1 淫羊藿苷最大给药量法灌胃给药对小鼠脏器系数的影响(± s,n = 10)Tab.1 Effect of intragastric administration of icariin by maximum dose method on organ coefficient in mouse(± s,n = 10)
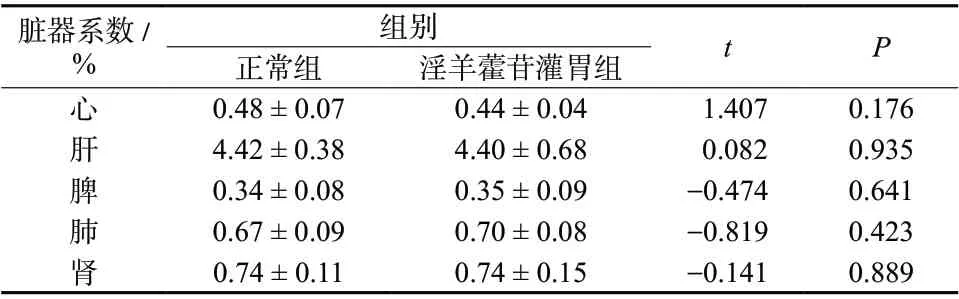
表1 淫羊藿苷最大给药量法灌胃给药对小鼠脏器系数的影响(± s,n = 10)Tab.1 Effect of intragastric administration of icariin by maximum dose method on organ coefficient in mouse(± s,n = 10)
脏器系数/%组别 t P正常组 淫羊藿苷灌胃组心 0.48 ± 0.07 0.44 ± 0.04 1.407 0.176肝 4.42 ± 0.38 4.40 ± 0.68 0.082 0.935脾 0.34 ± 0.08 0.35 ± 0.09 -0.474 0.641肺 0.67 ± 0.09 0.70 ± 0.08 -0.819 0.423肾 0.74 ± 0.11 0.74 ± 0.15 -0.141 0.889
3.2 淫羊藿苷静脉给药急性毒性试验结果
3.2.1 淫羊藿苷静脉给药急性毒性预试验 不同剂量给药组出现不同数量的动物毒性反应,中毒症状相似,表现为痉挛、竖毛、震颤、呼吸抑制等。各组小鼠死亡数及死亡率的试验结果,见表2,可以初步确定50 mg/kg 为淫羊藿苷静脉给药LD0,200 mg/kg为淫羊藿苷静脉给药LD100。

表2 各组小鼠死亡数及死亡率Tab.2 Death number and mortality of mouse in each group
3.2.2 淫羊藿苷静脉给药急性毒性正式试验
(1)静脉给药对小鼠死亡率的影响 淫羊藿苷静脉给药后各组小鼠的死亡数及死亡率见表3,尾静脉给药小鼠溶媒对照组未出现死亡,而给药组小鼠随着给药剂量增加,小鼠的死亡率逐渐增高,中毒的潜伏期逐渐缩短,中毒症状相似,出现痉挛、竖毛、震颤、呼吸抑制等。
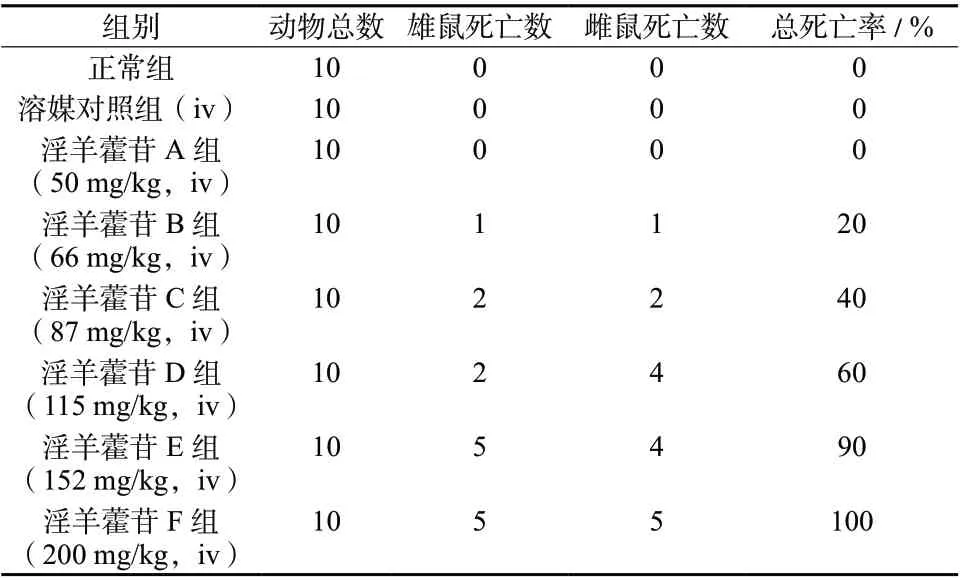
表3 各组小鼠死亡数及死亡率Tab.3 Death number and mortality of mouse in each group
(2)孙氏改良寇氏法计算淫羊藿苷静脉给药LD50此法是根据剂量对数与死亡率呈“S”型曲线所包涵的面积推导出死亡率为50%的剂量。当最小剂量组的死亡率为0%,最大剂量组的死亡率为100%时,计 算 公 式 为LD50= lg-1[Xm–i(∑P– 0.5)],L D50的95%可信限计算公式为lg-1(lgLD50± 1.96 ×Sx50),其中
i为组间距[11](相邻两组对数剂量的差值),Xm为最大剂量的对数,p为各组动物的死亡率(以小数表示),q为各组剂量存活率,n是各组动物数,Sx50是log(LD50)的标准误差。计算得出LD50为97 mg/kg,95%可信区间范围为83.80 ~ 112.28 mg/kg。
(3)静脉给药对小鼠脏器系数的影响 各组死亡小鼠即刻解剖,其余存活小鼠常规饲养14 d 后处死解剖。解剖后立即肉眼观察各组小鼠的心、肝、脾、肺、肾的大小以及形状、色状、色泽、质地等。观察发现,各组小鼠的重要脏器的外观大小、颜色、质地等均正常,未发现有明显的脏器病变。各组小鼠的脏器系数分析结果见表4,小鼠各组间的脏器系数差异均无统计学意义(P> 0.05)。
表4 淫羊藿苷静脉给药对小鼠脏器系数的影响(± s,n = 10)Tab.4 Effect of intravenous administration of Icariin on organ coefficient in mouse (± s,n = 10)
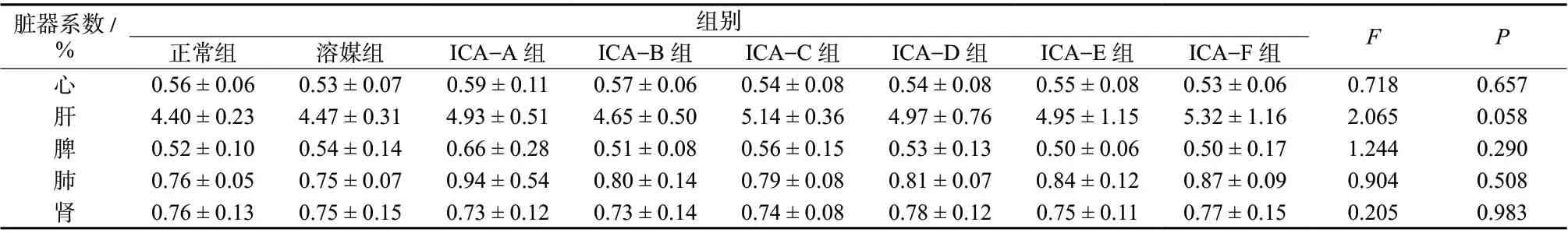
表4 淫羊藿苷静脉给药对小鼠脏器系数的影响(± s,n = 10)Tab.4 Effect of intravenous administration of Icariin on organ coefficient in mouse (± s,n = 10)
脏器系数/%组别 F P正常组 溶媒组 ICA-A 组 ICA-B 组 ICA-C 组 ICA-D 组 ICA-E 组 ICA-F 组心 0.56 ± 0.06 0.53 ± 0.07 0.59 ± 0.11 0.57 ± 0.06 0.54 ± 0.08 0.54 ± 0.08 0.55 ± 0.08 0.53 ± 0.06 0.718 0.657肝 4.40 ± 0.23 4.47 ± 0.31 4.93 ± 0.51 4.65 ± 0.50 5.14 ± 0.36 4.97 ± 0.76 4.95 ± 1.15 5.32 ± 1.16 2.065 0.058脾 0.52 ± 0.10 0.54 ± 0.14 0.66 ± 0.28 0.51 ± 0.08 0.56 ± 0.15 0.53 ± 0.13 0.50 ± 0.06 0.50 ± 0.17 1.244 0.290肺 0.76 ± 0.05 0.75 ± 0.07 0.94 ± 0.54 0.80 ± 0.14 0.79 ± 0.08 0.81 ± 0.07 0.84 ± 0.12 0.87 ± 0.09 0.904 0.508肾 0.76 ± 0.13 0.75 ± 0.15 0.73 ± 0.12 0.73 ± 0.14 0.74 ± 0.08 0.78 ± 0.12 0.75 ± 0.11 0.77 ± 0.15 0.205 0.983
4 讨论
淫羊藿在《神农本草经》中被称作“仙灵脾”,《本草备要》也描述其“补命门,益精气,坚筋骨”,所以它具有补肝肾、强筋骨、祛风湿的功效,可用于治疗肾阳虚衰、阳痿遗精、风湿痹痛、筋骨痿软及肢体麻木[15]等症。淫羊藿含有黄酮类、多糖、木脂素、生物碱等成分[16],其中,黄酮类成分如淫羊藿苷是其主要活性成分[17]。现代药理学研究发现淫羊藿苷对免疫、骨代谢、神经、心血管系统等相关疾病均具有一定的改善作用[18]。
目前,淫羊藿苷药理学研究中采用灌胃给药和注射给药方式,因此,有必要对这两种不同给药方式的急性毒性试验进行研究。《中药、天然药物急性毒性研究技术指导原则》指出急性毒性试验指的是受试动物1 次或24 h 内多次染毒后观察其毒性反应的试验。给药途径不同,受试物的吸收速度、吸收率和暴露量会有所不同,因此需要采用不同给药途径进行急性毒性试验[11],通过急性毒性试验计算LD50,为后续药理学试验中剂量设计与分组提供参考。因此,本研究采用灌胃给药及静脉注射给药两种途径探究淫羊藿苷对小鼠的急性毒性反应,为其安全性评价提供依据。
前期关于淫羊藿苷小鼠急性毒性试验研究表明,小鼠灌胃给药最大给药量为28.8 g/kg,提示淫羊藿苷口服毒性小,临床剂量下用药安全[19]。本研究通过采用CMCC-Na 配制淫羊藿苷混悬液灌胃给药后发现淫羊藿苷对于小鼠的最大给药量可达54 g/kg。淫羊藿苷采用最大给药量法灌胃给药后发现给药组和空白对照组小鼠体质量正常增长,一般情况观察无明显异常表现,未见组织器官发生病变,脏器系数无显著性差异,动物无死亡,表明淫羊藿苷在此剂量下灌胃给药是安全可靠的。
淫羊藿苷静脉给药预试验结果初步确定给药最大非致死剂量LD0为50 mg/kg,绝对致死剂量LD100为200 mg/kg。正式试验中利用孙氏改良寇氏法计算得出淫羊藿苷静脉给药LD50为97 mg/kg,这表明淫羊藿苷静脉给药存在一定的毒性。
5 结论
本研究开展了淫羊藿苷两种给药途径的急性毒性试验研究,结果发现淫羊藿苷最大给药量法灌胃给药无法测出LD50,而静脉给药的LD50值为97 mg/kg。该试验结果为淫羊藿苷的安全性评价提供依据,同时也为其后续的药理学研究、机制研究等提供理论依据。但是本研究主要探讨了淫羊藿苷两种给药方式的急性毒性试验比较,而淫羊藿苷可能还存在慢性毒性、亚慢性毒性、生殖毒性、发育毒性等,因此对于淫羊藿苷的安全性评价需要对以上各毒性研究结果进行综合考虑。

