直接前方入路全髋关节置换术后是否放置引流管的对比研究
纪小枫,尚希福,李国远,程鹏,罗正亮,陈敏
(中国科学技术大学附属第一医院骨科,安徽 合肥 230001)
全髋关节置换术后是否放置引流管一直没有统一标准[1-2]。引流管放置的目的是减少血肿形成,促进切口愈合,降低感染风险。但放置引流管可能会增大出血量,造成输血需求增加。以上研究结果大多针对的是后外侧入路,对于直接前方入路,术后放置与不放置引流管又有什么不同呢?本文选取我科自2018年1月至2018年12月收治的50例直接前方入路全髋关节置换病例作对比研究,现报告如下。
1 资料与方法
1.1 一般资料 本组病例共50例,男28例,女22例;左髋27例,右髋23例;年龄29~87岁,平均(56.5±12.6)岁。纳入病例标准:股骨头坏死(Ficat Ⅲ、Ⅳ期),髋骨关节炎,髋关节类风湿性关节炎。排除标准:翻修手术,髋臼及股骨侧形态异常而手术难度增加者,凝血功能异常,血红蛋白低于10 g/L;血小板低于100×109/L;服用氯吡格雷、阿司匹林药物3个月以上。患者按入院顺序分为未放引流组与放置引流组各25例。两组患者的一般资料比较差异无统计学意义(P>0.05),具有可比性(见表1)。
1.2 治疗方法 手术均由同一术者完成,全身麻醉,采用侧卧位直接前方入路,从髂前上棘的下外方2 cm处向腓骨小头作纵行切口,止于股骨大转子外缘斜坡处。逐层切开皮肤、皮下组织,在阔筋膜张肌表面切开深筋膜,从阔筋膜张肌与缝匠肌间隙进入,将阔筋膜张肌及臀中肌牵向外侧,缝匠肌及股直肌牵向内侧,在股骨转子区显露旋股外侧动脉的升支,电凝结扎该分支动脉,显露关节囊,切除关节囊,处理髋臼周围的骨赘及盂唇,打磨髋臼后安装假体(前倾约20°,外展约45°),股骨侧按需松解部分外旋肌,扩髓后置入股骨假体,复位髋关节,生理盐水冲洗,再次检查结扎的旋股外侧动脉升支及其他部位是否有活动性出血,关闭切口。两组均安装生物型假体,术中给予生理盐水20 mL加氨甲环酸1.0 g关节腔注射。放置引流组放置自然引流管,需夹闭至第2天早上打开。术后均常规抗凝治疗。术后抗生素使用24 h,必要时延长至48 h。放置引流组24~48 h拔除引流管。
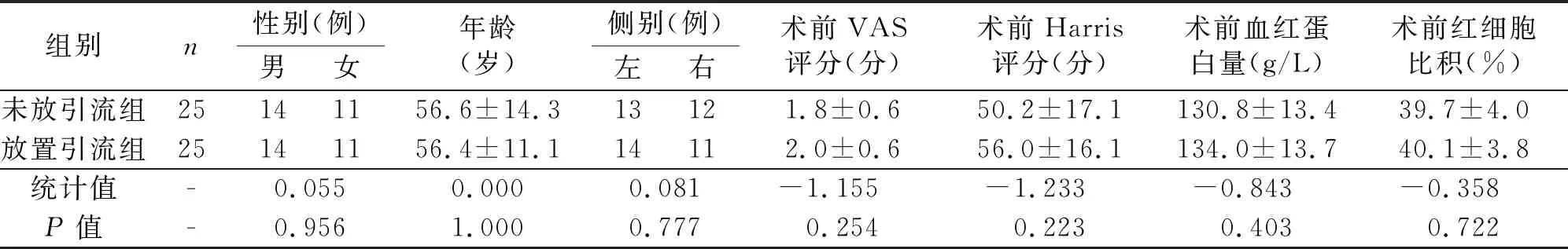
表1 两组患者术前一般资料比较
1.3 观察指标 记录术后24 h和术后第3天的血红蛋白量(hemoglobin,HGB)及红细胞比积(hematocrit,Hct)、疼痛视觉模拟评分(visual analogue scale,VAS)、切口愈合情况、术后感染情况、术后1年的髋关节功能评分(Harris评分)。
1.4 统计学方法 数据采用SPSS 19.0软件系统进行统计分析,计量资料采用独立样本t检验、计数资料采用卡方检验检测相关指标变化,P<0.05为差异具有统计学意义。
2 结 果
两组患者的术中出血量比较差异无统计学意义(P>0.05),术后24 h及第3天的血红蛋白量和红细胞比积、术后第3天VAS评分及术后1年Harris评分差异无统计学意义(P>0.05,见表2)。所有患者切口均一期愈合,均未发现浅表感染及深部感染。两组术后髋关节功能的优良率均为100%(Harris评分80分以上为优良)。
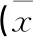
表2 两组患者术后相关资料比较±s)
3 讨 论
放置引流管的一个重要原因就是减少术后血肿的形成。人工全髋关节置换术由于手术显露比较广泛,损伤较大,臀大肌局部渗血,外旋肌断端出血,股骨近端髓腔的出血,以及假体周围空腔的形成,术后功能锻炼及早期下床活动,术后抗凝药物的使用等,使得术后血肿形成的风险大[3]。血肿的形成,一方面增大切口的张力,从而造成局部肿胀疼痛,甚至压迫神经,造成严重的临床后果[4];另一方面为细菌的繁殖提供了一个良好的培养基,增大感染的风险,并且后期血肿机化形成瘢痕组织,影响患者的关节功能恢复,降低患者的满意率。而直接前入路是肌间隙入路,是当前盛行的微创入路,它不损伤肌肉,只是必要时需要松解部分外旋肌,出血较少、手术创伤小、术后恢复快、并发症少,受到越来越多骨科医生的青睐[5]。所以本组病例中,未放置引流管并未增加术后血肿的风险。这点除了与入路有关外,术中的彻底止血也很关键,特别是旋股外侧动脉的升支,要结扎电凝止血,关闭切口前再次检查,如有活动性出血,需缝扎止血。另外,局部应用氨甲环酸,也是防止出血增多的另一重保护。
随着外科无菌技术的进步,手术技术的提高,手术时间的缩短以及抗生素的应用,全髋关节置换术后感染的发生率呈下降趋势。但由于THA术后感染治疗的周期长,花费高,耗费患者及医生巨大的精力,处理起来很棘手,是人工髋关节置换术后最具破坏性的并发症,给患者带来沉重的负担,仍然是当前关节外科医生需要面对的一个挑战性难题[6-7],所以THA术后感染的预防仍然是临床工作的重点。THA术后感染的因素是多方面的,有些学者认为放置引流管可以有效降低感染率。相反,有些学者认为术后放置引流管增加了术后感染的风险。Patel等[8]认为在初次全髋关节置换与全膝关节置换术(total knee arthroplasty,TKA)中,引流管的放置与术后感染的发生率有相关性,引流管每延长1 d,THA和TKA的术后感染率分别增加42%和29%。吴永光等[9]对334例全髋关节置换的随访研究中也认为引流管放置时间长是术后感染的独立危险因素。而Parker等[2]对8项研究作Meta分析,其中患者3 495例,切口3 689个,其结果表明引流管组与非引流管组在术后感染方面差异无统计学意义。而本组病例中,两组均未出现术后切口感染,表明引流管的放置与否和术后感染无明显相关性。认为引流管降低感染风险的理论基础是引流管可以促进积血的排出,防止血肿的形成,而正是因为血肿增加了感染的发生率。直接前方入路是真正的微创入路,术中及术后出血较少,一般不形成血肿,所以从这一点来说,直接前方入路术后不放置引流管也不会增加感染的风险。而认为放置引流管增加感染风险的学者认为,切口周围皮肤的细菌可能顺着引流管迁移进入切口,从而增加感染的机会。但Weinrauch等[10]认为引流管末端细菌培养对感染的诊断敏感性为0,特异性为99.2%,因此临床意义不大。金哲等[11]对84例单侧关节置换的前瞻性研究中也发现术后引流管尖端细菌培养结果用来诊断关节感染价值不大。
THA术后放置引流管可能增加了术后出血量,其理论基础是:髋关节周围血肿的形成具有填塞作用,而放置引流管阻碍了血肿的形成,破坏了这种填塞作用,引发新的出血,从而增加了术后出血量。同时,术后抗凝的使用以及早期下床活动也增加了出血的风险。Matsuda等[12]对40例(40髋)患者进行前瞻性研究,随机分成两组(各20例),结果发现引流和非引流对THA术后3 d血红蛋白量及红细胞比积影响差异无统计学意义。但高源等[13]使用全髋关节置换治疗82例股骨颈骨折患者,发现引流组在术后第3天,其血红蛋白变化值、总失血量均高于无引流组。Walmsley等[14]对552例全髋置换患者的前瞻性随机研究中发现,引流和非引流对术后血红蛋白的影响差异无统计学意义,但引流组术后输血率要明显高于非引流管组。其他一些学者研究也发现放置引流管确实增加了输血的需求[1-2]。但也有些学者研究发现引流和非引流对术后输血的需求差异无统计学意义[15]。本组病例中术后24 h及3 d的血红蛋白和红细胞比积差异无统计学意义,说明了引流管没有显著增加术后的出血量;术中出血无明显差异,术后也均无输血,说明引流管的放置与否对直接前方入路术后输血的需求没有影响。
综上所述,直接前方入路是一种有效的微创入路,损伤小,术中、术后出血少,不放置引流管术后效果满意,简化了术后护理流程,但并未增加术后疼痛及感染发生率,建议不用常规放置引流管。本研究的不足之处:一方面在于样本量较少,随访时间较短;另一方面缺少引流管放置对患者主观情绪的影响研究。希望以后进行更大样本的长期随访研究,观察是否放置引流管与并发症之间有无相关性。

