熔融氯化盐传蓄热性能的研究
李争光,刘向春,邓 韬,白宁娜,张叶雯
(西安科技大学材料科学与工程学院,西安 710054)
0 引 言
随着化石燃料的消耗和能源使用量的增加,科学家对太阳能的研究越来越多,高温传蓄热技术是太阳能高温利用的核心技术[1-2]。熔融盐作为传热蓄热的介质,相比于水、有机导热油、液态金属等具有高传热系数、高热稳定性、高热容量、腐蚀性小、导电性高以及价格便宜等优点而得到应用[3-4]。
氯化盐熔盐储热材料的制备及应用非常广泛,为了在此基础上提高氯化盐熔盐材料的热物性和热稳定性,急需寻找一种性能优异的复合材料。Gao等[5]实验发现二氧化硅纳米粒子的掺入将显著改变PMMA/SAN共混物的相图,从而增加相分离温度,提高使用温度;Li等[6]研究发现,微胶囊石蜡@SiO2相变复合材料熔融温度、潜热分别为56.5 ℃和45.5 J/g,复合材料的高储热能力和良好的热稳定性使其在实际应用中成为储存热能的潜在材料。从而发现二氧化硅在掺杂中对材料的比热容、稳定性、热导率等方面的性能有很大程度的提高,同时具有很好的储热性能。Xu等[7]在研究固体颗粒性质对填充床熔融盐温床蓄热系统热性能的影响时发现,碳化硅的导热系数最高,为120 W/(m·K)。故具有很好的储热性能和热导率的碳化硅也具有制备优异性能复合熔盐的潜能,同时碳化硅在一定温度时能转变成二氧化硅,这样既能研究他们之间的转化关系,探索从原料转变能否改变复合材料性能,进而做出比较,以求得到性能优异的熔盐储能材料。
目前太阳能传蓄热介质使用最多的熔盐体系是硝酸盐,但是它热导率低,在使用时容易产生局部过热的现象,熔盐不稳定,缓慢反应并有气体逸出,使混合物的熔点升高导致熔盐变质,需要定期更换熔盐,成本高,其最高使用温度较低为400~600 ℃[8]。氯化盐具有较大的相变潜热,液态时粘度很小,稳定性非常好,导热性能好,使用温度范围广和价格低廉等优势被普遍用作传热蓄热介质,但是其腐蚀性较大[9-10]。本实验以不同配比的二元混合氯盐为熔盐体系,对其进行热物性、热稳定性分析,然后在两种状态下来探索热腐蚀性的大小,以寻求使用温度较高,稳定性较好,腐蚀性小的配比。
1 实 验
1.1 复合熔盐传热蓄热材料的制备
取实验原料为NaCl、KCl、SiO2、SiC分别置于电热恒温干燥箱内干燥,设定温度为110 ℃,将物料烘干24 h,分别按表1比例称量好样品并充分混合,然后加适量的水使样品充分溶解,接着将适量的溶液置于刚玉坩埚中,利用马弗炉加热使坩埚中的水蒸发,然后加热至熔融状态并冷却至室温。然后将熔盐置于研钵中研磨分散并用200目筛过筛,获得熔盐样品,干燥后密封保存,利用上述方法配制其余的熔盐样品。
1.2 表 征
1.2.1 熔盐的热物性测量
利用型号为E4980A的综合热分析(TG-DSC)对复合熔盐的热物性进行测试,通过图像的峰位观察物相的变化及熔盐的使用范围和最高温度。
1.2.2 熔盐稳定性研究
采用X射线衍射仪(XRD)来测试熔盐的物相组成及使用差示扫描量热仪(DSC-200PC)推测熔盐发生的物化过程,通过对比来确定其稳定性。本实验XRD测试所使用的仪器型号是XRD-7000S型X射线衍射仪,X射线源是Cu(Kα),测试电压为40 kV,电流为30 mA,2θ变化范围为10°~80°,扫描速度是6°/min。通过重量法进行各个温度下质量的检测,以确定不同组分熔盐的质量损失率,从而判断熔盐的稳定性。采用金相显微镜(型号4X1)分析放入熔盐钢板的形貌,从而表征熔盐的腐蚀性。
2 结果与讨论
2.1 复合熔盐的组成及熔点的确定
图1为含10%SiO2的熔盐体系经800 ℃恒温50 h后的TG-DSC曲线。从DSC曲线可以看出,在84 ℃左右出现第一个吸热峰且对应的TG曲线的质量减少,说明此温度下熔盐脱去其物理吸附水,之后熔盐开始熔化并伴随着熔盐的挥发,在665 ℃时出现第二个吸热峰,且从TG曲线可以看出此温度时熔盐质量大幅减少,氯化物以离子对的形式分解被蒸发出去,同时排除了SiO2晶型转变的可能,说明此温度时熔盐熔化加剧,吸收一定的热量并伴随着熔盐的大量挥发,导致熔盐质量减少,所以熔盐的熔化峰值温度为665 ℃[11-12]。由于开始大量熔化的温度为362 ℃,一般熔盐的使用温度应该比熔点高50 ℃,因此SiO2复合熔盐的使用温度区间为412~715 ℃,宽于使用温度为720~1 000 ℃的传统NaCl-KCl体系,而且熔点更低[13]。从TG曲线可以看出熔盐的质量一直在减小,说明在整个反应过程中熔盐一经熔化便有挥发存在,683 ℃以上重量急剧减小,表明氯化物以离子对的形式蒸发,使熔盐发生了大量挥发,这一结果和TG-DSC测定结果一致。因此该熔盐体系能够稳定使用的最高温度为683 ℃。

图1 含10%SiO2的熔盐恒温后的TG-DSC曲线
Fig.1 TG-DSC curves of molten salt containing 10% SiO2at constant temperature

图2 含10%SiC的熔盐恒温后的TG-DSC曲线
Fig.2 TG-DSC curves of molten salt containing 10% SiC at constant temperature
图2为含10%SiC的熔盐经800 ℃恒温50 h后的TG-DSC曲线。从DSC曲线可以看出,在78 ℃时出现第一个吸热峰且TG曲线的质量减少,说明此温度下熔盐脱去物理吸附水。随后熔盐开始熔化并伴随着SiC的氧化,在363 ℃时熔盐与参比物的能量差为0,说明此温度时熔盐熔化吸收的热量与SiC氧化放出热的热量相同。在667 ℃时出现第二个吸热峰且熔盐质量大量减少,排除SiC氧化加剧的可能,因此此温度时熔盐剧烈熔化,其程度远大于SiC的氧化。一般熔盐的使用温度应该比熔点高50 ℃,因此SiC复合熔盐的使用温度区间为413~717 ℃,宽于传统的NaCl-KCl体系,而且熔点更低。从TG曲线上可以看出熔盐的质量一直在减小,说明在整个反应过程中熔盐挥发的质量始终大于SiC氧化增加的质量。对比图1和图2发现,在熔盐急剧挥发温度点以下,SiO2体系的重量减小约6%,而SiC体系重量减小约4%。在熔盐状态和用量等同、实验条件相同的条件下,后者复合熔盐重量减少较小,结合下文XRD物相分析说明SiC在此过程发生了氧化反应。在676 ℃之后,熔盐的质量大幅度减小,因此含10%SiC的熔盐能够稳定使用的最高温度为676 ℃。
比较图1、图2可知:在100 ℃之前,图1的DSC曲线和TG曲线的斜率皆大于图2,说明含10%SiO2的熔盐脱去物理吸附水的速度大于含10%SiC熔盐的速度;100 ℃之后,在相同温度下图2的DSC曲线对应的纵坐标均大于图1中DSC曲线对应的纵坐标,这表明在加热过程中SiC氧化放出的热量一部分用于补充熔盐熔化吸收的热量,因此含10%SiC的熔盐熔化需要外界供给的热量小于含10%SiO2的熔盐熔化需要的热量;图2的TG曲线的斜率小于图1的TG曲线的斜率,原因是SiC氧化时质量增加,相当程度的减小了熔盐挥发时质量的减小;含10%SiO2熔盐的最高使用温度大于含10%SiC的最高使用温度,这与文献得出的结论一致[14-15]。由于热分析结果影响因素很多,由其得出的热效应温度参数往往与实际温度偏差较大,因此,为较为准确的评价熔融盐的热稳定性,还采用了XRD及重量法作为对比检测手段。
2.2 熔盐热稳定性研究
2.2.1 熔盐储热过程质量损失
图3为四种不同配比熔盐在10 h的质量损失柱状图。由图可以看出:在700 ℃时含5%SiO2、10%SiO2、30%SiO2熔盐的质量损失率较小,分别为5%、10%、1%,说明在此温度下熔盐具有很好的稳定性,而含10%SiC熔盐的质量损失率为-2%,所测熔盐质量损失率为负数的原因是在加热过程中SiC氧化增加的质量弥补了熔盐熔融过程中挥发带来的质量损失。与图4对比可知在各个温度段加热2 h熔盐的质量均下降,说明在此温度下熔盐的熔融加剧,挥发出大量的盐,SiC氧化增加的质量不能弥补其挥发的质量损失。从8 h后熔盐的质量大幅度增加,表明此时SiC的氧化反应加剧占主导作用,故由数据分析可知熔融过程中伴随的氧化反应,使得SiC体系的熔盐的质量损失率很小,熔盐的质量变化相当稳定[16-17]。
图4为含10%SiO2的熔盐体系经重量法测质量损失率得出的质量损失曲线。由图可以看出:在700 ℃时熔盐的质量损失率较小,约10%,说明在此温度下熔盐体系相对稳定,可以在此温度下长时间使用,而目前单纯NaCl-KCl体系的稳定使用温度为500 ℃左右[18]。因此论文研究的SiO2复合熔盐体系比工业中NaCl-KCl体系的应用温度高约200 ℃。当温度增加为800 ℃、900 ℃时,熔盐的质量损失率明显增加,分别约为35%和75%。通过图还可以观察到,在700 ℃时不同时间段,熔盐的质量有所增加,而在800 ℃、900 ℃时熔盐质量持续减少,与图1的熔盐的TG曲线符合。
综上分析可知:相同的熔盐体系中,SiO2含量越高,熔盐的质量损失率越小,熔盐相对越稳定。含SiO2的熔盐,在整个熔融过程中,总体质量减小,质量损失率为正,但含SiC的熔盐,由于加热过程中SiC的氧化,总体质量增加,质量损失率为负。

图3 700 ℃下四种不同配比熔盐在10 h的质量损失
Fig.3 Mass loss of four molten salts with different proportions in 10 h at 700 ℃

图4 含10% SiO2熔盐的质量损失曲线
Fig.4 Mass loss curves of molten salt containing 10% SiO2
2.2.2 熔盐储热前后组成的变化
图5为含5%SiO2熔盐恒温50 h和热循环后的XRD谱。由图可知:恒温50 h和热循环后熔盐体系依旧为NaCl-KCl-SiO2,没有新的物相产生,说明含5%SiO2体系的熔盐经恒温50 h与热循环后性能保持基本稳定。

图5 含5%SiO2的熔盐恒温和热循环后的XRD谱
Fig.5 XRD patterns of the molten salt containing 5% SiO2at constant temperature and thermal cycle

图6 含10%SiC的熔盐恒温和热循环后的XRD谱
Fig.6 XRD patterns of the molten salt containing 10% SiC at constant temperature and thermal cycle
图6为含10%SiC熔盐恒温50 h和热循环后的XRD谱,由图可知:恒温50 h与热循环后熔盐体系均有新的物相SiO2生成,在加热过程中随着温度的升高,SiC被氧化生成SiO2,SiC的氧化会导致熔盐体系质量增加,这与图2中TG曲线下降缓慢和图6中总体质量损失率为负数的结果相符合。
图7为含10%SiO2熔盐恒温50 h与热循环后的XRD谱。由图可知:恒温50 h与热循环后熔盐体系均没有新的物相生成,即熔盐体系在恒温50 h和热循环后熔盐体系能保持基本稳定。
图8为含30%SiO2熔盐恒温50 h与热循环后的XRD谱。由图分析得:经恒温50 h与热循环处理后熔盐体系依旧为NaCl-KCl-SiO2,熔盐体系没有新的物相产生,与含5%SiO2和10%SiO2体系熔盐一样,在恒温50 h和热循环后熔盐体系性能保持稳定[19-20]。
由图5~图8可知:含SiC熔盐体系在加热过程中不稳定,SiC会被氧化成SiO2并伴随熔盐体系质量的增加;含SiO2熔盐体系无论SiO2含量的多少,熔盐体系在恒温和热循环处理过程中均没有发生化学反应且没有生成新的物相,熔盐的性能保持基本不变[21]。

图7 含10%SiO2的熔盐恒温和热循环后的XRD谱
Fig.7 XRD patterns of the molten salt containing 10% SiO2at constant temperature and thermal cycle
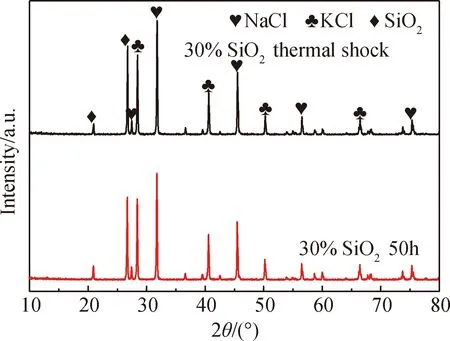
图8 含30%SiO2的熔盐恒温和热循环后的XRD谱
Fig.8 XRD patterns of the molten salt containing 30% SiO2at constant temperature and thermal cycle
2.3 复合熔盐材料的腐蚀性
采用质量相同的不锈钢片,经过9 h的腐蚀后比较图9~图12可得:在加热9 h的温度段内,无论是SiO2还是SiC熔盐体系,恒温50 h后的熔盐对316H不锈钢的腐蚀均比热冲击后熔盐对316H不锈钢的腐蚀大,这与金相照片相符,而且在9 h的温度段内恒温50 h和热冲击,含10%SiO2的熔盐体系对316H不锈钢的腐蚀均比含10%SiC熔盐体系对316H不锈钢的腐蚀小[22-24]。
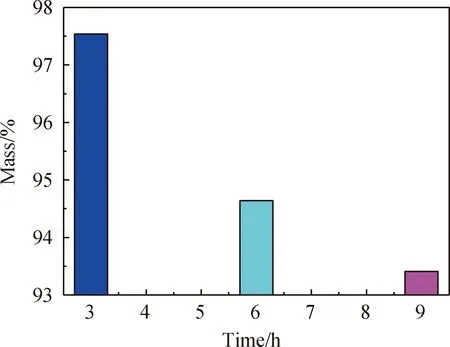
图9 恒温腐蚀50 h后含10%SiO2熔盐的质量损失率
Fig.9 Mass loss rate of molten salt containing 10% SiO2after 50 h of constant temperature corrosion

图10 热循环腐蚀后含10%SiO2熔盐的质量损失率
Fig.10 Mass loss rate of molten salt containing 10% SiO2after thermal cyclic corrosion
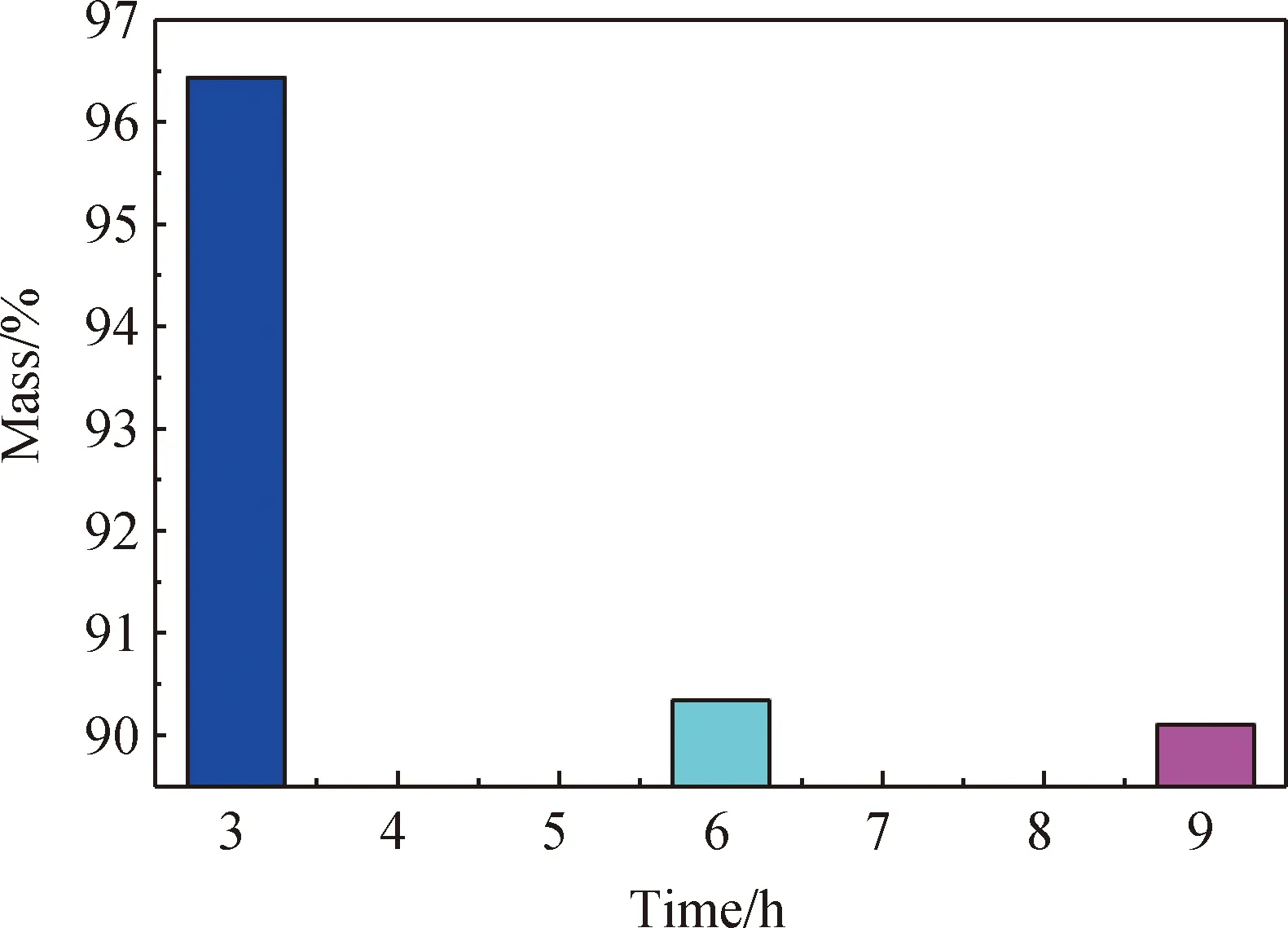
图11 恒温腐蚀50 h后含10%SiC熔盐的质量损失率
Fig.11 Mass loss rate of molten salt containing 10% SiC after 50 h of constant temperature corrosion
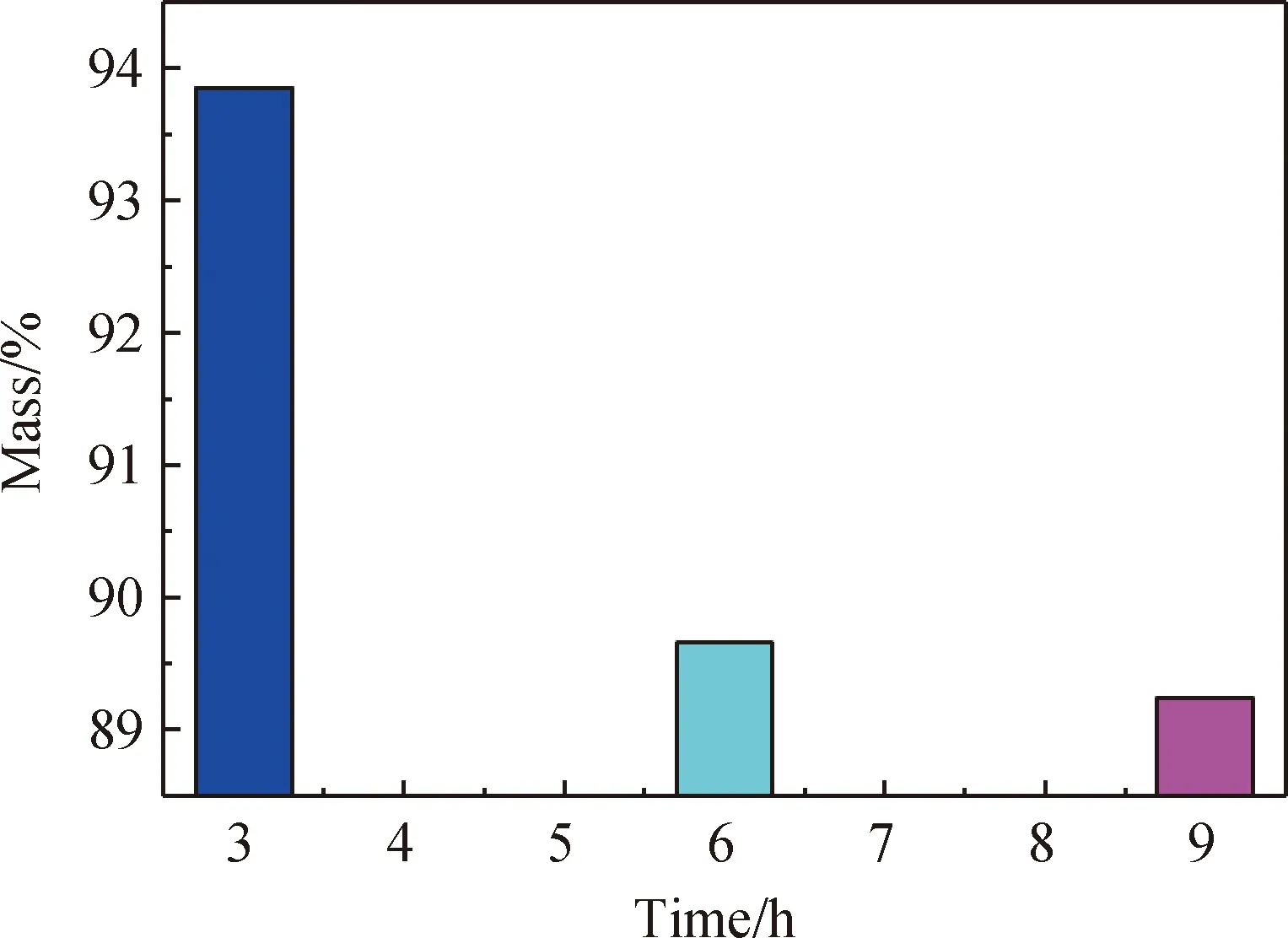
图12 热循环后含10%SiC熔盐的腐蚀质量损失率
Fig.12 Mass loss rate of molten salt containing 10% SiC after thermal cyclic corrosion
从图13中可以看出(注:形状不规则的片状暗色区域为腐蚀区域):316H不锈钢被腐蚀的面积由大到小分别为:图13(b)~(e)与图9~图12所测的质量损失相符合,并且可以观察出含10%SiO2的熔盐体系对316H不锈钢腐蚀的面积比较分散,而含10%SiC的熔盐体系对316H不锈钢腐蚀的面积比较集中。经过观察熔盐对不锈钢片的腐蚀面积和称量每组不锈钢的质量发现,称量结果和观察的腐蚀面积的大小,以及采用图像软件计算的腐蚀面积的大小基本一致[25-26]。

图13 不锈钢腐蚀的状态
Fig.13 Stainless steel corrosion state
3 结 论
(1)当SiC和SiO2熔盐体系的配比相同时,SiO2体系的最高使用温度比较高。
(2)经恒温50 h和热循环后,SiO2体系的熔盐反应前后没有产生新的物相,而SiC体系的熔盐在恒温50 h和热循环过程中被氧化生成SiO2。
(3)10%SiO2复合熔盐的使用温度区间为412~715 ℃,可稳定长时间(10 h)使用于683 ℃,宽于传统的NaCl-KCl体系,而且熔点更低。
(4)熔盐体系相同时,恒温比热循环处理后的熔盐对不锈钢的腐蚀大;当处理手段相同时,恒温处理和热循环中的SiO2体系的熔盐对不锈钢的腐蚀都比SiC的腐蚀小。

