聚乙二醇双官能基异端修饰的研究进展
张佳唯,廉明明,石立旺,张大鹏,唐淑坤,彭海生
·综述·
聚乙二醇双官能基异端修饰的研究进展
张佳唯,廉明明,石立旺,张大鹏,唐淑坤,彭海生
150076 黑龙江,哈尔滨商业大学药学院(张佳唯);163319 黑龙江,哈尔滨医科大学大庆校区药学院(廉明明、石立旺、张大鹏、唐淑坤、彭海生)
聚乙二醇(PEG)是一种惰性、非致癌性聚合物,目前是修饰生物活性分子和纳米粒子表面的首选聚合物之一[1-2]。聚乙二醇已被证明可以增强疏水性药物、蛋白质、核酸、脂质体的溶解性、提高稳定性和延长循环时间[3-4]。此外,PEG 还能通过增强渗透和保留(EPR)效应实现特异性肿瘤靶向治疗[5-6]。PEG 现已成为生物技术和生物医学界关注的焦点,广泛应用于大分子与表面的连接、药物和脂质体的靶向性、纳米颗粒功能化等诸多领域[7-11]。
近年来,科研工作者们将重点放在将两个不同生物活性部分连接到单个 PEG 链上,从而使靶向基团和治疗剂同时与单个 PEG 链连接[12-14]。我们把这种可以连接两个不同生物活性部分的 PEG 称为异双官能 PEG,异双官能 PEG 具有 X-PEG-Y 结构,其中 X 和 Y 是不同的功能基团,可以定向选择性连接不同基团,应用于大分子与表面的连接,位点特异性药物和脂质体的靶向性,以及纳米颗粒的功能化[15]。例如一端为甲氧基封端的 PEG(MeO-PEG)可以在其另一端修饰为巯基、羟基、氨基、羧基等活性基团。巯基可以进一步与金表面连接形成纳米金;羧基、氨基、巯基等活性基团可以与蛋白和多肽连接,提高其分子大小,增加水溶性,优化其特征的同时还可以保留其主要生物活性;异双官能 PEG 还可以与紫杉醇等疏水性抗癌药物连接形成疏水胶束,达到缓释作用;将异双官能 PEG 一端与靶向基因相连,另外一端与治疗剂相连,不仅可以延长药物在体内的循环时间减少给药频率,还可以实现药物的靶向治疗,具有提高药效的潜力[16-18]。这种异双官能的 PEG在有机合成、高分子合成、多肽合成[19]、药物的缓释控释以及靶向释药等方面均有广阔的应用前景。
异双官能 PEG 衍生物的合成方法可分为三类。第一类通过链式倍增法获得;第二类无需色谱纯化即可合成双官能聚乙二醇;第三类通过去环化法。本综述将根据以上三种分类方式介绍近年来异双官能基聚乙二醇的合成方法及研究进展。
1 通过链式倍增法获得双官能聚乙二醇
通过链式倍增法获得双官能聚乙二醇,是以被活化的四甘醇衍生物或设计一个连接起始物为起始合成原料,通过在四甘醇衍生物或连接起始物上逐步添加四甘醇、八甘醇或环氧乙烷等单体实现链长的延伸。2009 年英国研究人员将羟基保护基分为 Pd/H 条件下可以脱除的苄基保护基和酸性条件下可以脱除的叔丁基、三苯甲基保护基两种类型。以廉价易得的四甘醇作为原料,合成一端为苄基保护,另一端为三苯甲基(BnO-EG8-OTr)或叔丁基(BnO-EG8-OBu)保护的八甘醇。将以上合成化合物在 Pd/H 条件下脱除苄基生成 HO-EG8-OTr 或 HO-EG8-OBu,酸性条件下脱除三苯甲基或叔丁基生成 BnO-EG8-OH。将后者的剩余羟基用 Ts 活化生成 BnO-EG8-OTs,与前者发生 Williamson 成醚反应得 BnO-EG16-OTr 或 BnO-EG16-OBu,重复上述过程可得更高阶单分布聚乙二醇(PEG32, PEG48)[20](图 1)。
六氢三嗪衍生物在碱性环境中状态稳定且满足阴离子开环聚合(AROP)的要求。2016 年 Decker 及其同事对该结构的稳定性进行了实验和理论研究,发现在酸性介质中,六氢三嗪结构单元可水解成醛和胺,这使得该类官能团成为获得伯胺而不影响AROP 的有效保护基[21-24]。2019 年,Blankenburg 和 Frey[25]首次使用市售的羟乙基六氢三嗪(TrAz)作为阴离子引发剂与环氧乙烷进行开环聚合反应,由于六氢三嗪由 3 个相连的氨基组成,且含有 3 个端羟基结构,因此形成了具有六氢三嗪核的聚醚 3 臂星形聚合物。这些星形聚合物具有不耐酸的六氢三嗪核,酸性水解导致臂的开裂,便得到分子量范围为 3 ~ 15 kg/mol 的窄分子量分布(Mw/Mn < 1.1)的 α-氨基-ω-羟基异双官能聚乙二醇(NH2-PEG-OH)(图 2)。此种异双官能聚乙二醇在蛋白质和药物的表面修饰等方面是一种极具价值的生物结合结构。
2014 年,Székely 等[26]报道了一种获得异端、单分布的聚乙二醇新方法。以四甘醇为原料通过 3 ~ 4 步反应,合成了一端羟基 4,4'-二甲氧基三苯基甲基(Dmtr)保护,另一端羟基保留(DmtrO-EG8-OH)或对甲苯磺酰活化的八甘醇衍生物(DmtrO-EG8-OTs)。将 DmtrO-EG8-OH 与三溴甲基苯反应,得到末端 Dmtr 保护的八甘醇三臂 PEG 结构,将该结构作为起始原料,通过二氯乙酸脱保护及 DmtrO-EG8-OH 参与的 Williamson 成醚反应,实现链的扩增,重复上述反应得到单分散三臂聚乙二醇结构(单臂含56 个乙氧基重复单元)。链端衍生化后,通过温和氢解方法断裂核心三苄基结构,得到一端有羟基,另一端甲苯磺酰活化或叔丁基酯衍生的单分布 PEG 链(HO-EG56-OTs、HO-EG56-OCH2COOBu)。游离的单链 PEG 结构可进一步衍生成具有良好交联功能(-OH、-COOH、-NH2、-N3)的异端双官能单分散聚乙二醇(图 3)。

图 1 链式倍增法

图 2 α-氨基-ω-羟基双官能 PEG 的合成策略
2013 年,意大利Zona 等[27]报道了以廉价的四甘醇为起始原料,在碱性条件两端羟基与溴丙烯反应,高产率得到双溴丙烯修饰(收率93%)或单溴丙烯修饰产物(收率51%)。其中前者可通过 O3氧化再还原策略实现四甘醇的链增长,得到六甘醇,理论重复上述过程可得高阶单分布聚乙二醇。作者还应用单丙烯基修饰的四甘醇为原料,首先将游离羟基衍生成可参与点击反应的叠氮基,另一侧丙烯基实现了多种官能团转化,例如炔基修饰、乙酰基巯基、双乙酰基巯基、羟基、醛基、羧基、氨基、生物素修饰等(图 4)。
2 无需色谱纯化合成双官能聚乙二醇
近年来,已存在一些制备单分散聚乙二醇的方法。然而,由于聚乙二醇极性高,常规相色谱法难以纯化所需产物。因此,通常需要反相色谱法或凝胶渗透色谱法。这种冗长的纯化方法极大地限制了单分散 PEG 的可用性。为此,氟化物技术提供了许多方便的纯化方法,如氟化物液相萃取、氟化物固相萃取(FSPE)和氟化物高效液相色谱(FHPLC)。2014 年,武汉大学Li 等[28]设计了一个氟化物标签作为 PEG 中羟基的保护基团及氟纯化的分离标记。在合成过程中,成功地采用了氟化物固相萃取来简化纯化。首先以 4-(甲氧羰基)苯基硼酸和-(全氟辛基)-乙基碘化物为原料通过 3 步反应合成了含溴的氟化合物标签(Rf-Br)。市场上具有确定的分子量且价格合理的四甘醇被选为合成组成部分。用三苯基选择性地保护四甘醇中的一个羟基后,通过对甲苯磺酰基活化剩余羟基,合成改性的四甘醇 TrO-EG4-OTs。将改性四甘醇重复地连接到氟标记物上(图 5),便合成了具有 4n(n = 2,3,4,5)四甘醇单元的单分散 PEG。这样,所有的合成中间体都含有一个氟标签,在脱保护和偶联链延伸循环过程中,氟固相萃取(FSPE)和固相萃取(SPE)可以有效地纯化中间体。

图 3 基于 Homostar 合成单分散双官能 PEG

图 4 引入烯丙基来控制聚乙二醇单/双向延伸
2016 年,Wawro 等[29]报道了一种大规模合成单侧对甲苯磺酰修饰且单分散寡聚聚乙二醇的新方法,该方法无需色谱纯化,合成工艺简单,产率高,纯度高。单对甲苯磺酰聚乙二醇(HO-PEGn-Ts)是合成各种异端双官能聚乙二醇衍生物的重要中间体。以市售廉价的四甘醇为原料,通过非选择性的部分三苯甲基保护(步骤一),剩余羟基的对甲苯磺酰基活化(步骤二),以及与四甘醇发生的 Williamson 成醚反应(步骤三),和随后体系剩余羟基的 Ts 活化(步骤四)最终实现链增长。重复步骤三、四,可实现不同链长单端 Ts、单端三苯甲基修饰的寡聚聚乙二醇(TrO-PEGn-OTs,n = 8,12,16)与双侧三苯甲基修饰寡聚聚乙二醇(TrO-PEG-OTr)的混合物共合成。最后通过 Pd/C 加氢反应,脱除体系中全部三苯甲基,所得产物即为单侧羟基 Ts 保护的寡聚聚乙二醇(HO-PEGn-OTs,n = 8,12,16)与未修饰寡聚聚乙二醇(HO-PEG-OH)的混合物。应用这两类物质在有机相、水相中溶解性的不同,经由乙酸乙酯和盐水的液-液萃取实现 HO-PEGn-OTs 的高效分离与纯化。由于 HO-PEGn-OTs 两侧端基表现出完全不同的反应性,可以进一步修饰成异双官能团 PEG 化合物(图 6),如叠氮基、氨基、巯基、羧酸基团等。采用高效液相色谱法,对产品的单分散性进行了验证。它具有无色谱纯化和高纯度的特点,据报道,这是第一个生产不对称取代单分散聚乙二醇的无色谱合成方法。
2014 年,Zhang 等[30]介绍了一种利用简单、廉价的 THP(2-四氢吡喃)醚保护/脱保护策略快速、可扩展合成双官能化聚乙二醇的方法,THP 保护基在催化量的 TsOH 下便可脱除,脱保护后易于去除多余的水溶性双羟基 PEG 和 THP 醚(图 7),无需柱色谱分离,工艺简便。THP 在中性和碱性条件下具有良好的稳定性,是一种高效的醇保护基团。因而在中性或碱性条件下将合适的官能团(R = Ts, Bn)结合到单 THP 保护的 PEG 上形成双官能 PEG,单 THP 保护的四甘醇通过 NaH 脱质子化,并与甲苯磺酰化后单THP 保护的四甘醇偶联,得到链长延伸的八甘醇衍生物。这些结果表明,该方法可以快速合成单官能和双官能聚乙二醇衍生物,操作简便无需色谱纯化,且纯度高。

图 5 氟化物标签法合成双官能 PEG
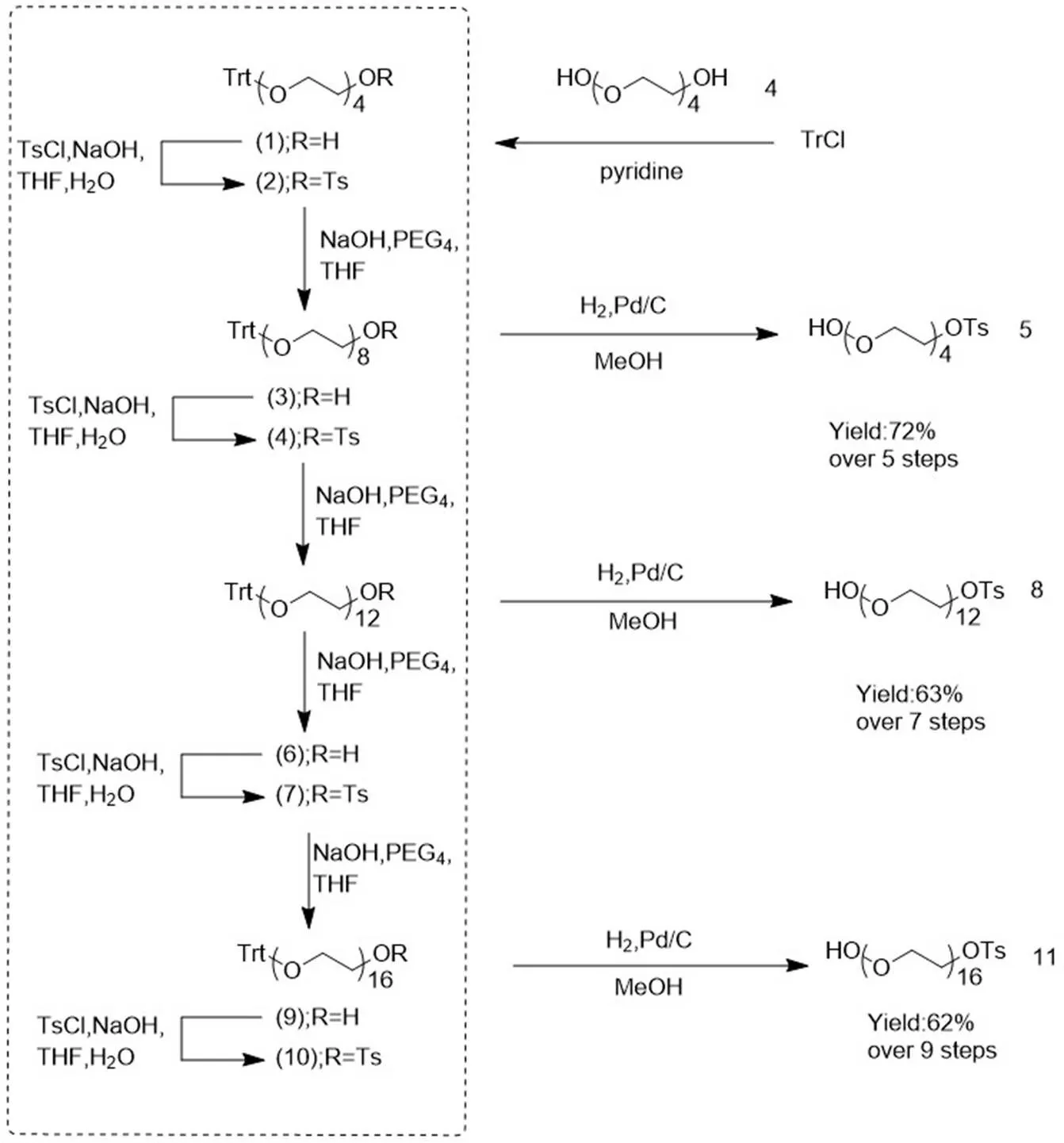
图 6 对甲苯磺酸盐杂化双官能 PEG 及其衍生物的合成

图 7 THP 醚保护/脱保护无色谱法合成单/双官能化 PEG

图 8 固相合成法逐步合成双官能 PEG
2017 年,美国Khanal和Fang[31]报道了一种用固相技术逐步合成单分散聚乙二醇及其衍生物的方法。以廉价的四甘醇为原料,通过 3 ~ 4 步反应,合成了一端羟基 4,4'-二甲氧基三苯基甲基(Dmtr)保护,另一端被对甲苯磺酰活化的四甘醇衍生物(DmtrO-EG4-OTs)。选择 Wang 树脂作为固体载体,首先用BuOK 等碱处理树脂,使其暴露出醇盐端基,DmtrO-EG4-OTs 单体通过 Williamson 成醚反应偶联到聚苯乙烯固体载体,接下来通过反复的 Williamson 成醚反应逐步加入 DmtrO-EG4-OTs 单体实现链延伸。最后用三氟乙酸将链扩增后的 PEG 从固体载体上切下,便以高收率获得了具有不同末端端基的 PEG 产品(图8)。
2009 年,La Ferla等[32]提出了一种新的、简单的、通用的 PEG 不对称化方法。该方法基于将聚乙二醇的一个末端羟基与固体载体连接,然后将剩余的自由羟基转化为不同的功能基团(Br、N3、SSH、OBn)或进行链的延伸。最终将其从固体载体上裂解,即获得双官能聚乙二醇。研究者使用硅胶 60(230 ~ 400 目)作为起始原料,用 3-氨基丙基-三乙氧基硅烷在 Dean-Stark 装置中回流,通过硅烷化反应制备了硅胶表面氨基修饰的甲苯悬浮液。随后用丁二酸酐处理固体载体,将表面氨基转化为游离羧基。作者将聚乙二醇通过酯键单端连接到固体载体上,再将余下的“自由”羟基进行官能化,最后将该官能化的聚乙二醇经氨甲醇溶液处理,从硅胶载体上裂解下来,最后用 MeOH 过滤和洗涤,滤液低压浓缩,无需进一步纯化程序即可获得产率良好的异端基聚乙二醇衍生物,所得化合物的剩余羟基可进一步改性以产生其他期望的双官能聚合物(图 9)。

图 9 硅胶负载型双官能 PEG 的合成
3 通过去环化制备双官能聚乙二醇
2014 年,Zhang 等[33]开发了一种基于大环硫酸盐(MCS)的单分散聚乙二醇(M-PEGs)及其单官能化衍生物的制备方法。将双侧醇羟基的 PEG 在 DIEA、DMAP 等碱性条件下缓慢添加 SOCl2使其转化成相应的环状硫酸盐,在开环反应中充当保护基团和活化基团。寡聚乙二醇的大环化提供的大环硫酸盐(最多 62 个乙氧基重复单元的大环)作为一系列单官能化 M-PEG 的通用前体。在不进行基团保护和活化的情况下,通过 MCS 开环反应,可以制备一系列 M-PEG。然后进一步通过 MCS 的一锅法亲核开环反应探索了 PEG 的单官能化,得到四甘醇(Nu-PEG-OH),将其与一系列含 O-、S-、C-、N- 和 F- 的亲核试剂反应,方便地制备了多种单官能化四甘醇(图 10)。这些开环反应表明 MCS 对亲核试剂具有高度反应性。因此,这种基于 MCS 的 PEG 单官能化方法为合成单官能化 PEG 衍生物提供了一种新的高效替代方法。
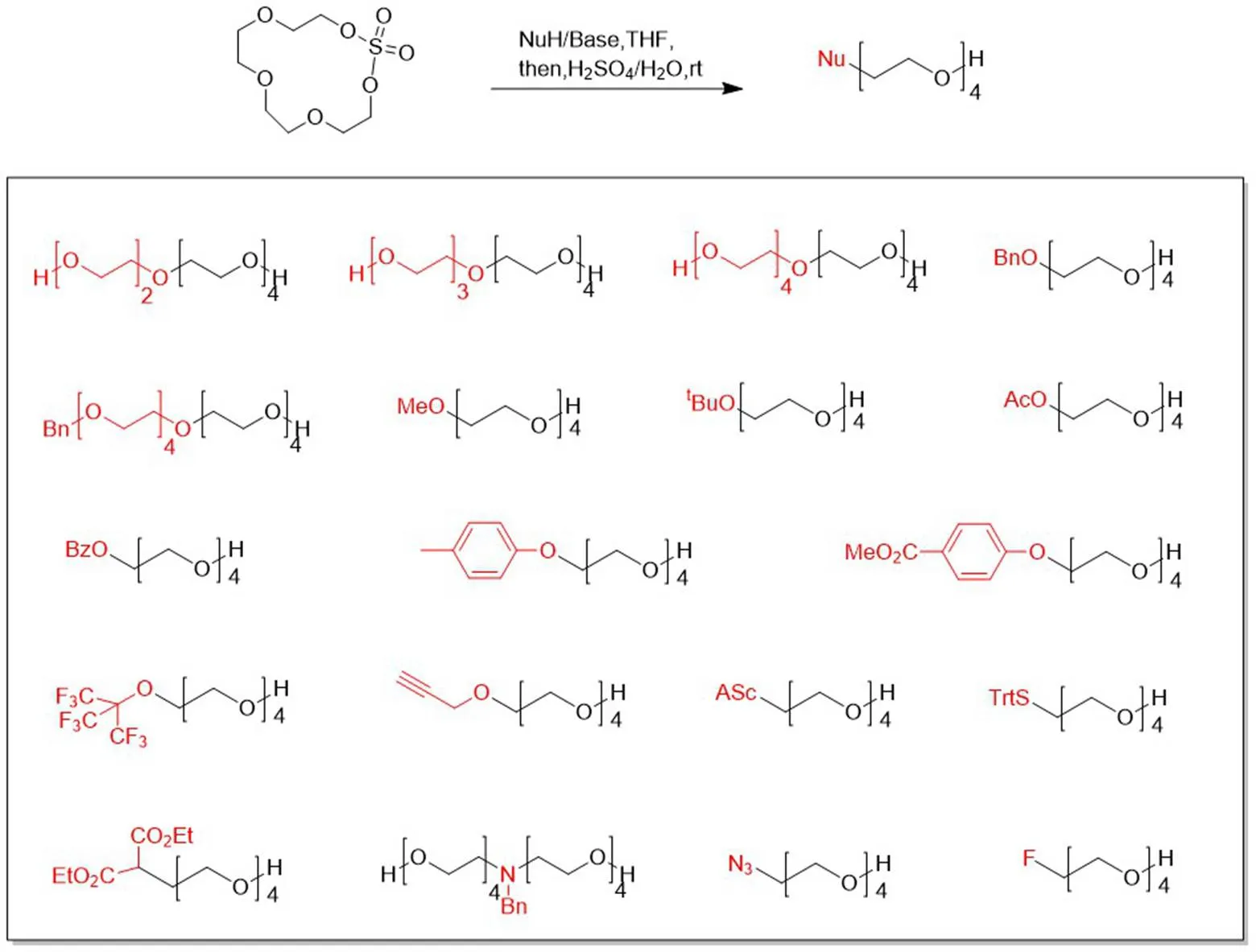
图 10 PEG 经大环硫酸酯的单官能化

图 11 冠醚去环化制备异双官能低聚乙二醇
2013 年,Abronina 等[34]提出了一种基于冠醚(18-冠-6)去环化制备异端双官能寡聚聚乙二醇衍生物(n = 6,7)的新方法。该方法合成的异双官能团 PEG 比相同链长的市售 PEG 的合成操作简便,成本低廉。该方法成功的关键是使用硝基苯作为反应溶剂,使反应温度提高到 135 ℃。冠醚(18-冠-6)与 ZrCl4在该高温条件下发生开环反应,生成产物 HO-PEG6-Cl。将其与 NaN3(DMF,75 ℃)反应,获得叠氮化物 HO-PEG6-N3。应用该中间体进一步合成了一系列更有价值的异端双官能聚乙二醇,如一端氨基,一端羧基的聚乙二醇以及具有六乙二醇基间隔基的 N-乙酰氨基葡萄糖衍生物(图 11)。
4 结语与展望
聚乙二醇具有多种独特的性能,在生物医药领域中的应用非常广泛。特别是异双官能聚乙二醇,比同端基聚乙二醇更有利于进行分子裁剪,能够选择性地进行偶联反应,从而可以获得结构清晰可控的生物医药材料,满足一些特殊的应用需求。因此,异双官能聚乙二醇聚合物的制备一直是国际上研究的热点。研究人员已经证明,异双官能聚乙二醇不仅可以延长体内循环,降低患者给药频率,还可以将药物附着到靶向部位。据先前报道已证明,双官能的 PEG 可以同时与靶向和药物连接实现靶向治疗的作用。异双官能 PEG 也成为生物传感器和其他通过将靶向部分连接到表面等离子共振 SPR 传感器和纳米颗粒的分析设备发展的关键组成部分。本文综述了许多制备杂化异双官能 PEG 的合成技术,为进一步研究这些材料的潜在应用提供了一个平台。
[1] Ukawa M, Ando H, Shimizu T, et al. Pharmaceutics of nanoparticles// Lu ZR, Sakuma S. Nanomaterials in pharmacology. New York: Humana Press, 2016:219-238.
[2] Furusho H, Kitano K, Hamaguchi S, et al. Preparation of stable water-dispersible PEGylated gold nanoparticles assisted by nonequilibrium atmospheric-pressure plasma jets. Chem Mater, 2009, 21(15):3526-3535.
[3] Yang C, Liu SQ, Venkataraman S, et al. Structure-directing star-shaped block copolymers: supramolecular vesicles for the delivery of anticancer drugs. J Control Release, 2015, 208:93-105.
[4] Kataoka K, Harada A, Nagasaki Y. Block copolymer micelles for drug delivery: design, characterization and biological significance. Adv Drug Deliv Rev, 2012, 64(1):37-48.
[5] Kircheis R, Schüller S, Brunner S, et al. Polycation-based DNA complexes for tumor-targeted gene delivery in vivo. J Gene Med, 2015, 1(2):111-120.
[6] Yan X, Scherphof GL, Kamps JA. Liposome opsonization. J Liposome Res, 2005, 15(1-2):109-139.
[7] Nelson CE, Kintzing JR, Hanna A, et al. Balancing cationic and hydrophobic content of PEGylated siRNA polyplexes enhances endosome escape, stability, blood circulation time, and bioactivity in vivo. ACS Nano, 2013, 7(10):8870-8880.
[8] Bartlett DW, Su H, Hildebrandt IJ, et al. Impact of tumor-specific targeting on the biodistribution and efficacy of siRNA nanoparticles measured by multimodality in vivo imaging. Proc Natl Acad Sci U S A, 2007, 104(39):15549-15554.
[9] Xiao K, Li Y, Luo J, et al. The effect of surface charge on in vivo biodistribution of PEG-oligocholic acid based micellar nanoparticles. Biomaterials, 2011, 32(13):3435-3446.
[10] Duncan R, Vicent MJ. Polymer therapeutics-prospects for 21st century: the end of the beginning. Adv Drug Deliv Rev, 2013, 65(1):60-70.
[11] Chen H, Chen Y, Sheardown H, et al. Immobilization of heparin on a silicone surface through a heterobifunctional PEG spacer. Biomaterials, 2005, 26(35):7418-7424.
[12] Hiki S, Kataoka K. Versatile and selective synthesis of "click chemistry" compatible heterobifunctional poly(ethylene glycol)s possessing azide and alkyne functionalities. Bioconjug Chem, 2010, 21(2):248-254.
[13] Nagasaki Y, Kutsuna T, Iijima M, et al. Formyl-ended heterobifunctional poly(ethylene oxide): synthesis of poly(ethylene oxide) with a formyl group at one end and a hydroxyl group at the other end. Bioconjug Chem, 1995, 6(2):231-233.
[14] Akiyama Y, Otsuka H, Nagasaki Y, et al. Selective synthesis of heterobifunctional poly(ethylene glycol) derivatives containing both mercapto and acetal terminals. Bioconjug Chem, 2000, 11(6):947-950.
[15] Chen X, Park R, Hou Y, et al. MicroPET imaging of brain tumor angiogenesis with 18F-labeled PEGylated RGD peptide. Eur J Nucl Med Mol Imaging, 2004, 31(8):1081-1089.
[16] Lima AA, Soares-Sobrinho JL, Silva JL, et al. The use of solid dispersion systems in hydrophilic carriers to increase benzonidazole solubility. J Pharm Sci, 2011, 100(6):2443-2451.
[17] Iversen F, Yang C, Dagnaes-Hansen F, et al. Optimized siRNA-PEG conjugates for extended blood circulation and reduced urine excretion in mice. Theranostics, 2013, 3(3):201-209.
[18] Rabanel JM, Hildgen P, Banquy X. Assessment of PEG on polymeric particles surface, a key step in drug carrier translation. J Control Release, 2014, 185:71-87.
[19] Ewert KK, Kotamraju VR, Majzoub RN, et al. Synthesis of linear and cyclic peptide-PEG-lipids for stabilization and targeting of cationic liposome-DNA complexes. Bioorg Med Chem Lett, 2016, 26(6):1618- 1623.
[20] Rabanel JM, Hildgen P, Banquy X. Assessment of PEG on polymeric particles surface, a key step in drug carrier translation. J Control Release, 2014, 185:71-87.
[21] French AC, Thompson AL, Davis BG. High-purity discrete PEG-oligomer crystals allow structural insight. Angew Chem Int Ed Engl, 2009, 48(7):1248-1252.
[22] Sawatzky E, Drakopoulos A, Rölz M, et al. Experimental and theoretical investigations into the stability of cyclic aminals. Beilstein J Org Chem, 2016, 12:2280-2292.
[23] Pradipta AR, Tanaka K. Unexplored reactivity of N-Alkyl unsaturated imines: a simple procedure for producing optically active 1,3-diamines via a stereocontrolled formal [4+2] and [4+2+2] iminocycloaddition. Bull Chem Soc Japan, 2016, 89(3):337-345.
[24] Ashweek NJ, Coldham I, Haxell TF, et al. Preparation of diamines by lithiation-substitution of imidazolidines and pyrimidines. Org Biomol Chem, 2003, 1(9):1532-1544.
[25] Blankenburg J, Frey H. Convenient access to α-amino-ω-hydroxyl heterobifunctional peg and ppo via a sacrificial hexahydro-triazine star strategy. Macromol Rapid Commun, 2019, 40(9):e1900020.
[26] Székely G, Schaepertoens M, Gaffney PR, et al. Beyond PEG2000: synthesis and functionalisation of monodisperse PEGylated homostars and clickable bivalent polyethyleneglycols. Chemistry, 2014, 20(32): 10038-10051.
[27] Zona C, D'Orazio G, La Ferla B. Controlled-length efficient synthesis of heterobifunctionalized oligo ethylene glycols. Synlett, 2013, 24(6): 709-712.
[28] Li Y, Guo Q, Li XF, et al. Fluorous synthesis of mono-dispersed poly(ethylene glycols). Tetrahedron Lett, 2014, 55(13):2110-2113.
[29] Wawro AM, Muraokaabc T, Kinbara K. Chromatography-free synthesis of monodisperse oligo(ethylene glycol) mono-p- toluenesulfonates and quantitative analysis of oligomer purity. Polym Chem, 2016, 7(13):2389-2394.
[30] Zhang QX, Ren H, Baker GL. ChemInform abstract: A practical and scalable process to selectively monofunctionalize water-soluble α,ω-Diols. ChemInform, 2014, 45(46).
[31] Khanal A, Fang S. Solid phase stepwise synthesis of polyethylene glycols. Chemistry, 2017, 23(60):15133-15142.
[32] La Ferla B, Zona C, Nicotra F. Easy silica gel supported desymmetrization of PEG. Synlett, 2009, (14):2325-2327.
[33] Zhang J, Teng Z, Song Y, et al. Inhibition of monoacylglycerol lipase prevents chronic traumatic encephalopathy-like neuropathology in a mouse model of repetitive mild closed head injury. J Cereb Blood Flow Metab, 2015, 35(3):443-453.
[34] Abronina PI, Zinin AI, Orlova AV, et al. An easy access to asymmetrically substituted oligoethylene glycols from 18-crown-6. Tetrahedron Lett, 2013, 54(34):4533-4535.
国家自然科学基金面上项目(81671814);国家自然科学基金青年基金(21506044);黑龙江省自然科学基金重点项目(ZD2016013);黑龙江省自然科学基金青年基金(QC2015016)
彭海生,Email:fisher1688@163.com
2019-12-04
10.3969/j.issn.1673-713X.2020.02.020

