香芋皮水溶性膳食纤维超声提取及其结构表征
陈秋娟 ,谢微*,韦师 ,陈隆志,谢军琳,胡月芳
1. 贺州学院材料与化学工程学院(贺州 542899);2. 广西碳酸钙资源综合利用重点实验室(贺州 542899);3. 贺州学院食品科学与工程技术研究院(贺州 542899)
膳食纤维(DF)主要包括多糖、低聚糖、木质素,以及其他对人体有益的植物组织[1],被列为七大营养素之一[2]。根据其溶解性可分为水溶性膳食纤维(SDF)和不溶性膳食纤维(IDF)。随着生活水平提高、饮食日趋精细,忽略膳食营养的平衡性,容易引发肥胖和高血压、高血糖、高血脂等问题[3]。研究表明,膳食纤维具有降低血糖与血脂[4-5],调节血压和预防肠胃疾病等功效[6-7],膳食纤维食品成为食品工业的一个主要发展方向[8],所以寻找合适的原料进行膳食纤维的开发和利用显得尤为重要。
贺州香芋是贺州市八步区的传统名牌产品,在香芋加工过程中,香芋皮大都被作为废弃物丢弃,造成严重的资源浪费和环境污染。香芋皮的研究主要集中在吸附金属作用,而利用香芋皮提取膳食纤维的研究鲜有报道。膳食纤维的提取与开发是再利用香芋皮的一条有效途径。
试验以香芋皮为原料制备膳食纤维,对香芋皮SDF的持水力和持油力进行研究分析,通过红外光谱分析、X射线衍射、扫描电子显微镜和热重分析测定其结构,为香芋皮水溶性膳食的开发与利用提供依据。
1 材料与方法
1.1 材料、仪器与设备
香芋皮(市售):清洗干净于烘箱中80 ℃烘干8 h后粉碎,加适量乙酸乙酯脱脂,抽滤,烘干,加5%过氧化氢脱色,烘干后置于干燥得到香芋皮粗样品(TS),密封保存备用。
盐酸、乙酸乙酯、过氧化氢、正丁醇、三氯甲烷、无水乙醇(均为分析纯,西陇化工股份有限公司);电子天平(JJ500,常熟市双杰测试仪器厂);pH计(ST2100,奥豪斯仪器(常州)有限公司);扫描电子显微镜(SEM)(JSM-7610F,日本JEOL);傅里叶红外光谱仪(FTIR)(Spectrum Two,Perkin Elmer公司);X射线衍射仪(XRD,日本ULTIMA IV公司);热重仪(TGA)(TGA 4000,Perkin Elmer公司)。
1.2 香芋皮膳食纤维提取流程
香芋皮粗样品(TS)→加入pH 4的HCl溶液→超声→抽滤→滤液浓缩→加入Sevag(正丁醇与三氯甲烷体积比1︰4)溶液除蛋白→抽滤→加入4倍体积的无水乙醇→抽滤→烘干得到SDF→计算SDF提取率
1.3 单因素试验
单因素试验中分别考察提取剂种类(HCl,H2SO4,CH3COOH和NaOH)、料液比(1︰20,1︰25,1︰30,1︰35,1︰40,1︰45和1︰50 g/mL)、超声时间(10,20,30,40,50,60和70 min)、温度(30,40,50,60和70 ℃)、浸提剂pH(2,3,4,5和6)对香芋皮水溶性膳食纤维提取率的影响。
1.4 膳食纤维提取率的计算

式中:m为原样品质量,g;m1为干燥后SDF质量,g。
1.5 香芋皮水溶性膳食纤维的性质及结构分析
1.5.1 持水力的测定
参照文献[9],称取0.5 g SDF与IDF,置于80 mL烧杯中,加入20 ℃纯水10 mL,在常温下浸泡1 h,用定量滤纸自然滤去水分,快速转入表面皿上并称质量,平行试验3次,取平均值。用式(2)计算持水力。

式中:m2为样品湿质量,g;m1为样品干质量,g。
1.5.2 持油力的测定
参照文献[10],称取0.5 g SDF与IDF,置于15 mL离心管中,加入5 mL食用花生油,静置1 h后搅拌均匀,在3 500 r/min的速度下离心30 min,除去上层清液,用滤纸把离心管内多余的油脂吸干,静置5 min后称量残渣的质量,平行试验3次,取平均值。用式(3)计算持油力。

式中:m3为吸附后样品质量;m1为样品干质量,g。
1.5.3 红外光谱分析
分别取适量干燥过后的SDF与溴化钾混合,研磨细后制片,在400~4 000 cm-1区间上进行红外光谱扫描分析。
1.5.4 SDF扫描电镜观察
将SDF粉碎后,采用离子溅射方法喷金,通过扫描电子显微镜对制备好的样品进行分析、观察,得到相应的扫描电镜照片。
1.5.5 X射线衍射分析
将SDF进行干燥、粉碎,随后将样品均匀洒入框内,略高于框板面,并用不锈钢片压实样品,确保样品紧密平整且表面光滑,与框紧密结合,将样品框插在测角仪中心的底座上,进行测试。
1.5.6 热重分析
将最佳提取条件提取出来的SDF放入到热重分析仪中,在100~650 ℃内以一定速率升高温度。
2 结果与分析
2.1 浸提剂对香芋皮水溶性膳食纤维提取率的影响
分别称取4份1 g香芋皮粗样品,放入4个80 mL烧杯中,分别加入pH 4的HCl、H2SO4、CH3COOH和pH 9 NaOH,料液比1︰30(g/mL),超声30 min,抽滤,滤渣洗至中性后烘干称量,计算IDF提取率。滤液浓缩、除蛋白后加入4倍体积无水乙醇,沉淀8 h后抽滤,烘干称量,计算SDF提取率;平行试验3次,取平均值。
由图1可知,采用盐酸作为提取剂,得到的SDF提取率最高,醋酸最为浸提剂得到的SDF提取率最低。因此,试验选择盐酸作为浸提剂。
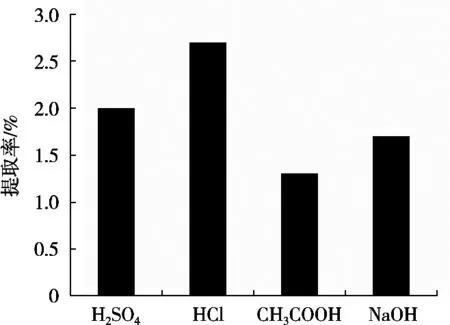
图1 浸提剂对SDF提取率的影响
2.2 料液比对香芋皮水溶性膳食纤维提取率的影响
分别称取7份1 g香芋皮粗样品,置于100 mL烧杯中,分别加入料液比1︰20,1︰25,1︰30,1︰35,1︰40,1︰45和1︰50(g/mL)的HCl溶液,在超声时间30 min、浸提温度40 ℃、浸提剂pH 4条件下考察不同料液比对膳食纤维提取率的影响。结果如图2所示。
由图2可知,料液比在1︰20~1︰40(g/mL)时水溶性膳食纤维的提取率呈上升趋势,料液比1︰40(g/mL)时提取率达到最大,1︰40(g/mL)后再增大料液比时,水溶性膳食纤维提取率反而开始程下降趋势,这可能是因为料液比1︰40(g/mL)时,酸的量足够,如果加入更多的酸,会对可溶性膳食纤维产生降解作用[11],因此最佳料液比为1︰40(g/mL)。
2.3 超声时间对香芋皮水溶性膳食纤维提取率的影响
分别称取7份1 g香芋皮粗样品,置于100 mL烧杯中,在料液比1︰40(g/mL),浸提温度40 ℃,浸提剂pH 4条件下,考察超声时间10,20,30,40,50,60和70 min对膳食纤维提取率的影响。结果如图3所示。
结果显示,在超声时间在10~30 min时,水溶性膳食纤维提取率上升明显;超声时间30 min时,提取率达到最大;增加超声时间,水溶性膳食纤维提取率变化稍下降,后渐趋于平稳。因此最佳超声时间为30 min。

图2 料液比对水溶性膳食纤维提取率的影响

图3 超声时间对水溶性膳食纤维提取率的影响
2.4 温度对香皮水溶性膳食纤维提取率的影响
分别称取5份1 g香芋皮粗样品,置于100 mL烧杯中,在料液比1︰40(g/mL),超声时间30 min,浸提剂pH 4条件下考察浸提温度30,40,50,60和70 ℃对膳食纤维提取率的影响。结果如图4所示。
结果显示,温度对水溶性膳食纤维的影响比较明显,在浸提温度30~50 ℃之间,水溶性膳食纤维的提取率快速上升;到50 ℃时达到最大;温度超过50 ℃后,水溶性膳食纤维的提取率开始缓慢下降,这可能是因为过高的温度使盐酸的挥发加快,使得浸提剂中的盐酸含量降低,从而导致细胞壁破坏效率下降,水溶性膳食纤维的提取率趋于平稳。因此最佳浸提温度为50 ℃。
2.5 pH对香芋皮水溶性膳食纤维提取率的影响
分别称取7份1 g香芋皮粗样品,置于100 mL烧杯中,在料液比1︰40(g/mL),超声时间30 min,浸提温度50 ℃条件下考察浸提剂pH 2,3,4,5,6,7和8对膳食纤维提取率的影响。结果如图5所示。
结果显示,浸提剂的pH对水溶性膳食纤维的提取率有明显影响,香芋皮水溶性膳食纤维提取率随着pH上升而快速上升,pH 4时水溶性膳食纤维的提取率最大,达到6%;pH大于4后,水溶性膳食纤维的提取率反而下降。这可能是果胶质的水解是在一定酸性条件下发生,如果盐酸浓度过高,水解反应将会进行得很激烈,导致果胶脱脂裂解[12-13],从而影响水溶性膳食纤维提取率;盐酸浓度低,水解反应将会变得很缓慢,甚至不发生反应,因此水溶性膳食纤维提取率会下降。因此试验选择最佳pH为4。
综上,确定提取香芋皮SDF适宜条件为:提取溶剂采用盐酸、料液比1︰40(g/mL)、超声时间30 min、反应温度50 ℃、反应pH 4.0,此条件下SDF提取率可达6.0%。
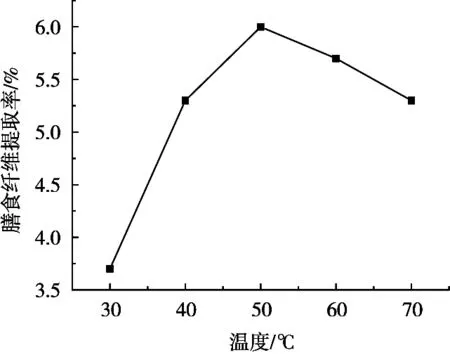
图4 温度对水溶性膳食纤维提取率的影响
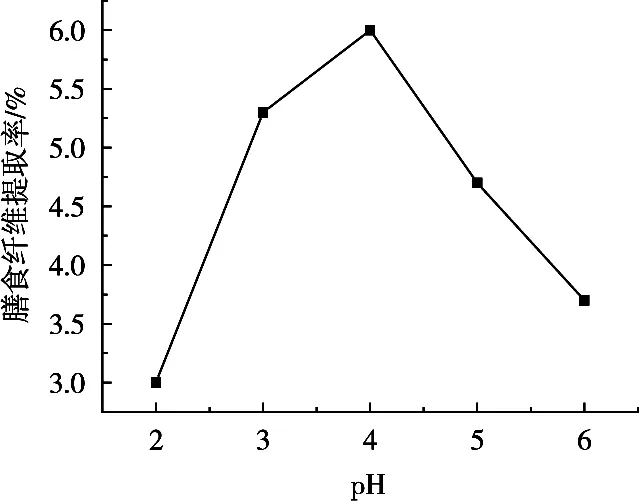
图5 pH对水溶性膳食纤维提取率的影响
2.6 香芋皮水溶性膳食纤维理化性质结果分析
持水力越大,其生理活性越好。持水力与糖尿病、“三高”等疾病的预防和治疗有重要关系,因此测定其几个性质,可以看出其是否能够较好被人体多利用[14]。评价膳食纤维的持油能力在食品加工领域及维持人体健康方面具有重要意义[15]。持油能力越高,表明膳食纤维抑制食品中脂肪流失的能力越高[16],也表明膳食纤维降低血液中胆固醇的能力越高[17]。试验对最佳条件工艺条件下制得的香芋皮水溶性膳食纤维进行持水力、持油力的测定。结果为:持水力2.12 g/g,持油力1.68 g/g。
潘虹等[18]以莲藕渣为原料提取SDF的持水力为2.28 g/g。鞠健等[19]采用超声法制备得到的山药皮SDF,测其持水力和持油力分别为2.01和1.27 g/g。罗磊等[20]提取的绿豆皮SDF持油力为1.42 g/g。说明试验所得香芋皮SDF具有很好的持水力和持油力。持水力和持油力较高的SDF容易使人产生饱腹感,降低食欲,进而控制肥胖,并能刺激肠道蠕动,将粪便中的有害物质及时排出体外,减少肠道癌、痔疮等患病的风险。因此,香芋皮SDF是一种优良膳食纤维,可作为添加剂应用于食品加工。
2.7 红外光谱分析
物质的红外光谱吸收峰位移和强度与原子振动频率、化学组成和化学键的类型密切相关。图6显示,约2 927 cm-1处有一个不明显的波峰,为糖类亚甲基C—H的反对称伸缩振动[21]。1 460~1 350 cm-1处的吸收峰为—OH的变性振动,表明该组分为多聚糖,含末端甲基类单糖[22]。约1 027和1 186 cm-1处存在较大吸收峰,是由C—O—C环内醚中C—O伸缩振动和C—O—H变角振动,也是多糖类的特征吸收峰[23]。1 620 cm-1处可能为糖分子C=O伸缩振动吸收峰[24],这说明可能含有糖醛酸[22]。在约3 264 cm-1处出现明显宽峰,为—OH伸缩振动峰,说明分子结构存在分子间氢键。893和667 cm-1是糖分子β-型的C—H直立键的变角振动吸收[8]。总体分析,香芋皮SDF的红外光谱具有纤维素多糖的特征吸收峰。

图6 SDF红外光谱图
2.8 X射线衍射分析
图7 显示,香芋皮SDF有着较好的结晶区[25],在扫描角度2θ为21°左右处有明显的结晶衍射峰,同时在2θ为32°处也有衍射峰,这些峰表明SDF具有纤维素I型的X射线衍射曲线特征[26],说明香芋皮SDF的晶型与其他植物源的膳食纤维相同,未引入新的晶型。
2.9 香芋皮SDF超微结构分析
对香芋皮SDF进行超微结构分析,分别在不同放大倍数下扫描,得到扫描电子显微镜图,如图8所示。
从图8可以看出其结构疏松,带有明显的小片状结构,且颗粒较小,几乎没有球状淀粉,可见膳食纤维含量高,经优化提取已去除淀粉和大部分蛋白[9]。从超微结构分析可推测,超声法得到的香芋皮SDF纯度高。
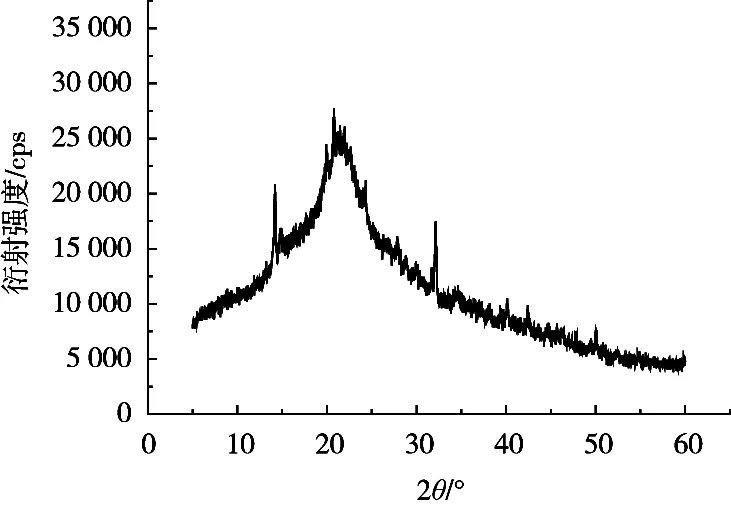
图7 SDF的X射线衍射图

图8 SDF的扫描电子显微镜图
2.10 香芋皮SDF的热重分析
如图9所示,SDF的热分解曲线分为4个阶段:干燥阶段、预碳化阶段、碳化阶段、燃烧阶段。SDF干燥阶段温度范围为30~106.12 ℃,失重率为5.35%。这个阶段主要为SDF分子内自由水、结晶水的失去,这一阶段不会影响其化学组成。预碳化阶段温度范围为106.12~230.02 ℃,失重率为1.5%,这是一个过渡阶段,主要为大分子物质逐渐解聚的一个缓慢过程。碳化阶段的温度范围为230.02~569.41 ℃,失重率为78.6%,主要是SDF分子发生热解反应造成的[27]。温度高于569.41 ℃,碳化阶段结束进入燃烧阶段。从热重分析可以看出,香芋皮SDF在100 ℃以下是稳定的,有较好热稳定性。

图9 SDF的TG曲线图
3 结论
研究以香芋皮为原料,采用超声法提取SDF。确定超声提取香芋皮SDF制备条件:料液比1︰40(g/mL)、超声时间30 min、反应温度50 ℃、反应pH 4.0。此条件下SDF提取率可达6.0%,具有较好持水性和持油性。通过红外光谱、SEM、XRD、TGA对SDF进行表征,证明所得香芋皮SDF纯度较高,具有不规则片状结构,为纤维素I型,热稳定性较好。后续将对SDF生理功能进行探究,为香芋皮有效利用提供理论依据。

