功能化间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物的制备及其对U(Ⅵ)的吸附行为研究
许玉历,张 康,肖方竹,王 成,罗佳琦,刘 永,4,彭国文,,4,*
(1.南华大学 化学化工学院,湖南 衡阳 421001;2.南华大学 资源环境与安全工程学院,湖南 衡阳 421001;3.南华大学 公共卫生学院,湖南 衡阳 421001;4.南华大学 湖南省铀尾矿库退役治理工程技术研究中心,湖南 衡阳 421001)
新能源在我国经济可持续发展和国防建设中占有重要的地位,而核能作为一种低碳环保的新能源,具有明显的优势。但在核燃料循环及核技术应用过程中会产生大量的放射性废水。铀作为放射性废水中的一种主要元素[1-3],如果排放到环境中将对人类和其他物种构成严重威胁[4-5],因此必须得到妥善处理。另外,从含铀废水中对U(Ⅵ)进行回收利用对缓解我国铀资源的供需矛盾具有重大的现实意义。目前,含铀废水的主要处理方法有化学沉淀法、离子交换法[6]、吸附法[7-8]、液液萃取法等,其中,吸附法由于易操作和成本低,是一种优良的方法[9]。
杯芳烃是由苯酚单元通过亚甲基相连的环状低聚物,是继冠醚、环糊精之后的第3代超分子主体化合物[10-11],它既具有冠醚的空穴结构和空间延展性,又具有环糊精的亲水疏水等优点,因此杯芳烃有几个明显的特点:空腔可调节、构象可变换、易于对其上下沿进行化学改性和修饰等。正是由于杯芳烃独特的性能,使得其作为继环糊精和冠醚之后的第3代超分子化合物,在分子(离子)识别、膜传输、金属离子的分离和回收、酶模拟、化学传感器、光电材料等领域展现了具大的应用潜力[12-15]。目前,已有不少国内外研究人员将合成的杯芳烃类衍生物作为吸附剂应用于含铀废水的处理,但对杯[4]芳烃同时进行上沿羧基化和下沿硫化得到间羧基苯偶氮基杯[4]芳烃对称硫醚类化合物用于含铀废水的处理还鲜有文献报道。
本文拟采用化学合成法,制备一种新型的吸附剂材料间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物,通过仪器分析对合成的新材料进行结构表征,并探讨其对U(Ⅵ)的吸附行为。
1 实验
1.1 主要仪器和试剂
SHT型数显恒温搅拌电热套,山东省鄄城新华电热仪器有限公司;AL104 电子天平,梅特勒-托利多仪器(上海)有限公司;UV-Vis 8500型紫外-可见分光光度计,上海天美科学仪器有限公司;pHS-3C型精密pH计,上海雷磁仪器厂;SHZ-D(Ⅲ)循环水式真空泵,台州求精真空泵有限公司;DF205电热鼓风干燥箱,北京中兴伟业仪器有限公司;IR Prestige-21型傅里叶变换红外光谱仪,日本岛津公司。
对叔丁基苯酚,99%,化学纯,阿拉丁生化科技股份有限公司;间氨基苯甲酸,分析纯,天津市科密欧化学试剂有限公司;铀标准溶液,采用文献[12]方法配制(根据实验需要稀释成对应浓度);脱叔丁基杯[4]芳烃参照文献[16]合成。其他试剂均为分析纯。
1.2 间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物的合成
间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物的合成路线示于图1。
首先向烧杯中加入10 mL质量分数为6%的氢氧化钠溶液,再加入1.7 g间氨基苯甲酸,水浴加热直至溶解,然后冷却至室温,加入0.7 g亚硝酸钠溶解;在搅拌下分批滴加到冰水和浓硫酸混合液中,温度保持在0 ℃以下,在冰浴中反应15 min后加入0.2 g尿素搅拌15 min;再将混合液缓慢滴加到混有1.8 g对叔丁基杯[4]芳烃的80 mL N,N-二甲基酰胺(DMF)中(冰水浴),用质量分数为25%的醋酸钠调节pH=6~7,溶液由砖红色逐渐变成大红色,有大量泡沫产生;在冰水浴中反应1.5 h后,用浓盐酸调节pH<1,在室温下静置过夜,然后抽滤,干燥后得暗红色固体粗产品,产率为86%,将粗产品溶解到50 mL碳酸氢钠溶液中,再加入1 g活性炭加热搅拌至60 ℃趁热抽滤,收集滤液,用浓盐酸酸化沉淀,抽滤,固体真空干燥得暗红色固体(产物a),产率为77%。
称取1.8 g产物a、1 g无水K2CO3,移取3 mL 1,3-二溴丙烷(98%)、38 mL CH3CN加入到100 mL单口圆底烧瓶中,在N2保护下,70 ℃磁力搅拌加热回流48 h后,冷却至室温,真空旋转蒸至剩余少量溶剂和固体残余物,向残余物中加入稀盐酸和CHCl3(各20 mL)。水洗至中性,萃取分离有机相,并加入无水MgSO4干燥后过滤,加20 mL甲醇静置得产物b,产率68.5%。
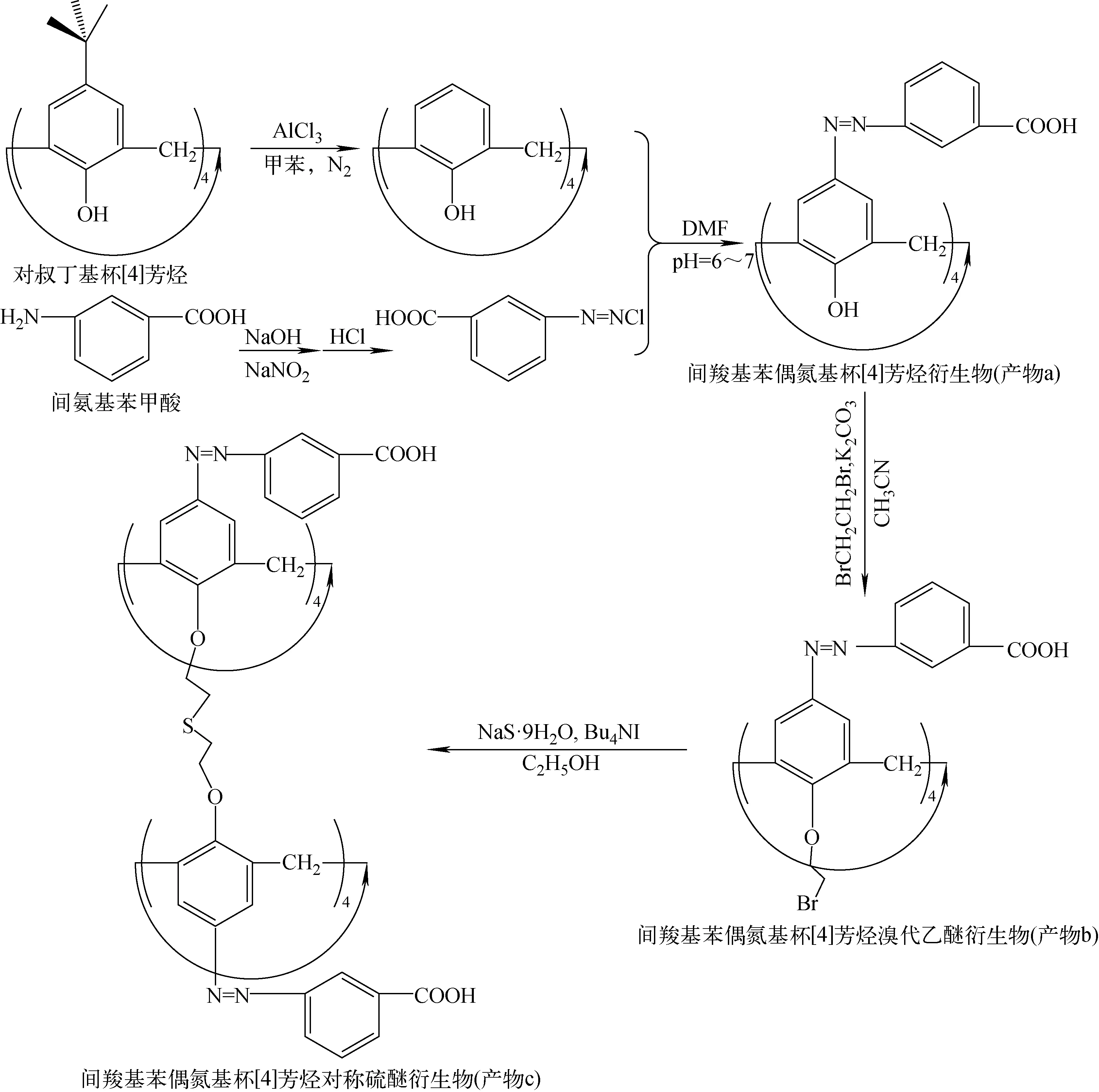
图1 间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物的合成路线Fig.1 Synthesis route of m-carboxyphenyl azo calix[4]arene symmetrical sulfide derivative
称取1.2 g产物b、1.45 g四丁基碘化铵和0.48 g Na2S·9H2O,加入10 mL蒸馏水和25 mL无水乙醇于100 mL单口圆底烧瓶中,在N2保护下,70 ℃磁力搅拌加热回流12 h后,冷却至室温,真空旋转蒸发,有机相用饱和NaCl溶液洗涤至中性后,用蒸馏水洗去残余的NaCl,再用无水MgSO4干燥后过滤,加入20 mL甲醇静置得最终产物c,产率为69.3%。
1.3 间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物对铀的吸附
在一系列50 mL具塞锥形瓶中加入10 mL一定浓度的铀标准溶液,再加入一定量的间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物,用0.05 mol/L HCl和0.05 mol/L NaOH调节溶液pH值,将具塞锥形瓶置于25 ℃恒温水浴摇床内以250 r/min恒温振荡吸附4 h,静置5 min分层,移取1 mL上清液,加入10 mL比色管中,再在比色管中依次加入1 mL 0.05%的偶氮胂Ⅲ、适量醋酸-醋酸钠缓冲溶液(pH=4)定容,振荡摇匀后静置10 min。用紫外可见分光光度计在波长652 nm处分别测其吸光度,并根据以下公式计算相应的吸附率P(%)和吸附容量qt(mg/g)。
(1)
(2)
其中:c0为铀初始浓度,mg/L;ct为t时刻铀的剩余浓度,mg/L;V为所用铀溶液体积,L;m为吸附剂质量,g。
2 结果与讨论
2.1 间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物的结构表征
1) FT-IR分析

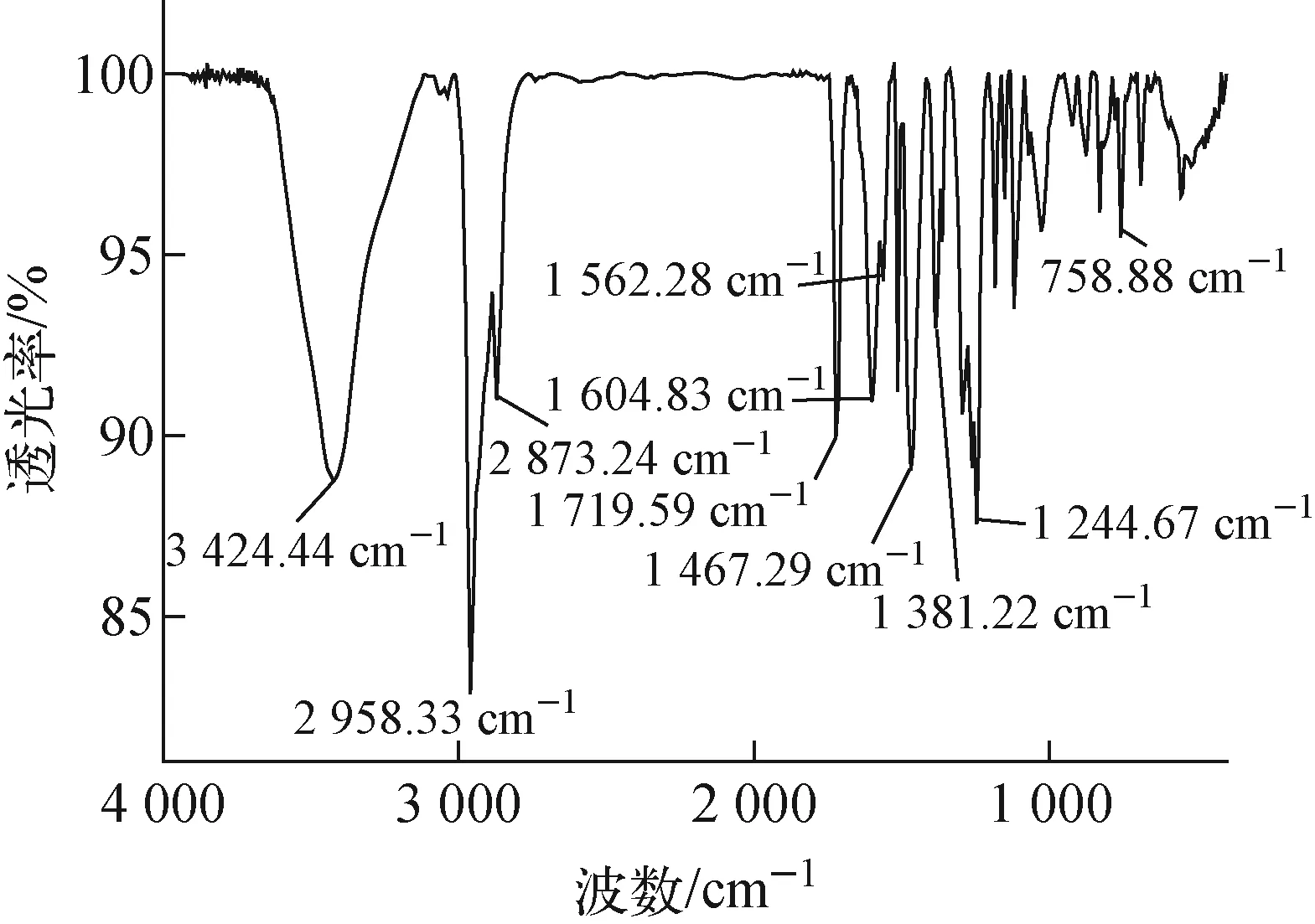
图2 间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物的FT-IR谱Fig.2 FT-IR spectrum of m-carboxyphenyl azo calix[4]arene symmetrical sulfide derivative
2)1H NMR分析

图3 间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物的1H-NMR谱Fig.3 1H-NMR spectrum of m-carboxyphenyl azo calix[4]arene symmetrical sulfide derivative
间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物的1H-NMR谱示于图3。从图3可知,6.882~7.358 ppm处对应苯环上的氢,3.409~4.096 ppm处对应亚甲基上的氢,1.746~1.067 ppm处对应叔丁基上的氢。由此可知,该物质具备间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物的基本官能团[18]。
2.2 间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物对U(Ⅵ)吸附效果的影响因素分析
1) 初始pH值
c0=10 mg/L、m=10 mg、T=25 ℃、t=4 h条件下,初始pH值对吸附的影响示于图4。
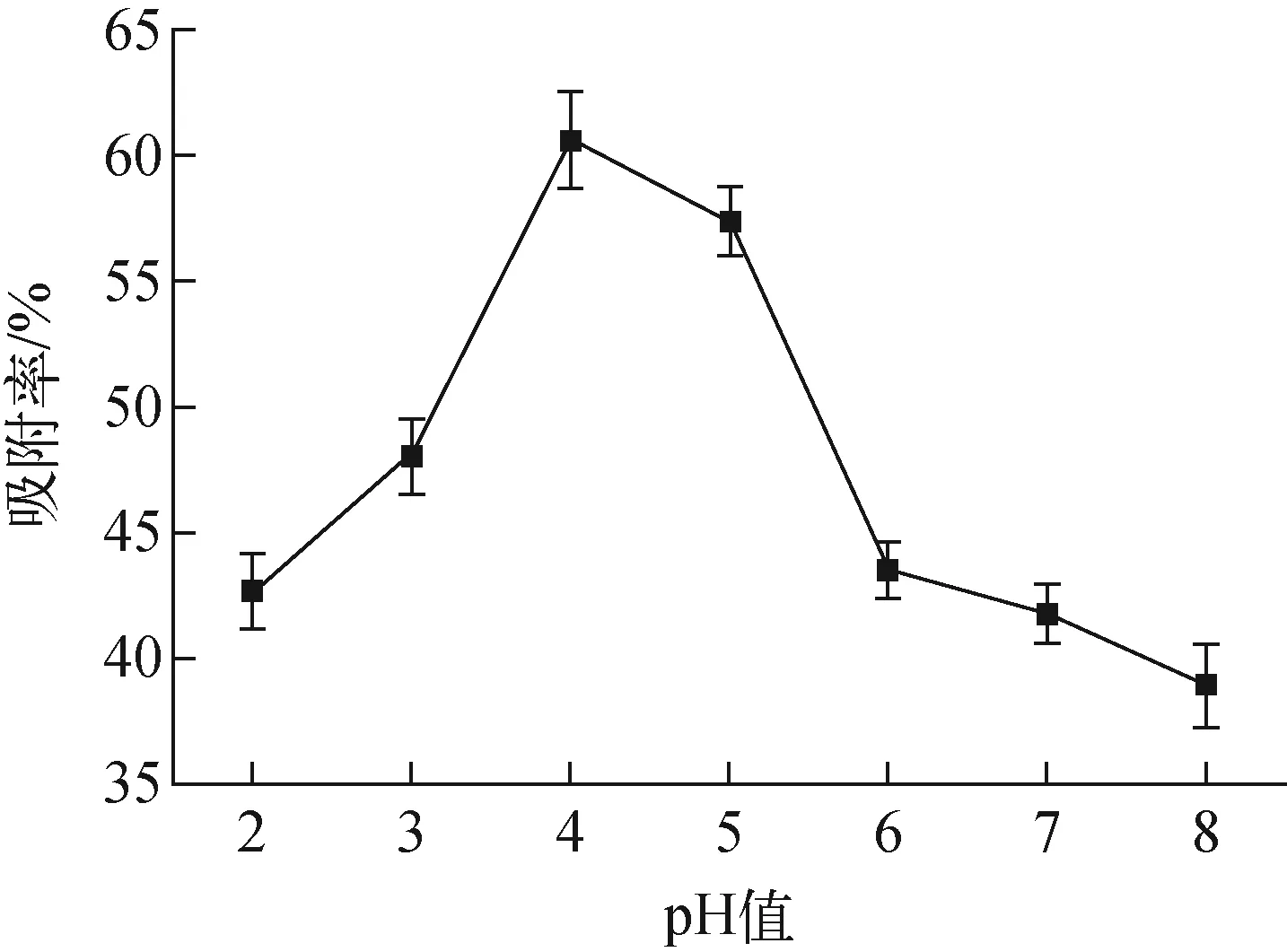
图4 初始pH值对吸附的影响Fig.4 Effect of initial pH on adsorption
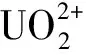
2) 吸附剂用量
c0=10 mg/L、T=25 ℃、t=4 h、初始pH=4条件下,吸附剂用量对吸附的影响示于图5。
从图5可看出,吸附率随吸附剂用量的增加而提高。这可能是因为随吸附剂浓度的增加,相应地也增加了吸附活性位点和空穴,从而使吸附率上升;当吸附剂用量增加到一定程度时,如趋近于10 mg时,吸附趋于平衡状态,吸附率无明显上升,综合考虑,吸附剂最佳用量为10 mg。

图5 吸附剂用量对吸附的影响Fig.5 Effect of dosage of adsorbent on adsorption
3) 铀初始浓度

图6 铀初始浓度对吸附的影响Fig.6 Effect of initial concentration of uranium on adsorption
m=10 mg、T=25 ℃、t=4 h、初始pH=4条件下,铀初始浓度对吸附的影响示于图6。从图6可看出,随铀初始浓度的增加,吸附剂对铀的吸附率逐渐减小。这可能是由于在不同浓度但体积相同的溶液中添加相同质量的吸附剂,当铀初始浓度较低时,吸附剂与铀酰离子能充分接触,吸附率较高。但一定质量下的吸附剂其活性位点有限,当吸附达到平衡时,吸附位点逐渐饱和,之后随着铀初始浓度的增高,吸附剂对铀的吸附率则降低。综合考虑,最佳的铀初始浓度为10 mg/L。
4) 吸附动力学
c0=10 mg/L、m=10 mg、T=25 ℃、初始pH=4条件下,吸附时间对吸附的影响示于图7。
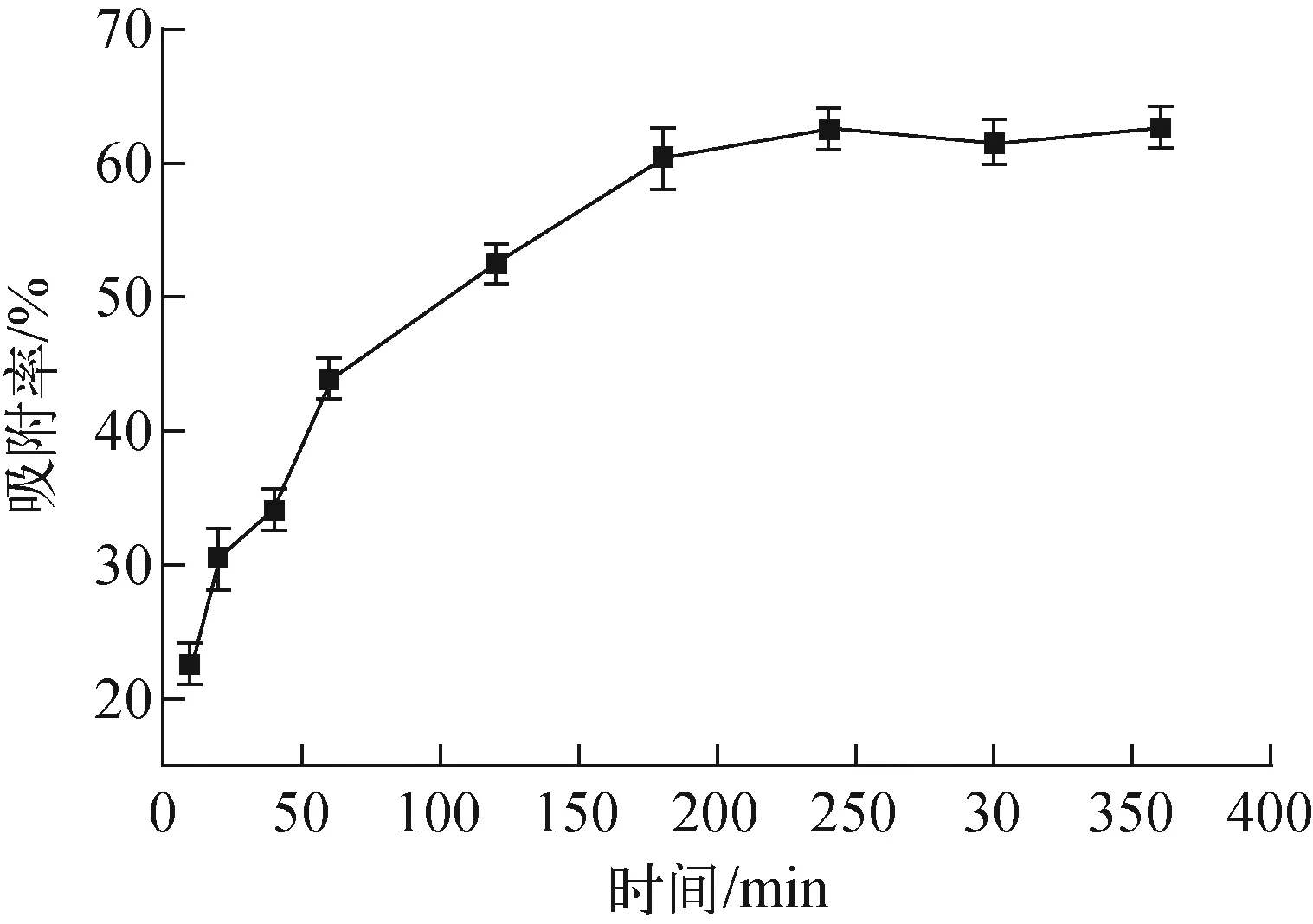
图7 吸附时间对吸附的影响Fig.7 Effect of adsorption time on adsorption
由图7可看出,间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物对U(Ⅵ)的吸附率随时间的增加而增大,在0~4 h内,随时间的增加吸附率快速增大,这是因为刚加入吸附剂时,U(Ⅵ)吸附位点数量多,而溶液中U(Ⅵ)的浓度也较大,因此两者之间的结合概率增加;随着吸附时间的延长,在吸附时间接近4 h时,吸附剂上与U(Ⅵ)的吸附位点接近饱和,直到4 h时达到平衡。
为进一步探讨间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物对U(Ⅵ)的吸附动力学,在c0=10 mg/L、m=10 mg、T=25 ℃、pH=4条件下,采用准一级动力学模型和准二级动力学模型对吸附数据进行线性拟合分析。
准一级动力学拟合方程为:
(3)
准二级动力学拟合方程为:
(4)
其中:k1为准一级反应吸附速率常数,min-1;k2为准二级反应吸附速率常数,g/(mg·min);qe为平衡吸附容量,mg/g。
准一级、准二级动力学模型拟合参数列于表1。

表1 间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物对U(Ⅵ)的吸附动力学参数Table 1 Kinetic parameter for adsorption of U(Ⅵ) by m-carboxyphenyl azo calix[4]arene symmetrical sulfide derivative
由表1可见,准一级动力学模型的拟合系数R2=0.857 7,小于准二级动力学模型的R2=0.988 3,因此间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物对U(Ⅵ)的吸附特性更符合准二级动力学模型,说明该吸附过程主要以化学吸附为主。
5) 吸附温度
c0=10 mg/L、m=10 mg、t=4 h、初始pH=4条件下,吸附温度对吸附的影响示于图8。

图8 温度对吸附的影响Fig.8 Effect of temperature on adsorption
从图8可看出,随着温度的升高,吸附率逐渐上升,这可能是由于升高温度后,反应体系内紊乱程度上升,吸附剂与U(Ⅵ)的碰撞概率增大,使得吸附率上升。温度达到35 ℃时,吸附率达到峰值,此时再升高温度,吸附率不再升高反而下降,这可能是由于高温条件下吸附剂活性有所降低,考虑到现实环境中的自然因素,选25 ℃作为实验温度。
6) 吸附等温线分析
为进一步研究间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物对U(Ⅵ)的吸附过程,采用Langmuir和Freundlich吸附等温模型拟合间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物对U(Ⅵ)的等温吸附过程。
Langmuir吸附等温模型为:
(5)
Freundlich吸附等温模型为:
(6)
其中:qmax为单层饱和吸附容量,mg/g;ce为平衡时溶质的浓度,mg/L;b为Langmuir吸附常数,L/mg;k为Freundlich吸附常数;1/n为不均匀因子。
分别对ce/qe-ce和lgqe-lgce作图,结果示于图9。
从图9可看出,由Langmuir吸附等温模型所得相关拟合系数R2=0.984 8。而由Freundlich吸附等温模型所得相关拟合系数R2=0.928 8。由于Langmuir吸附等温模型的R2大于Freundlich吸附等温模型的R2,且Langmuir吸附等温模型的qmax与实验值非常接近,表明该吸附过程更符合Langmuir吸附等温模型,即吸附剂通过其表面的吸附位点对金属离子进行吸附,形成单分子吸附层,且被吸附的离子间无相互作用。则说明间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物对U(Ⅵ)的吸附以单层吸附为主。

图9 间羧基苯偶氮基杯[4]芳烃对称硫醚衍生物吸附U(Ⅵ)的吸附等温线Fig.9 Adsorption isotherm for adsorption of U(Ⅵ) by m-carboxyphenyl azo calix[4]arene symmetrical sulfide derivative
3 结论


