葫芦素B 固体分散体的制备
程佳慧武 倩刘喜纲
(承德医学院中药研究所,河北省中药研究与开发重点实验室,河北 承德067000)
葫芦素B 是葫芦科植物中提取分离得到的一种四环三萜类化合物[1],用于治疗肝炎、肝癌等[2],对卵巢癌[3]、乳腺癌[4]、胃癌[5]、肺癌[6]、直肠癌[7]等,表现出良好的药理作用,有望成为有效的抗肿瘤药物,但它在生物药剂学分类系统中为第Ⅳ类药物,即低溶解性-低渗透性药物,在水中溶解度仅为22 μg/mL,绝对生物利用度仅为1.37%[8],极大程度限制了临床应用。目前,葫芦素B 剂型有磷脂复合物[9-10]、水-醇凝胶[11]、脂肪乳注射剂[12]、纳米混悬凝胶剂[13]、固体脂质纳米粒[14-15]、纳米胶束[16]等,其中固体分散技术简单可行,易实现工业化生产。
固体分散体是指药物以分子、胶态、微晶或无定形状态分散在适宜载体材料中形成的固体分散体系,对药物溶出度、生物利用度均有显著提高。本实验采用溶剂法制备葫芦素B 固体分散体后,通过结晶抑制实验筛选载体,对其溶出度进行考察,再通过SEM、XRD 等进行物相表征,以期为相关新剂型研发提供参考。
1 材料
Agilent 1260 高效液相色谱仪(美国Agilent 公司);AG-254 电子分析天平、STARe SW 11.00 热分析仪(瑞士梅特勒-托利多公司);RC806 溶出试验仪(天津市天大天发科技有限公司);SU8020扫描电镜(日本日立公司);Nicolet 6700 红外光谱仪(美国Thermo Nicolet 公司);D8-Advance X 射线衍射仪(德国Bruker 公司);KQ-1000E 超声波清洗器(昆山市超声仪器有限公司)。
葫芦素B 对照品(中国食品药品检定研究院,批号111945-201301);交联聚乙烯吡咯烷酮(北京凤礼精求医药股份有限公司,批号95314575L0);PEG-4000(天津市光复精细化工研究所,批号20160310);低取代羟丙基纤维素(湖州展望药业,批号20160346);PVPk30(德国BASF 公司,批号G53326PT0)。乙腈、磷酸为色谱纯(美国迈瑞达公司);其他试剂均为分析纯;水为蒸馏水。
2 方法与结果
2.1 样品制备
2.1.1 固体分散体 采用溶剂法。按一定比例精密称取葫芦素B、载体适量,溶于适量二氯甲烷中,超声完全溶解后混匀,50 ℃下减压,挥去二氯甲烷,待呈黏稠状后取出置干燥器中干燥24 h,研成细粉,即得,密封保存。
2.1.2 物理混合物 按一定比例精密称取葫芦素B、载体适量,置于研钵中混合均匀,即得,密封保存。
2.2 处方筛选
2.2.1 色谱条件 C18色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈-0.1% 磷酸(58∶42);体积流量1.0 mL/min;柱温30 ℃;检测波长228 nm;进样量10 μL。
2.2.2 药载比筛选 根据预实验结果,选择PVP K30 作为载体,按1∶3、1∶5、1∶7、1∶11 比例精密称取葫芦素B、载体适量,按“2.1.1”项下工艺制备固体分散体。按照2015 年版《中国药典》 第四部通则中0931 项下“溶出度与释放度测定法”下桨法测定溶出度,取样品(相当于原料药3 mg)适量置于900 mL 纯水中,介质温度(37±0.5)℃,转速100 r/min,于5、10、15、20、30,45,60 min 各取样2 mL,0.45 μm 微孔滤膜过滤,补加同体积等温溶出介质,续滤液在“2.2.1”项下色谱条件进样测定,结果见图1。
由此可知,溶出60 min 时固体分散体累积溶出度明显高于原料药;随着药载比升高,累积溶出度也随之增加,即1∶11 时溶出效果最优,与原料药比较提高了277.2%,其次为1∶7。因此,选择药载比1∶11、1∶7 进行物相表征。
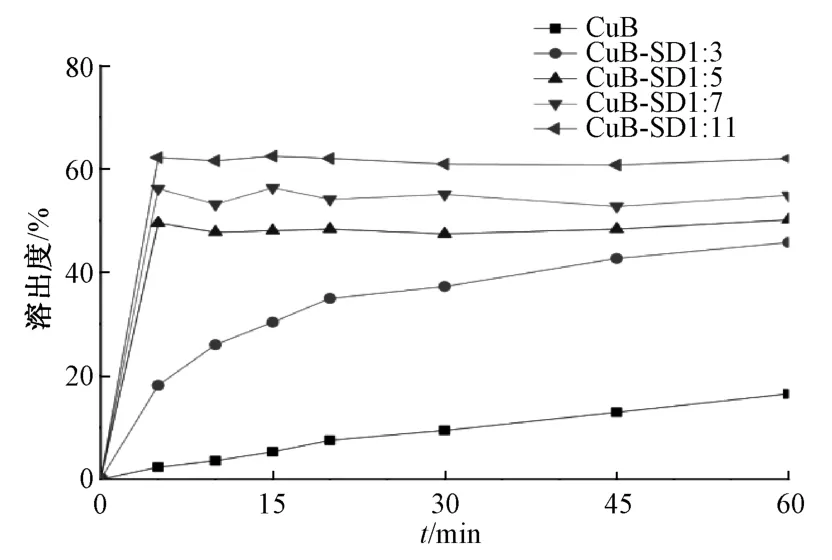
图1 样品溶出曲线Fig.1 Dissolution curves for samples
2.3 物相表征[17]
2.3.1 扫描电子显微镜(SEM)测定条件为电流10 mA,加速电压5.0 kV,观察原料药、PVP K30、固体分散体(药载比1∶7、1∶11)、物理混合物(药载比1∶7、1∶11)外观形貌和晶型结构,记录图像,结果见图2。由此可知,原料药(图2A)以棱柱状或锥状结晶存在;PVP K30(图2B)呈球状或类球形,大小不完全相同;物理混合物(图2D、2F)存在原料药、PVP K30 球状结构,表示只是药物和载体的简单混合;固体分散体(图2C、2E)呈紧实的不规则团块状,与原料药、PVP K30 显微结构完全不同,而且原料药晶体形状消失。
2.3.2 傅里叶变换红外光谱(FTIR)将原料药、PVP K30、固体分散体(药载比1∶7、1∶11)、物理混合物(药载比1∶7、1∶11)与适量KBr 研磨、混匀后压片,在4 000~500 cm-1波数范围内进行扫描,结果见图3。由此可知,原料药存在2 个特征峰,分别是3 450 cm-1左右的羟基峰和1 718、1 693 cm-1处的酮基峰;PVP K30 由于共轭效应的存在,C=O 的伸缩振动峰向低频方向移动,出现在1 655 cm-1左右;物理混合物在3 450 cm-1左右仍存在原料药特征峰,同时PVP K30 C=O 的伸缩振动峰也清晰可见,表明它是两者简单叠加;固体分散体中原料药羟基峰向低频方向移动至3 420 cm-1,酮基峰由1 718、1 693 cm-1合并为单峰,向低频方向移动而且峰变宽,与载体羰基峰基本重合,出现在1 650 cm-1处,未出现其他特征峰,表明原料药与PVP K30 可能发生氢键相互作用。

图2 样品SEM 图(×200)Fig.2 SEM images for samples(×200)

图3 样品FTIR 图谱Fig.3 FTIR spectra for samples
2.3.3 差示扫描量热(DSC)取原料药、PVP K30、固体分散体(药载比1∶7、1∶11)、物理混合物(药载比1∶7、1∶11)适量,均匀放入铝盘内,测定条件为升温速度10 ℃/min,扫描温度范围30~400 ℃,样品气氮气,结果见图4。由此可知,原料药特征熔点峰出现在181.57 ℃,与文献报道一致;PVP K30 熔点峰出现在71.56 ℃;物理混合物中原料药、PVP K30 特征熔点峰均存在,但前者强度变弱,表明其结晶度降低,但仍以晶体形式存在;固体分散体中未出现原料药特征熔点峰,仅有PVP K30 的,表明原料药晶型发生了改变。

图4 样品DSC 曲线Fig.4 DSC curves for samples
2.3.4 X 射线衍射(XRD)取葫芦素B、PVP K30、固体分散体(药载比1∶7、1∶11)、物理混合物(药载比1∶7、1∶11)适量,测定条件为波长(Cu 靶)1.540 6 nm,工作电流40 mA,工作电压40 kV,扫描范围3°~50°,结果见图5。由此可知,原料药在6.80°、7.22°、13.15°、13.60°、16.65°、17.62°、20.77°等处均存在晶体峰;PVP K30 峰较宽而平缓,无晶型结构存在,为无定形结构;物理混合物(药载比1∶ 7)在7.22°、13.15°、16.69°、17.62°、20.77°仍可见强度变弱的原料药特征峰,表明原料药仍以晶体形式存在;物理混合物(药载比1∶11)中原料药特征峰不明显,可能是其浓度较低所致;固体分散体中未发现原料药晶体衍射峰,表明它可能以无定形状态存在。

图5 样品XRD 图谱Fig.5 XRD patterns for samples
3 讨论
葫芦素B 难溶于水,生物利用度较低,而将其制备成固体分散体时可在一定程度上改善这些问题。本实验考察了PVPP、PEG-4000、低取代羟丙基纤维素、PVP K30 这4 种常用载体,通过比较四者抑晶效果,筛选出最佳载体为PVP K30。
制备固体分散体时选择二氯甲烷作为溶剂,它对葫芦素B 的溶解性较好,同时挥发性优于无水乙醇,故在制备过程中既能保证该成分和载体完全溶解,又可使溶剂用量较少。结果表明,葫芦素B制成固体分散体后溶出度高于原料药;在一定范围内其溶出度随载体比例的增大而升高,可能是因为它在载体PVP K30 中为无定形状态,从而分散度得到提高;它可能以无定形状态存在,改变了原有晶体结构,故在很大程度上提高了累积溶出度。
综上所述,以PVP K30 为载体、1∶11 为药载比时,葫芦素B 固体分散体的体外溶出度显著提高,对相关制剂开发具有一定应用价值。

