二硝酰胺盐溶解度的测定及拟合
戴 赟,李斌栋
(南京理工大学化工学院,江苏 南京 210094)
引 言
新型氧化剂二硝酰胺铵(ADN)是一种白色化合物,密度1.812g/cm3,有极强的吸水性,极易溶于水,摩擦感度72N,撞击感度5.0N·m[1]。ADN由于生成热大、含氧量高,既可以作为氧化剂,也可以作为炸药。与高氯酸铵(AP)相比,ADN分子中没有氯元素,燃烧时无烟,可以减少污染、增加武器的隐蔽性。以ADN取代AP可以使助推器推力增加14%,同时每次载荷量可以增加4t[2]。ADN通常采用氨基磺酸法制备[3],为了降低副产物的量,可以先将氨基磺酸与碱反应生成氨基磺酸盐,随后在硝硫混酸下生成二硝酰胺酸,与氨基磺酸盐反应生成FOX-12、KDN与ADN。由于此法在合成过程中会产生大量的离子盐杂质,其中混有的AN会进一步增强ADN的吸水性。降低ADN吸水性的途径包括球形化、包覆以及重结晶。德国 Thomas等[3]的途径采用微胶囊等新技术,在 ADN 颗粒上涂上溶有乙基纤维素的环己烷溶液以降低 ADN的吸水性。对ADN进行重结晶提纯的同时进行晶型的缺陷修饰,抑制ADN的分解,也一定程度上降低了吸水性[4]。溶解度数据是研究重结晶的理论依据,具有重要意义。而目前对于二硝酰胺盐的研究主要集中在合成与热分析上,尚无关于溶解度方面研究的报告。脒基脲二硝酰胺盐(FOX-12)制取二硝酰胺钾(KDN)与ADN的过程中反应介质与重结晶溶剂通常选择水与醇类溶剂,而二硝酰胺盐具有紫外特征吸收峰[6],故本研究采用紫外分光光度法研究3种二硝酰胺盐在水和醇类溶剂中的溶解度(以无水乙醇及异丙醇等溶剂为例),为二硝酰胺盐重结晶提纯及研究溶解过程提供理论依据。
1 实 验
1.1 试剂与仪器
脒基脲二硝酰胺盐(FOX-12)、二硝酰胺钾(KDN)、二硝酰胺铵(ADN),均为自制后重结晶提纯,纯度大于99%,高效液相色谱(HPLC)测试[7-8];无水乙醇、异丙醇、正丁醇,均为分析纯,上海泰坦科技股份有限公司;去离子水,南京中东化玻仪器有限公司。
集热式恒温加热磁力搅拌器,上海东玺制冷仪器设备有限公司;低温恒温反应浴,南京大卫仪器设备有限公司;电子天平,常州市衡正电子仪器有限公司;紫外可见分光光度计38(液),美国THERMO FISHER公司。
1.2 合成路线
ADN的合成路线如图1所示。
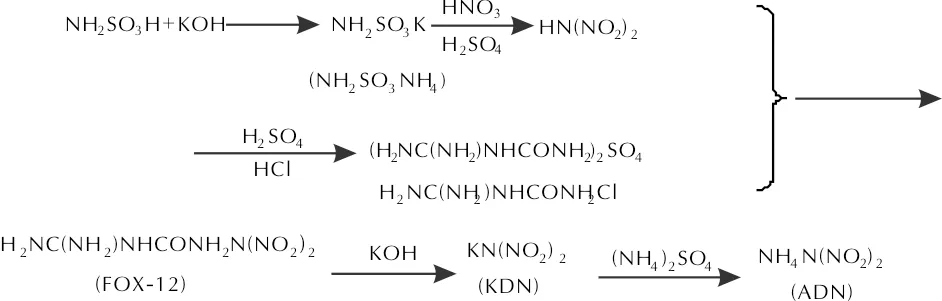
图1 ADN的合成路线[5] Fig.1 Synthesis route of ADN
1.3 实验过程
1.3.1 标准曲线的绘制
准确称取二硝酰胺盐溶于一定量的溶剂中,完全溶解后,利用容量瓶配成具有一定质量浓度梯度的标准溶液,FOX-12、KDN、ADN标准溶液的质量浓度范围控制在10~100mg/L之间。随后对标准溶液进行紫外测试,吸收波长λ(单位nm)为横坐标,纵坐标为吸光度A绘制紫外谱图[6]。
1.3.2 二硝酰胺盐溶解度的测定
设定水浴锅温度并加热,达到设定温度后,向带有夹套的试管中加入一定的溶剂与过量的溶质后放入水浴锅中,开启磁力搅拌器,2h后停止搅拌,恒温下静置30min以上,保证固液相完全分离。在容量瓶中加入一定溶剂后盖上盖子,称出质量记为m0;随后快速吸取部分上层饱和清液加入容量瓶中,盖上瓶盖以防溶剂挥发,称出此时的质量m1;随后用溶剂稀释至刻度线处,测出此时在333nm处的吸光度,观察是否落在标准曲线上,若没有则继续稀释直至落在标准曲线上,计算最终稀释后的体积V。根据标准曲线,计算出稀释后的质量浓度为c。
该温度下的溶解度s可以利用式(1)计算:
(1)
溶解度x表示每摩尔溶液中溶质的摩尔分数,计算公式如下:
(2)
式中:MA、MB分别为溶质与溶剂的摩尔质量,g/mol。
为了确保恒温静置后固液分离完全,可以在取样测试溶解度后静置一段时间再取样测试,直到多次测试得到的溶解度数据基本一样,即得到溶质在该温度下的溶解度数据。
2 结果与讨论
2.1 标准曲线分析
3种二硝酰胺盐不同溶剂中在210、285、333nm处有最大吸收峰,如图2所示。随后分别拟合3个最大吸收波长处的吸光度A与所对应的质量浓度c(mg/L)(见图3),发现210nm处拟合度很差;而285nm处纵截距太大,当待测液质量浓度较小时计算得到的质量浓度误差太大;而333nm处拟合度较高,纵截距也小,故选择333nm处的吸光度A与质量浓度c拟合标准曲线。3种二硝酰胺盐在不同测试溶剂中333nm处吸光度A与质量浓度c的拟合曲线方程见表1。
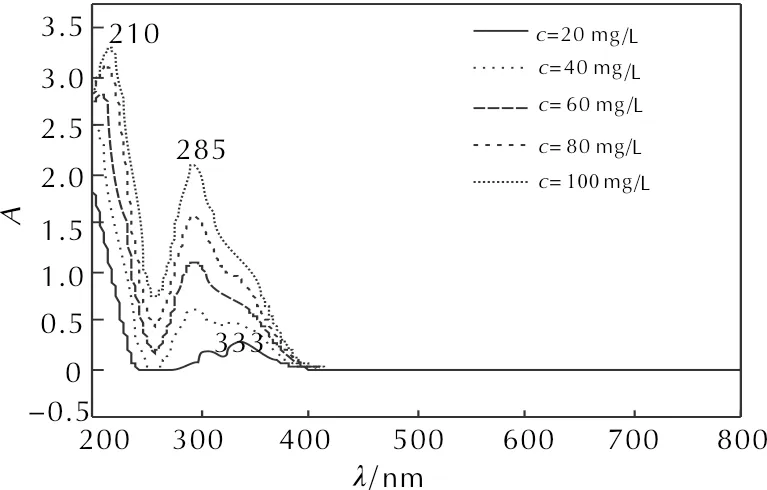
图2 FOX-12水溶液的紫外谱图Fig. 2 UV spectra of FOX-12 aqueous solution
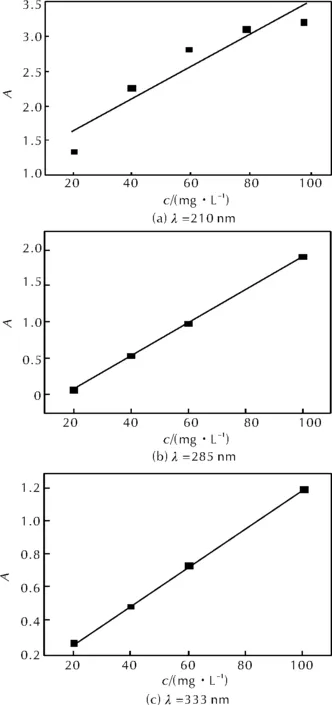
图3 FOX-12在水中不同波长处质量浓度c与吸光度A的拟合曲线Fig.3 Fitting curves of mass concentration c and absorbance A of FOX-12 in water at different wavelengths
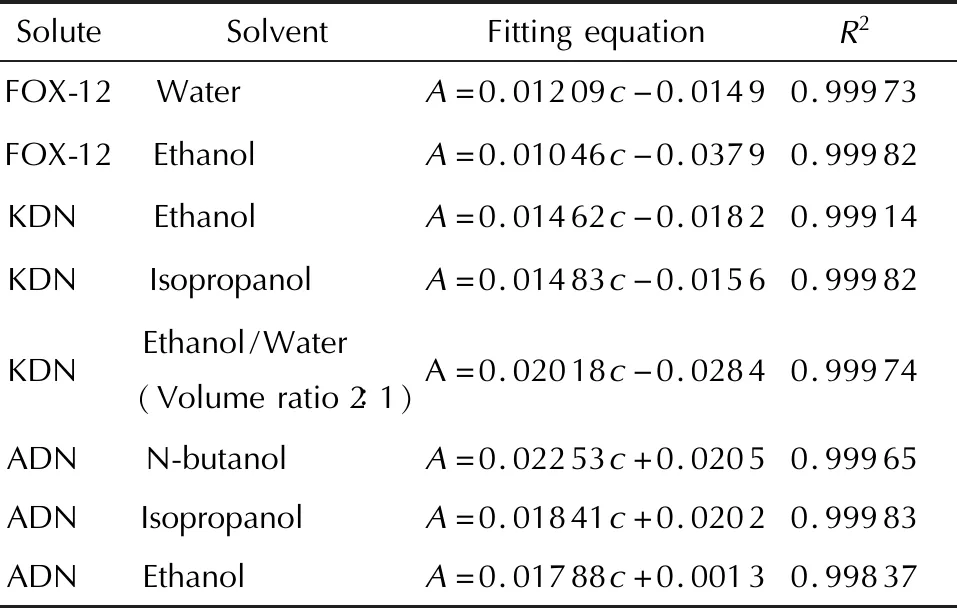
SoluteSolventFittingequationR2FOX-12Water A=0.01209c-0.01490.99973FOX-12Ethanol A=0.01046c-0.03790.99982KDN Ethanol A=0.01462c-0.01820.99914KDN Isopropanol A=0.01483c-0.01560.99982KDN Ethanol/Water (Volumeratio2∶1)A=0.02018c-0.02840.99974ADN N-butanol A=0.02253c+0.02050.99965ADN Isopropanol A=0.01841c+0.02020.99983ADN Ethanol A=0.01788c+0.00130.99837
2.2 3种二硝酰胺盐的溶解度分析
FOX-12在水和无水乙醇中的溶解度曲线如图4(a)所示;KDN在无水乙醇、异丙醇、无水乙醇/水(体积比2∶1)中的溶解度曲线如图4(b)所示;ADN在无水乙醇、异丙醇、正丁醇中的溶解度曲线如图4(c)所示。
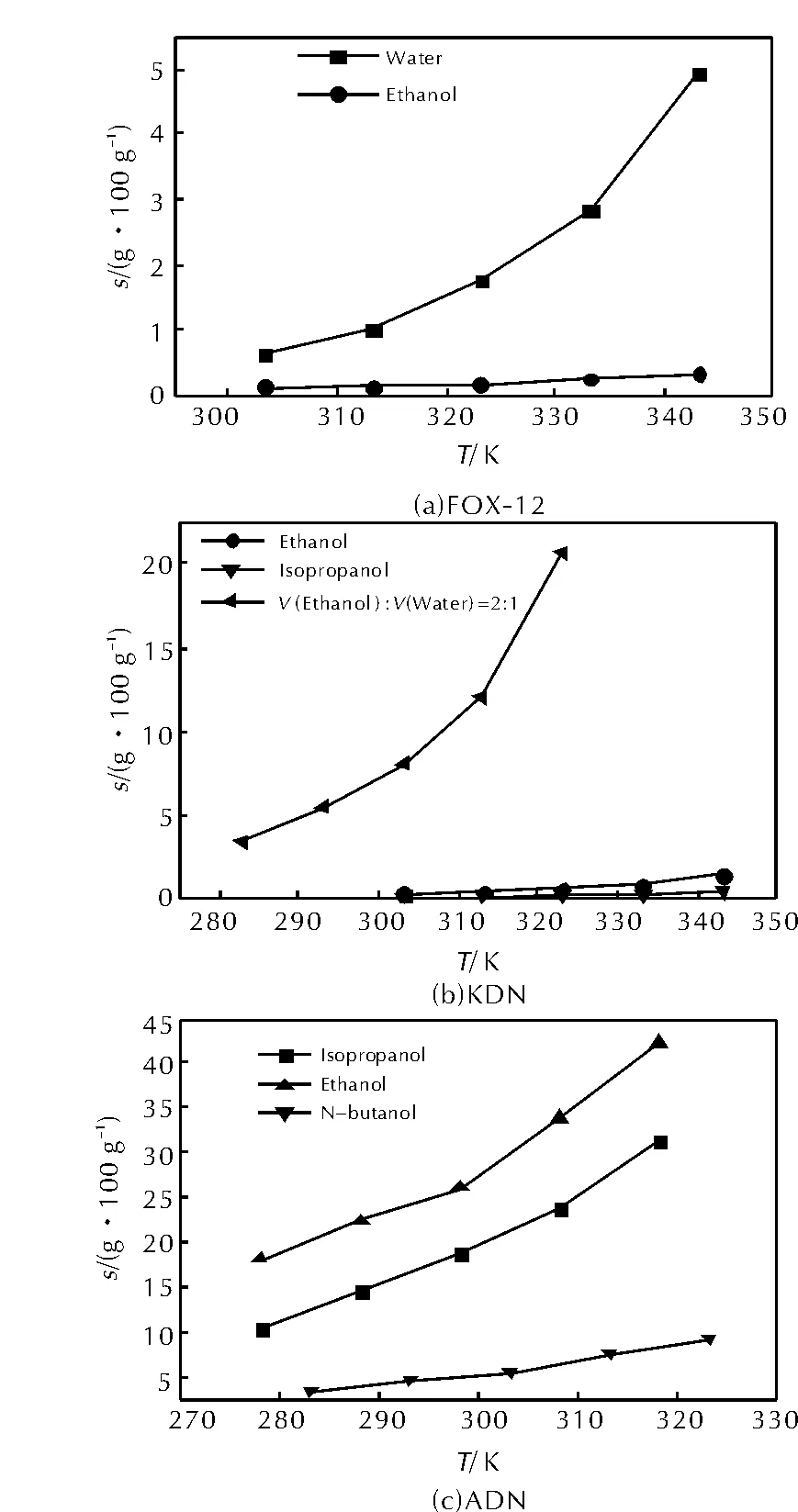
图4 二硝酰胺盐在不同溶剂中的溶解度曲线Fig.4 Solubility curves of three dinitramide salts in different solvents
由图4可知,在无水乙醇中,在10~70℃时,3种二硝酰胺盐溶解度由大到小的顺序为:ADN>KDN>FOX-12,FOX-12与KDN的溶解度小于1g,且相差不大;而ADN的溶解度大于10g,与其他两种二硝酰胺盐溶解度相比差异很大。
3种二硝酰胺盐的溶解度均随温度升高而增大,FOX-12在低温下微溶于水,高温下易溶于水,故水可以作为FOX-12重结晶的溶剂。KDN在乙醇水溶液中高温和低温下溶解度差别较大,故乙醇水溶液可以提纯KDN。
FOX-12在乙醇中溶解度小于水;KDN在异丙醇中溶解度小于无水乙醇;ADN在无水乙醇中溶解度最大,正丁醇中最小;故随着溶剂分子中所含碳原子的减少,溶质二硝酰胺盐的溶解度不断增大。
2.3 模型拟合
溶解度的拟合模型可以为重结晶工艺提供依据,当压力一定时,溶解度是温度的函数,故对于固液平衡数据的处理,可以通过纯经验方程法[9-11]、状态方程法[12-13]、λh方程[14]及活度系数法等进行关联。由于状态方程法一般研究气液平衡,研究固液平衡有很大的误差,而活度系数法拟合时要知道溶质的熔点以及熔化焓变,而λh方程也要知道溶质的熔点,故本实验采用经验方程法进行拟合。
2.3.1 热力学框架
在恒压下,固态活度定义式如下所示[13]:
(3)
(4)
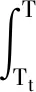
(5)
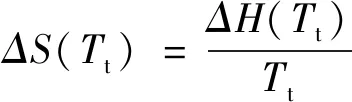
(6)
式中:ΔCp=Cp(液体)-Cp(固体);Tt为三相点温度,K。
联立上式,并且假设ΔCp在T~Tt之间是常数,可以得到:
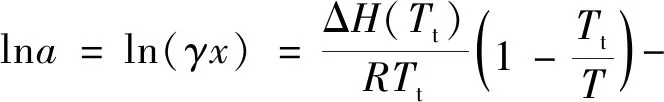
(7)
式中:γ为溶质的活度系数;x为溶质在溶剂中的摩尔溶解度;T为溶解温度,K;Tt为溶质在三相点的温度,K;ΔH(Tt)为溶质在三相点时的熔化焓变,kJ/mol;R为理想气体常数,J/(K·mol)。
引入平均相对偏差,计算公式如下:
(8)
式中:xcal为计算值;x为实验值;n为试验次数。
2.3.2 Apelblat方程
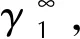
(9)
(10)
(11)
因此上述方程可以表示为:
(12)
式中:a、b、c为模型参数;T为热力学温度,K;x为溶质的摩尔溶解度。
本研究几个体系的Apelblat溶解度模型的回归结果见表2。
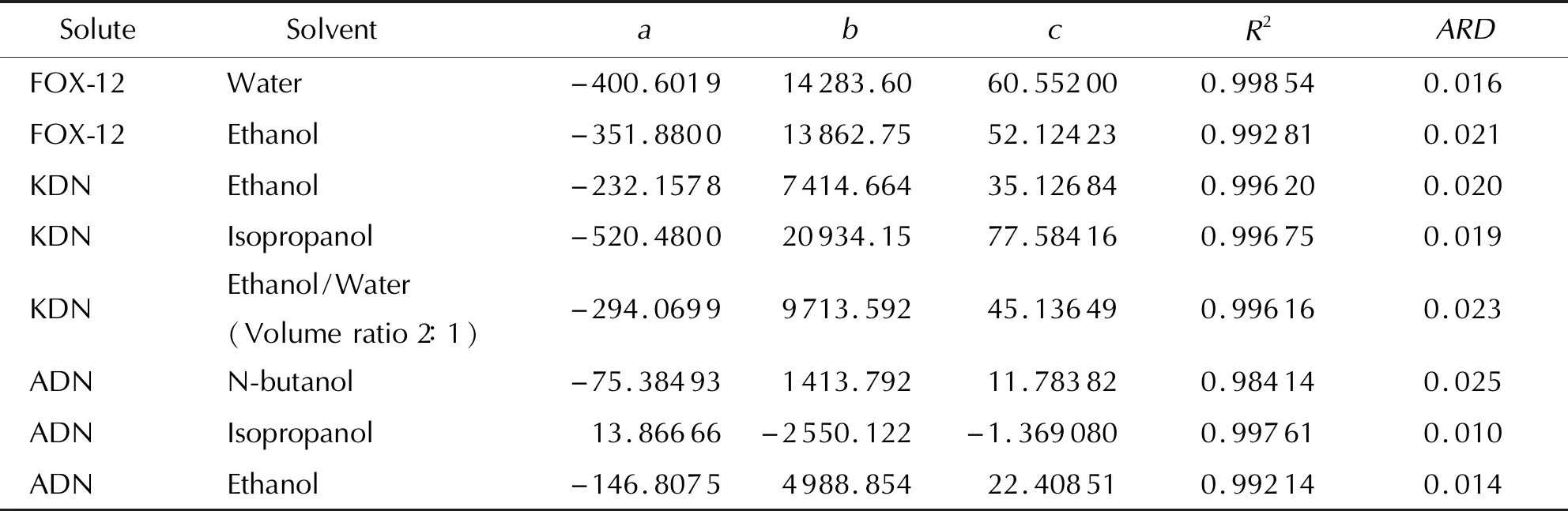
表2 二硝酰胺盐溶解度的Apelblat模型拟合
由表2可以看出,Apelblat方程拟合FOX-12、KDN与ADN在不同溶剂中的溶解度相对偏差范围在0.009~0.025之间,实验值与计算值吻合非常好,说明Apelblat方程可以很好地关联溶解度数据。
2.3.3 理想溶液模型
由于式(7)后面两项符号相反,且贡献不如第一项,尤其是T与Tt差别不大时,可以忽略后面两项,只考虑第一项,因此得到以下公式:
(13)
Prausnitz等[11]指出,在远离临界温度时,溶液中组分的活度系数对温度依赖是微弱的,故可以简化为:
(14)
式中:A、B为模型参数;T为热力学温度,K;x为溶质的摩尔溶解度。
本研究几个体系的理想溶液模型的回归结果见表3。
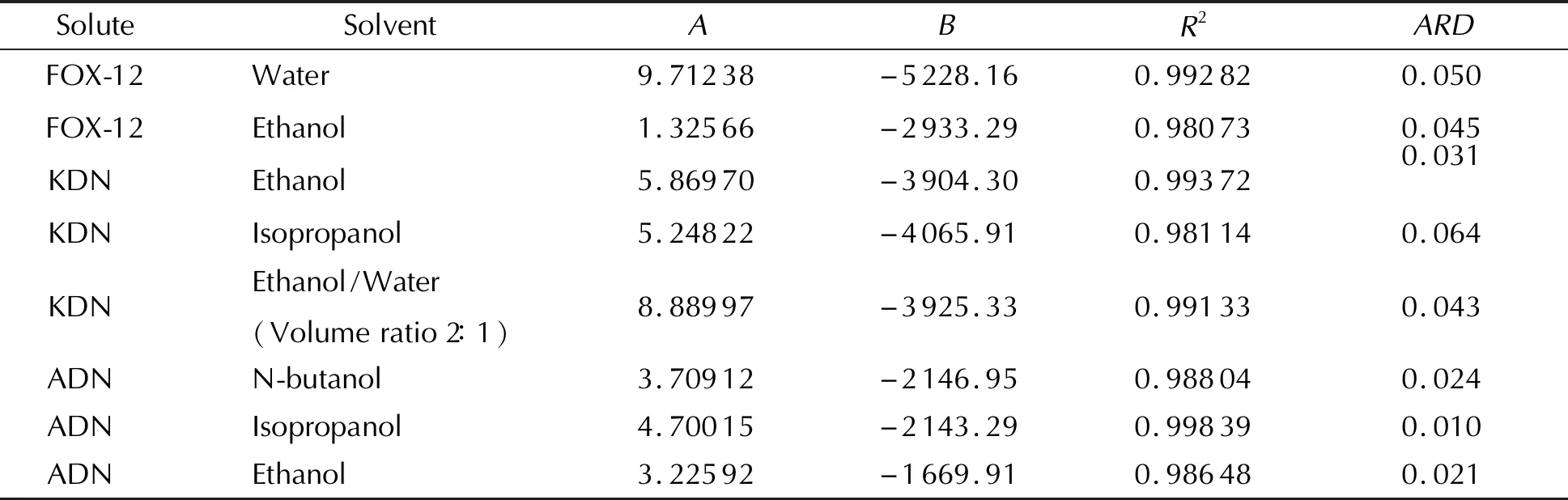
表3 3种二硝酰胺盐溶解度的理想溶液模型拟合
由表3可以看出,理想溶液模型拟合度在0.98073~0.99839之间,相对误差最大为6.4%,没有Apelblat模型拟合度高,故Apelblat模型更能拟合本研究的溶解度数据。
2.4 二硝酰胺盐溶解热力学函数的计算
对于理想溶液体系,可以用Van′t Hoff方程来描述溶质的摩尔分数与温度之间的关系[15]:
(15)
根据Van′t Hoff方程,lnx对1/T求斜率可求得[16]。
ΔGsol=ΔHsol-TΔSsol
(16)
式中:ΔHsol(kJ/mol)、ΔSsol(J/(mol·K))、ΔGsol(kJ/mol)分别为溶质溶解过程的焓变、熵变和吉布斯自由能变化。计算结果如表4所示。
由表4可以看出,FOX-12、KDN与ADN在考察的几种溶剂中溶解焓变均为正值,说明溶质的溶解过程均为吸热过程;ADN溶解过程的焓变明显小于其他两种二硝酰胺盐,这是因为ADN在溶解过程中电离出的铵根与溶剂分子形成氢键放出热量,抵消了一部分溶解热,而氢键的存在也增加了其溶解度,使得溶解过程更易进行,这与ADN易溶于醇相一致;二硝酰胺盐溶解过程的吉布斯自由能均大于0,说明溶解过程是非自发过程。
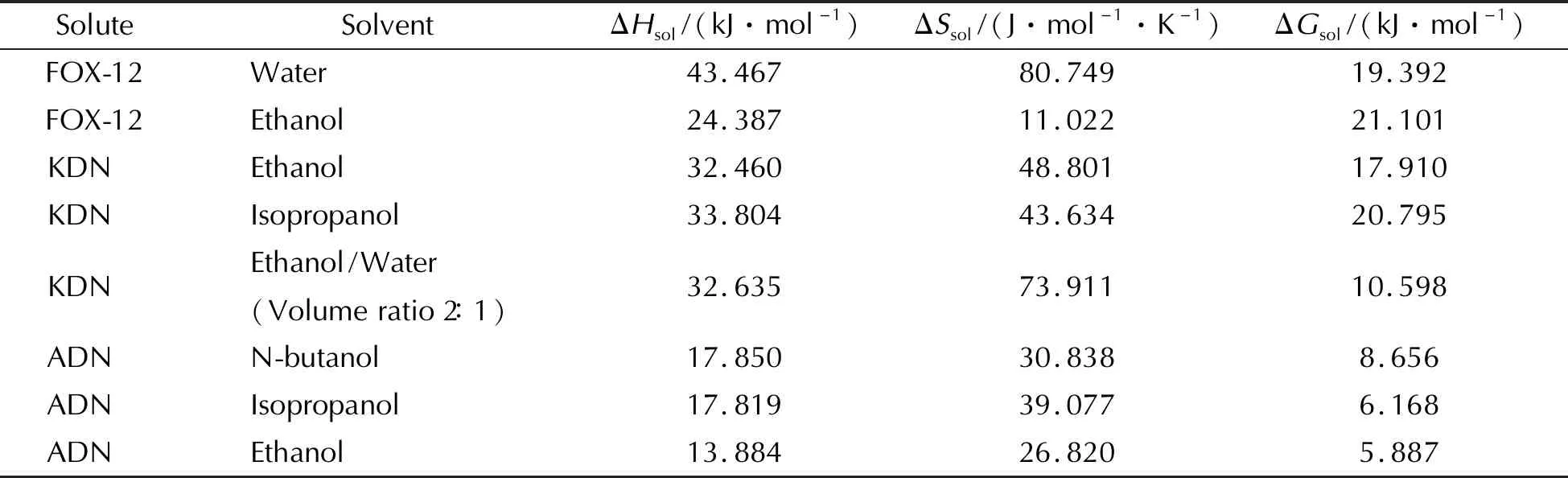
表4 3种二硝酰胺盐的热力学函数计算结果(T=298.15 K)
3 结 论
(1)采用平衡法中的紫外分光光度法测试吸光度,用拟合的标准曲线法分别计算了3种二硝酰胺盐的溶解度。二硝酰胺盐溶解度均随温度升高而增大。且同一种溶质的溶解度随着溶剂分子中所含碳原子数目的减少而增大,且在无水乙醇中ADN的溶解度远大于FOX-12与KDN。
(2)采用Apelblat方程与理想溶液模型拟合溶解度方程,发现使用Apelblat方程拟合时误差最小,平均误差不超过2%。
(3)用Van′t Hoff方程计算溶解过程的热力学函数,发现溶质溶解过程的焓变与熵变均大于0,说明溶解是吸热过程,升高温度有利于溶解,这与实验数据相一致,而溶解过程的吉布斯自由能均大于0,说明溶解过程是非自发过程。

